文章编号:1004-0609(2016)-10-2222-08
铜冶炼烟气中单体硫生成影响因素的热力学分析
张家靓1, 2,张建坤3,胡军涛1,张立峰1, 2
(1. 北京科技大学 冶金与生态工程学院,北京 100083;
2. 北京科技大学 稀贵金属绿色回收与提取北京市重点实验室,北京 100083;
3. 谦比希铜冶炼有限公司,基特韦 999134,赞比亚)
摘要:利用FactSage软件对铜熔炼的气相进行热力学平衡研究,分析烟气中单体硫生成的机理,详细考察了气相初始含量和温度等因素对平衡烟气中单体硫含量的影响规律,并为降低单体硫的含量提供了可行的技术方案。结果表明:CO对SO2、H2O具有还原作用,从而生成S2、H2S、H2等气体物质。平衡烟气中单体硫含量随着CO和SO2初始含量的升高以及H2O初始含量的降低而升高。适当提高烟气温度对于减少单体硫的生成是有利的。在烟气中通入一定量的富氧空气可使单体硫的含量大幅下降,但通入过量的空气会降低烟气的温度,对单体硫的去除反而不利。
关键词:单体硫;热力学分析;火法炼铜;烟气
中图分类号:TF811 文献标志码:A
烟气中单体硫含量超标是铜的火法冶炼工艺中的常见问题,也是长期以来困扰铜冶金工作者的技术难题[1-2]。单体硫是指以单质形式存在的硫,当含有单体硫的冶炼烟气进入到熔炼过程后续的除尘、制酸系统中时,由于温度骤降会导致部分的单体硫从烟气中析出,造成设备腐蚀、堵塞[3],严重影响烟气处理工艺的正常运行,此外单体硫的存在还会降低硫的总回收率[4]。因此,铜冶炼工艺中需要严格控制烟气中的单体硫含量,一般要求单体硫的含量低于1 g/m3。
结果表明,单体硫生成的主要来源为铜精矿中黄铜矿(CuFeS2)、黄铁矿(FeS2)等高价硫化物的分解反 应[5]。若铜精矿在入炉后不能迅速与氧气接触进而反应,就会造成分解反应加剧从而产生大量的单体硫进入烟气中[6]。因此,生产中往往通过降低精矿中含硫量、增大喷枪风量加强搅拌等方式[7]抑制单体硫的生成,但这些操作参数的改变一方面会对熔炼过程本身产生影响,且也不能彻底地解决单体硫超标的问题。
另一方面,生产中发现熔炼时为了维持温度而加入的煤也会对单体硫的含量造成影响[8],其原因可能是因为煤(或是其未充分氧化生成的CO)会将烟气中的SO2部分地还原为单体硫[9],但目前相关的理论研究很少。此外,由于高温下烟气的成分检测较为困难,因此生产中往往只能对出口烟气的部分组分(单体硫含量一般不能检测)进行分析,而诸如烟气中的SO2、H2O、CO等组分之间如何相互反应、烟气各组分的含量对单体硫的影响如何等问题目前并不明确。因而,当前亟需对铜熔炼气相的热力学进行研究,明确单体硫在烟气中的生成机理及其与气相各组分含量间的对应关系。
然而,铜熔池熔炼的烟气是一个含有众多组分的复杂体系,因此,想要通过化学平衡研究中最常用的平衡常数法中来计算非常困难。FactSage热力学软件是由F*A*C*T/FACT-Win 和ChemSage 两个热化学软件整合而成,现已广泛应用于冶金反应过程的优化、炉渣物理化学性能的预测、材料设计等领域[10-11]。
FactSage可基于吉布斯自由能最小化原理,并借助于软件包含的热力学数据库,实现多元多相体系的热力学平衡计算。
许多研究者采用Factsage软件对气相组分较为复杂的体系进行热力学平衡计算。张婷等[12]利用Factsage对煤气化反应系统进行热力学平衡计算,研究了体系中主要含硫化合物的生成特性并对其主要影响因素进行了分析。WANG等[13]则通过Factsage对煤/水/氧化钙的气化体系进行了热力学分析,考察不同气化操作温度、压力、煤的类型以及H2O/C下的氢气产量,结果表明:平衡气相的组分含量的实验值与计算值较为接近。YAKABOYLU等[14]对超临界水气化粪便后的气相平衡组成进行了热力学计算,该研究者首先利用过往文献中的实验数据对Factsage计算的准确性进行了验证,结果表明:Factsage对700 ℃、27.6 MPa下乙醇气化[15]以及不同温度、24 MPa下丙三醇气化[16]后的平衡气相组成均有很好的预测效果。
本文作者利用Factsage软件对铜熔炼的气相进行热力学平衡研究,重点考察气相组成、温度等因素对平衡烟气中单体硫含量的影响规律。基于热力学计算的结果,分析烟气中单体硫生成的机理,并为降低单体硫的含量提供了技术方案。
1 计算方法
对于一个封闭体系来说,当体系的温度、压力一定时,平衡状态下体系的总吉布斯自由能达到最小值,此即为吉布斯自由能最小化原理[17]。该原理如式(1)所示:
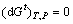 (1)
(1)
本研究中所采用的Factsage 6.4热力学软件的Equilib模块,正是利用这一原理,实现多元多相复杂体系的热力学平衡计算。
在给定的温度、压力以及组分的条件下,体系的总吉布斯自由能如式(2)所示:
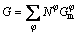 (2)
(2)
式中: 为组分
为组分 的摩尔量;
的摩尔量; 为其摩尔吉布斯自由能[18]。对于多相体系,体系的总吉布斯自由能可表达为式(3):
为其摩尔吉布斯自由能[18]。对于多相体系,体系的总吉布斯自由能可表达为式(3):


 (3)
(3)
式中:ig、pcp、s分别代表理想气体、纯固相以及溶液相;ni为组分i的摩尔量;pi为组分i的气体分压与总压(本研究中为0.1 MPa)的比值;xi、γi、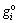 分别为组分i的摩尔分数、活度因子以及标准摩尔吉布斯自由能[14]。Factsage 6.4软件中的纯物质数据库FactPS中提供了接近五千种物质的标准摩尔吉布斯自由能的数据。借助于这一强大的数据库功能,Equilib模块可通过求解得到吉布斯自由能最小时ni、pi、xi的值,也就是得到了体系的平衡组成。由于求解过程中无需列出所有可能存在的化学反应,因此,较为适合于本研究所涉及的复杂体系的热力学计算,具体的数学求解方法详见文献[18]。
分别为组分i的摩尔分数、活度因子以及标准摩尔吉布斯自由能[14]。Factsage 6.4软件中的纯物质数据库FactPS中提供了接近五千种物质的标准摩尔吉布斯自由能的数据。借助于这一强大的数据库功能,Equilib模块可通过求解得到吉布斯自由能最小时ni、pi、xi的值,也就是得到了体系的平衡组成。由于求解过程中无需列出所有可能存在的化学反应,因此,较为适合于本研究所涉及的复杂体系的热力学计算,具体的数学求解方法详见文献[18]。
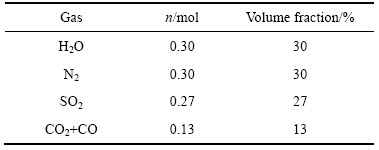
参考某艾萨炼铜厂的实际生产数据,给出了烟气初始组分(总的物质的量设为1 mol)的体积分数,如表1所示。计算中当变动某一组分的初始摩尔量以考察其影响时,其余组分的初始摩尔量均固定为此初始值。
表1 气相组分的初始含量
Fig. 1 Initial amounts of gaseous components
本研究中分别考察CO、SO2、H2O、O2的初始含量、温度等对平衡气相组成、SO2的还原率、还原产物含硫摩尔分数的影响,其中SO2还原率、还原产物含硫摩尔分数的计算式分别如式(4)、(5)所示:
 (4)
(4)
 (5)
(5)
式中:η为SO2的还原率;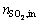 、
、 分别为SO2的初始量和平衡量,mol;yi为还原产物含硫摩尔分数;ni为还原产物的平衡含量,mol;s为还原产物含硫原子数。
分别为SO2的初始量和平衡量,mol;yi为还原产物含硫摩尔分数;ni为还原产物的平衡含量,mol;s为还原产物含硫原子数。
2 计算结果与讨论
2.1 CO初始含量的影响
固定CO2和CO的初始摩尔量之和为0.13 mol,在平衡温度为1250 ℃的条件下,计算不同CO初始摩尔量下的平衡气体含量(其结果如图1所示)。平衡后气相由108种气体组成,其中含硫气体达到30种,本研究中只对摩尔量大于1 mmol的气体进行分析讨论。
从图1中可以看到,CO的加入使平衡气相中出现S2、H2、H2S等气体,并且随着CO含量的升高,上述气体的含量不断升高,而初始气相中存在的SO2、H2O的含量则逐渐降低。由此可见在1250 ℃的条件下,CO对SO2、H2O具有还原作用,从而生成单体硫等气体物质。
可能存在的反应方程式:
4CO+2SO2 4CO2+S2 (6)
4CO2+S2 (6)
CO+H2O CO2+H2 (7)
CO2+H2 (7)
2H2+S2 2H2S (8)
2H2S (8)
SO2的还原率及还原产物含硫摩尔分数如图2所示。从图2中可以看到,SO2的还原率随着初始CO含量的升高不断升高,当初始CO含量为0.13 mol时,SO2的还原率高达18.8%。还原后的含硫产物主要包括S2、H2S、SSO等,其中S2的摩尔分数在80%以上。
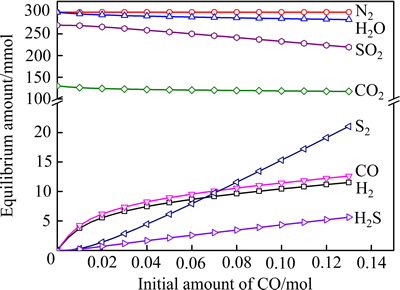
图1 CO初始含量对平衡气体含量的影响
Fig. 1 Effect of initial amount of CO on equilibrium gaseous amount

图2 CO初始含量对SO2还原率及还原产物含硫摩尔分数的影响
Fig. 2 Effect of initial amount of CO on reduction rate of SO2 and mole fraction of reduction products
通过计算求得在1250 ℃以及表1所示的初始含量条件下,只有当CO的初始体积分数低于1.07%时,平衡气相中S2的浓度才不致于超标。因此,在实际的熔炼过程中,应尽可能地降低煤的加入量,同时保证加入的煤可与氧气充分燃烧生成CO2,否则一旦CO进入气相,极易引起单体硫浓度的超标,使熔炼过程无法正常进行。
2.2 SO2初始含量的影响
在温度为1250 ℃、CO初始含量为0.03 mol的条件下,考察SO2初始含量对平衡气体含量、SO 2还原率及还原产物含硫摩尔分数的影响,其结果分别如图3和4所示。由图3和4可以看到,随着SO2初始含量的升高,SO2的还原率不断下降,而S2的含量逐渐升高,并且其在还原气体中含硫的摩尔分数也有所升高。通过计算得到不同SO2初始含量下,当平衡气相中S2的含量为1 g/m3时的初始CO含量,也就是一定条件下所能允许的CO初始含量的最高值,如图5所示。由图5可以看出,随着SO2初始含量的降低,其值略有上升。但即使SO2含量从0.4 mol降至0.1 mol,所能允许的CO初始含量的最高值也仅从0.0098 mol升至0.0148 mol。因此,无论是产出高浓度含硫烟气的强化炼铜工艺还是产出较低浓度烟气的鼓风炉熔炼工艺,都必须严格控制烟气中CO的含量。
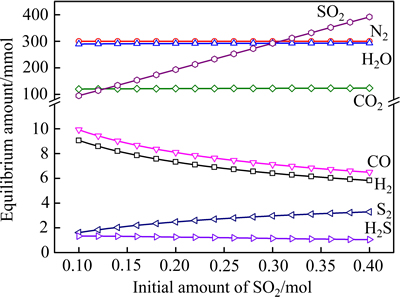
图3 SO2初始含量对平衡气体含量的影响
Fig. 3 Effect of initial amount of SO2 on equilibrium gaseous amount
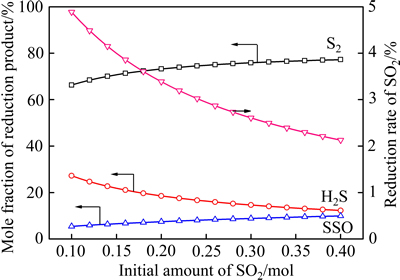
图4 SO2初始含量对SO2还原率及还原产物含硫摩尔分数的影响
Fig. 4 Effect of initial amount of SO2 on reduction rate of SO2 and mole fraction of reduction products
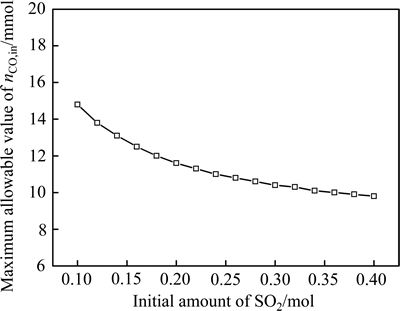
图5 不同SO2初始含量下所能允许的CO初始含量(nCO,in)的最高值
Fig. 5 Maximum allowable value of nCO,in at different initial amounts of SO2
2.3 H2O初始含量的影响
在温度为1250 ℃、CO初始含量为0.03 mol的条件下,考察H2O初始含量对平衡气体含量、SO 2还原率及还原产物含硫摩尔分数的影响,其结果分别如图6和7所示。由图6和7可以看出,随着H2O初始含量的升高,SO2的还原率下降,生成的S2含量逐渐降低,而H2、H2S等逐渐上升。这是因为H2O含量的升高使得CO对其还原作用增强,相应地对SO2的还原作用减弱。不同H2O初始含量下所能允许的CO初始含量的最高值如图8所示。由图8可以看出,随着H2O浓度的上升,其值不断上升。上述结果均表明,H2O含量的上升可以在一定程度上抑制气相中S2的生成。
2.4 O2初始含量的影响
在熔炼过程中,鼓入的O2在与入炉物料反应后必然还有一部分的残留,加上因炉体漏风而吸入的空气,因此在初始气相中可能还存在一定的O2。在温度为1250 ℃、CO初始含量为0.03 mol的条件下,考察O2初始含量对平衡气体含量、SO 2还原率及还原产物含硫摩尔分数的影响,其结果分别如图9和10所示。由图9和10可以看出,随着O2初始含量的提高,平衡气相中CO、S2、H2等还原性气体含量均大幅下降。当初始O2含量为0.0125 mol时,反应后S2的含量仅为3.4×10-5 mol。图11所示的不同O2初始含量下所能允许的CO初始含量的最高值。由图11可看出,提高初始O2含量,初始CO含量的上限值可大幅提升。由此可见,增加气相中O2的含量对降低烟气中单体硫的含量十分有利。
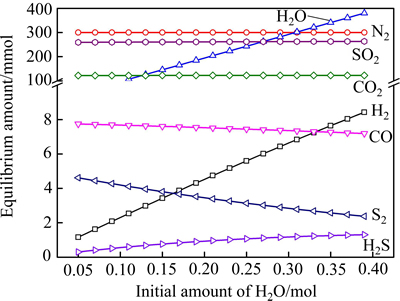
图6 H2O初始含量对平衡气体含量的影响
Fig. 6 Effect of initial amount of H2O on equilibrium gaseous amount
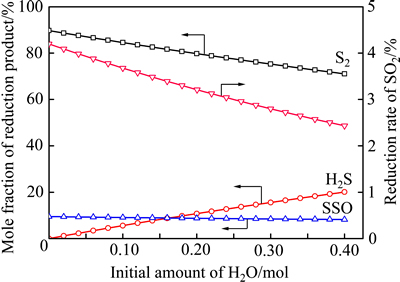
图7 H2O初始含量对SO2还原率及还原产物含硫摩尔分数的影响
Fig. 7 Effect of initial amount of H2O on reduction rate of SO2 and mole fraction of reduction products
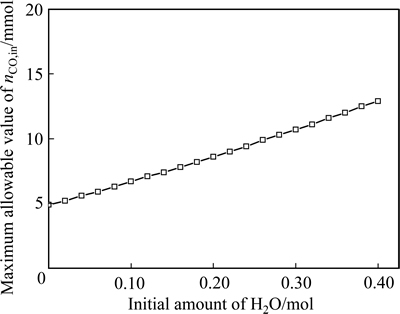
图8 不同H2O初始含量下所能允许的CO初始含量的最高值
Fig. 8 Maximum allowable value of nCO,in at different initial amounts of H2O
2.5 平衡温度的影响
在CO初始含量为0.03 mol的条件下,考察烟气温度对平衡气体含量、SO 2还原率及还原产物含硫摩尔分数的影响,其结果分别如图12和13所示。由图12和13可以看出,随着温度的升高,平衡气相中CO、H2的含量不断升高,H2S的含量则不断下降。在500~900 ℃的温度区间内,气相中S2的含量随温度升高逐渐上升,但当温度超过900 ℃,S2的含量逐渐下降,并且此时SO2的还原率也逐渐降低。图14所示为不同温度下所能允许的CO初始含量的最高值。由图14可以看出,当温度大于900 ℃时,提高温度可以增大CO初始含量的上限值。如当温度为1400 ℃时,该值为0.0173 mol,较900 ℃时提高3倍以上。由于火法炼铜工艺中烟气的温度一般都高于1000 ℃,因此适当提高烟气温度对减少单体硫的生成是有利的。
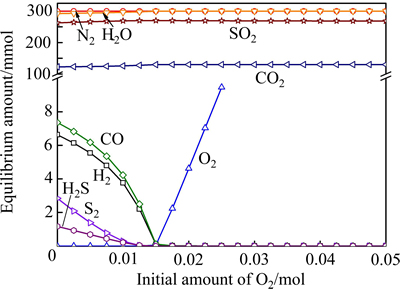
图9 O2初始含量对平衡气体含量的影响
Fig. 9 Effect of initial amount of O2 on equilibrium gaseous amount

图10 O2初始含量对SO2还原率及还原产物含硫摩尔分数的影响
Fig. 10 Effect of initial amount of O2 on reduction rate of SO2 and mole fraction of reduction products
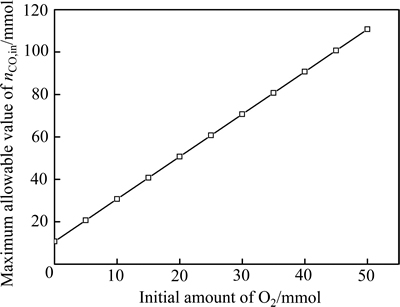
图11 不同O2初始含量下所能允许的CO初始含量的最高值
Fig. 11 Maximum allowable value of nCO,in at different initial amounts of O2
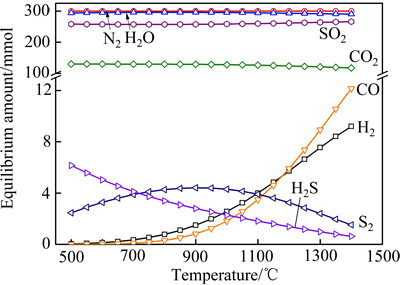
图12 温度对平衡气体含量的影响
Fig. 12 Effect of temperature on equilibrium gaseous amount
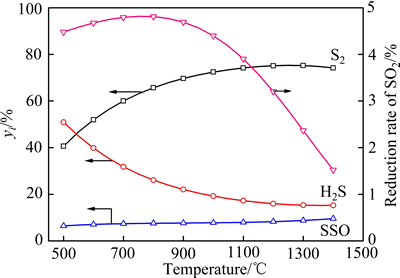
图13 温度对SO2还原率及还原产物含硫摩尔分数的影响
Fig. 13 Effect of temperature on reduction ratio of SO2 and molar fraction of reduction products
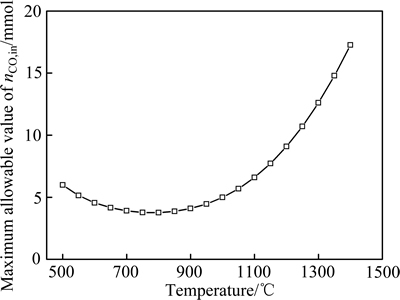
图14 不同温度下所能允许的CO初始含量的最高值
Fig. 14 Maximum allowable value of nCO,in at different temperatures
2.6 通入空气对单体硫去除效果的影响
通过前述的热力学分析结果可以发现,提高O2的初始含量可以显著地降低烟气中单体硫的含量。实际上该方法也已广泛地用于生产实践中,富邦铜业通过在富氧侧吹炼铜炉的侧墙引入二次风、在余热锅炉的上升烟道引入三次风的方法,使氧与单体硫充分反应,采取上述措施后,硫酸净化系统未出现单体硫超标的现象[19-20]。吉林镍业则通过在奥斯麦特炉喷枪管道上使用套筒风挡板,使上套筒风不进入熔池而直接进入烟气中,提高烟气中氧气的含量以降低单体硫的生成[21]。由此可见,通过鼓入空气(或富氧空气)是较为有效的降低烟气中单体硫含量的方法,但通入的空气量、空气含氧浓度、温度对单体硫去除效果的影响仍需进一步考察。
假定反应过程为绝热过程,通过热力学计算考察了空气加入量对平衡气相S2含量、温度的影响,如图15所示。由图15可以看出,在不同的起始S2含量下,通过加入一定量的空气均可使平衡后S2的含量大幅下降。从平衡温度的变化曲线可知,S2的氧化反应是一个放热反应,因此,即使通入空气的温度只有100 ℃,反应后烟气的温度仍会上升,但随着空气加入量的进一步增大,单体硫的氧化反应逐渐减弱,平衡后烟气的温度逐渐降低,因此,通入过量的空气对单体硫的去除反而不利。
富氧空气浓度、温度对平衡气相中S2的含量、温度的影响如图16和17所示。由图16和17可以看出,随着通入气体含氧浓度的升高,平衡后烟气中S2的含量变化不大,但烟气的平衡温度逐渐上升,显然提高富氧浓度可以促进单体硫的氧化反应更快地进行;而当通入空气的温度从50 ℃提高至150 ℃时,平衡烟气中S2的含量和温度的变化都很小,因此,提升通入空气的初始温度对于降低烟气中单体硫含量的效果不大。

图15 空气加入量对平衡气相中S2的含量和温度的影响
Fig. 15 Effect of addition amount of air on equilibrium amount of S2 and temperature

图16 富氧空气浓度对平衡气相中S2的含量和温度的影响
Fig. 16 Effect of O2 concentration on equilibrium amount of S2 and temperature

图17 通入空气温度对平衡气相中S2的含量、温度的影响
Fig. 17 Effect of air temperature on equilibrium amount of S2 and temperature
3 结论
1) CO对SO2、H2O具有还原作用,从而生成S2、H2S、H2等气体物质。在实际的熔炼过程中应尽可能地降低煤的加入量,同时保证加入的煤可与氧气充分燃烧生成CO2,否则一旦CO进入气相,极易引起单体硫浓度的超标。
2) 平衡烟气的单体硫含量随着SO2初始含量的升高、H2O初始含量的降低而升高;提高O2的初始含量可以显著降低烟气中的单体硫含量。
3) 当平衡烟气温度超过900 ℃时,S2的含量随温度逐渐下降,适当提高烟气温度对于减少单体硫的生成是有利的。
4) 在烟气中通入一定量的空气可使S2的含量大幅下降,但通入过量的空气会降低烟气的温度,对单体硫的去除反而不利。提高通入气体的氧浓度可提升烟气的平衡温度,从而提升单体硫的氧化反应速度。
REFERENCES
[1] 朱祖泽, 贺家奇. 现代铜冶金学[M]. 北京: 科学出版社, 2003: 37-38.
ZHU Zu -ze, HE Jia-qi. Modern copper metallurgy[M]. Beijing: Science Press, 2003: 37-38.
[2] 彭容秋. 铜冶金[M]. 长沙: 中南大学出版社, 2004: 12.
PENG Rong-qiu. Copper metallurgy[M]. Changsha: Central South University Press, 2004: 12.
[3] SCHMITT G. Effect of elemental sulfur on corrosion in sour gas systems[J]. Corrosion, 1991, 47(4): 285-308.
[4] 王 森. 艾萨熔炼烟气单质硫超标的原因及解决措施[J]. 中国有色冶金, 2015, 44(5): 25-28.
WANG Sen. Causes of over standard of elemental sulfur in ISA smelting flue gas and its solution[J]. China Nonferrous Metallurgy, 2015, 45(5): 25-28.
[5] 刘清漓. 喀拉通克铜镍矿富氧侧吹炉烟气中单体硫析出的治理[J]. 新疆有色金属, 2014, 37(2): 67-68.
LIU Qing-li. Prevention of the generation of elemental sulfur in flue gas from the oxygen-enriched side-blown furnace of Kelatongke Copper-Nickel Mine[J]. Xinjiang Nonferrous Metals, 2014, 37(2): 67-68.
[6] 张建玲. 炼铜密闭鼓风炉单体硫产生及治理的研究[J]. 云南冶金, 1999, 2: 42-45.
ZHANG Jian-ling. Formation of elemental sulfur and its prevention in hermetic copper blast furnace[J]. Yunnan Metallurgy, 1999, 2: 42-45.
[7] 孙来胜. 金昌冶炼厂Ausmelt炉烟气单体硫超标浅析[J]. 中国有色冶金, 2007, 36(2): 30-33.
SUN Lai-sheng. Analysis of the cause for free sulfur content exceed the standard of Ausmelt furnace in Jinchang Smelter[J]. China Nonferrous Metallurgy, 2007, 36(2): 30-33.
[8] 孙林权, 王举良. 富氧侧吹熔池熔炼炉炼铜的生产实践[J]. 中国有色冶金, 2011, 40(4): 15-18.
SUN Lin-quan, WANG Ju-liang. Production practice of copper smelting in oxygen-enriched side-blown bath smelting furnace[J]. China Nonferrous Metallurgy, 2011, 40(4): 15-18.
[9] 傅志华, 王立川, 陈晓芸. 白银炉烟气中单体硫的形成(Ⅰ)[J]. 中南矿冶学院学报, 1994, 25(4): 530-534.
FU Zhi-hua, WANG Li-chuan, CHEN Xiao-yun. Formation mechanism of elemental sulphur in flue gas of Baiyin furnace (Ⅰ)[J]. Journal of Central & South Institute of Mining and Metallurgy, 1994, 25(4):530-534.
[10] BALE C W, CHARTRAND P, DEGTEROV S A, ERIKSSON G, HACK K, BEN MAHFOUD R, MELANCON J, PELTON A D, PETERSEN S. FactSage thermochemical software and databases[J]. Calphad, 2002, 26(2): 189-228.
[11] 曹战民, 宋晓艳, 乔芝郁. 热力学模拟计算软件FactSage及其应用[J]. 稀有金属, 2008, 32(2): 216-219.
CAO Zhan-min, SONG Xiao-yan, QIAO Zhi-yu. Thermodynamic modeling software FactSage and its application[J]. Rare Metals, 2008, 32(2): 216-219.
[12] 张 婷, 郭庆华, 梁钦锋, 于广锁. 煤气化过程中含硫化合物生成特性的热力学研究[J]. 中国电机工程学报, 2011, 31(11): 32-39.
ZHANG Ting, GUO Qing-hua, LIANG Qin-feng, YU Guang-suo. The generation properties of sulfur compounds during coal gasification by thermodynamic equilibrium simulation[J]. Proceedings of the CSEE, 2011, 31(11): 32-39.
[13] WANG Zhi-hua, ZHOU Jun-hu, WANG Qin-hui, FAN Jian-ren, CEN Ke-fa. Thermodynamic equilibrium analysis of hydrogen production by coal based on coal/CaO/H2O gasification system[J]. International Journal of Hydrogen Energy, 2006, 31(7): 945-952.
[14] YAKABOYLU O, HARINCK J, SMIT K G G, JONG W D. Supercritical water gasification of manure: A thermodynamic equilibrium modeling approach[J]. Biomass & Bioenergy, 2013, 59(1): 53-63.
[15] TAYLOR J D, HERDMAN C M, WU B C, WALLY K, RICE S F. Hydrogen production in a compact supercritical water reformer[J]. International Journal of Hydrogen Energy, 2003, 28(11): 1171-1178.
[16] BYAD A J, PANT K K, GUPTA R B. Hydrogen production from glycerol by reforming in supercritical water over Ru/Al2O3 catalyst[J]. Fuel, 2008, 87(13/14): 2956-2960.
[17] ABBOOT M M, SMITH J M, NESS H C V. Introduction to chemical engineering thermodynamics[M]. Boston: McGraw- Hill, 2001: 619-626.
[18] ERIKSSON G, HACK K. ChemSage-A computer program for the calculation of complex chemical equilibria[J]. Metallurgical & Materials Transactions B, 1990, 21(6): 1013-1023.
[19] 王志超, 李东泽, 李国军. 富邦富氧侧吹炼铜炉二次风改造生产实践[J]. 有色矿冶, 2014, 30(4): 40-42.
WANG Zhi-chao, LI Dong-ze, LI Guo-jun. Reformation and production practice for secondary air Fubang oxygen-enriched side blown copper melting furnace[J]. Nonferrous Mining and Metallurgy, 2014, 30(4): 40-42.
[20] 罗银华, 王志超. 富邦富氧侧吹熔池炼铜炉生产实践[J]. 有色金属(冶炼部分), 2013, 7: 19-22.
LUO Yin-hua, WANG Zhi-chao. Plant practice of Fubang oxygen-enriched side-blown bath smelting copper furnace[J]. Nonferrous Metals (Extractive Metallurgy), 2013, 7: 19-22.
[21] 李景峰. 澳斯麦特炉烟气单质硫超标浅析[J]. 中国有色冶金, 2014, 43(5): 13-16.
LI Jing-feng. Discussion on exceeding standard of elemental sulfur in flue gas from Ausmelt furnace[J]. China Nonferrous Metallurgy, 2014, 43(5): 13-16.
Thermodynamic analysis for influence factors on generation of elemental sulfur in copper-smelting flue gas
ZHANG Jia-liang1, 2, ZHANG Jian-kun3, HU Jun-tao1, ZHANG Li-feng1, 2
(1. School of Metallurgical and Ecological Engineering,
University of Science and Technology Beijing, Beijing 100083, China;
2. Beijing Key Laboratory of Green Recycling and Extraction of Metals,
University of Science and Technology Beijing, Beijing 100083, China;
3. Chambishi Copper Smelter Limited, Kitwe 999134, Zambia)
Abstract: The thermodynamic equilibrium was investigated for the gaseous system of copper smelting using Factsage software. The mechanism was analyzed for the generation of elemental sulfur. The effects of initial amounts on gaseous components and temperature on the equilibrium amount of elemental sulfur were assessed. Obviously, the technical method for reducing the amount of elemental sulfur was presented. The results show that CO can reduce SO2, H2O to generate the low-valence gas, such as S2, H2S, H2. The equilibrium amount of S2 increases with the increase of CO, SO2 and the decrease of H2O. Increasing the temperature properly is beneficial to inhibit the generation of elemental sulfur. The S2 amount sharply decreases by blowing a certain amount of oxygen-enriched air into the flue gas, but excess air will reduce the temperature of flue gas, which is harmful for the removal of elemental sulfur.
Key words: elemental sulfur; thermodynamic analysis; copper pyrometallurgy; flue gas
Foundation item: Project(FRF-TP-15-068A1) supported by the Fundamental Research Funds for the Central Universities, China
Received date: 2016-03-10; Accepted date: 2016-07-26
Corresponding author: ZHANG Jia-liang; Tel: +86-13041080080; E-mail: jialiangzhang@ustb.edu.cn
(编辑 李艳红)
基金项目:中央高校基本科研业务费专项资金资助项目(FRF-TP-15-068A1)
收稿日期:2016-03-10;修订日期:2016-07-26
通信作者:张家靓,博士,讲师;电话:13041080080;E-mail: jialiangzhang@ustb.edu.cn