文章编号:1004-0609(2009)04-0749-05
镍电解阳极液深度除铜
赵中伟,陈爱良,孙培梅,陈星宇,霍广生,李洪桂
(中南大学 冶金科学与工程学院,长沙 410083)
摘 要:将“活性硫化镍法”所用的除铜试剂“硫化镍”视为先导化合物,按电子等排原理,通过分子修饰进行类型衍化,修饰阴离子,以一种新设计的含硫化学结构取代S2-,得到的新型除铜剂为NAS和硫化镍混合物。结果表明:当NAS纯度α≥73%(NAS在混合物中所占比例)、除铜剂用量为理论量的1.2倍、溶液pH值为4.0、反应温度为60 ℃时反应80 min后,采用新型除铜剂从镍电解阳极液中除铜,除铜后溶液中的铜浓度c(Cu2+)可降至1.57×10-5 mol/L,除铜渣中铜镍质量比不小于25,远优于工业生产的要求(c(Cu2+)≤1.57×10-5 mol/L,渣中铜镍质量比不小于15);NAS在自然条件下放置62 d后,其除铜效果仍然能够满足生产要求,且NAS在除铜过程中没有引入有害离子进入溶液。
关键词:镍电解阳极液;除铜;电子等排原理
中图分类号:TF 811 文献标识码: A
Removing copper from nickel electrolyte solution
ZHAO Zhong-wei, CHEN Ai-liang, SUN Pei-mei, CHEN Xing-yu, HUO Guang-sheng, LI Hong-gui
(School of Metallurgical Science and Engineering, Central South University, Changsha 410083, China)
Abstract: New highly effective removing copper reagent, NAS, was obtained through lead generation by molecule modification based on the theory of isostere principle. Regarded as a leading compounds, NiS was used as a kind of reagent for removing copper in the technology of active nickel sulfide. NAS was designed by replacing S2- of NiS with a kind of new chemical structure through modifying anion. The results show that removing copper with NAS will achieve the best result when NAS purity α is more than 73%, the dosage of NAS is 1.2 times of theoretical value, and when pH value is 4.0 at 60 ℃. The concentration of copper can reach 1.57×10-5mol/L in the electrolyte solution and the mass ratio of copper to nickel is more than 25 in the residue after removing copper. Especially, after NAS is kept for 62 d, it can still satisfy the demand of removing copper. Moreover, the copper sulfide, with small solubility product constant, is produced after removing copper with NAS. No harmful ions enter into the nickel electrolyte solution.
Key words: nickel electrolyte solution; removing copper; isostere principle
目前,在镍电解精炼过程中,国内外对某些杂质(如铁和钴)净化工艺控制得较好,惟有除铜工艺仍不能令人满意[1-5]。由于镍/铜元素化学性质相似,其有效分离成为长期困扰国内外冶金界的难题。针对这一难题,我国早在“八五”和“九五”计划中两次将这项研究列为重点攻关项目,也曾有专家尝试开发了各种方法[6-10],但是至今尚未解决这一难题。由于问题长期未能得到解决,某些企业的技术要求也不得不适当放宽。除铜后溶液中的铜含量由2 mg/L(3.15×10-5 mol/L)提高到3 mg/L(4.72×10-5 mol/L),除铜渣中铜镍质量比则由20降低到15。
由于铜元素性质强烈亲硫,采用硫化法除铜具有较好的选择性。目前开发的各种除铜方法中选择性和除铜深度均较好的除铜剂大都利用了铜的这一性质,不同的只是需提供合适的硫的化学形式。前已有研究中硫化除铜方法[11-12]有效除铜的关键在于使溶液中S2-维持一个适当的有效浓度或者说活度。如果浓度(或活度)过高,比如直接加入硫化钠,则在除铜酸度条件下(pH≤4),酸性环境中的硫将以硫化氢的形式大量逸出,不但造成浪费,更会污染环境。而如果溶液中S2-有效浓度太低,则除铜能力下降[13-14],目前,金川公司使用的镍精矿除铜就属于后一种情况,由于镍精矿中NiS活性太低(NiS有多种晶型,矿物在地下经过了漫长的地质年代演变,化学结构和性质已经趋于十分稳定,其溶度积可取较小的值10-26),相应可维持的溶液S2-离子浓度较低,影响除铜效果。
利用新制备的“活性硫化镍”反应活性较高的特点,可使除铜效果大大增强,且又不致产生硫化氢气体,这就形成了“所谓活性硫化镍法”。但活性硫化镍十分容易发生化学转化,生成惰性Ni(OH)S而使试剂迅速在6 h 后就失效。
镍铜深度分离的关键在于寻找新的试剂,运用分子设计的思想和方法定向设计或寻找某些具有特定功能的化学结构。
1 新试剂的寻找
在药物化学中,一个新药物的设计开发一般包括如下两个关键阶段。首先是要获得一个具有显著效果的化学结构,这一化学结构称为“先导化合物”。再在“先导化合物”的基础上对化学结构进行修饰、改造,进行“类型衍化”。据文献[15-16],有六大药物化学原理可作为借鉴,它们分别为同系原理、同烯系原理、同电异素原理、同分异构原理、同型原理和拼合原理。
见百熙[15]探讨了这些原理在选矿药剂开发中借鉴应用的可能性,并指出实际上许多选矿药剂之间都符合药物化学的六大原理。见百熙[15]和赵中伟等[16]分别探讨了使用电子等排(即同电异素)原理开发冶金用沉淀剂、萃取剂、离子交换剂等的可能性。通过分析医药、农药、分离试剂之间性质的异同,认为虽然药物类与分离试剂之间存在一些差别,例如对于医药、农药,受体为有机组织;而对于提取冶金中的分离试剂,受体为待分离的金属离子。但从化学原理上讲,其效果均需要在作为试剂的有机物(也可包括无机物)与受体之间的相互作用中体现,因而应遵循相同的化学规律。进行电子等排取代的原则流程,其流程图如图1所示[16]。

图1 电子等排取代的原则流程图[16]
Fig.1 Flowsheet of replace with isostere principle[16]
为了合理等排取代,等排体不仅要具有相同总数的外层电子,还应在分子大小、形状(包括键角和杂化度)、构象、电子分布(极化度、诱导效应、共轭效应、电荷和偶极等)、脂水分布系数、pKc、化学反应活性和氢键形成能力等方面存在相似性。当然,要求所有这些参数均相似很难,只要对化合物的生物性质起决定作用的参数能够匹配即可。因而,所得化合物按其类似性质不同可分别称为疏水性等排体、电性等排体、立体性等排体、等电性、等疏水性及等立体性生物电子等排体。由于生物等排体不具通用性,有时适合于某一系列的生物等排体,但对另一系列化合物并不适用。
生物电子等排体(Bioisostere)按化合价可分为如下5 类[16]:
1价:―X,―OH,―SH,―NH2,―CH3。
2价:―O―,―S―,―Se―,―Te―,―NH―,―CH2―。
3价:―N=,―P=, ―As= ,―Sb=,―CH=。
4 价:=C=,=N+=,=P+=,=As+=,Sb+=。
环等排体: ―CH=CH―,―CH= N―,―S―,―O―,―N=,―CH=。
借鉴这些观点和方法,本文作者认为有可能利用分子设计的原理和方法,通过寻找合适的先导化合物,再在此基础上进行类型衍化,从而最终得到理想的镍/铜分离试剂。
3 新型除铜试剂的分子设计
根据铜镍特性,可以将“硫化镍”作为研究的起点,当成研究新试剂时的“先导化合物”,通过分子的修饰、改造,以获得最佳分子结构,从而实现镍/铜的高效分离。
与有机药物相比,硫化镍组成极为简单,只有镍和硫两种原子。不管晶型如何,都是通过镍和硫原子在空间的规律性重复排列而成。对这种先导化合物进行改造,有两条途径:一是改变其晶体结构,使其以化学活性最高的状态赋存。但由前人工作可知,按这条路实际仍是“活性硫化镍法”;另一种就是对化学组成进行改造,通过引进有机或无机结构修饰、替换其结构中的镍离子或硫离子,或者干脆将镍和硫都加以修饰。本文作者只讨论利用分子设计方法修饰阴离子的研究,即保留阳离子镍而修饰阴离子硫,则涉及到采用什么样的阴离子替代硫离子的问题。
考虑到前面提及的以硫化物分离铜的优越性,新设计的阴离子应当含有元素硫,且该元素硫可以在适当的工作条件下与溶液中的杂质铜形成牢固化学结合而将铜除去。
硫醇基似乎是一个不错的选择,但水溶性硫醇的挥发性极强(特别是在酸性条件下),有令人窒息的臭味,且价格昂贵。黄药类也有类似问题,且在酸性环境中很不稳定。硫代硫酸根曾为许多研究者所看好,但制备流程冗长,导致成本居高不下。采用多硫根也不成功。
硫醇基、黄原酸基、硫代硫酸根和多硫根都可看成广义的电子等排体,故有关这些功能基的镍盐作为除铜试剂的研究其实都可以看成在有意无意地运用电子等排原理。
因此,进一步使用这一原理对先导化合物进行衍化,并尽可能详细地考虑到所得新结构的化学活性,及使用过程中的转化产物对后续流程的影响,则有望通过逐步修正、逼进,从而获得高效除铜试剂。
作为除铜剂的有机或无机镍盐应当具有适当大的溶度积,以保证具有较好的化学活性。以“硫化镍”作为参比,新的有机和无机阴离子应具有较大的离子半径以减少与镍离子间的库仑作用力,增大阴阳离子作用位阻。阴离子本身可与铜牢固结合除去,溶液无残留,或者阴离子性质不稳定,在除铜过程中分解生成铜的硫化物,且溶液中也不引入有害离子。
基于这样的设计原则,确定了一种新的新型除铜剂NAS。
3 除铜剂的应用
在pH=4.0、除铜剂用量(实际加入量为理论量的倍数)为1.2、温度为60 ℃、中速磁力搅拌80 min的条件下,考察NAS纯度α(除铜剂为NAS和硫化镍混合物,α为NAS所占份额)及NAS的陈化时间对除铜后溶液的铜浓度c(Cu2+)、除铜渣中铜镍质量比的影响,其结果分别如表1和2所列。
从表1和2可看出:除铜剂陈化时间相同,当NAS纯度大于0(0表示活性NiS含量为100%)时,除铜后溶液的铜浓度随着α的增加而降低,除铜渣中铜镍质量比随着α的增加而增加。说明随着α的增加,活性NiS所占含量减少。相反,NAS基团所占含量增加,与铜成键共价性强,极性小,与溶液中Cu2+反应彻底;当NAS纯度α一定时,随着NAS陈化时间的延长,除铜后溶液的铜浓度增加,除铜渣中铜镍质量比减少,这是由于除铜剂活性降低由溶液中的Cu2+反应能力减弱引起的。当NAS纯度α超过83%之后,除铜效果明显变好。当α=100%时(即全为NAS),除铜剂陈化92 d,除铜效果仍然还好。其原因主要是由于随着反应深度的增加,NAS分子中阴离子尺度加大,但阴离子的电荷数并未变化。这样一来,阴阳离子间的库仑作用力变弱,NAS的化学活性相应提高,除铜能力也得以增强。
表1 NAS的纯度α及其陈化时间对除铜后溶液中铜浓度的影响
Table 1 Effect of purity and aging time of NAS on copper concentration in electrolyte after removing copper

表2 NAS纯度α及NAS陈化时间对除铜渣中铜镍质量比的影响
Table 2 Effect of purity and aging time of NAS on mass ratio of copper to nickel in residue after removing copper

将不同NAS纯度α下,能够维持足够除铜活性的时间如表3所示。从表3可以看出,随着NAS纯度α增加,除铜后溶液中的Cu含量、除铜渣中铜镍质量比同时达到生产要求(c(Cu2+)≤1.57×10-5mol/L,铜镍质量比不小于15)时能够使NAS保持活性的时间增长。当α≤73%时,此两项指标均难于达到生产要求,但当α为73%~ 100%时,保持活性时间甚至能达到0~62 d。
表3 不同NAS纯度α下NAS保持活性的时间
Table 3 Keeping activity time of NAS after removing copper at different purity of NAS

采用NAS除铜后,对除铜渣进行XRD分析,其结果如图2所示。
从图2可以看出:除铜渣中只有NiS和CuS两种物质,且其峰很尖锐。说明NAS的阴离子性质不稳定,在除铜过程中分解生成铜的硫化物,且经过溶液分析,溶液中没有引入有害离子。
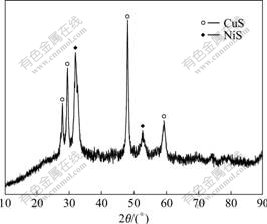
图2 除铜渣的XRD谱
Fig.2 XRD pattern of residue after removing copper
4 结论
1) 基于新型除铜剂应当具有适当的较大的溶度积、以保证具有好的化学活性的原则,以“硫化镍”作为参比,借鉴分子设计的原理和方法寻找了一种新的除铜剂。
2) 当除铜剂纯度不小于73%时,在用量为理论用量的1.2倍,溶液pH值为4.0,反应温度为60 ℃,时间80 min的条件下,除铜后溶液中的铜浓度可降至1.57×10-5 mol/L,除铜渣中铜镍质量比不小于25,远优于工业生产中对铜的要求。
3) 除铜技在自然条件下放置62 d后,除铜效果仍然能够满足生产要求。除铜产物为硫化物,溶液中没有引入有害离子。
REFERENCES
[1] 黄其兴, 王立川, 朱鼎元. 镍冶金学[M]. .北京: 中国科学技术出版社, 1990: 8-10.
HUANG Qi-xing, WANG Li-chuang, ZHU Ding-yuan. Nickel metallurgy[M]. Beijing: Science and Technology Press, 1990: 8-10.
[2] PICKLES C A. Microwave heating behaviour of nickeliferous limonitic laterite ores[J]. Minerals Engineering, 2004, 17(6): 775-784.
[3] LAZARIDIS N K, PELEKA E N, MATIS K A. Copper removal from effluents by various separation techniques[J]. Hydrometallurgy, 2004, 74(1/2): 149-156.
[4] KIRJAVAINEN V, SCHREITHOFER N, HEISKANEN K. Effect of some process variables on flotability of sulfide nickel ores[J]. Int J Miner Process, 2002, 65(2): 59-72.
[5] ZHANG Hong-guang, DREISINGER D B. The adsorption of gold and copper onto ion-exchange resins from ammoniacal thiosulfate solutions[J]. Hydrometallurgy, 2002, 66(1/2): 67-76.
[6] IVANOV I M, NIKOLAEO A V, GINDIN L M, KHEIFEZ L V, VOLKOV L V, MAIZLISH R S. Solvent extraction removal of cobalt and other impurity elements from nickel electrolytes[J]. Hydrometallurgy, 1979, 4(4): 377-387.
[7] KONG D, MARTELL A E, MOTEKAITIS R J, REIBENSPIES J H. Two novel homodinuclear Ni(Ⅱ) and Cu(Ⅱ) complexes with a 24-membered octadentate hexaazamacrocyclic ligand: stability and X-ray crystal structures[J]. Inorganica Chimica Acta, 2001, 317(1/2): 243-251.
[8] GOBI K V, OHSAKA T. Electrochemical and spectral properties of novel dinickel(Ⅱ) and dicopper(Ⅱ) complexes with N,N-linked bis(pentaazacyclotetradecane)[J]. Electrochimica Acta, 1998, 44(2/3): 269-278.
[9] XU Guang-ri, CHANG H Y, CHO H. Macrocyclic nickel(Ⅱ) complex and hydrophilic polyurethane film electrodes for the electrocatalytic oxidation and selective detection of norepinephrine[J]. Electrochimica Acta, 2004, 49(24): 4069-4077.
[10] LEE C I, YANG Wan-fa, HSIEH C I. Removal of copper (Ⅱ) by manganese-coated sand in a liquid fluidized-bed reactor[J]. Journal of Hazardous Materials B, 2004, 114(1/3): 45-51.
[11] RESENDE P C, BARRADO F S, MARTINS A H. Sulfuric activation of a brazilian manganese ore for heavy metals removal[J]. Hydrometallurgy, 1999, 51(3): 325-333.
[12] RIBEIRO A B, MEXIA J T. A dynamic model for the electrokinetic removal of copper from a polluted soil[J]. Journal of Hazardous Materials, 1997, 56(3): 257-271.
[13] GAMMONS C H, SEWARD T M. Stability of manganese (2) chloride complexes from 25 to 300 ℃[J]. Geochimica et Cosmochimica Acta, 1996, 60(22): 4295-4311.
[14] MATLOCK M M, HENKE K R, ATWOOD D A. Effectiveness of commercial reagents for heavy metal removal from water with new insights for future chelate designs[J]. Journal of Hazardous Materials B, 2002, 92(2): 129-142.
[15] 见百熙. 浮选药剂的分子结构及其规律性―用高等药物化学原理探讨浮选药剂分子的设计[J]. 有色金属, 1983, 35(1): 48-57.
JIAN Bai-xi. The structure and regularity of flotation reagent molecules―survey of flotation reagent molecular design with the principles of pharmaceutical chemistry[J]. Nonferrous Metals, 1983, 35(1): 48-57.
[16] 赵中伟, 李洪桂, 霍广生. 电子等排原理及利用其设计分离试剂的可行性[J]. 中南工业大学学报, 2002, 33(6): 584-587.
ZHAO Zhong-wei, LI Hong-gui, HUO Guang-sheng. Application of isostere principle in molecular design of separation reagents[J]. Journal of Central South University of Technology, 2002, 33(6): 584-587.
基金项目:国家重点基础研究发展计划资助项目(2007CB613603);国家高技术研究发展计划资助项目(2006AA06Z122)
收稿日期:2008-06-02;修订日期:2008-12-29
通讯作者:赵中伟,教授,博士;电话:0731-8830476;E-mail: zhaozw@mail.csu.edu.cn
(编辑 李艳红)