PS转炉造渣过程的动态控制模型
宋海鹰1, 2,桂卫华1,阳春华1,王雅琳1
(1. 中南大学 信息科学与工程学院,湖南 长沙,410083;
2. 广东技术师范学院 自动化学院,广东 广州,510635)
摘 要:为了对Peirce-Smith(PS)转炉造渣过程进行优化控制,基于冶金反应动力学建立造渣过程的动态控制模型。该动态控制模型为1组具有12个状态变量的多输入多输出常微分方程组。采用现场生产数据对建立的动态控制模型进行仿真实验,并与检验数据进行对比。仿真结果表明:该动态模型计算准确,其中模型的组分Fe3O4计算值平均相对误差为1.7%,铜锍热力学温度的最大绝对误差低于5 K;该模型可用于造渣过程的优化控制。
关键词:PS转炉铜锍吹炼;动态模型;机理模型
中图分类号:TF355.2 文献标识码:A 文章编号:1672-7207(2009)04-1028-07
Dynamic controlling model for slag making process of PS converter
SONG Hai-ying1, 2, GUI Wei-hua1, YANG Chun-hua1, WANG Ya-lin1
(1. School of Information Science and Engineering, Central South University, Changsha 410083, China;
2. College of Automation, Guangdong Polytechnic Normal University, Guangzhou 510635, China)
Abstract: In order to optimize and control the slag making process of Peirce-Smith(PS) converter, the dynamic control model based on metallurgy reaction kinetic was established. This dynamic control model includes 12 state variables, and can be set up by a group of multi-input and multi-output ordinary differential equations. Simulation experiment of this dynamic model was carried out using the practical production data from a copper plant and compared with test data. The results show that the dynamic model computes accurately. The average relative error of components Fe3O4 computed by the model is 1.7%, and the maximum absolute error of matte temperature is lower than 5 K. The dynamic model can be used in the optimization and control of the slag making process.
Key words: PS converter matte converting; dynamic model; mechanism model
Peirce-Smith(PS)转炉铜锍吹炼过程为间歇式熔池反应过程,是一个具有非线性、强耦合的非封闭系统。目前,吹炼过程的操作由工人依据自身经验进行,导致生产中工艺指标波动较大,难以保证吹炼过程的优化运行,因此,研究铜锍吹炼过程的动态优化控制方法,对于实现铜锍吹炼过程的节能降耗、提高生产过程的技术经济指标具有重大意义,而建立描述反应过程的动态数学模型,是实施动态优化控制的基础[1-2]。目前,国内外已有的关于铜锍吹炼的数学模型,均是基于热力学原理的静态平衡计算模型。其中:Goto[3-4]基于Brinkly平衡计算方法建立了多相多组分平衡计算模型;在此基础上,Tan等[5]开发了用于铜锍熔炼和吹炼的热力学计算程序;Chen等[6]基于吉布斯自由能最小热力学平衡计算方法计算了6个炉次的造渣期和造铜期内渣成分及铜锍的温度变化;Degterov等[7-8]则利用FACT软件的计算包,计算了铜锍反应中的热力学数据库。此外,Chaubal等[9-10]基于反应进度计算方法,模拟了铜锍去除杂质的过程。在引入动力学传质系数后,Kyllo等[11-12]基于Goto模型开发了一个考虑传质过程的PS转炉计算模型。这些基于物、热平衡计算的静态数学模型需要通过复杂的迭代计算方法求解,从而导致这些模型难以适用于铜锍吹炼过程的优化控制。为准确描述铜锍组分和温度的时变过程,本文作者根据冶金反应动力学原理,建立铜锍吹炼造渣过程的动态数学模型。
1 铜锍吹炼过程
吹炼过程通常在卧式PS转炉内进行,化学反应在激烈搅动着的熔体和气体中进行。依靠硫化物的氧化放热,维持作业温度为1 200~1 300 ℃。鼓入转炉的气体一般为浓度不太高的富氧空气。吹炼过程分为2个阶段:第1阶段,是使铜锍中的铁氧化造渣,故称为造渣期;第2阶段,Cu2S氧化成粗铜,故称为造铜期。其中,造渣过程是决定产品质量的关键工序。
在造渣过程中,为使FeS顺利地形成硅酸铁炉渣,需加入石英熔剂(SiO2)。同时,从风口向炉内熔体中鼓入富氧空气。通过空气搅拌,在造渣过程中,FeS首先被氧化生成氧化物FeO和SO2。其中,FeO立即熔解于熔体内,随着熔体的翻腾,由密度低而浮在熔池表面的SiO2进行造渣。氧化反应和造渣反应所产生的热是造渣期的主要热量来源。
在铜锍吹炼中,为平衡吹炼产生的大量剩余热,需要不断地加入冷料。由于造渣期和造铜期吹炼的目的不同,故所加的冷料种类也不同。其中,造渣期的冷料为含铁的低铜冷料,主要是床下物和锢铍。其中,床下物将随同铜锍于吹炼开始前由包子吊车从转炉口以直投方式投入转炉,而锢铍在吹炼过程中连续加入。
2 吹炼造渣期的动态控制模型
杭家栋等[13-14]针对铜锍吹炼过程进行了大量宏观反应动力学研究,认为FeS的脱硫速率随着空气中氧浓度的增加而增加,也随着空气流速的增加而增加,但是,当温度增加时,氧化速度的增加程度不明显。杭家栋等[13-14]给出了氧化反应的反应系数和反应级数,还对Fe3O4-FeS-FeO-SiO2反应体系中造渣反应和还原反应进行了动力学研究,确定了其反应级数和反应系数。这些研究成果是建立铜锍吹炼过程动态控制模型的基础。
2.1 造渣期中的化学反应
铜锍吹炼造渣期的主要反应有4个,即:

造渣期中,铜锍反应体系的组分和温度都由上述4个化学反应共同决定,因此,可根据反应(1)~(4)的耦合关系,建立描述造渣期过程的反应动力学模型。
2.2 动态模型
仿真实验结果表明,在吹炼过程中,转炉内反应体系的体积变化相对于转炉中物料总体积较小,因此,可近似认为转炉内物料的总体积基本不变,PS转炉反应系统可近似为恒容系统;另一方面,假设在吹炼过程中,反应体系中的铜锍相和渣相在鼓入富氧的作用下相互混合。
基于上述分析,将铜锍组分浓度和铜锍温度都作为动态控制模型中的状态变量。此外,由于添加进转炉的冷料和熔剂无法立即反应,因此,将转炉中冷料和熔剂的质量也设置为状态变量。由于冷料的添加方式不同,为准确描述冷料变化情况,分别对炉口直投的冷料和通过给料装置连续添加的冷料定义了不同的状态变量。动态控制模型中的决策变量包括鼓风量、熔剂添加量、冷料添加量以及排风速率。
针对造渣期过程,建立一组具有12个状态变量、4个操作变量的多输入-多输出的动态控制模型。该模型由12个常微分方程(ODE)组成,其中各变量的定义如下:x1为转炉中直投固体冷料的质量,kg;x2为转炉中连续投放固体冷料的质量,kg;x3为铜锍熔体中Cu2S的浓度,kmol/m3;x4为熔体中FeS的浓度,kmol/m3;x5为熔体中FeO的浓度,kmol/m3;x6为熔体中2FeO?SiO2的浓度,kmol/m3;x7为熔体中Fe3O4的浓度,kmol/m3;x8为反应产生的SO2的质量,kg;x9为反应产生的N2质量,kg;x10为转炉中熔剂的质量,kg;x11为熔体的热力学温度,K;x12为直投冷料的热力学温度,K;u1为鼓入富氧的流速,m3/min;u2为添加的SiO2熔剂的流速,kg/min;u3为炉气的排出流速,kg/min;u4为连投固体冷料的操作速率,kg/min。
2.2.1 固体冷料的质量变化
固体冷料的质量变化速率与从高温熔体传到固体冷料的传热速率成正比,与高温熔体和固体冷料的温度差成正比,冷料熔化时,接受熔化潜热以及温差造成的传递热。
a. 直投冷料的质量变化。通常,从炉口直投的添加冷料随着入炉铜锍一起添加进转炉。直投冷料的平均传热系数kther1=0.2 kW/(K?m2),冷料的平均接触面系数karea1≈0.05 m2/kg。因此,直投冷料的熔化速率可定义为:

b. 连续投放冷料的质量变化。造渣期所加入的锢铍,其成分与低品位铜锍近似,平均传热系数为kther2=0.06 kW/(K?m2),冷料的平均接触面系数约为karea2=0.31 m2/kg。
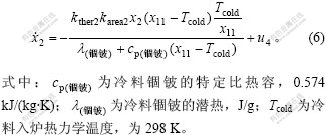
2.2.2 硫化亚铜的浓度变化
在造渣期中,铜锍中的硫化亚铜不参加化学反应,因此,随着冷料熔化进入转炉的Cu2S是影响转炉中硫化亚铜浓度变化的原因。

2.2.3 硫化亚铁的浓度变化
影响转炉中硫化亚铁浓度变化的因素有冷料熔化后进入转炉的FeS和硫化亚铁的氧化。
a. 硫化亚铁氧化。杭家栋等[13]通过实验方法确定了铜锍吹炼中高品位铜锍(含Cu 70%)中FeS的脱硫 速率:

由式(8)可知,FeS氧化反应的活化能较小,表明反应速度很快,受温度影响比较小。杭家栋等[13]进一步建立了FeS氧化脱硫速率与空气流速率间的关系(当气流速率小于210 cm3/min时):

而在实际生产中,铜品位一般为50%~60%。莫鼎成[15]认为,铁和硫的氧化速度与其在反应体系中的浓度有关,反应级数一般等于1。基于上述分析,本文依据式(9)建立硫化亚铁氧化反应动力学方程,即

b. 硫化亚铁被Fe3O4还原的速率。杭家栋等[13]认为,当铜硫反应体系中Fe3O4未饱和时,反应(4)的反应速率为:
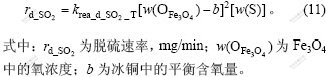
当温度为1 200~1 300 ℃时,反应(4)的反应速率常数为[14]:
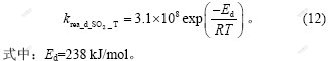
基于上述研究,建立反应(4)的动力学方程:

c. 添加的冷料对硫化亚铁的影响。

由式(10),(13)和(14)可建立硫化亚铁的浓度变化计算公式:
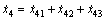 。 (15)
。 (15)
2.2.4 氧化亚铁的浓度变化
影响氧化亚铁浓度变化的因素有4种:硫化亚铁氧化生成的氧化亚铁;氧化亚铁造渣时消耗的量;氧化亚铁被进一步氧化生成Fe3O4所消耗的量。同时,还有部分Fe3O4被FeS还原生成的FeO。
a. 由硫化亚铁氧化生成的氧化亚铁。由反应(1)产生的氧化亚铁量,可根据式(10)得出:
 。 (16)
。 (16)
b. 氧化亚铁造渣消耗的量。华一新等[14]认为,在1 000~1 300 ℃时,SiO2除了一部分与FeO生成硅酸盐熔体外,未反应的SiO2将以固态存在。因此,造渣反应(2)为液-固反应,并且该反应是关于FeO浓度的一级不可逆反应,其动力学方程为:

当温度为1 150~1 300 ℃时,
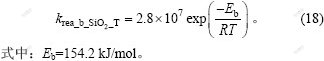
因此,氧化亚铁造渣速率可基于式(17)和(18)建立:
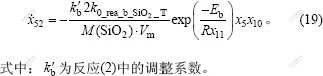
c. 氧化亚铁氧化生成Fe3O4的速率。对于反应(3),莫鼎成[15]认为,Fe2+反应速度是其浓度的一级反应,并给定了其反应常数:
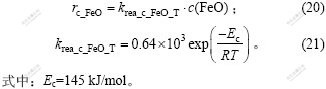
因此,由反应(3)所消耗的氧化亚铁的量,可基于式(20)和(21)建立如下:

d. Fe3O4被FeS还原生成的FeO。由反应(4)所产生的氧化亚铁量,可基于式(14)推算得到:
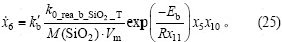
由式(16),(19),(22)和(23)可建立硫化亚铁的浓度变化计算公式:
 。 (24)
。 (24)
2.2.5 2FeO?SiO2的浓度变化率
依据式(20)可得到2FeO?SiO2的浓度变化速率:
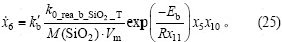
2.2.6 Fe3O4的浓度变化率
依据式(22)和(23),可得Fe3O4的浓度变化速率:
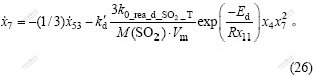
2.2.7 炉气中SO2的质量变化率
炉气中的SO2由3个因素决定,即:FeS的氧化和Fe3O4的还原所产生的SO2,以及由排气系统排出的SO2。而炉气排出流速是决定排气能力的惟一影响因素。
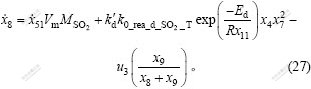
2.2.8 炉气中N2的质量变化率
炉气中的N2由3个因素决定,即:随喷入富氧带进的N2;进入转炉的外界空气中的N2;由排气系统排出的N2。其中,炉气排出流速是决定排气能力的唯一影响因素。
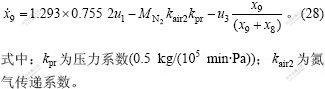
2.2.9 转炉内熔剂的质量变化率
连续投入的熔剂量和造渣所消耗的熔剂量是影响熔剂质量变化的原因。
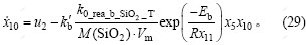
2.2.10 吹炼过程中产生和损失的热能
吹炼中的化学反应是在定压下,当若干物质相混合时发生的。而定压过程所吸收的热等于焓的增量。建模时,只考虑上述化学反应所涉及物质在1 200 ℃左右时的自由焓,化学反应产生的化学能可通过纯物质相对焓差计算得到。而各物质的相对生成焓(J/mol)可根据无机物物性手册[16]查得。再通过化学反应当量关系,得到转炉吹炼造渣期内各种化学反应热的计算公式。
a. 对于反应(1),有:
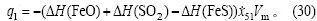
b. 对于反应(2),有:

c. 对于反应(3),有:
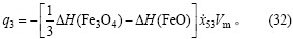
d. 对于反应(4),有:
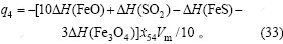
e. 加热、熔化固体冷料时的热损失为:
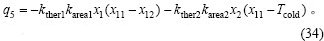
f. 由漏入炉中的空气造成的热损失为:
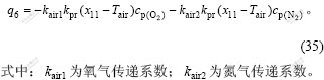
g. 由鼓风系统造成的热损失为:
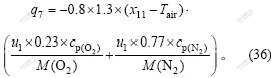
h. 由水冷墙热辐射造成的热损失为:

式中:ε为炉体黑度(0.8);S为炉体表面积(对应直径为4 m、长度为9 m的PS铜转炉,其表面积约为140 m2)。
根据上述计算,可得到吹炼过程产生的总热能qt:
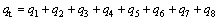 。 (38)
。 (38)
2.2.11 熔体的温度变化
影响熔体温度的因素是吹炼过程中产生和消耗的能量qt,因此,熔体的温度变化速率为总热能除以铜锍和渣的比摩尔定压热容(此处假设渣和铜锍的温度相同)与熔体中各物质的量之积。
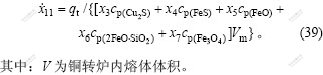
2.2.12 直投冷料的温度
直投冷料温度为
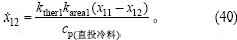
3 动态控制模型的仿真实验及结果分析
利用4号转炉第33炉次的生产操作数据对建立的动态控制模型进行仿真实验,入炉铜锍、底渣和冷料的组分数据见表1。
表1 每100 g入炉物料中各组分的平均物质的量
Table 1 Average molar quantities of components in 100 g
materials entering PS converter mol
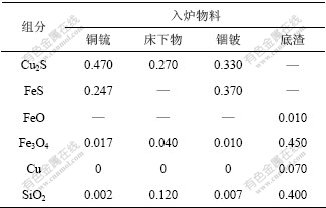
注:铜锍、床下物、锢铍、底渣的参考入炉温度分别为1 423,298,298和1 400 K。
对吹炼造渣S1期(即第1个鼓风吹炼将铜锍中的铁、硫杂质氧化脱杂)进行仿真计算,各入炉物料参数如下:底渣质量约6.2 t;加入含铜60%的铜锍质量为130 t,入炉铜锍热力学温度为1 423 K;所需冷料总量如下:床下物11.6 t,锢铍3.78 t;而所需熔剂总量8.82 t。另外,出渣量为50 t,渣中SiO2含量为21.92%,吹炼57 min。
依据熔剂、冷料的添加总量和吹炼时间可算得熔剂和冷料的平均给料率,其中熔剂给料率为154 kg/min,连投冷料给料率为66 kg/min;另外,在仿真实验中,富氧空气(含氧23%)的供风速率为560 m3/min,而排风速率设定为400 kg/min。
由于吹炼开始前,转炉内残留着上炉的底渣,因此,仿真计算时将底渣中的Fe3O4和FeO均作为状态初始值进行考虑。S1期组分浓度的仿真计算结果如图1所示。
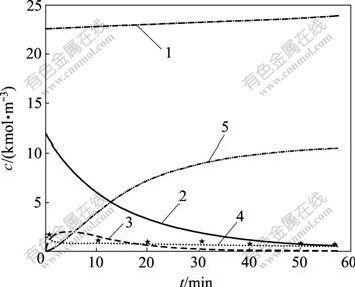
1―Cu2S; 2―FeS; 3―FeO; 4―Fe3O4;
5―2FeO?SiO2; ★―Fe3O4
图1 S1期组分浓度变化
Fig.1 Variation concentration of components at stage S1
由图1可知,在吹炼过程中,随着冷料的连续加入,熔体中Cu2S的量逐步增加。由于造渣过程中Cu2S不发生氧化反应,因此,Cu2S含量只增加不减少。随着氧化反应的进行,FeS几乎呈线性速率进行氧化反应,这使得FeS氧化产生的FeO在开始吹炼后迅速增加。但随着造渣反应的进行,FeO将不断地被造渣成2FeO?SiO2,同时,其中部分FeO不可避免地被过氧化为Fe3O4,Fe3O4的摩尔浓度约为2.2 kmol/m3,约占总渣量的22.3%(摩尔分数)。而实际化验结果中,渣中Fe3O4约占总渣量的21.2%(摩尔分数),可见,运用该模型所得计算结果准确。
铜锍热力学温度随时间的变化见图2。由图2可见,造渣期动力学模型计算的铜锍温度的最大绝对误差为4.8 K。在吹炼过程的初始阶段,温度略有下降。这是因为,开吹初始阶段氧化反应所产的自热还不够多,但随着反应的进行,铜锍温度迅速上升。但由于较好地控制了冷料量和富氧气体鼓风速率,在整个吹炼过程中,铜锍温度均保持在正常范围内。对4号转炉其他一些炉次进行仿真计算,仿真结果见表2,其中:Mc为冰铜加入质量,t;x为冰铜品位,%,y1为实际出渣质量,t;y2为渣量计算值,t;z1为渣中Fe3O4含量的实际值,%;z2为渣中Fe3O4含量的计算值,%。
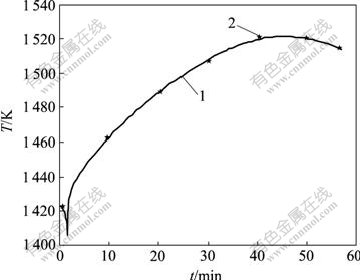
1―温度计算值;2―温度实测值
图2 铜锍温度随时间的变化
Fig.2 Relationship between matte temperature and time
表2 仿真结果与生产数据比较
Table 2 Comparison of simulation results and
production data
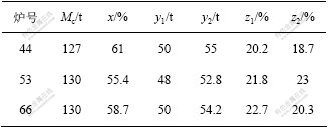
由表2可知,因为出渣时进行了压渣操作,部分炉渣将保留在转炉内,使得出渣量计算值与实际值有一定误差。与实际检测数据相比,渣中Fe3O4含量的平均相对误差为1.7%,由此可见,本文所建立的反应动力学模型可以有效地用于描述吹炼过程中组分和温度的动态变化过程。
4 结 论
a. 针对铜锍吹炼过程,经过合理简化,建立了造渣期的动态控制模型。
b. 仿真结果表明,该非线性动力学模型能准确描述吹炼过程中铜锍组分和温度的动态变化情况,其中,反映渣品质的渣中Fe3O4含量的计算值平均相对误差低于2%,而铜锍温度的最大绝对误差低于5 K。由此可见,建立的动态模型可用于PS转炉铜锍吹炼过程的动态优化控制。
参考文献:
[1] 吴 敏, 雷 琪, 曹卫华. 基于多工况分析的焦炉加热过程火道温度模糊控制[J]. 中南大学学报: 自然科学版, 2008, 39(1): 155-161.
WU Min, LEI Qi, CAO Wei-hua. Flue temperature fuzzy control for coke oven heating process based on multi-operative modes analysis[J]. Journal of Central South University: Science and Technology, 2008, 39(1): 155-161.
[2] 宋海鹰, 桂卫华, 阳春华. 基于核偏最小二乘法的动态预测模型在铜转炉吹炼中的应用[J]. 中国有色金属学报, 2007, 17(7): 1201-1206.
SONG Hai-ying, GUI Wei-hua, YANG Chun-hua. Application of dynamical prediction model based on kernel partial least squares for copper converting[J]. The Chinese Journal of Nonferrous Metals, 2007, 17(7): 1201-1206.
[3] Goto S. Equilibrium calculations between matte,slag and gaseous phases in copper smelting[C]//Proceedings of Copper Metallurgy Practice and Theory. Jones M J, eds. London: Institute of Mining and Metallurgy, 1975: 23-24.
[4] Goto S. The Application of Thermodynamic Calculations to Converter Practice[C]//Proceedings of Copper and Nickel Converters. Johnson R E, eds. The Metallurgical Society of AIME, 1979: 33-55.
[5] TAN Peng-fu. CuModel―A thermodynamic model and computer program of copper smelting and converting processes and its industrial applications[C]//Proceedings of the TMS Fall Extraction and Processing Conference. Charlotte, United States, 2004: 411-422.
[6] CHEN Chun-lin, ZHANG Jia-yun, ZHOU Tu-ping, et al. Thermodynamic study on process in copper converters (the slag-making stage)[J]. Journal of University of Science and Technology Beijing: Mineral Metallurgy Materials (Eng Ed), 1999, 6(3): 187-192.
[7] Degterov S A, Pelton A D. Thermodynamic modeling of lead distribution among matte, slag, and liquid copper[J]. Metallurgical and Materials Transactions B, 1999, 30(6): 1033-1044.
[8] Degterov S A, Dessureault Y, Pelton A D. Thermodynamic modeling of zinc distribution among matte, slag and liquid copper[J]. Canadian Metallurgical Quarterly, 2000, 39(1): 43-54.
[9] Chaubal P C, Nagamori M, Sohn H Y. Volatilization and slagging of lead in copper matte converting: computer simulation[J].Canadian Metallurgical Quarterly, 1984, 23( 4): 405-411.
[10] Chaubal P C, Nagamori M. Volatilization of arsenic and antimony in copper matte converting[J]. Metallurgical Transactions B: Process Metallurgy, 1983, 14B(2): 303-306.
[11] Kyllo A K, Richards G G. A kinetic model of the Peirce-Smith converter: Part Ⅰ. Model formulation and validation[J]. Metallurgical and Materials Transactions, 1998, 29B(1): 239-250.
[12] Kyllo A K, Richards G G. A kinetic model of the Peirce-Smith converter: Part Ⅱ. Model application and discussion[J]. Metallurgical and Materials Transactions, 1998, 29B(1): 251-259.
[13] 杭家栋, 刘纯鹏. 高品位锍吹炼动力学的研究[J]. 有色金属, 1989, 41(1): 42-48.
HANG Jia-dong, LIU Chun-peng. An investigation on converting high grade Cu-Fe matte in a molten state[J]. Nonferrous Metals, 1989, 41(1): 42-48.
[14] 华一新, 刘纯鹏. Fe3O4-(xFeS・yCu2S)-FeO-SiO2体系的反应动力学[J]. 金属学报, 1986, 22(6): A540-A542.
HUA Yi-xin, LIU Chun-pen. The reduction kinetics of Fe3O4-(xFeS・yCu2S)-FeO-SiO2 system[J]. Acta Metallurgica Sinica, 1986, 22(6): A540-A542.
[15] 莫鼎成. 冶金动力学[M]. 长沙: 中南工业大学出版社, 2004.
MO Ding-cheng. Metallurgy kinetics[M]. Changsha: Press of Central South University of Technology, 2004.
[16] 叶大伦, 胡建华. 实用无机物热力学数据手册[M]. 北京: 冶金工业出版社, 2002.
YE Da-lun, HU Jian-hua. Practical inorganic thermodynamics data book[M]. Beijing: Metallurgical Industry Press, 2002.
收稿日期:2008-08-29;修回日期:2008-11-28
基金项目:国家“973”计划项目(2002CB312200);国家自然科学基金资助项目(60634020,60574030)
通信作者:宋海鹰(1975-),男,江苏泰州人,博士,讲师,从事工业过程建模、优化与控制研究;电话:0731-88830394;E-mail: songhaiying1975@163.com