���±�ţ�1004-0609(2007)07-1213-06
ˮ��ʯǰ�����Ʊ���Al-Li������������Ĥ������
Ҷ 𩣬����ԣ��� �����ܽ�ƽ���Ծ�ï
(����������ѧ ���Ͽ�ѧ�빤��ѧԺ������ 100029)
ժ Ҫ������ˮ��ʯǰ�����ڸߴ�����������LiԪ�أ�Ȼ��ͨ�����������ڸߴ��������Ʊ�Al-Li������������Ĥ������XPS��XRD��SEM�����������绯ѧ�迹�����о�����Ĥ�����ܡ����������ͨ��ˮ��ʯǰ�������Ʊ�Al-Li������������Ĥ��Ĥ��Li �����ɴ�8%���봿������Ĥ��ȣ���������Ĥ�������ܣ������Ƿ��գ�Al-Li��������Ĥ������NaCl��Һ�е���ʴ�Զ��ϴ�������Ĥ���á�
�ؼ��ʣ�ﮣ�ˮ��ʯ����������Ĥ��������ʴ
��ͼ����ţ�TB 33; TG 146.21; TG 172���� ���ױ�ʶ�룺A
Properties of Al-Li anodic films by hydrotalcite precursor method
YE Hao, ZHAO Xu-hui, ZUO Yu, XIONG Jin-ping, ZHAO Jing-mao
(Faculty of Materials Science and Engineering, Beijing University of Chemical Technology, Beijing 100029, China)
Abstract: Lithium element was introduced into high purity aluminum by a hydrotalcite precursor method, and an amorphous Al-Li composite anodic film was obtained by anodizing. The methods of XPS, XRD, SEM, potentiodynamic polarization and electrochemical impedance spectroscopy (EIS) were used to investigate the properties of the films. The results show that a composite Al-Li anodic film is obtained by the method, and Li content in the film is up to 8%. The composite film is more compact than the anodic film on pure aluminum. No matter sealing or not, in NaCl solution, the composite anodic film shows higher corrosion resistance than the anodic film on pure aluminum.
Key words: lithium; hydrotalcite; anodic film; aluminum; corrosion
������Ͻ����������Ĥ��һ��ϱ����赲��ͽϺ�Ķ�ײ㹹�ɣ����ж���ԡ���Ӳ�ȡ�����ʴ�Ժ;�Ե�Ե����ܣ���������������Ͻ����;��Ϊ�˽�һ����������Ĥ����ʴ����ѧ�����ܣ��Ͻ�Ԫ�س����������Ե���Ĥ����ɺͽṹ[1-2]���Ʊ�������������Ĥ�������������Ƿ�չ�˶��ֲ�ͬ���������Ͻ�����Լ�����Ĥ����������Ԫ�أ��磺�ڵ��Һ�м������Ƽ�[3]������Mo��Zr��Ta��Nb�Ȼ�÷Ǿ�̬�Ͻ����[4-6]�����������[7-8]������ע��Ti��Ni��[ 9-10 ]��ͨ����������Ĥ�ķ�մ�������Ce��Mo��[11 ]��
Li�����Ͻ���һ����Ҫ����ǿԪ��[12]������ǰ�˵��о�����Al-Li�Ͻ�����������У��Ͻ��й������е��ԭ�����������γɵķǾ�̬������Ĥ��ϣ����Ʋ�Li+����Ǩ���ٶȱ�Al3+��[13]��Skeldon��[14]�о���Al-Li�Ͻ�����Ĥ�Ľ��ǿ�����ܡ�McCafferty[4]�о��˼��ֲ�ͬԪ�ض�����0.1 mol/L NaCl��Һ�п�ʴ��λ��Ӱ�죬�����������棬Li�����뽵���˿�ʴ��λ����ָ��Zr��Ta��Si������(���ǵ�������ĵȵ�λ�����Al2O3��)���뽫��������Ĥ�����ԣ����¿�ʴ��λ���ߡ��෴��Zn��Li������(���ǵ�������ĵȵ�λ�����Al2O3��)�����뵼�¿�ʴ��λ���͡���Щ�о���Ҫ�����Al-Li�Ͻ𣬶�Al-Li������������Ĥ�ĵ绯ѧ�����о����١�
��������ͨ��ˮ��ʯǰ�����ڸߴ�����������LiԪ�ؽ��������Ͻ�����Ʊ�Li/Al������������Ĥ�������õ绯ѧ���Լ���(EIS)�ͱ�������ֶ�(XRD, SEM��XPS)�о�Al-Li������������Ĥ�����ܼ�LiԪ�ص��������������Ĥ�۽ṹ��Ӱ�졣
1��ʵ��
1.1�������Ʊ�
ʵ�����Ϊ�ߴ���(99.999%), �����ߴ�Ϊ25 mm��10 mm��0.5 mm�����ȣ��������������ò�ͬ�ȼ���SiCˮɰֽ��ĥ(800#)��ȥ����ˮ��ϴ����ͪ��֬�����ţ���50 g/L NaOH ��Һ�����³���3 min��ȥ����ˮ��ϴ������200 g/L HNO3�����³���1 min��ȥ����ˮƯϴ����紵�ɣ�Ȼ����363 K����0.1 mol/L Li2SO4 (pH=11.00)��Һ�У����ݲ�ͬʱ�䣬��ȡ���ڸ����������·���24 h���������������������������������������Ϊ2 A/dm2(������ѹΪ25~30 V)������ҺΪ200 g/L H2SO4 (98%)+20 g/L C2O4H2.2H2O+��15 g/L C3H5(OH)3�������¶�291 K������ʱ��60 min������Ĥ���Լ 30 ��m��Ϊ�˱Ƚϣ���δ��Li2SO4 (pH=11.00)��Һ�н��ݵĸߴ���������ͬ�������½�������������
1.2 ���ܲ���
���ô�ͳ���缫��ϵ���Լ������ߺͽ����迹������Ĥ����Ϊ�����缫(��¶���Լ0.5 cm2)�����ʹ��缫Ϊ�αȵ缫�����缫Ϊ�����缫����������Ϊ273 A ���λ�Ǽ�5210����Ŵ�����������ҺΪ������1 mol/L NaCl (pH7), �����¶�Ϊ(293��2) K�������迹����Ƶ�ʷ�ΧΪ100 kHz~0.01 Hz, �����źŷ�ֵ����10 mV���������߲���ɨ������Ϊ 0.66 mV/s��
��XRD����Ĥ�Ľṹ�;��Σ���XPS(MICROLAB MK��)����Ĥ�ı���ɷ֣��ó�����SEM�۲�����Ĥ����ò��
2 ���������
2.1 XRD����
ͼ1��ʾΪ�ߴ���������0.1 mol/L Li2SO4��(pH =11.00���¶�368 K)����96 h������XRD�ס���ͼ1���Կ�������XRD���г���������Li-Al��״˫�ǻ��������ࣨLHD����������[15]�����������������γ���Li-Al LDH��ͼ2��ʾΪ��Li2SO4��Һ�н��ݺ��پ��������������������������XRD�ס���ͼ2���Կ���������Ĥ�ʷǾ�̬����˵��Li�����벢δ�ı�����Ĥ�ķǾ�̬�ṹ��
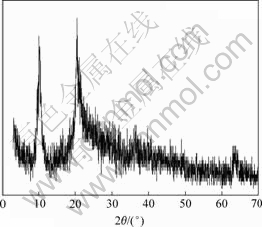
ͼ1����0.1 mol/L Li2SO4��(pH=11.00)����96 h (T=363 K)��ߴ������������XRD��
Fig.1 XRD pattern of surface of aluminum immersed in ��0.1 mol/L Li2SO4 (pH = 11.00) at 363 K for 96 h
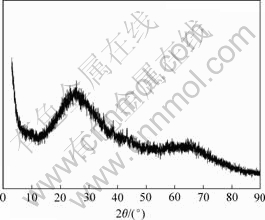
ͼ2 �ߴ�����0.1 mol/L Li2SO4��(pH=11.00)����96 h��(T=363 K)�������������������������XRD��
Fig.2 XRD pattern of surface of aluminum immersed in 0.1 mol/L Li2SO4 (pH = 11.00) at 363 K for 96 h and then anodized at constant current density of 2 A dm-2 at 291 K for 60 min
2.2��XPS����
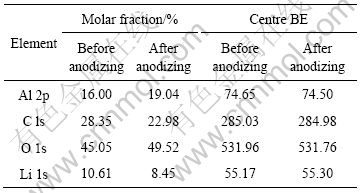
ͼ3��ͼ4��ʾ�ֱ�Ϊ���ߴ���������Li2SO4��Һ�н��ݺ�δ�����������������������������XPSͼ�ס������Ƿ�������Li ��������XPSͼ�ж������ɼ�����1����Ϊ���治ͬԪ�صĺ����ͽ���ܡ���������ǰ������Li-Al LDH���γɣ�Liԭ���ڱ��溬��Լ10%������������������Լ8% Li�����������������Ĥ���Դ��ڴ�����LiԪ�ء�
�ӱ�1���Կ�������������ǰ��Li�ڱ���Ľ���ֱܷ�Ϊ 55.17 eV��55.3 eV��Li+��LiOH�н����Ϊ 54.8~55.2 eV������Li2O�н����Ϊ55.3~55.7 eV[16]����˵����������ǰLi�������LiOH��ʽ���ڣ������������������Ҫ��Li2O��ʽ���ڣ��γ���Al-Li�ĸ���
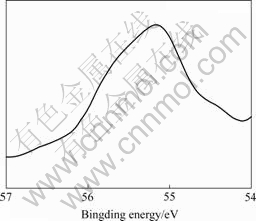
ͼ3 ��0.1 mol/L Li2SO4 (pH=11.00)��Һ�н���96 h (T=363 K)��δ�������������ĸߴ������������XPSͼ
Fig.3 X-ray photoelectron spectroscopy of Li element on surface of aluminum immersed in 0.1mol/ L Li2SO4 (pH=11.00) at 363 K for 2 h
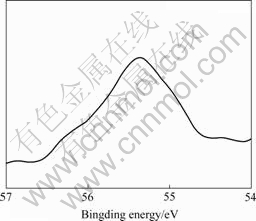
ͼ4 ��0.1 mol/L Li2SO4(pH=11)��Һ�н���96 h(T=363 K)�����������������ĸߴ������������XPSͼ��
Fig.4 X-ray photoelectron spectroscopy of Li element on surface of aluminum immersed in 0.1mol /L Li2SO4 (pH=11.00) at 363 K for 2 h and then anodized at constant current density of 2 A dm-2 at 291 K for 60 min
����Ĥ��
ͼ5��ʾΪ��������Ĥ������ͬʱ�佦���LiԪ�ص�XPSͼ����ͬ����ʱ�������Ĥ��LiԪ�صĺ������2��ʾ��LiԪ��������Ĥ�еĺ����潦��ʱ����ӳ������͡�������30 min�����Ĥ��LiԪ�غ�����Լ��4%����˵��LiԪ�ش���������Ĥ��һ����ȷ�Χ�ڣ�������Ĥ�����Li�����ϸߡ����ܵ�ԭ���ǣ����������������У�����Al3+��O2-Эͬ�������ã�����Ĥͬʱ��Ĥ/���Һ�ͽ���/Ĥ��������[17]����Li+��O����(146 kJ/mol)����Al3+��O����(281 kJ/mol)��Li+��Ǩ���ٶȽ�Al3+��[13,��18]��
��1 ��������XPS�������
Table 1 Surface analysis results by XPS
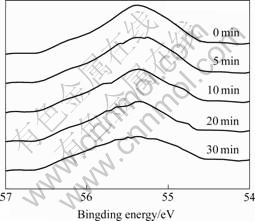
ͼ5 ��ͬʱ�佦�����������LiԪ�ص�XPSͼ
Fig.5 X-ray photoelectron spectroscopy of Li element on surface of anodic aluminum after different sputtering time
��2 �������澭��ͬʱ�佦���LiԪ�صĺ���
Table 2 Li content on surface of anodic film with different sputtering time

2.3 SEM����Ӳ�ȷ���
ͼ6(a)��ʾΪδ����LiԪ����������Ĥ��SEM����ͼ�ɼ���Ĥ����Ĥ���洹ֱ�������ϳ���������������У��ױں������൱����Լ50 nm��ͼ6(b)��ʾΪ����LiԪ�غ���������Ĥ��SEM����ͼ�ɼ��� LiԪ�����������Ĥ���������ò�нϴ�ı仯������С���ҿ��ܶȽ��ͣ�Al-Li����Ĥ��������ܡ�

ͼ6 ��������Ĥ���������SEM��
Fig.6 SEM image of anodic film surface: (a) Without Li introduction; (b) With Li introduction
ͼ7��ʾΪ������ͬ����ʱ�������Ĥ�����������Ӳ�ȡ���ͼ7��֪��Al-Li��������Ĥ�������Ӳ�����Ը���δ����Li�Ĵ�����������Ĥ�������Ӳ�ȣ�����Ӳ�ȶ�������ʱ����ӳ�������
 2.4 �������߲���
2.4 �������߲���
ͼ8��ʾΪδ��մ���������Ĥ����������NaCl (1 mol/L)��Һ�еļ������ߡ�ͼ9��ʾΪ��ˮ��մ���������Ĥ����������NaCl (1 mol/L)��Һ�еļ������ߡ���ͼ8��ͼ9�п��Կ����������Ƿ��մ�����Al-Li
��������Ĥ������NaCl��Һ�еĶۻ��������ǽϵ�
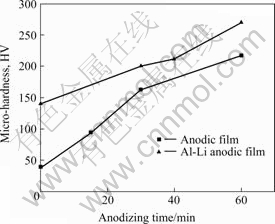
ͼ7 ����Ĥ�����������Ӳ��������ʱ��ı仯
Fig.7 Micro-hardness of anodic film at 2A/dm2 anodic current density for different anodizing time
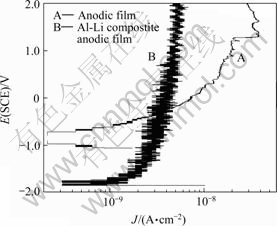
ͼ8 δ��մ�������������Ĥ����������1 mol/L NaCl��Һ�еļ�������
Fig.8 Polarization curves of anodic samples without sealing in neutral 1 mol/L NaCl solution
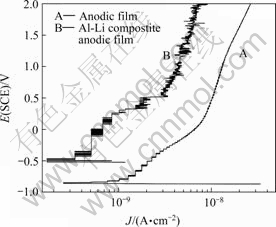
ͼ9 ��ˮ��մ�������������Ĥ����������1mol/L NaCl��Һ�м�������
Fig.9 Potentiodynamic polarization curves of anodic samples with boiling water sealing for 30 min in neutral 1 mol/L NaCl solution
�ģ�����LiԪ�ص����������Ĥ����ʴ�ԡ�
2.5 EIS����
ͼ10��ʾΪδ���з�մ���������Ĥ����������1 mol/L NaCl��Һ�еĽ����迹�ס���ͼ10�п��Կ������ڲ���Ƶ�ʷ�Χ�ڶ�ֻ��ʾ��һ��б��ֱ�ߡ�����δ��յ�����Ĥ��˵�����ڸߵ����Եĵ������Һ��������Ĥ���ڣ���ײ㲻�ܱ����������迹������Ҫ��ӳ�赲�����Ϣ[19-21]����Ƶ��Ϊ10-2 Hzʱ������LiԪ�غ��Al-Li����Ĥ�迹ģֵ|Z|ԼΪ4��107 ��?cm2, ��δ����LiԪ�ص�����Ĥ�迹ģֵ|Z|�ϵͣ�Լ9��106����?cm2����˵������Ĥ������LiԪ�غ��������赲����迹��
ͼ11��ʾΪ��մ����������Ĥ����������NaCl (1mol/L)��Һ�еĽ����迹Bodeͼ����մ�������Bodeͼ��Ƶ�����Գ�����һ��ƽ̨�����迹�ֳ�������ֱ�����������о�[19-22]�Ѿ�������Ƶ������Ҫ��ӳ�赲����Ϣ�����и�Ƶ����Ҫ��ӳ��ײ���Ϣ����ͼ11�п��Կ������ӵ�Ƶ����Ƶ�ķ�Χ�ڣ�LiԪ�������ĸ�������Ĥ�迹ģֵ|Z|����δ����LiԪ�صĴ���˵�����ڷ�պ������Ĥ��LiԪ�ص�����Ҳ�����˶�ײ��迹��
EIS�����ʾ�������Ƿ��գ�����LiԪ�غ������Ĥ���赲��Ͷ�ײ���迹��������ģ��ܸ�������Ĥ����ʴ�ԡ�������Ǹ���Al2O3-Li2O����Ĥ���γɵ�����Ĥ���ܶȵĽ��ͣ��谭�˸�ʴ�����ڶ��Ĥ�е�Ǩ�ơ����⣬Al2O3��һ��n�Ͱ뵼��Ĥ[23-24]���ϵͼ�̬��Li+���ӽ����µ���Ũ�ȵĽ��ͺ���ʴ�Ե���ߡ�Li2O�Ľϵ͵��ӵ�����[25]Ҳ�ܵ���Ĥ���迹���͡�����ǰ�漫�����߽��һ�¡�
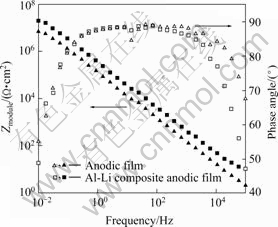
ͼ10 δ��մ�������������Ĥ����������1 mol/L NaCl��Һ�е�Bodeͼ
Fig.10 Bode plots of anodized samples without sealing in neutral 1mol/L NaCl solution
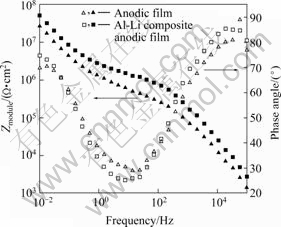
ͼ11 ��ˮ��մ�������������Ĥ����������1 mol/L NaCl��Һ�е�Bodeͼ
Fig.11 Bode plots of Al-Li composite anodic samples with water sealing in neutral 1 mol/L NaCl solution (pH 7.0)
3 ����
1) ͨ��ˮ��ʯǰ�������ڸߴ�����������LiԪ�أ�����ͨ�����������Ʊ��Ǿ�̬��Al/Li������������Ĥ��Al/Li��������Ĥ��������ܣ����ܶ����Խ��͡�
2) �绯ѧ���Խ��������Li�����룬����������Ĥ����ʴ�ԡ����۷���������������Ĥ������NaCl��Һ�ж����и��õ���ʴ�ԡ�
REFERENCES
[1] P��ez M A, Foong T M, Ni C T, Thompson G. E, Shimizu K, Habazaki H, Skeldon P, Wood G. C. Barrier-type anodic film formation on an Al-3.5wt% Cu alloy[J]. Corrosion Science, 1996, 38(1): 59-72.
[2] Brown G M, Shimizu K, Kobayashi K, Skeldon P, Thompson G E, Wood G C. The growth of a porous oxide film of a unique morphology by anodic oxidation of an Al-0.5wt% Ni alloy[J]. Corrosion Science, 1998, 40(9): 1575-1586.
[3] Tammy L M, Robert L P, Edward T K. Passivation of metal alloys using sol-gel-derived materials-a review[J]. Progress in Organic Coating, 2001, 41: 233-238.
[4] MacCafferty E. Semiconductor aspects of the passive oxide film on aluminum as modified by surface alloying[J]. Corrosion Science, 2003, 45(2): 301-308.
[5] Wolf G K. An historical perspective of ion bombardment research for corrosion studies[J]. Surface and Coating Technology, 1996, 83:1-9.
[6] Inturi R B, Szklarska-Smialowska Z. Dependence of the pitting potential of Al alloys on solubility of alloying element oxides[J]. Corrosion Science, 1993, 34(4): 705-710.
[7] Vetter J. Aluminium-titanium nitride coatings deposited by cathodic vacuum arc evaporation[J]. Metal Powder Report, 1998, 53(4): 40-41.
[8] Kulmala S, Kulmala A, Ala-Kleme T, Pihlaja J. Primary cathodic steps of electrogenerated chemiluminescence of lanthanide(��) chelates at oxide-covered aluminum electrodes in aqueous solution[J]. Analytica Chimica Acta, 1998, 367(1/3): 17-31.
[9] TIAN Lian-peng, ZUO Yu, ZHAO Xu-hui, ZHAO Jing-mao, XIONG Jin-ping .The improved corrosion resistance of anodic films on aluminum by nickel ions implantation[J]. Surface and Coatings Technology, 2006, 201(6): 3246-3256.
[10] ������, �� ��, �Ծ�ï, �ܽ�ƽ, ������, �����. Ti����ע���Al��������Ĥ���迹���ʵ�Ӱ��[J]. ����ѧ��, 2005, 41(8): 804-808.
TIAN Lian-peng, ZUO Yu, ZHAO Jing-mao, XIONG Jin-ping, ZHANG Xiao-feng, ZHAO Xu-hui. Effect of Ti ion implantation on the impedance properties of anodic oxide film on aluminum[J]. Acta Metallurgica Sinica, 2005, 41(8): 804-808.
[11] TIAN Lian-peng, ZHAO Xu-hui, ZHAO Jing-mao, ZHANG Xiao-feng, ZUO Yu. Electrochemical behaviors of anodic alumina sealed by Ce-Mo in NaCl solutions[J]. Trans Nonferrous Met Soc China, 2006, 16(5): 1178-1183
[12] Tzoganakoua K, Skeldona P, Thompsona G E, Zhou X, Kreissig U, Wieser E, Habazaki H, Shimizu K. Mobility of lithium ions in anodic alumina formed on an Al-Li alloy[J]. Corrosion Science, 2000, 42(6): 1083-1091.
[13] Lou A, Lloyd D J, Gupta A, Youdelis W V. Precipitation and dissolution kinetics in Al-Li-Cu-Mg alloy 8090[J]. Acta Metallurgica et Materialia, 1993, 41(3): 769-776.
[14] Skeldon P, Zhou X, Thompson G E. Adhesion of anodic films on aluminium-lithium alloy[J]. Corrosion, 1999, 55: 561-565.
[15] Shimizu K, Kobayashi K, Skeldon P, Thompson G E, Wood G C. An atomic force microscopy study of the corrosion and filming behavior of aluminum[J]. Corrosion Science, 1997, 39(4): 701-718.
[16] Moulder J F, Sttickle W F, Sobol P D. Hand book of X-ray photoelectron spectroscopy[M]. USA: Perkin-Elmer Corporation Physical Electronics Division, 1992.
[17] Lide D R. Handbook of physics and chemistry[M]. New York: CRC Press, 1978.
[18] Grace S T, Vishnu Kamath P. The double hydroxide of Al with Li: mechanism of formation and reversible thermal behavior[J]. Materials Research Bulletin, 2002, 37(4): 705-713.
[19] Hoar T P, Wood G C. The sealing of porous anodic oxide films on aluminum[J]. Electrochimica Acta, 1962, 7(3): 333-353.
[20] Hitzig J, J��ttner K, Lorentz W J, Paatsch W. AC-impedance measurements on porous aluminum oxide films[J]. Corrosion Science, 1984, 24(11/12): 945-952.
[21] �����, �� ��, �Ծ�ï. ����������Ĥ��NaCl��Һ�еĵ绯ѧ����[J], �й���ɫ����ѧ��, 2004, 14(4): 562-567.
ZHAO Xu-hui, ZUO Yu, ZHAO Jing-mao. Electrochemical properties of anodized aluminum in sodium chloride solution[J]. The Chinese Journal of Nonferrous Metals, 2004, 14(4): 562-567.
[22] Suay J J, Gim��nez E, Rodr��guez T, Habbib K, Saura J J. Characterization of anodized and sealed aluminum by EIS[J]. Corrosion Science, 2003, 45(3): 611-624.
[23] Bockris J O'm, Kang Y K. The protectivity of aluminum and its alloys with transition metals[J]. J Solid State Electrochem, 1997, 1(1): 17-35.
[24] Kobotiatis L, Kioupis N, Koutsoukos P G. Electronic properties of passive films grown on Al 7075 in solutions containing oxalate and chromate[J]. Corrosion, 1997, 53(7): 562-571.
[25] Varsano F, Decker F, Masetti E, Croce F. Lithium diffusion in cerium�Cvanadium mixed oxide thin films: A systematic study[J]. Electrochimica Acta, 2001, 46(13/14): 2069-2075.
(�༭������Ⱥ)
������Ŀ��������Ȼ��ѧ����������Ŀ(50571006)
�ո����ڣ�2006-09-20�������ڣ�2007-04-02
ͨѶ���ߣ����������ڣ���ʿ����ʦ����ʿ���绰��010-64423795�����棺010-64434908��E-mail: zuoy@mail.buct.edu.cn