文章编号:1004-0609(2013)10-2890-07
pH值及助剂对氢化态Mg-Mn复合物水反应性能的影响
白雪蕊1,于元春2,张文丛1
(1. 哈尔滨工业大学(威海) 材料科学与工程学院,威海 264209;
2. 哈尔滨工业大学(威海) 海洋科学与技术学院,威海 264209)
摘 要:为了提高氢化态Mg-Mn复合物的水反应性能,采用改变反应水溶液pH值和在水溶液中加入不同助剂的方法,通过测量反应过程中不同时刻产生的氢气量对助剂在水反应中的作用进行表征,利用SEM和XRD等测试手段对反应产物进行表征和测试,对反应机理进行分析。结果表明:改变反应溶液的pH值对反应程度及放氢速率的影响不大,且pH值越大,越不利于反应的进行;在溶液中添加助剂焦磷酸钾、六偏磷酸钠、羟基乙叉二膦酸(HEDP)对提高氢化态Mg-Mn复合物的放氢速率有显著促进作用;相比之下,应采用添加磷酸盐助剂的方法来改善氢化态Mg-Mn复合物水反应性能。
关键词:氢化态Mg-Mn复合物;助剂;水反应性能
中图分类号:TG139.7 文献标志码:A
Influence of pH value and additives on water reaction performance of hydrogenated Mg-Mn composites
BAI Xue-rui1, YU Yuan-chun2, ZHANG Wen-cong1
(1. School of Materials Science and Engineering, Harbin Institute of Technology at Weihai, Weihai 264209, China;
2. School of Marine Science and Technology, Harbin Institute of Technology at Weihai, Weihai 264209, China)
Abstract: In order to improve the water reaction performance of hydrogenated Mg-Mn composites, the pH value of the hydrolysis solution was changed and different additives were added in the solution. The amount of hydrogen produced by different kinds of samples was used to characterize the hydrolysis reactivity. SEM, XRD and other testing methods were used to characterize and test the hydrolysis products. The reaction mechanism was analyzed. The results show that changing the pH value of the reaction solution has a little influence on the hydrolysis rate and the reaction degree, and the higher the pH value, the more disadvantageous the reaction. The addition of additives of the potassium pyrophosphate, sodium hexametaphosphate and HEDP plays a significant role in promoting the hydrogen desorption rate. In contrast, the method of adding phosphate additives should be used to improve the water-reactive properties of the hydrogenated Mg-Mn composites.
Key words: hydrogenated Mg-Mn composites; additives; water reaction performance
氢能是21世纪一种重要的二次能源,人们对氢能源的开发利用寄予极大希望[1-3]。氢能与质子膜燃料电池进行匹配,能将化学能直接转化为电能,极具吸引力[4-6]。
近年来,金属氢化物制氢技术得到了快速发展[7]。早期采用硼氢化钠水溶液制氢,可以满足不同功率燃料电池的需要,但硼氢化钠高昂的制氢成本限制其推广和应用[8]。氢化态镁基复合物与水在低温条件下反应制氢,这种方法充分发挥了镁的大容量储氢功能(7.6%,质量分数),在低温水反应过程既放出存储的氢气,又使水中部分氢原子以氢气的形式放出,理论储氢量可达15.31%(质量分数,水循环利用)。目前,急需解决的问题是如何使MgH2水解反应能够快速、充分地完成,反应能够充分完成的前提是水反应产物Mg(OH)2的形貌发生改变,不以致密钝化膜的形式存在[9-10]。
LUKASHEV等[11]将MgH2和MgH2-石墨二元复合材料体系进行机械球磨后与水反应。研究表明,在MgH2的机械合金化过程中加入石墨可起到分散剂的作用,阻止MgH2颗粒团聚,增大反应的比表面积并提高缺陷密度,改善了反应动力学性能,但是,这种改善以提高石墨的含量为前提。GROSJEAN等[12]对Mg和MgH2基材料添加Ni元素,同样利用机械球磨制备单质Ni在基体材料中均匀分布的复合材料,水解反应过程中,两相之间形成大量的微原电池,从腐蚀的角度以期促进Mg(OH)2钝化膜的去除,虽然氢释放量有一定的提高,但没有从燃料电池工作的整个流程出发,没有充分发挥电池产物高温纯净水促进水解进程的特点,也没有考虑水解产物的回收问题。HU等[13]通过机械球磨MgH2粉末,使其由多晶转变成为纳米晶,增大了其比表面积,在一定程度上提高了MgH2与水反应初始阶段的反应速率与反应程度,但是其水反应初始阶段结束后的反应速率对于实际应用而言仍然太慢。刘冠鹏等[14]为了提高Mg的水反应活性及抗氧化性能,采用复杂气相沉积及液相沉积技术在Mg粉表面进行二次包覆处理,在一定程度上改善了上述不足,该方法制备工艺复杂,主要停留在实验室阶段。
目前,大多数研究者采用改变静态的初始条件(如镁盐种类等)来控制Mg(OH)2晶体结构和形貌,尚无改变反应pH值、加入有机助剂对其形貌规律影响的研究。实际上,在Mg(OH)2生成过程中,随着加入有机助剂的变化,镁离子和氢氧根离子的相对浓度也是不断变化的,这些是直接影响晶体成核和生长速率的关键因素。
近年来,本课题组先后开发了氢化态Mg-Ni-MnO2复合物、氢化态AZ91、氢化态Mg-Mn复合物等系列材料配方,其反应过程中表现出良好的水反应动力学性能。本文作者对氢化态Mg-Mn复合物进行实验,通过改变反应过程中溶液的pH值和在溶液中加入不同助剂来研究反应的放氢速率和放氢程度。
1 实验
1.1 主要试剂
金属镁(Mg)粉(纯度>99%,由上海试剂公司提供);高纯锰(Mn)粉(纯度>99.99%,由天津光复精细化工研究所提供);高纯氢(H2) (纯度99.999%,由山东省半导体研究所提供);氢氧化钠、柠檬酸钾、焦磷酸钾(KPP)、十二烷基磺酸钠(SDBS)、酒石酸钠、柠檬酸钠、六偏磷酸钠(SHMP)和羟基乙叉二膦酸(HEDP)均为分析纯试剂,反应水为二次去离子水。
1.2 MgH2粉末的制备
采用充氢球磨方法,将Mg粉与Mn粉按照一定比例(95%Mg+5%Mn,质量分数)混合,放入行星式球磨机的4个球罐中,先对球罐进行抽真空,然后充氢气达到一定的压力进行球磨,球磨过程中不断地补充氢气,球磨72 h后取出粉末。其中,Mn粉在Mg粉的氢化和后期MgH2的水解过程中都起到一定的催化作用。
1.3 MgH2与水反应过程中改变溶液pH值和加入助剂
MgH2的水反应性能的测试采用自制的装置(见图1),包括反应装置、冷凝装置和集气装置3部分。反应装置由磁振子、250 mL的广口试剂瓶以及恒温水浴锅组成。广口试剂瓶是氢化物与水反应的容器,广口试剂瓶放入恒温水浴锅中用于保持一定的反应温度,磁振子在电磁力作用下对反应体系进行搅拌,使氢化物与水接触更充分。由于在反应温度下反应产生的气体(包括水蒸气和氢气)会有一定程度的体积膨胀,在一定程度上会影响到最终的氢气测量结果,故在氢气收集前需进行冷凝。本实验中采用排水集气法收集气体,反应产生的氢气通过冷凝装置后进入量筒,量筒中的水被氢气排出,读取氢气体积,保持其他条件不变,不加入氢化物,进行空白实验,读取气体体积,在原实验数据中扣除,从而使氢气体积更准确[15]。反应前,记录量筒的初始刻度值;反应开始后,前7 min每隔0.5 min记录刻度1次,然后每间隔1 min记录1次,共计20 min,从而得到不同时刻的放氢量。
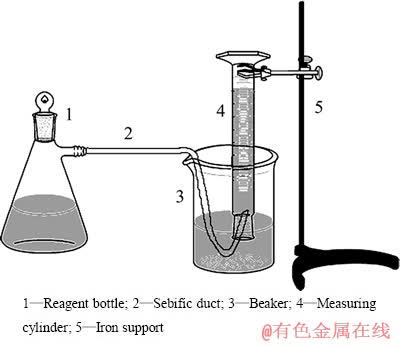
图1 MgH2水反应性能测试装置示意图
Fig. 1 Schematic diagram of MgH2 water reaction device
将氢氧化钠固体配制成一定体积、不同pH值的溶液,分别取150 mL不同pH值的溶液与0.2 g MgH2粉末在如图1所示测试装置中进行反应;按照上述方法记录生成氢气量与相应时间,为后续处理提供原始数据。在反应完成后,对广口试剂瓶中的反应产物进行抽滤,将反应产物留在滤纸上,放入50 mL的小烧杯中,用保鲜膜封口,放置到真空干燥箱中,在室温下真空干燥24 h后取出,即可得到完全干燥的反应产物。
分别在150 mL水溶液中加入不同量的柠檬酸钾、焦磷酸钾、十二烷基磺酸钠、酒石酸钠、柠檬酸钠、六偏磷酸钠和HEDP,与定量的MgH2粉末在如图1所示实验装置中进行反应,后续处理与不同pH值条件下处理相同。
1.4 样品表征
对反应产物Mg(OH)2的表征包括观察改变pH值前后和加入不同助剂前后的反应产物电子显微镜照片(捷克TESCAN公司生产的5136SM扫描电子显微镜),对反应物和产物的物相分析(北京普析通用有限公司生产的XD-2型X射线衍射仪)。
2 结果与讨论
2.1 水反应性质
在不同pH值溶液反应的动力学曲线如图2所示。纯水条件下加入不同助剂时的反应动力学曲线图如图3所示。
改变反应溶液的pH值和加入各种助剂是为了加快MgH2的水反应速率,MgH2的水反应活性可以通过反应过程中产生的氢气量和放氢速率来体现。

图2 不同pH值条件下氢化态Mg-Mn复合物水反应动力学曲线
Fig. 2 Water reaction kinetics curves of hydrogenated Mg-Mn composites at different pH values
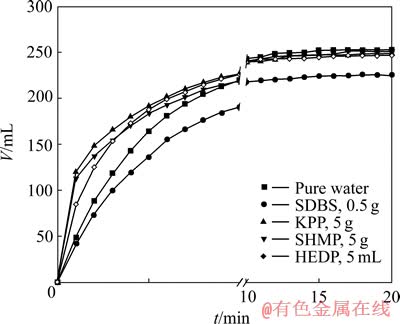
图3 纯水条件下加入不同助剂时的氢化态Mg-Mn复合物水反应动力学曲线
Fig. 3 Water reaction kinetics curves of hydrogenated Mg-Mn composites by adding different additives under condition of pure water
从图2中可以看出,改变溶液pH值前后放氢速率改变不明显,pH为8.80时的初始放氢速率稍高于原始放氢速率,随着pH值的增大,反应越来越不完全,当pH为14.22时反应进行的程度最低,说明改变溶液中pH值对反应的影响不大。
从图3中各反应曲线的斜率可以看出:在溶液中分别加入六偏磷酸钠(SHMP)、HEDP和焦磷酸钾 (KPP)时的初始反应速率远远超过纯水溶液的;加入十二烷基磺酸钠(SDBS)并不能促进反应进行和加快反应速率。
2.2 产物的SEM像
在不同pH值溶液中反应产物的SEM像如图4所示。Mg(OH)2晶体属于六方结构,在一定的温度下,Mg(OH)2通过克服其颗粒表面吸附大量的自由水,减小晶体长大的阻力,最终形成晶粒大、比表面积小、规则的六方片状组织。这种片状组织的存在能避免致密钝化膜形貌形成,有利于氢化物与水反应充分进行。从图4中可以看出,在纯水条件下,Mg(OH)2颗粒为不规则形状,颗粒表面存在一些细片状组织,呈无序状态;其他不同pH值条件下的形貌并无明显改善,但当pH值为14.22时,Mg(OH)2颗粒出现了更多的团聚,大量细片状颗粒聚集成不规则的颗粒团,这种形貌不利于MgH2水反应的充分进行。这与前面的水反应曲线分析结果一致。

图4 不同pH值溶液中反应样品的SEM像
Fig. 4 SEM images of samples at different pH values
分别加入酒石酸钠0.1、0.5、5和10 g,焦磷酸钾0.1、0.5和5 g,柠檬酸钾0.1和0.5 g,十二烷基磺酸钠0.1和0.5 g,六偏磷酸钠0.1、0.5、5和10 g, HEDP 2.5和5 mL,研究加入不同种类助剂以及不同助剂用量对反应速率和反应程度的影响,在本研究的分析中只引用部分实验数据。加入各助剂前后样品的SEM像如图5所示。
从图5中可以看出,在纯水条件下,Mg(OH)2颗粒尺寸分布均匀,呈不规则形状,颗粒表面存在大量细片状组织,呈无序状态;加入0.5 g十二烷基磺酸钠时,Mg(OH)2的粒径相对较大,形状不规则、不均匀,有部分Mg(OH)2颗粒形成颗粒团;加入5 g六偏磷酸钠时,Mg(OH)2颗粒尺寸明显缩小且比较均匀,出现大量的片状结构,有少量的颗粒团聚;加入5 mL HEDP时,Mg(OH)2粒径较小,出现一些片状组织,边缘出现颗粒团聚现象。
通过Mg(OH)2的SEM像分析,结合图3所示水反应曲线,可以说明磷酸盐能促进氢化物水反应的进行。原因可能如下:1) 磷酸根与镁离子结合性强,夺去了Mg(OH)2的镁离子,形成了大量能溶于溶液的络合物,破坏了MgH2表面的Mg(OH)2钝化膜;2) 由于加速了MgH2的水反应速率,瞬间大量气泡将MgH2表面的镁离子冲散,减少了MgH2表面的Mg(OH)2的量,破坏了致密性Mg(OH)2膜的形成。加入其他助剂时,对MgH2与水反应促进作用不明显。可能是由于这些物质对镁离子的结合性不及对氢氧根离子的结合性,不能减少Mg(OH)2在MgH2表面的附着量。
2.3 产物的XRD分析
不同pH值时以及加入各助剂前后产物的XRD谱如图6所示。

图5 加入助剂前后样品的SEM像
Fig. 5 SEM images of samples before and after addition of additives
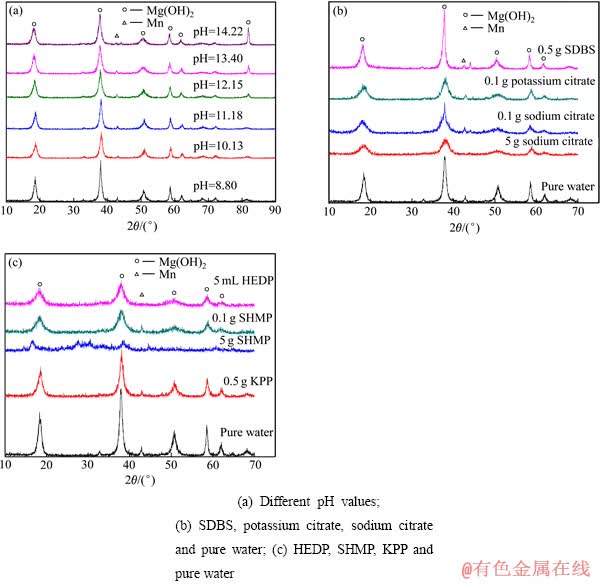
图6 不同pH值时以及加入不同助剂前后反应产物的XRD谱
Fig. 6 XRD patterns of reaction products at different pH values before and after adding different additives
由图6可以看出:以上样品的XRD谱中都只出现了Mg(OH)2和Mn的衍射峰,尽管不同条件下的衍射峰强度有所变化,但均没有出现其他物质(包括添加的助剂)的衍射峰。说明在改变溶液pH值和加入不同的助剂情况下没有在反应过程中引入太多的杂质,所以对反应产物的回收没有影响。
2.4 反应机理分析
该反应的机理如下:MgH2中H-具有强还原性,还原H2O中的H+,生成H2,在溶液中反应生成的Mg2+和OH-所形成的结构单元为Mg(OH)64-负离子配位八面体,Mg2+位于八面体的中心,OH-离子则在八面体的顶角上。
在溶液中存在的生长基元Mg(OH)64-与晶体结构基元一致,它采用不同的方式进行连接,形成生长基元的团聚体,从而促使晶体生长,使形成的晶体具有不同的形貌。Mg(OH)2作为极性晶体具有极轴,而且极轴两端的界面结构有差异,负极面为OH-,正极面为Mg2+,通过添加不同离子到溶剂中以改变溶剂和晶界面之间的相互作用,从而对晶体中各晶面间的相对生长速率进行控制,使晶体的生长习性得到控制[15]。
改变溶液中pH值,也即改变溶液中参加反应的OH-浓度,等同于改变反应中的水量。加入不同的助剂(酸盐),反应过程中不同的酸根可以与Mg2+结合,使Mg(OH)2沉淀不易形成,而形成溶解性更好的大分子配合物,减小MgH2与水反应的阻力,可以使MgH2与水的反应程度大幅增大。
3 结论
1) 与在二次去离子水溶液中进行反应相比,改变反应溶液的pH值,并没有改变反应的实际历程,对反应程度及放氢速率影响都不大,对反应改善不明显;在一定程度上,pH值越高,越不利于反应的进行。
2) 与在二次去离子水溶液中进行反应相比,加入磷酸盐助剂时,反应中的酸根离子先与Mg2+形成络合,不形成Mg(OH)2沉淀,从而可以使MgH2与水的反应程度显著增大,当络合物饱和后,Mg2+逐步与OH-结合,最终形成Mg(OH)2沉淀,助剂表现为催化剂的性质,并不参与反应,对氢化态Mg-Mn复合物的放氢速率有显著促进作用。
3) 应采用添加磷酸盐助剂的方法来改善氢化态Mg-Mn复合物的水反应性能。
REFERENCES
[1] GAYATHRI V, DEVI N R, GEETHA R. Hydrogen storage in coiled carbon nanotubes[J]. International Journal of Hydrogen Energy, 2010, 35(3): 1313-1320.
[2] IOANNATOS G E, VERYKIOS X E. H2 storage on single- and multi-walled carbon nanotubes[J]. International Journal of Hydrogen Energy, 2010, 35(2): 622-628.
[3] WANG Yi, DENG Wei-qiao, LIU Xue-wei, WANG Xin. Electrochemical hydrogen storage properties of ball-milled multi-wall carbon nanotubes[J]. International Journal of Hydrogen Energy, 2009, 34(3): 1437-1443.
[4] 陈霖新. 中国氢能源利用现状及发展潜力[J]. 气体分离, 2005(2): 13-16.
CHEN Lin-xin. The utilization and development potential of hydrogen energy in China[J]. Gas Separation, 2005(2): 13-16.
[5] 张祥春. 水电解制氢概况[J]. 气体分离, 2009(3): 9-11.
ZHANG Xiang-chun. Overview of water electrolysis hydrogen production[J]. Gas Separation, 2009(3): 9-11.
[6] 徐钟平, 周敏莉, 虞利强, 潘相敏. 燃料电池汽车及氢能源的发展现状与安全对策[J]. 消防科学与技术, 2010, 29(11): 1019-1021.
XU Zhong-ping, ZHOU Min-li, YU Li-qiang, PAN Xiang-min. Present situation and safety measures of fuel cell powered vehicle and hydrogen energy source[J]. Fire Science and Technology, 2010, 29(11): 1019-1021.
[7] 张 翔, 孙奎斌, 周俊波. 硼氢化钠水解制氢技术研究进展[J]. 无机盐工业, 2010, 42(1): 9-12.
ZHANG Xiang, SUN Kui-bin, ZHOU Jun-bo. Progress in hydrogen production technology from hydrolysis of sodium borohydride[J]. Inorganic Chemicals Industry, 2010, 42(1): 9-12.
[8] 徐东彦, 张华民, 叶 威. 硼氢化钠水解制氢[J]. 化学进展, 2007, 19(10): 1598-1605.
XU Dong-yan, ZHANG Hua-min, YE Wei. Hydrogen production from sodium borohydride[J]. Progress in Chemistry, 2007, 19(10): 1598-1605.
[9] KOJIMA Y, SUZUK I, KAWAI Y. Hydrogen generation by hydrolysis reaction of magnesium hydride[J]. Journal of Materials Science, 2004, 39: 2227-2229.
[10] HUOT J, LIANG G, SCHULZ R. Magnesium-based nanocomposites chemical hydrides[J]. Journal of Alloys and Compounds, 2003, 353(1/2): 12-15.
[11] LUKASHEV R V, YAKOVLEVA N A, KLYAMKIN S N, TARASOV B P. Effect of mechanical activation on the reaction of magnesium hydride with water[J]. Russian Journal of Inorganic Chemistry, 2008, 53(3): 343-349.
[12] GROSJEAN M H, ZIDOUNE M,  L, HUOT J Y. Hydrogen production via hydrolysis reaction from ball-milled Mg-based materials[J]. International Journal of Hydrogen Energy, 2006, 31: 109-119.
L, HUOT J Y. Hydrogen production via hydrolysis reaction from ball-milled Mg-based materials[J]. International Journal of Hydrogen Energy, 2006, 31: 109-119.
[13] HU Lian-xi, WANG Er-de. Hydrogen generation via hydrolysis of nanocrystalline MgH2 and MgH2-based composites[J]. Transactions of Nonferrous Metals Society of China, 2005, 15(5): 965-970.
[14] 刘冠鹏, 郭效德, 段红珍, 姜 炜, 李凤生. Mg粉的新型包覆处理及其水反应特性[J]. 中国有色金属学报, 2007, 17(12): 1999-2004.
LIU Guan-peng, GUO Xiao-de, DUAN Hong-zhen, JIANG Wei, LI Feng-sheng. New surface coating on Mg powers and their characteristics of reaction with water[J]. The Chinese Journal of Nonferrous Metals, 2007, 17(12): 1999-2004.
[15] 南群智. 氢化态Mg-Mn复合物水反应行为研究[D]. 哈尔滨: 哈尔滨工业大学, 2011: 8-9.
NAN Qun-zhi. Research on reaction behavior of hydride Mg-Mn composites with water[D]. Harbin: Harbin Institute of Technology, 2011: 8-9.
(编辑 陈卫萍)
基金项目:对俄科技合作专项(2012DFR50850)
收稿日期:2012-09-25;修订日期:2013-08-07
通信作者:张文丛,教授,博士;电话:0631-5672167;E-mail: zhangwencong@hit.edu.cn