����La�Ħ�-Ni(OH)2���Ʊ����绯ѧ����
����ƽ, ��ƽ��, ���ѱ�, ���и�, ������, ɣ�̱�
(���ϴ�ѧ ��ѧ����ѧԺ, ���� ��ɳ, 410083)
ժҪ: �û�ѧ���������Ʊ�����La��Ni(OH)2�� ͨ��X��������ͺ�����Բ���La��Ni(OH)2���нṹ����, ������ģ���غ�ѭ������������绯ѧ���ܽ����о��� �о��������: ����La��Ni(OH)2�������-Ni(OH)2���Ƶľ���ṹ, ���нϴ�IJ���, ���������ӵ�Ǩ��, ������е�OH-���ٴ������ɹ���״̬, ���뾧���е�ˮ���ӷ��������, ��δ���ӵ�Ni(OH)2�ھ�������и����ˮ���ӡ� ������La��Ħ������Ϊ6.32%ʱ, ����La��Ni(OH)2�ķŵ����߱Ƚ�ƽ̹, ���нϸߵķŵ�ƽ̨�� �ϸߵĻ�ԭ��λ��������λ, ��ѭ�������ԽϺá�
�ؼ���: ��-Ni(OH)2; La; ����; �绯ѧ����
��ͼ�����:TM912.2 ���ױ�ʶ��:A ���±��: 1672-7207(2005)06-0988-06
Preparation and electrochemical performance of
lanthanum doping ��-Ni(OH)2
YANG You-ping, ZHANG Ping-min, ZHANG You-biao,
TANG You-gen, LIU Kai-yu, SANG Shang-bin
(School of Chemistry and Chemical Engineering, Central South University, Changsha 410083, China)
Abstract: Lanthanum doping nickel hydroxide samples were prepared by chemical co-precipitation method. The structure characteristics of the lanthanum doping nickel hydroxide were analyzed by X-ray diffraction and infrared spectrum. The electrochemical performances of the lanthanum doping nickel hydroxide were studied by means of laboratory cell and cyclic voltammetry. The results show that the structure of the lanthanum doping nickel hydroxide is similar to that of ��-nickel hydroxide, and it has a large interlayer distance, which is helpful for the diffusion of proton; OH- group in lanthanum doping nickel hydroxide is no longer at free structure phase, which interact with the molecule of water in the lattice. When the mole fraction of lanthanum doping is 6.32%, lanthanum doping nickel hydroxide has flat discharge curve, higher discharge plateau, higher deoxidation potential, higher oxygen evolution potential, and good cyclic reversibility.
Key words: ��-nickel hydroxide; lanthanum; doping; electrochemical performance
�����⻯��-��(MH-Ni)��ؾ��б������ߡ� ����Ⱦ�� ����ЧӦ�� ���ºʹ�����ŵ��������á� �ɿ��ٳ�ŵ硢 �����õ�����ŵ����Ե��ŵ�, ��һ������������ɫ���ε��[1]�� ��MH-Ni��ص���ɽṹ��, ���������Բ���Ni(OH)2�����۱�����Ϊ289 mA�� h/g, ����������Ͻ�ı������ߴ�330 mA��h/g���ϡ� ���, �������ϳ�����ԼMH-Ni��ط�չ�ġ�ƿ����, Ҫ���MH-Ni��صľ�������������Ӧ�÷�Χ, �ؼ������Ʊ������ܵ�MH-Ni����������ϡ���Ni(OH)2��
Ni(OH)2�Ц�-Ni(OH)2�ͦ�-Ni(OH)22��, ��ĿǰMH-Ni��������õ������������ʾ�Ϊ��-Ni(OH)2, ���������û�ѧ���Ʊ�����ͨ�����ε�Ni(OH)2��Ϊ���;���, ����-Ni(OH)2�����ڼ�Һ�в��ȶ��� �Ʊ��Ѷȴ�Ȳ���[2], �ܶ�ѧ�߰��������Ǻϳɦ�-Ni(OH)2�����е�һ�ֽ���̬�� ���ͦ����־���Ni(OH)2���ܶȺ�����̬��ͬ, ��-Ni(OH)2������ڦ�-Ni(OH)2�IJ���[3]�� ����, ��-Ni(OH)2���γ���c��Ϊ�Գ�����в�ṹ, �Ҳ���������Ƕ��ˮ���Ӽ�������������, ���, ��-Ni(OH)2�������ͷŵ�Ч�ʶ��ϸߡ�
Ϊ�˽����-Ni(OH)2��ǿ������еĽṹ�ȶ�������, ����3�����ֽ���Ԫ��(��Co[4-7], Al[8-12], Fe[13, 14]��ϡ��Ԫ��[15-18]��)��Ni(OH)2�ľ�����, �õ�ˮ��ʯ�͵�˫����������, ��Щ������������-Ni(OH)2��ͬ�Ľṹ, ������ǿ����������ȶ���, �п�����Ϊ���������缫�IJ��ϡ� �ڴ�, ���߲��û�ѧ���������Ʊ�����La��Ni(OH)2, ͨ��X��������(XRD)�ͺ������(IR)�Բ���La��Ni(OH)2��Ʒ���нṹ����, ������ģ���غ�ѭ������������绯ѧ���ܽ����о���
1 ʵ ��
1.1 ��Ҫ�������Լ�
��Ҫ����Ϊ: LX-PCBT-128D-A�͵�س̿ز�����(�人���˵�Դ����˾����); Chi660A�绯ѧ�ۺϲ�����(�Ϻ�����������˾����); DZF6050����ո�����(�Ϻ�����ʵ���豸����˾����); JA2003�͵�����ƽ(�Ϻ���ƽ��ѧ��������˾����); SHB-3��ѭ��ʽ������ձ�(�Ÿ�����������); ����ѹƬ��(����)��
��Ҫ�Լ�Ϊ: NaOH, KOH, LiOH (���ϻ���¥��ѧ�Լ�������); Ni(NO3)2(����ʦ���Լ�������); La(NO3)3(�й�ҽҩ�����Ϻ�ҽҩ������); ���� (�Ϻ��ڶ�ұ��������); �ܷ�(�й�ҽҩ�����Ϻ���ѧ�Լ���˾����); ���ķ���ϩ(PTFE); ����ϩ��(PVA); ����Ͻ��(�����д�߿Ƶ�ز�������˾����); �ʻ�����(���ϴ�ѧ��ĩұ���о�Ժ����)��
1.2 �����������Ʊ�
�ֱ�2 mol/L NaOH��Һ������6�ݲ�ͬ����ȵ�1 mol/L Ni(NO3)2��0.135 mol/L La(NO3)3�Ļ����Һ��(����1, ����, xΪԭ��������), ��Ӧ�¶ȿ�����40~50 �档 ��������ɫ��������ȹ���, ������ˮ���Ҵ�ϴ�ӳ������, Ȼ��, ��60~80 ����ո��T������������Ʒ��
�� 1 ����������Ʒ���Ʊ�
Table 1 Preparation of Ni(OH)2 samples

1.3 �ṹ����
����X���������Ǻ���Ҷ�任��������Ƕ����Ʊ��������������нṹ����, XRD�ⶨʱɨ�����Cu�з���, ����Ϊ0.154 18 nm, ��ѹΪ30 kV, ����Ϊ36 mA, ɨ���ٶ�Ϊ4(��)/min��
1.4 �绯ѧ���ܲ���
���ÿ���ʽ˫�缫��ϵ, �����缫Ϊ���������缫, �����缫Ϊ����Ͻ�缫, ������Զ�������������缫����, ���ҺΪ6 mol/L KOH��Һ(���к���15 g/L LiOH)�� �ڵ�س̿ز������Ͻ��е绯ѧ�������ԡ�
1.4.1 ����Ͻ�Ƭ���Ʊ�
������Ͻ�ۺ��ʻ����۰�������Ϊ2��1�ı�������, ������������������Ϊ3%�ľ��ķ���ϩ��Һ��ճ���, ��Ͼ���, ����ո����, ��Ni����������, �ڵ���ѹƬ����ѹ��ֱ��Ϊ10 mm�� ���Ϊ5 mm�ĸ���Ƭ��
1.4.2 ������������Ƭ���Ʊ�
��ȡһ���������������ۡ� �ܷۺ�����, ��m(Ni(OH)2��m(Co)��m (Ni)=90��5��5��Ͼ���, ������������������Ϊ3%�ľ���ϩ����Һ�;��ķ���ϩ��Һ��Ϊճ���, �Ƴɺ�״, �õ�Ƭ�ε���ĭ��������, ��ո��
1.4.3 �绯ѧ�����IJⶨ
���ú������ŵ緽�������绯ѧ������ �Ƚ�����Ƭ���л, �ٽ���0.2C���ʳ�ŵ���ԡ� 0.2C���ʳ�ŵ����Ϊ: ��40 mA���120 min, Ȼ����8 mA�ŵ���1.00 V��
���������ķŵ���������ʽ����:
C=It/m��(1)
ʽ��: CΪ�ŵ�����, mA��h/g; IΪ�ŵ����, mA; tΪ�ŵ�ʱ��, h; mΪ��������������, g��
1.5 ѭ���������ߵIJⶨ
���õ绯ѧ�ۺϲ����Ƕ�ģ���ؽ���ѭ���������߲ⶨ�� ����, �����������缫Ϊ�о��缫, ����Ͻ�缫Ϊ�����缫, Hg/HgO(6 mol/L KOH)�缫Ϊ�αȵ缫�� ѭ�������ĵ�ѹɨ�跶ΧΪ0~800 mV, ��ɨ������Ϊ20 mV/s��ѭ����������10~20��, ʹѭ���������ߴﵽ�ȶ�Ϊֹ��
2 ���������
2.1 X�����������
ͼ1��ʾΪNi(OH)2��Ʒ��X����������ͼ(����, xΪĦ������)�� ������1�ɼ�, δ���ӵ�Ni(OH)2(��Ʒ1)��XRDͼ��ʾ����-Ni(OH)2������, �侧�����a=0.310 nm, c=0.450 nm�� ������2��3�ɼ�, ����La��Ni(OH)2(��Ʒ4��6)��XRDͼ��δ���ӵ�Ni(OH)2�����Բ�ͬ, ��������[19]�����Ĵ���-Ni-(OH)2��XRD��ͼ��������, ˵����������-Ni(OH)2���Ƶľ���ṹ, ��������ϵ�� ��Ʒ4�ľ������a=0.306 nm, c=0.790 nm; ��Ʒ6�ľ������a=0.302 nm, c=0.760 nm��
����La��Ni(OH)2��cֵ��Ҫ��δ���ӵ�Ni(OH)2��cֵ��ö�, ˵������La��Ni(OH)2�IJ���ϴ� �����缫�ķ�Ӧ������, ���ӵ���ɢ�����ٿ�����, �ϴ��������ɢϵ�����н�С�ķ�Ӧ������ ����La��Ni(OH)2���нϴ�IJ���, ���������ӵ�Ǩ����ѳ�, ʹ����нϸߵ�������ɢϵ���� ���, ��绯ѧ��Ӧ�������Ȧ�-Ni(OH)2��С��
2.2 ���������
ͼ2��ʾΪNi(OH)2��Ʒ�ĺ������ͼ�� �Ƚ�ͼ2�еĸ����߿ɼ�, Ni(OH)2��Ʒ��3448 cm-1����һ�������մ�, ������H2O�������������, ��Щˮ���Ӵ����ڿ������������;������϶; ��1635 cm-1���������ն�Ӧ����ˮ������; ��1384 cm-1����һ���շ�, �����ɷ�����������(��CO2-3)����������ġ�
��ͼ2�е�����1�ɼ�, δ���ӵ�Ni(OH)2��3645 cm-1����һխ���շ�, �����ɴ������ɹ���״̬OH����������������ġ� ������2~4�д�խ���շ�����ʧ, ��˵�������е�OH���Ų��ٴ������ɹ���״̬, ���뾧���е�ˮ���ӷ�������á� ���, ����La�Ħ�-Ni(OH)2�Ȧ�-Ni(OH)2�ھ�������и����ˮ���ӡ�
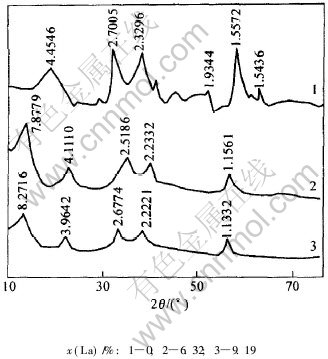
ͼ 1 Ni(OH)2��Ʒ��XRDͼ
Fig. 1 XRD patterns of Ni(OH)2 samples
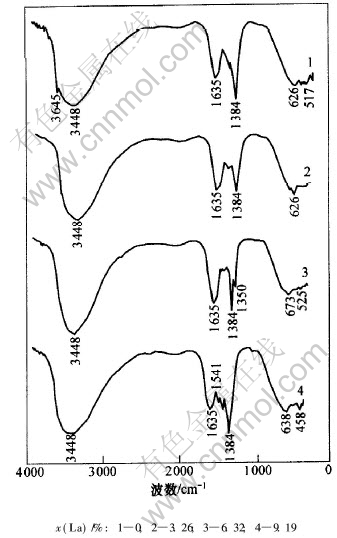
ͼ 2 Ni(OH)2��Ʒ��IRͼ
Fig. 2 IR spectra of Ni(OH)2 samples
2.3 �绯ѧ���ܲ��Խ��
2.3.1 �����
ͼ3��ʾΪ��ͬLa��������Ʒ����ܵ�Ӱ�졣 ���Կ���, ����La����������, ��Ʒ�Ļ�������ӡ� δ����La�Ħ�-Ni(OH)2�ڵ�2���ѭ���ʹﵽ�������, �����ʮ�������� ����, La��������Ʒ�ķŵ������Ӱ��ܴ� ����La����������, ��Ʒ�ķŵ�������Ƚ��ͺ�����, Ȼ���ֽ���, ͼ��x(La)= 6.32%(����Ʒ4)�ķŵ��������ߡ�
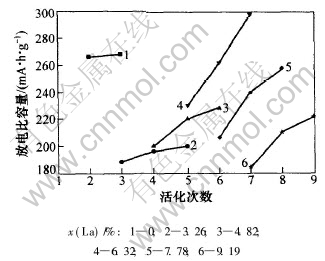
ͼ 3 La������Ni(OH)2��Ʒ����ܵ�Ӱ��
Fig. 3 Effect of La content on activation performance of Ni(OH)2 samples
2.3.2 0.2C���ʳ�ŵ�����
ͼ4��ʾΪLa������Ni(OH)2��Ʒ0.2C���ʳ�����ܵ�Ӱ�졣 ���Կ���: ��Ʒ2, 3��6�Ħ�-Ni(OH)2����Ʒ1�Ħ�-Ni(OH)2�нϸߵij���ѹ; ��Ʒ4��5�Ħ�-Ni(OH)2����Ʒ1�Ħ�-Ni(OH)2�нϵ͵ij���ѹ�� ���ϵ͵ij���ѹ����������������Ӧ�ķ���, ��ߵ缫�ij��Ч��, ���, ��-Ni(OH)2�ij�����߱Ȧ�-Ni(OH)2�ij�����߸�Ϊƽ̹, ������ѹ�������ߡ�
ͼ5��ʾΪNi(OH)2�缫��0.2C�����µĺ�����ŵ����ߡ� ��ͼ�ɼ�, ����La����Ʒ�ķŵ�ƽ̨�Ƚ�ƽ��, ��δ���ӵ���Ʒ�ķŵ�ƽ̨�Ƚ϶�, ������La����Ʒ�ڵ���ŵ��յ�֮ǰ, ��ѹ�½��Ͽ졣 ���Ӧ�-Ni(OH)2�ķŵ�ƽ̨�߶���ƽ��, �ŵ���ѹ���ﵽ1.18 V, ��δ������������(1.14 V)�ķŵ���ѹ��, �������ķŵ����������ʺܸ�, �ŵ�ʱ��λ�����϶�ά����1.10 V����, ���δ���ӵ���������������������Խ�ԡ�
��ͼ5���ɿ���, ����La����������, �ŵ��ѹ����ƽ̨б���Ƚϴ���С, ������Ʒ4(��x(La)=6.32%)�ķŵ��ѹ����ƽ̨б����С��

ͼ 4 La������Ni(OH)2��Ʒ0.2C���ʳ�����ܵ�Ӱ��
Fig. 4 Effect of La content on 0.2C rate charge performance of Ni(OH)2 samples
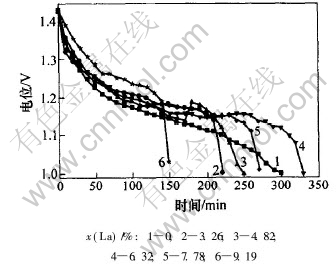
ͼ 5 La������Ni(OH)2��Ʒ0.2C���ʷŵ����ܵ�Ӱ��
Fig. 5 Effect of La content on 0.2C rate discharge performance of Ni(OH)2 samples
2.4 ѭ���������߲��Խ��
ͼ6��ʾΪ�Ʊ��IJ���La�Ħ�-Ni(OH)2��δ���ӵĦ�-Ni(OH)2�缫��10��ѭ������ͼ�� ͼ�е�������ͻ�ԭ��ֱ��Ӧ�����צá��͡������צ�������Ӧ�������ͻ�ԭ���̡� ��ͼ�ɼ�, ����La�Ħ�-Ni(OH)2��������λ����ͨ��-Ni(OH)2��������λ��100 mV���ϡ�
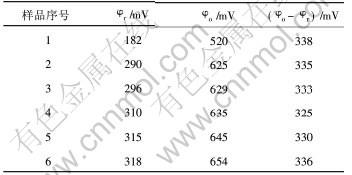
��ѭ������ͼ�зֱ�ȡ���缫��������λ�� ��ԭ��λ�� ������λ, ��������֮��IJ�ֵ, ���2��ʾ�� �������������λ(��o)�뻹ԭ���λ(��r)֮���������缫��Ӧ�Ŀ�����, ��o-��rԽ��,�缫��Ӧ�Ŀ�����Խ� ��ͼ6�ͱ�2���Կ���, ����La����һ���̶�����������缫��Ӧ�Ŀ�����, ���缫������������������, ��������Ʒ4��Ч��������, ���缫����������������, ���缫�ij��Ч�ʺͻ������ʵ���������ߡ� ���, ����ϡ��Ԫ��La��һ���̶�������˵缫��Ӧ�Ŀ����ԡ�
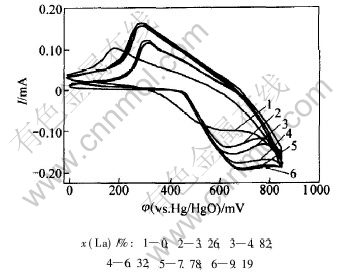
ͼ 6 Ni(OH)2��Ʒ��ѭ������ͼ
Fig. 6 Cyclic voltammogram of Ni(OH)2 samples
�� 2 Ni(OH)2��Ʒ��������λ
Table 2 Characteristic potentials of Ni(OH)2 samples
3 �� ��
a. ���û�ѧ���������Ʊ��˲���La��Ni(OH)2, ����La��Ni(OH)2�������-Ni(OH)2���Ƶľ���ṹ; ����La�Ħ�-Ni(OH)2��δ���ӵ�Ni(OH)2�ھ�������и����ˮ���ӡ�
b. ����La����������, ����La��Ni(OH)2��Ʒ�Ļ���ܱ��, ��La��Ħ������Ϊ6.32%ʱ, ��Ʒ�ķŵ�������ϴ�, �ŵ�ƽ̨�ϸ�, �ŵ�����ƽ��, ���缫��ѭ�������ԽϺá�
�����:
[1]������, ���º�, ������. ��ѧ��Դ�������ԭ�������켼��[M]. ��ɳ: ���Ϲ�ҵ��ѧ������, 2000.
GUO Bing-kun, LI Xin-hai, YANG Song-qing. Chemical Power Sources��Theory and Manufacture Technique of Batteries[M]. Changsha: Central South University of Technology Press, 2000.
[2]�����, ��Ϊ��. ������ص���״�뷢չ����[J]. ���, 2001, 31(2): 58-61
YU Cheng-zhou, LAI Wei-hua. Current situation and development direction of MH/Ni battery[J]. Battery Bimonthly, 2001, 31(2): 58-61.
[3]Ԭ����, �ż���, �ܳ���. ���缫�о���չ[J]. ��Դ����, 2001, 25(1): 53-59.
YUAN An-bao, ZHANG Jian-qing, CAO Chu-nan. Research progress of nickel hydroxide electrodes[J]. Chinese Journal of Power Sources, 2001, 25(1): 53-59.
[4]Armstrong R D, Briggs G W D, Charles E A. Some effects of the addition of cobalt to the nickel hydroxide electrode[J]. J Appl Electrochem, 1988, 18(2): 215-219.
[5]ZHU Wen-hua, KE Jia-jun, YU Hong-mei, et al. A study of the electrochemistry of nickel hydroxide electrodes with various additives[J]. Journal of Power Sources, 1995, 56: 75-79.
[6]ZHANG Heng-Bin, LIU Han-San, CAO Xue-Jing, et al. Effect of some metal ion dopants on electrochemical properties of Ni(OH)2 film electrode[J]. Chemical Research in Chinese Universities, 2003, 19(4): 494-498.
[7]Jayashree R S, Kamath P V. Modified nickel hydroxide electrodes[J]. J Electrochem Soc, 2002, 149 (6): A761-764.
[8]Wang C Y, Zhong S, Konstantinov K, et al. Structural study of Al-substituted nickel hydroxide[J]. Solid State Ionics, 2002, 148: 503-508.
[9]������, ����Ӣ, ������, ��. ����Al�Ħ�-Ni(OH)2�ĵ绯ѧ����[J]. Ӧ�û�ѧ, 2000, 17(1): 35-38.
ZHAO Pei-zheng, ZHANG Xiu-ying, ZHAO Lin-zhi, et al. Electrochemical properties of Al doped ��-Ni(OH)2[J]. Chinese Journal of Applied Chemistry, 2000, 17(1): 35-38.
[10]������, ����ӡ. ����������������������ṹ���绯ѧ����[J]. ��Դ����, 2002, 26(2): 74-77.
DU Xiao-hua, JIANG Chang-yin. Structural and electrochemical performance of aluminum substituted nickel hydroxide used in power battery [J]. Chinese Journal of Power Sources, 2002, 26(2): 74-77.
[11]��ӵ��, ����, �����, ��. ��ȡ�����������Ʊ��� �ṹ��绯ѧ����(��)�����绯ѧ����[J]. ��Դ����, 2000, 24(2): 77-80.
LENG Yong-jun, LIU Bing, WANG Feng-jun, et al. Preparation, structure and electrochemical performance of aluminum-substituted nickel hydroxide (I): Electrochemical performance [J]. Chinese Journal of Power Sources, 2000, 24(2): 77-80.
[12]LIU Bing, ZHANG Yun-shi, YUAN Hua-tang, et al. Electrochemical studies of aluminum substituted ��-Ni(OH)2 electrodes[J]. International Journal of Hydrogen Energy, 2000, 25: 333-337.
[13]DING Yun-chang, YUAN Jiong-liang, CHANG Zhao-rong. Cyclic voltammetry response of coprecipitated Ni(OH)2 electrode in 5 mol/L KOH solution[J]. Journal of Power Sources, 1997, 69(1-2): 47-54.
[14]��ӵ��, ���Ϸ�, �Ŵ��, ��. ��ȡ�����������Ʊ��� �ṹ��绯ѧ����(��)�����ṹ����[J]. ��Դ����, 2000, 24(1): 32-35.
LENG Yong-jun, MA Zi-feng, ZHANG Cun-gen, et al. Preparation, structure and electrochemical performance of iron-substituted nickel hydroxide (��): Structure analysis[J]. Chinese Journal of Power Sources, 2000, 24(1): 32-35.
[15]MI Xin, YE Mao, YAN Jie, et al. High temperature performances of spherical nickel hydroxide with additive Y2O3[J]. Journal of Rare Earths, 2004, 22(3): 422-426.
[16]������, ������, ����, ��. ��Ԫ�ض����缫���ܵ�Ӱ��[J]. ���ܲ���, 2002, 33(3): 291-293.
CHANG Zhao-Rong, REN Xing-Tao, PENG Peng, et al. Effect of Ce on the properties of nickel hydroxide electrode[J]. Journal of Functional Materials, 2002, 33(3): 291-293.
[17]Oshitani M, Watada M, Shodai K, et al. Effect of lanthanide oxide additives on the high-temperature charge acceptance characteristics of pasted nickel electrodes[J]. J Electrochem Soc, 2001, 148(1): A67-A73.
[18]����͢, �¸���, ����, ��. ���Ʀ�-Ni(OH)2���о�[J]. Ӧ�û�ѧ, 2001, 18(9): 689-692.
YANG Shu-ting, CHEN Gai-rong, YIN Yan-hong, et al. Study on the Y-doped ��-Ni(OH)2 [J]. Chinese Journal of Applied Chemistry, 2001, 18(9): 689-692.
[19]Kamathp V, Dixt M, Indira L, et al. Stabilized ��-nickel hydroxide as electrode material for alkaline secondary cells[J]. J Electrochem Soc, 1994, 141(11): 2956-2959.
�ո�����:2005-06-08
������Ŀ: ���ҡ�863���ƻ���Ŀ(2001AA501433)
�����: ����ƽ(1964-), Ů, ���������, ������, ��ʿ�о���, ���»�ѧ��Դ������о�
������ϵ��: ����ƽ, Ů, ������; �绰: 0731-8879765(O); E-mail: youpingyang@sohu.com