文章编号: 1004-0609(2005)08-1294-06
新型锂离子电池正极材料Li3V2(PO4)3的合成及其性能
刘素琴, 唐联兴, 黄可龙, 张 静
(中南大学 化学化工学院, 长沙 410083)
摘 要: 以LiOH·H2O、 V2O5和NH4H2PO4为原料, C为还原剂, 采用高温固相法合成了锂离子电池正极材料磷酸钒锂(Li3V2(PO4)3)。 考察了合成温度等条件对产物组成和晶相的影响。 结果表明: 随着焙烧温度的升高, 杂相的衍射峰相对强度逐渐减弱, 当煅烧温度达到800℃时, 杂相衍射峰消失, 所得样品为纯相的Li3V2(PO4)3样品; 按Li、 V、 P的摩尔比为3∶2∶3将原料在800℃下焙烧24h, 合成得到正极材料。 该材料在0.1C充放电制度下, 首次充电比容量达到135mA·h/g, 首次放电比容量130mA·h/g, 充放电效率达96.3%; 经过20次循环后, 放电容量仍然高达110mA·h/g。 对经过20次循环后的样品进行了X射线衍射分析, 结果发现, 经过20次循环后样品仍然具有单斜晶体结构, 样品各主要衍射峰强度都急剧减弱, 说明样品在充放电过程中晶体结构发生了变化; 采用最小二乘法对样品充放电前后的晶胞参数进行了计算, 发现样品在经过充放电循环后晶胞参数都有不同程度的增加, 晶胞体积增大0.6%左右。
关键词: Li3V2(PO4)3 ; 正极材料; NASCION结构 中图分类号: TM912.9
文献标识码: A
Synthesis and electrochemical characteristics of
cathode materials Li3V2(PO4)3 for lithium-ion batteries
LIU Su-qin, TANG Lian-xing, HUANG Ke-long, ZHANG Jing
(School of Chemistry and Chemical Engineering,Central South University, Changsha, 410083, China)
Abstract: The cathode material Li3V2(PO4)3 was prepared by solid-state reaction of LiOH·H2O, V2O5 and NH4H2PO4, with carbon as the reduction agent. The effects of reaction conditions such as temperature on the structure were investigated by X-ray diffractrometry. The results show that the sample synthesized from the raw materials with molar ratio of Li, V and P of 3∶2∶3 at 800℃ for 24h has a pure monoclinic crystal structure, which derives a initial discharge specific capacity of 130mA·h/g. After charged/discharged at 0.1C rate for 20cycles, the sample retaines a discharge specific capacity of 110mA·h/g. XRD patterns show that it retains monoclinic crystal structure, but the intensity of diffraction declines sharply. Least square method was used to calculate the unit-cell parameters of the sample before and after cycling, it is found that all of the parameters increase to some extend, and the unit-cell volume increases by 0.6%.
Key words: Li3V2(PO4)3; cathode materials; NASCION structure
具有NASCION结构的化合物Li3M2(XO4)3(其中M=V, Fe等, X=P, S, As, Si等)由于其在充、 放电过程中的稳定性而受到广泛的注视[1-9]。 Goodenough等[2]认为具有NASCION结构的化合物有望作为高能量密度电池中的固体电解质。 Padhi 等[3]也认为具有NASCION结构的化合物是最具发展潜力的锂离子电池正极材料之一。 另一方面, 在NASCION结构中, 由于金属离子相隔较远, 以至于减小了电子的迁移率, 使得该结构具有较低的电子电导率[3, 10]。 通常的解决方法是通过掺杂对材料进行改性, 提高电子电导率[7]。
目前文献报道Li3V2(PO4)3作为锂离子二次电池正极材料的合成方法主要是高温固相法, 且都是用纯H2作为还原剂[4, 11]。 其他软化学方法合成Li3V2(PO4)3正极材料还未见文献报道。 与软化学方法相比, 高温固相法有着重要的优势就是更易实现工业化。
Sato等[7]以Li2CO3为Li源, 采用高温固相法在高达1100℃的条件下合成了Zr掺杂的正极材料Li2.8(V0.9Zr0.1)(PO4)3 , 放电比容量为103mA·h/g. 本文作者采用LiOH·H2O作为Li源, V2O5和NH3H2PO4为原料, 合成了正极材料磷酸钒锂(Li3V2(PO4)3)。 考虑到C是一种很好的还原剂, Barker等[5]曾采用碳热还原法(carbo-thermal reduction)合成了一系列化合物。 本文作者结合原料钒需要还原以及合成材料电子电导率低的特点, 采用了碳热还原法。 向原料中加入过量C不但可以作为还原剂, 同时过量的C还可以作为导电剂, 提高材料的电子导电率, 从而提高其电化学性能。 同为固相法, 所采用的以C为还原剂比文献报道的以纯H2作为还原剂更具可行性, 更适合于工业化批量生产。
1 实验
将按化学计量比的LiOH·H2O(天津市化学试剂研究所), NH4H2PO4(广州化学试剂厂), 和V2O5(湖南湘中精细化学品厂)置于玛瑙研钵仔细研磨, 混合均匀。 将混合物送入SRJX-4-13型马弗炉中(长沙市远东电炉厂)以300℃左右预处理2~4h, 使其放出NH3、 H2O等。 随炉子自然冷却, 取出样品仔细研磨。 加入过量(25%)碳, 将样品与碳混合均匀, 然后将样品送入管式炉在N2保护下以800℃左右焙烧24h, 随炉温冷却至室温, 反应结束后取出样品用玛瑙研钵研磨准备做检测和电化学测试。
用XD-98型全自动X射线衍射仪进行样品的物相分析(CuKα)。 管电压为40kV, 管电流40mA, 扫描范围10°~70°, 扫描速度为4.0(°)/min。
用武汉力兴公司制造的PCBT-32D-D程控电池测试仪检测样品的电化学性能。 正极由合成样品、 乙炔黑和聚四氟乙烯(PTFE)按照80∶15∶5(质量比)组成, 将其混合均匀后, 置于真空干燥箱在120℃下烘干, 将烘干的样品在天津市科技高新技术公司制造的DY-20台式电动压片机上以20MPa压制成电极片, 以金属Li作为对电极, 电解液为1mol/L LiPF6/ECD+MC(1∶1)。 电池组装在充满氩气保护的MBRAUN手套箱中进行, H2O和O2浓度都小于1×10-6。 以0.1C进行恒电流充、 放电, 充电截至电压4.2V, 放电截至电压3.0V。 采用上海辰华仪器公司制造的电化学工作站进行循环伏安测试(CHI 660A程序)。
采用与文献[12]类似的方法对样品中残余碳含量进行了测定。 将一定质量的样品溶于1mol/L的硝酸中, 将溶液过滤, 用蒸馏水洗涤残留物, 然后干燥称取质量。
2 结果与讨论
2.1 温度对样品相组成的影响
为了考察不同煅烧温度对所得样品相组成的影响, 从微观角度分析煅烧温度对样品电性能影响的本质原因, 实验中对样品进行了X射线衍射分析, 结果如图1所示。 图1中曲线(a)、 (b)、 (c)、 (d)和(e)分别对应650、 700、 750、 800和850℃时合成的正极材料Li3V2(PO4)3的X射线衍射谱。
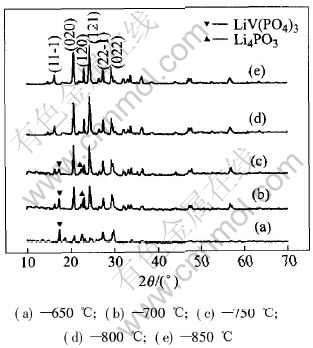
图1 不同温度下合成样品的X射线衍射谱
Fig.1 XRD patterns of samples synthesized at various temperatures
从图1可以看出, 随着反应温度的升高, 所得的Li3V2(PO4)3样品各晶面衍射峰的强度增加, 不同温度下各晶面衍射峰的相对强度不尽一致。 但是, 除650℃时(121)晶面还没有形成外, 衍射峰最强的晶面均为(121)晶面。 650、 700和750℃煅烧所得的样品中存在较多杂相峰。 随着温度的升高, 杂相的衍射峰相对强度逐渐减弱, 当煅烧温度达到800℃时, 杂相衍射峰消失, 所得样品为纯相的Li3V2(PO4)3样品。 这是因为温度对于Li3V2-(PO4)3晶核的形成核晶粒生长有很大的影响, 温度较低时, 离子扩散速度较小, 在相同时间内Li3V2-(PO4)3的构晶离子(Li+、 V3+、 PO3-4)来不及重排, 从而生成杂质相; 而温度升高原子振动加剧, 离子的扩散速度也增大, 因此温度升高有利于晶核的形成。 所以在相同时间内, 温度越高, 晶体生长越完善, 其各个晶面的衍射峰相对强度也越大。 在X射线衍射谱上观察不到晶态或无定形态碳的衍射峰, 同时也说明, 添加碳不会影响材料的晶体结构。
2.2 样品的电化学性能
2.2.1 循环伏安研究
常温下, 以不同扫描速率对样品进行了循环伏安扫描研究, 采用三电极体系, 工作电极为LiV2-(PO4)3, 对电极和参比电极均为Li片, 扫描电压范围2.7~4.6V, 结果如图2所示。
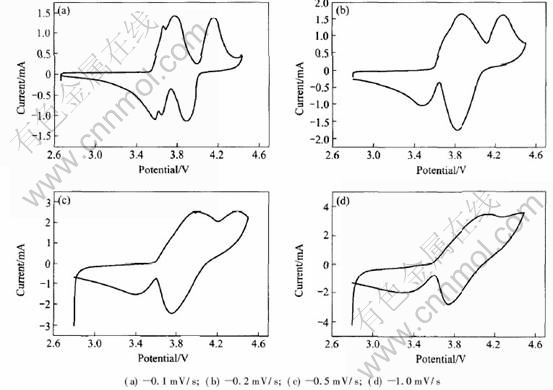
图2 不同扫描速率下样品的循环伏安图
Fig.2 CV curves of samples at various scanning speed
由图2可以看出, 较慢扫描速率下(0.1mV/s), 在扫描电压范围内, 有三对氧化还原峰, 充电(氧化) 时, 峰值分别为3.62、 3.73和4.10V; 放电(还原)时, 峰值分别为3.91、 3.68和3.58V; 低电势波峰间隔(ΔEp)分别为40和50mV, 均小于59mV, 说明电极的可逆性高; 高电势波峰间隔ΔEp=90mV。 随着扫描速度的增加, 峰宽加大, 前两对峰逐渐合并成为一对, 氧化峰向高电位移动, 还原峰向低电位移动, 极化增大。 当扫描速率达到1mV/s时ΔEp达到700mV, 说明电极反应为准可逆过程。 这可能是由于所制备的材料的电导率较低, 不太适用于大电流充放电, 与文献[3, 10]所报道的相一致。
在高速率扫描过后, 将模拟电池放置2h后,将同一样品重新采用0.1mV/s速率扫描, 结果如图3所示。 图3中曲线(a)所示为新做的模拟电池在0.1mV/s扫描速率下的循环伏安曲线; 曲线(b)表示在经过高速率扫描并放置一段时间后重新采用0.1mV/s速率扫描样品所得循环伏安曲线。 如图3所示, 经过高速率扫描后重新采用0.1mV/s扫描样品得到循环伏安曲线与第一次扫描一样具有三对氧化还原峰, 峰的位置没有发生偏移, 但是峰电流值有所减小, 表明在循环过程中材料的比容量有衰减。
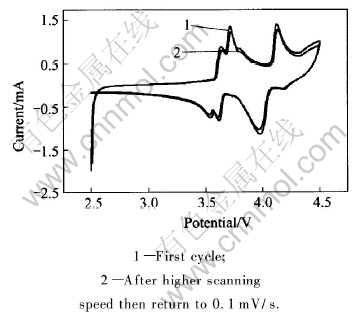
图3 样品0.1 mV/s扫描速率下的循环伏安图
Fig.3 CV curve of sample at speed of 0.1mV/s
2.2.2 充放电测试
以800℃下样品为例, 在常温下以C/10进行了充、 放电测试, 充电截止电压4.2V, 放电截止电压3.0V。 工作电极由合成样品、 乙炔黑和聚四氟乙烯(PTFE)按照80∶15∶5(质量比)组成, 以金属Li作为对电极, 电解液为1mol/L LiPF6/ECD+MC(1∶1)。 图4所示为800℃下合成样品首次循环充、 放电曲线。
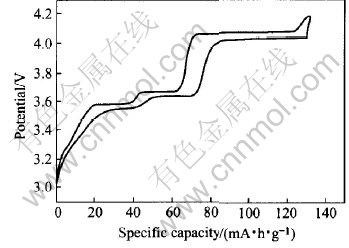
图4 合成样品的首次循环充放电曲线
Fig.4 First cycling curve of synthesized sample
由图4可知, 合成样品的充、 放电曲线都呈明显的3个平台, 充、 放电曲线呈L形, 表明放电过程为多相反应过程[13]。 样品首次充电比容量135mA·h/g, 放电比容量130mA·h/g, 与每个分子Li3V2(PO4)3脱出两个Li+的理论容量133mA·h/g 接近。 文献[4]的研究表明, 第三个锂离子在4.5V(vs Li/Li+)以上才能脱出。 考虑到本实验所用的电解液为LiPF6/ECD+MC体系, 在较高(>4.5V)的电压下容易分解, 因此, 未考察材料中第三个锂离子的脱、 嵌。
如图4所示, 样品的充、 放电曲线可以细分为3个区域, 分别对应Li3-xV2(PO4)3中x=0.0~0.5, x=0.5~1和x=1~2, 每个范围内都可以观察到明显的电压平台。 前两个Li+脱出的平均电压分别为3.62V(vs Li/Li+)和4.07V(vs Li/Li+)。 其中第一个Li+分两步脱出, 分别对应的电压平台3.58V(vs Li/Li+)和3.66V(vs Li/Li+), 对应比容量分别为33和34mA·h/g, 这与图2所示的循环伏安曲线在3.5~3.8V范围内有两对氧化还原峰相一致; 第二个Li+脱出对应电压平台4.07V(vs Li/Li+), 对应比容量67.5mA·h/g。 脱出的前两个Li+都是对应V3+/V4+氧化还原对, 所不同的是两个锂离子的位置不同[4, 14], 因此对应的位能不同, 第二个锂离子的位能更低, 更稳定, 因此脱出第二个锂离子需要的电压较高[4]。 放电时, 两个Li+重新嵌入LiV2(PO4)3中, 分别对应电压平台4.03, 3.64和3.55V。 充、 放电电压平台相差小于50mV, 表明了该体系具有高度的可逆性。
2.2.3 样品的倍率性能
考察了样品在不同倍率充放电下的性能, 分别以0.1、 0.2和0.5C对样品进行了充放电测试。 图5所示为样品在0.1、 0.2和0.5C下的首次充放电循环曲线。
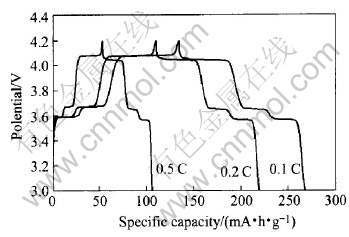
图5 不同倍率充、放电条件下样品的电性能
Fig.5 Electrochemical performance of sample charged/discharged at different rates
由图5可知随着充放电倍率的提高样品的首次充放电比容量逐渐减小。 以0.2C充放电样品首次放电比容量为115mA·h/g, 当达到0.5C时, 样品的首次放电比容量仅为53.6mA·h/g左右, 再次说明材料的导电性能较差, 不太适合大电流充放电。 这与前面循环伏安曲线得到的结论相一致。
2.2.4 样品的循环性能
为了考察样品的循环性能, 在上述充放电制度下(0.1C, 充电截止电压4.2V, 放电截止电压3.0V)对样品进行了循环充放电测试。 图6所示为前20次样品的放电比容量随循环次数的变化。
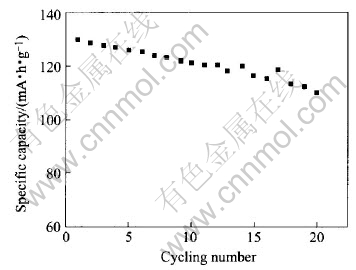
图6 0.1C充、放电条件下样品的循环性能
Fig.6 Cycling performance of sample charged/discharged at 0.1C rate
从图6可见, 随着循环次数的增加, 放电比容量逐渐减小, 第20次时样品的放电比容量仅有110mA·h/g, 为首次放电比容量的85%。 本文作者推测造成材料比容量衰竭的原因可能是充、 放电过程中活性物质的晶体结构有所改变, 因此实验中对经过20次充放电循环后的样品进行了X射线衍射分析。
图7给出了材料充放电前和经过20次充放电循环后的X射线衍射谱。 显然, 经过20次充放电循环后与充、 放电前样品的X射线衍射谱相似, 仍然具有单斜结构, 121晶面都具有最强的相对衍射强度, 并且没有其他杂相峰产生。 但是与充、 放电前相比, 121晶面和其他各主要峰的衍射强度急剧下降甚至消失, 说明晶体结构在充、 放电过程中遭到破坏, 与笔者推测样品充、 放电比容量下降的原因相一致。 对于所合成材料在充、 放电过程中晶体结构发生变化的原因有待于进一步研究。
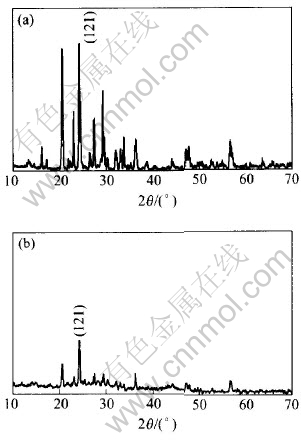
图7 充、放电循环前后样品的X射线衍射谱
Fig.7 XRD patterns of sample before charged (a) and after 20th cycle(b)
采用最小二乘法对样品充、 放电前后的晶胞参数做了计算, 比较其结果列于表1。
表1 合成样品的晶胞参数
Table 1 Unit-cell parameters for sample
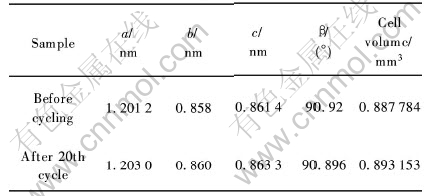
由表1可知, 样品的晶胞参数与文献[15, 16]报道的相一致。 在经过20次充放电后晶胞参数a、 b、 c均有不同程度的增加, 晶胞体积增大0.6%。 由于材料在脱出两个Li+形成LiV2(PO4)3结构其晶胞体积存在8.4%左右的变化[10], 因此材料在循环过程中可能存在分解粉化的情况, Saidi等[4]也有过这样的推测, 这可能同样是造成样品在循环过程中比容量衰减的原因, 有待进一步进行探讨。
3 结论
具有单一晶相组成的单斜结构的锂离子二次电池正极材料LiV2(PO4)3可以通过高温固相法, 以LiOH·H2O、 V2O5和NH3H2PO4为原料, C作为还原剂, 在N2气体保护下合成。 温度对样品的晶相组成具有较大影响。 800℃下合成的Li3V2-(PO4)3正极材料以0.1C进行充放电, 充电截止电压4.2V, 放电截止电压3.0V。 首次充电比容量达到135mA·h/g, 首次放电比容量130mA·h/g。 经过20次循环, 比容量为110mA·h/g。 进行充放电循环后, 材料的晶体结构有所变化。
REFERENCES
[1] Nanjundaswamy K S, Padhi A K, Goodenough J B, et al. Synthesis, redox potential evaluation and electrochemical characteristic of NASICON-related-3D framework compounds[J]. Solid State Ionics, 1996, 92: 1-10.
[2] Goodenough J B, Manivannan V, Padhi A K. Tuning the position of the redox couples in materials with NASICON structure by anionic subsitiution[J]. J Electrochem Soc, 1998, 145(5): 1518-1520.
[3] Padhi A K, Nanjundaswamy K S, Masquelier C, et al. Mapping of transition metal redox energies in phosphates with NASICON srtucture by lithium intercalation[J]. J Electrochem Soc, 1997, 144: 2581-2586.
[4] Saidi M Y, Barker J, Huang H, et al. Performance characteristics of lithium vanadium phosphate as a cathode materials for lithium-ion batteries[J]. J Power Sources, 2003, 119-121: 266-272.
[5] Barker J, Saidhi M Y, Swoyer J L. Electrochemical propertied of beta-LiVOPO4 prepared by carbothermal reduction[J]. J Electrochem Soc, 2004, 151(6): A796-A800.
[6] Masquelier C, Padhi A K, Nanjundaswamy K S, et al. New cathode materials for rechargeable lithium batteries: the 3-D framework structures Li3Fe2(XO4)3[J]. J Solid State Chem, 1998, 135: 228-234.
[7] Sato M, Ohkawa H, Yoshida K, et al. Enhancement of discharge capacity of Li3V2(PO4)3 by stabilizing the orthorhombic phase at room temperature[J]. Solid State Ionics, 2000, 135: 137-142.
[8] HUANG Huan, Shieh-Chieh Y, Tracy K, et al. Nanostructured composites: a high capacity, fast rate Li3V2(PO4)3/carbon cathode for rechargeable lithium batteries[J]. Adv Mater, 2002, 21: 1525-1528.
[9] Sylvain F, Frederic L C, Carole B, et al. Comparison between different LiFePO4 synthesis routes and their influence on its physico-chemical properties[J]. J Power Sources, 2003, 119-121: 252-257.
[10] Yin S C, Gronodey H, Strobel P, et al. Electrochemical property: structure relationships in monoclinic Li3-yV2(PO4)3[J]. J Am Chem Soc, 2003, 125(34): 10402-10411.
[11] Saidi M Y, Barker J, Huang H, et al. Electrochemical properties of lithium vanadium phosphate as a cathode materials for lithium-ion batteries[J]. Electrochemical and Solid-State Letters, 2002, 5(7): A149-A151.
[12] 吕正中, 周震涛. LiFePO4/C复合正极材料的结构与性能[J]. 电池, 2003, 33(5): 269-271.
L Zheng-zhong, ZHOU Zheng-tao. Structure and property of LiFePO4/C cathode materials[J]. Battery Bimonthly, 2003, 33(5): 269-271.
[13] 郭炳焜, 徐 徽, 王先友, 等. 锂离子电池[M]. 第一版.长沙: 中南大学出版社, 2002. 51-52.
GUO Bing-kun, XU Hui, WANG Xian-you, et al. Lithium-ion Batteries[M]. 1st ed. Changsha: Central South University, 2002. 51-52.
[14] Morgan D, Ceder G, Saidi M Y, et al. Experimental and computational study of the structure and electrochemical properties of Li3M2(PO4)3 compounds with the monoclinic and rhombohedral structure[J]. Chem Mater, 2002, 14: 4684-4693.
[15] Morgan D, Ceder G, Saidi M Y, et al. Experimental and computational study of the structure and electrochemical properties of monoclinic LixM2(PO4)3 compounds[J]. J Power Sources, 2003, 119-121: 755-759.
[16] Yin S C, Grondey H, Strobel P, et al. Charge ordering in lithium vanadium phosphate: electrode materials for lithiumion batteries[J]. J Am Chem Soc, 2003, 125(2): 326-327.
基金项目: 国家自然科学基金资助项目(20376086)
收稿日期: 2005-05-12; 修订日期: 2005-07-01
作者简介: 刘素琴(1966-), 博士, 副教授.
通讯作者: 黄可龙, 教授; 电话: 0731-8879850; E-mail: klhuang@mail.csu.edu.cn
(编辑 龙怀中)