DOI��10.19476/j.ysxb.1004.0609.2018.11.20
�����л�������ķ�Ӧ��Ϊ
����1������ǿ1���ܵ·�2��������1����С��1��������1����־��1�������1
(1. ���ϴ�ѧ ұ���뻷��ѧԺ����ɳ 410083��
2. ������ɽ��ҵ����˾����ɽ 663099)
ժ Ҫ������XRD��SEM-EDS (������)�о������ҵĹ��տ���ѧ�Լ����������Al��AlN��ˮ������������Һ�еķ�Ӧ��Ϊ����������������л�������Al��AlN�Ⱥ����϶࣬��AlN��������Al�ġ�������Al�������ο����������ڣ�Ҳ����SiǶ���γɺϽ�AlN�Դ������״����״�����������ڣ�Ҳ�����-Al2O3���棻����(��-Al2O3)���ڵ���̬��һ��NaCl�����ۼ����ڣ��ٲ��ֱ������ͷ�ɢ�����Ժ�������Al��AlN����ˮ��Ӧʱ����Ӧ��������Ӧ��С��AlN��Al����Ӧ��Al��ˮ��Ӧ���ɵ���������������Al�������谭�˷�Ӧ���С�����Ũ����������Һ��Ӧʱ�������е�Al��AlNѸ�ٷ�����ѧ��Ӧ��������0.5 h��Ӧ�ʾ��ﵽ80%���ϣ�����Al��AlN����Ӧ��Si��SiO2Ҳ�ᷢ����Ӧ��ͬʱ���¶�����������Al��AlN��ˮ��Ӧ��
�ؼ��ʣ����ң����������������տ���ѧ��ˮ����������
���±�ţ�1004-0609(2018)-11-2341-10���� ��ͼ����ţ�TF09���� ���ױ�־�룺A
�����������������У����������������[1-2]����������Ҫ���ڦ�-Al2O3��AlN��SiO2��MgO��Al��������Si��Al4C3���ʣ�Ҳ���ܺ��н϶��CaF2��NaCl��KCl��MgAl2O4��[3-5]������������һ�ֺ�����Դ����������һ��Σ�ϡ���������Һ�Ӵ�����Al��AlN��Si�Ȼ������෴Ӧ�����ױ�H2�ʹ̱�����NH3�����Ȼ��κͷ����οɽ�����Һ�У��Ӷ���Ⱦ������ˮ��[1, 6]����ˣ����ҵİ�ȫ��������һֱ���о����ȵ㣬Ҳ������������[1, 7]��
��ͳ��ת��¯(RSF)�ɻ��ս��������������һ����Ʊ�������ש���ͻ���ϵȷǽ�����Ʒ�͵�Ʒ���������ȡ������������̼��������������ʵ�(���ƷƷ�ʵ�)���ɱ�ƫ�ߡ����Ⱥͷ������Ѵ������豸��ʴ���ص�ȱ�㣬ͬʱ������ʵ����ȫ����������ˮ(��Һ)�Ӵ�Ҳ���ڽ϶�����[8-11]����������Ϊԭ�ϣ�ʪ���ϳɾۺ��Ȼ���(PAC)��AlPO4-5/CrAlPO-5����(��)-Al2O3��X�CAl��ˮ��ʯ(X=Mg��Ca��Zn)��(Mg,Si)Al2O4�⾧ʯ��Al-Si�Ͻ���ظ���[7, 12-14]��ʱ�ɱ��ͣ�����Ҫ��ȫ���������������ͽ�����Һ�е��Ȼ��κͷ����εȡ���ˣ����ҵİ�ȫ���ö��벻����������(Al��AlN��Si)���Ȼ��Ρ������εĴ�����SVEDBERG��[15]�о��˲�ͬpHֵ��85 ��ʱAlN��ˮ�ķ�Ӧ���ɣ�������ˮ�п����ɾ��в�ͬ������AlOOH��Al(OH)3�ࡣKRNEL��[16]���֣�AlNˮ�ⷴӦ֮ǰ�����յ��ڣ����յ��������¶ȵ����߶����̣�������ҺpHֵ�Ľ��Ͷ��ӳ���FUKUMOTO��[17]�о��������µ�100�������£���ĩ���ø÷�ĩ�ս��AlN�մɿ����ˮ����Ϊ��Ҳ��ΪAlN�ڷ���ˮ�ⷴӦ֮ǰ�����յ��ڣ��յ��������¶ȵ����߶����̣��ս���AlN�մɿ����������²�����ˮ�⣬��373 K��������ˮ�⣬ˮ����pHֵ���ﵽ8��������AlN��ˮ�ķ�Ӧ���Ʋ�δ��ֲ�����������[14]�����µ�[18]��������������������ķ�Ӧ���о�AlN��ˮ����Ϊ����ȷ���¶ȡ�Һ�̱ȡ���������ص�Ӱ����ɣ���������AlN�Ǻ�Al��Al2O3��Si������棬���Ժ������Ƕ�AlN��Ӧ��Ϊ��Ӱ�졣����������ʵ����Ҳ���֣�������Al��AlN��Si��Ӧ��Ϊ���ӣ���ˮ�б��ڼ�Һ�������Ͱ����ͷ�ʱ�䳤����Ҫԭ����������и�����տ���ѧ���ӣ��ڷ�Ӧ�����и����෴Ӧ��Ϊ�Ӱ������������һ������о�������ȷ���ۣ�Ҳ���������ҵ���లȫ�ۺ����á�
ּ��ʪ����ȫ�������ң��������������������л��Ժ�������(����������)��Ӧ��Ϊ���о��������и�����Ĺ��տ���ѧ�����������ڼ��Ժ�ˮ��ϵ�µķ�Ӧ��Ϊ��̽���˸����ض����һ��Ժ������෴Ӧ��Ӱ����ɡ�
1 ʵ��
1.1 ʵ��ԭ��
���Ҵ�����ij�����ѳ���ȡ�����������������������в��������ҡ����ҵ�������40~200 ��m֮�䣬d50Ϊ82.358 ��m(��ͼ1)��

ͼ1 ���ҵ����ȷֲ�
Fig. 1 Particle size distribution of aluminum dross
���ҵ�Xӫ�����(XRF)�������(����1)�����������е���ҪԪ��ΪAl��O��Cl��Na��F��Mg��Si��K��Ca����������Լ1.5%��Ԫ�ذ���Ti��Fe��Sr��S��V��Mn��In��Zn��P�ȡ�
��1 ��������ҪԪ�غ���
Table 1 Content of elements in aluminum dross (mass fraction, %)

1.2 ʵ�����
��ȡ3 g���Ҽ��뵽250 mLʢ����Һ�ĵ���Բ����ƿ�У�����ˮԡ�����Ʒ�Ӧ�¶ȣ��������裬����ϡ�������հ���������ˮ���ռ�������ʵ��������ͼ2��ʾ��
��Ӧ������Ӧ��Һ����ճ��ˡ���ˮϴ�ӣ�������60 ���º��24 h��Ȼ��������ٽ�����ò�����������

ͼ2 ʵ��װ������ʾ��ͼ
Fig. 2 Schematic diagram of experimental apparatus
1.3 ���Է���
ʹ��JSM-6360LV�ߵ����ɨ���������(�ձ����ӹ�˾)�۲���Ʒ����ò��ͬʱ��Ϊ��������������Ƕ�����ɣ�ȡһ���������Ҿ�������ˮ�Ҵ�����ˮ����ĥƬ���⣬Ȼ���ٽ��е羵��ɨ�������
ʹ��PW2424��Xӫ������Ƿ��������и�Ԫ�صĺ�����ʹ��LS-POP�ͼ������ȷֲ��Ƿ������ҵ���λ��(d50)��������ɲ����ձ���ѧ3014Z��X�������������(XRD)���з���������������Ϊ��Cu��K������Դ(��=1.5406 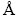 )���ܵ�ѹΪ40 kV��ɨ���ٶ�10 (��)/min������0.02 (��)/����ɨ��Ƕ�5��~75�㡣
)���ܵ�ѹΪ40 kV��ɨ���ٶ�10 (��)/min������0.02 (��)/����ɨ��Ƕ�5��~75�㡣
�����ռ�������ˮ����ֹ��ȷ��ⶨ������[19]��������ˮ���ⶨ���������
XRD����붨����������[20-21]��
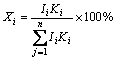 (1)
(1)
ʽ�У�XiΪi�������������Ii��Ij�ֱ�Ϊi��j����ǿ�����Ļ���ǿ�ȣ�Ki��Kj�ֱ�Ϊ ��
�� �ı�ֵ(��-Al2O3Ϊ�α���)��nΪ��������������
�ı�ֵ(��-Al2O3Ϊ�α���)��nΪ��������������
�˷�����û���ڱ�������Ҳ�ɽ��з��������ǵ�������������ᾧ�Ȳ�ͬ���붨��������Χ����5%��
�����л�������Al��AlN�ķ�Ӧ�ʦǣ�
 (2)
(2)
ʽ�У�V1Ϊ��Ӧ�ͷų���H2��NH3�����V0Ϊ������Al��AlN��ȫ��Ӧ���ͷų�H2��NH3�����
2 ���������
2.1 ��������Ҫ����ͷֲ�
����XRDͼ��ͼ3�������ʾ�������е���Ҫ����Ϊ��-Al2O3��AlN��Al��NaCl��Si��CaF2��MgAl2O4��KAl11O17��SiO2������Si��SiO2���������Ϊ���������١����ڦ�-Al2O3�ڳ��³�ѹ���ȶ���������Һ��Ӧ��������о��ж�����Ϊ�ǻ������࣬��AlN��Al��Si�ȶ���Ϊ�������ࡣ����Si�������к������٣�����Al��Ӧ��Ϊ���ƣ��ʲ��ص㿼�졣

ͼ3 ���ҵ�XRD��
Fig. 3 XRD pattern of aluminum dross
��һ����������44.69%���к���������з���(����2)�������ʾ��������68.58%Ϊ���Ժ������࣬�����������л��Ժ����������࣬������������Խ��١�ҲԤʾ�Ÿ�����Σ���Խϴ�
��2 ���Һ������������Ļ�ѧ���
Table 2 Al content in aluminum bearing substances of aluminum dross
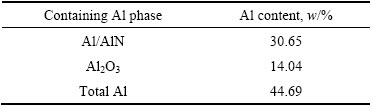
����XRD�ף���һ���붨���������Ժ�������ֲ����ɣ������ʾ���Ժ���������AlNռ65.4%��ÿ3 g���������ۿ��ͷ�185 mL NH3������Alռ34.6%��ÿ3 g���������ۿ��ͷ�223 mL H2��
���ҵ�SEM����ͼ4��ʾ����ͼ4��֪�����ҵ����ȷֲ��Ӽ�ʮ��200 ��m���ȣ������ȷֲ�ͼ1һ�¡������и��������ò���죬������ɳʾۼ�״̬��������ò�г���״����Ƭ״������״������״��˿��״�ȣ���ͬ��������֮��ֲ��Ƚ�ɢ���������������������Լ�����������

ͼ4 ���ҵ�SEM��
Fig. 4 SEM image of aluminum dross
�Բ�ͬ���Ϳ��������һ���о�Al��Si��O��Na��ClԪ�صķֲ���Ԫ����ɨ������ͼ5��ʾ��
ͼ5(a)��ʾΪ���������ں������ܺ����ɶ�ղ�ͬ���֡����ܴ���Ҫ��Na��ClԪ�أ��ҷֲ����ȣ�����NaCl���ࣻͬʱ������Al��OԪ�أ�ΪAl2O3���ࣻҲ����������SiԪ�ء�����������ο�������״����������������ɣ����ο�����Ҫ����Al��SiԪ�أ���AlԪ��Ϊ��������Al-Si����Ƕ��������Χδ�۲OԪ�صİ�����������Ͻ�Ϊ�����������ɿ�����Ҫ��Al��OԪ����ɣ��Ԧ�-Al2O3��ʽ��ϣ�������ʵ��λ��Ҫ�ǿ�����NaCl�ࡣ���Ϸ�����֪��������Al��O����γɦ�-Al2O3����ò�����г�˿��״�������״�ȣ�NaCl�ۼ����ڣ����Զ�������������ڣ�Ҳ����Al2O3�����Ƕ�������е���Al��Si�����Σ�Al-Si����Ƕ���γ��ȶ��Ͻ𣬱���������Ĥ��
������������Ҫ������е������ڵ����࣬Ҳ���Ƕ�������������࣬�������������ˮ���Ӧ��ΪӦ���Ǹ��ӵġ�
2.2 ������ˮ��Ӧ��Ϊ

ͼ5 ���ҵ�SEM�����Ԫ����ֲ�
Fig. 5 SEM images of aluminum dross and section- distribution of elements (Al, Si, O, Na and Cl)
�����л�������Al��AlN��ˮ��ϵ�¿��ܷ����Ļ�ѧ��Ӧ����ʽ���£�
 (1)
(1)
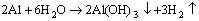 (2)
(2)
�ڱ���ʵ�������У�������Al��AlN�ķ�Ӧ����ʱ��ı仯������ͼ6��ʾ����ͼ6�п��Կ�����25 ��ʱ��8 h��Al��ˮ��������Ӧ��8 h��ʼ������Ӧ��24 h��Ӧ��ԼΪ9%����Զ��ԣ�AlN����ˮ��Ӧ�����淴Ӧʱ����ӳ�����Ӧ�������ߣ�24 h��Ӧ��Լ12%���������յ��ڣ����봿AlN��Ӧ��Ϊ��ͬ[16-17]����߷�Ӧ�¶�Ϊ60 �棬Al��AlN��ˮ��Ӧ�������ƣ�����Ӧ�ʾ������������뽪����[14]�Ľ��һ�¡���֮����ˮ�У�Al��AlN�ķ�Ӧ��Ϊ��һ�£���Ӧ�ʲ��ߣ�Al��Ӧ�ʺ��ڱ仯��С��AlN����Ӧ�����¶ȶԷ�Ӧ��Ӱ�����������Al��Ϊ�ˣ���Է�Ӧ�������������ֲ�������������Al��Al��ˮ�ķ�Ӧ��Ϊ��
2.3 ������ˮ��Ӧ������
������ˮ��Ӧ����XRD����ͼ7��ʾ���Ա�ͼ3��������ˮ��Ӧ1 h��ͼ7(a)�г�NaCl���������ʧ�⣬���еĦ�-Al2O3��KAl11O17��MgAl2O4��CaF2��Si��SiO2��Al��AlN�ȵ���������ԡ���Ӧ24 h��ͼ7(b)�г���������Al(OH)3������ǿ�壬Ҳ�Կɼ���-Al2O3��KAl11O17��MgAl2O4��CaF2��AlN������壬NaCl��SiO2��Si��Al�������ʧ����ˣ�60 ����1 h�ڣ�������NaCl���ܽ������Һ�У�Al��AlN��������Ӧ����ͼ6��������

ͼ6 ʱ������͵�������ˮ��Ӧ�ʵ�Ӱ��
Fig. 6 Effect of time on reaction rate of Al and AlN in water at different temperatures (Reaction time: t=0-24 h, aluminum dross: 30 g/L)

ͼ7 ������ˮ��Ӧ�������XRD��
Fig. 7 XRD patterns of residue after aluminum dross reacting with water (��=60 ��)
��Ӧ������SEM��Ԫ����ɨ������ͼ8��ʾ����ͼ8�п�֪����Ӧ���д���Al��AlN��Al2O3�����࣬ͬʱ�ɹ۲�ֲ�Si-O�Ĵ��ڣ�������û�з�����Ӧ����ʵ���ο���Ϊ����Al(������������Ͻ�)������Al�������ܱ߹۲쵽�ḻ��OԪ��(��ͼ8(b)��8(c))�����ͼ5��7���������Ϊ��������ˮ��Ӧ������������������������ΪAl����������������������һ�����㣬�谭����ˮ�ķ�Ӧ������Al�ķ�Ӧ��ά����һ��ֵ(��ͼ6(a))��ͬʱ��Ƕ����Al��������NaClû�б�����ܽ⣬˵���������Ƕ��������Ӱ���˿�����NaCl���ܽ⣻Si�����Է�Ӧ��
2.4 ����������������Һ��Ӧ��Ϊ
������Al��AlN������������Һ��ϵ�¿��ܷ����Ļ�ѧ��Ӧ����ʽ���£�
 (3)
(3)
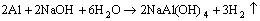 (4)
(4)
������Al��AlN������������Һ��Ӧ����ʱ��仯��ͼ9��ʾ����ͼ9�п��Կ�����������300 g/L����������25 ���60 ���¾����ҷ�Ӧ���ӽ���Ӧ��ȫ���Ҷ���0.5 h�ڷ�Ӧ�ʴ�80%���ϡ���25 ���£�3 h�ڵ���Al��AlN���������Ʒ�Ӧ�ʴ�97%���ϣ�����60 ��ʱ��Al�ķ�Ӧ��1 h֮�������ȶ�����98.6%��AlN�ķ�Ӧ��2 h֮�����ں㶨����97.3%���ɴ˿ɼ�����300 g/L����������Һ�£������е�Al��AlN�������䷴Ӧ�ͷų�H2��NH3�����¶�Խ�ߣ���Ӧ����Խ����Զ��ԣ�Al���������Ƶķ�Ӧ�ʸ���AlN���������Ƶķ�Ӧ�ʣ�������ˮ�з�Ӧ��Ϊ��ͬ��Al��AlN�ڼ�Һ�еĿ��ٷ�Ӧ��Ϊʪ��������ϵ�л���������һ�������ѡ�
2.5 ����������������Һ��Ӧ������
����������������Һ��Ӧ����XRD��ͼ10����ͼ10(a)�пɼ�����Ӧ���е�������Ҫ�Ц�-Al2O3��KAl11O17��All2MgO4��CaF2�ȣ�AlN������������Al������������˵��Al��AlN�����Է�Ӧ��NaCl��������ʧ��NaCl������Һ�С���ͼ10��b)��AlN�����������Al���������ʧ��������������������Һ��Ӧ����XRD��Ҳ��֪�������е�Al��AlN��������Ũ����������Һ��Ӧ���ҿ��Կ���Al�ķ�Ӧ���졣���ͼ7�н������֪���������Ƕ��������ʣ��ɴ˿�ʹԤ����-���ۺ����ø��ӻ���
��ͼ10(a)��(b)�л��ܷ��֣�Si��SiO2������嶼��ʧ����˵����Ũ���У������������·�Ӧ���������˺�����������Һ��
 (5)
(5)
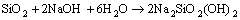 (6)
(6)
��Ӧ����SEM��Ԫ����ɨ������ͼ11����ͼ11��֪����Ũ�Ӧ0.5 h��Ӧ���д������ڵ�Ԫ������Al��O����Al��O��ɨͼ������ص�����Ҳ�е���Al-Si��������(��ͼ5������II�IJ�ͬ)������Al��������������һ������ͼ8������ͬ���ڼ���ϵ��Al��Ӧ������������Һ�����γ���������Ĥ��
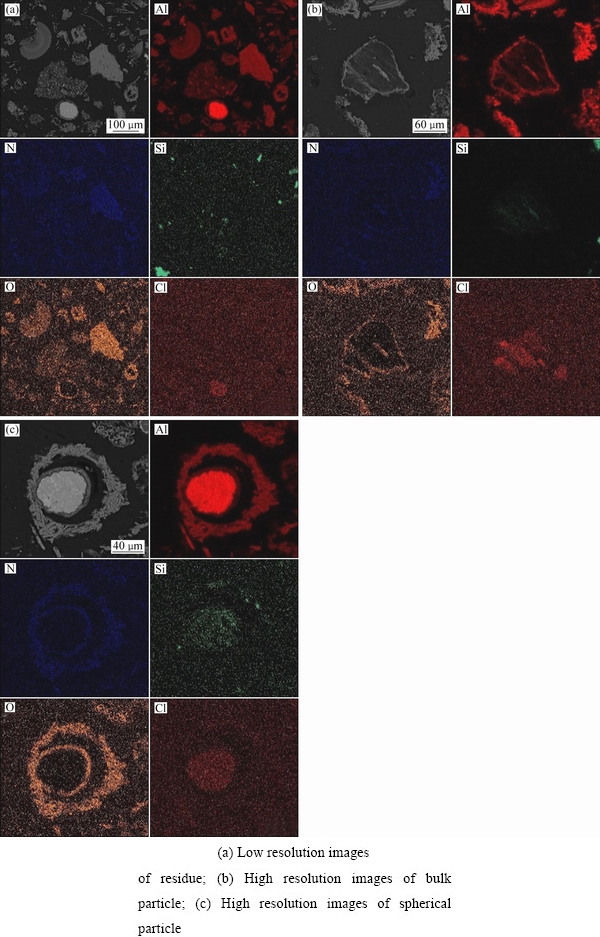
ͼ8 ������ˮ��60 ���·�Ӧ1 h�������Ԫ����ֲ�
Fig. 8 Section-distribution of elements (Al, N, Si, O and Cl) for residue after aluminum dross reacting with water at 60 �� for 1 h

ͼ9 ʱ������͵��������������Ʒ�Ӧ�ʵ�Ӱ��
Fig. 9 Effect of time on reaction rate of Al and AlN in NaOH solution at different temperatures (��NaOH=300 g/L, aluminum dross: 30 g/L)
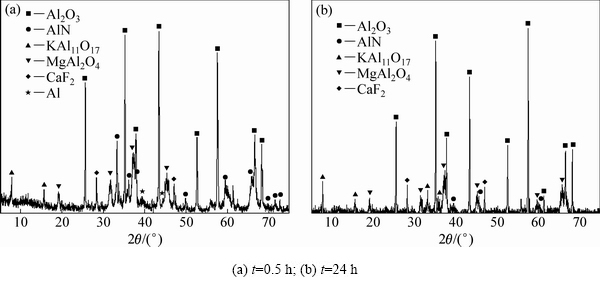
ͼ10 �������������Ʒ�Ӧ����XRD��
Fig. 10 XRD patterns of residue after aluminum dross reacting with NaOH solution (��=25 ��)
���ɹ۲쵽Al��N��OԪ����ɨͼ���ص�����AlN�Է��ο�״���֣������ϴ���Si�����Կ���״������������Ƕ����ʽ���ڡ��������������Al��AlN��Si��������˷�Ӧ������XRD�������һ�¡�
3 ����
1) ��������Ҫ����Ϊ��-Al2O3��AlN��Al��NaCl��Si��CaF2��MgAl2O4��KAl11O17��SiO2��������Al�������ο������ڣ�����SiǶ������������Ͻ�AlN���Դ������״����ʽ���ڣ�����(��-Al2O3)���ڵ���̬��һ��NaCl��ۼ����ڣ�Ҳ��Ƕ���ڦ�-Al2O3�С�������������ˮ������Ũ���У����л�������ɷ�Ӧ���Ȼ��οɽ�����Һ���������������ڲ����С�
2) ������������Al��AlN��ˮ��Ӧ�ʵͣ���Ӧ������AlN��Al����Ӧ���¶�����������Al��AlN��ˮ��Ӧ��Al��ˮ��Ӧ������������������Al�������谭�˷�Ӧ���У������������������е��Ȼ����ܽ�����Ҳ������Si����û�з�Ӧ��
3) Ũ����������Һ�У������е�Al��AlNѸ�ٷ�����ѧ��Ӧ��������0.5 h��Ӧ�ʾ��ﵽ80%���ϣ�2~3 h��Ӧ�ʴ�97%���ϣ���Ӧ�ų�H2��NH3��Si��SiO2Ҳ�ᷢ����Ӧ���ɹ����ƽ�����Һ��ͬʱ����Ũ�������£�Al�ķ�Ӧ����ǿ��AlN�ģ���������������������㡣
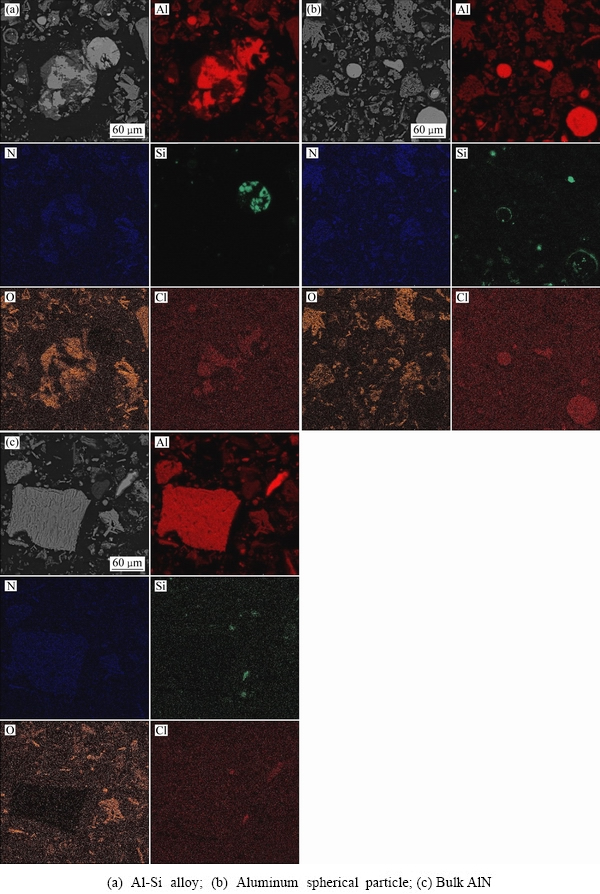
ͼ11 ����������������Һ��25 ���·�Ӧ0.5 h�������SEM�����Ԫ����ֲ�
Fig. 11 SEM images of residue and section-distribution of elements (Al, N, Si, O and Cl) for residue after aluminum dross reacting with NaOH solution at 25 �� for 0.5 h
REFERENCES
[1] HONG J P, WANG J, CHEN H Y, SUN B D, LI J J, CHEN C. Process of aluminum dross recycling and life cycle assessment for Al-Si alloys and brown fused alumina[J]. Transactions of Nonferrous Metals Society of China, 2010, 20(11): 2155-2161.
[2] ��ѧ��, �� ��, ���컪, �� ��. �������ҵ��¼��������о�[J]. ���ϴ�ѧѧ��(��Ȼ��ѧ��), 2012(3): 809-814.
GUO Xue-yi, LI Fei, TIAN Qing-hua, JI Kun. Recovery of aluminium from secondary aluminum dross using low-temperature alkaline smelting[J]. Journal of Central South University(Science and Technology), 2012(3): 809-814.
[3] MANFREDI O, WUTH W, BOHLINGER I. Characterizing the physical and chemical properties of aluminum dross[J]. JOM, 1997, 49(11): 48-51.
[4] FUKUMOTO S, HOOKABE T, TSUBAKINO H. Reaction between aluminum and water[J]. Journal of Japan Institute of Light Metals, 1998, 48(4): 199-203.
[5] ���콨, ���˱�, ������, �� ��, �� ��, �� ��. X�����������ҷ����е�Ӧ��[J]. ��������ѧ��, 2012, 31(s1): 219-221.
ZHANG Qing-jian, DING Shi-bing, FENG Li-li, SONG Fei, GUAN Song, GUO Bing. Application of X-ray techinque in analysis of aluminium dross[J]. Journal of Instrumental Analysis, 2012, 31(s1): 219-221.
[6] �� ��, ������, ���Ե�. �����ۺ����ù��ռ�����չ[J]. ��ɫ��������, 2016, 6(6): 45-49.
WU Long, HU Tian-lin, HAO Yi-dang. Progress of utilization technology for aluminum ash[J]. Nonferrous Metals Engineering, 2016, 6(6): 45-49.
[7] �����, ���Ʒ�, �����, ����, �� . �����ۺϻ������õĹ����⼼����״������[J]. �����, 2015(6): 1-4.
CHAI Deng-peng, ZHOU Yun-feng, LI Chang-lin, WANG Yan-fang, LIU Zhuo. The technology status and trends of comprehensive recovery and utilization of aluminum dross both at home and abroad[J]. Light Metals, 2015(6): 1-4.
[8] ��NL N, DROUET M G. Comparison of salt-free aluminum dross treatment processes[J]. Resources Conservation & Recycling, 2002, 36(1): 61-72.
[9] YOSHIMURA H N, ABREU A P, MOLISANI A L, DE CAMARGO A C, PORTELA J C S, NARITA N E. Evaluation of aluminum dross waste as raw material for refractories[J]. Ceramics International, 2008, 34(3): 581-591.
[10] EWAIS E M M, KHALIL N M, AMIN M S, AHMED Y M Z, BARAKAT M A. Utilization of aluminum sludge and aluminum slag (dross) for the manufacture of calcium aluminate cement[J]. Ceramics International, 2009, 35(8): 3381-3388.
[11] LUCHEVA B, TSONEV T, PETKOV R. Non-waste aluminum dross recycling[J]. Journal of the University of Chemical Technology and Metallurgy, 2005, 40(4): 335-338.
[12] ������, �� ƽ, л���, �� ��. �����м���ֻ��ռ��ۺ������о���չ[J]. ������ͨ��, 2017, 36(6): 1951-1956.
ZHANG Ning-yan, NING Ping, XIE Tian-jian, DUAN Gang. Research progress on recycling and comprehensive utilization of aluminum dross[J]. Bulletin of the Chinese Ceramic Society, 2017, 36(6): 1951-1956.
[13] �� ��, ��ѧ��, ���컪. ���������Ʊ���-Al2O3����[J]. �����Ƽ���ѧѧ��, 2012, 34(4): 383-389.
LI Fei, GUO Xue-yi, TIAN Qing-hua. Preparation process of ��-Al2O3 from secondary aluminium dross[J]. Journal of University of Science and Technology Beijing, 2012, 34(4): 383-389.
[14] �� ��, ������, ���Ѷ�, �� �, Ҧ Ȫ. ������AlN��ˮ����Ϊ[J]. �й���ɫ����ѧ��, 2012, 22(12): 3555-3561.
JIANG Lan, QIU Ming-fang, DING You-dong, SU Nan, YAO Quan. Hydrolysis behavior of AlN in aluminum dross[J]. The Chinese Journal of Nonferrous Metals, 2012, 22(12): 3555-3561.
[15] SVEDBERG L M, ARNDT K C, CIMA M J. Corrosion of aluminum nitride (AlN) in aqueous cleaning solutions[J]. Journal of the American Ceramic Society, 2010, 83(1): 41-46.
[16] KRNEL K, KOSMAC T. Protection of AlN powder against hydrolysis using aluminum dihydrogen phosphate[J]. Journal of the European Ceramic Society, 2001, 21(10): 2075-2079.
[17] FUKUMOTO S, HOOKABE T, TSUBAKINO H. Hydrolysis behavior of aluminum nitride in various solutions[J]. Journal of Materials Science, 2000, 35(11): 2743-2748.
[18] �� ��, ������, �� ˶, ФϸԪ. ��Ӧ���淨��������AlN��ˮ����Ϊ[J]. �й���ɫ����ѧ��, 2016, 26(4): 919-927.
ZHANG Yong, GUO Zhao-hui, WANG Shuo, XIAO Xi-yuan. Hydrolysis behavior of AlN in aluminum dross with response surface methodology[J]. The Chinese Journal of Nonferrous Metals, 2016, 26(4): 919-927.
[19] HJ 536��2009. ˮ�� �����IJⶨ ˮ����ֹ��ȷ�[S].
HJ 536��2009. Water quality��Determination of ammonia nitrogen ��Salicylic acid spectrophotometry[S].
[20] LI X, XU X, ZHOU Q, QI T, LIU G, PENG Z, CUI Y, LI J. Ca3WO6 prepared by roasting tungsten-containing materials and its leaching performance[J]. International Journal of Refractory Metals & Hard Materials, 2015, 52: 151-158.
[21] AL-JAROUDI S S, UL-HAMID A, MOHAMMED A R I, SALIH S. Use of X-ray powder diffraction for quantitative analysis of carbonate rock reservoir samples[J]. Powder Technology, 2007, 175(3): 115-121.
Reaction behavior of active phases in aluminum dross
LIU Gui-hua1, HUANG Wen-qiang1, XIONG De-fen2, WANG Hong-yang1, LI Xiao-bin1, ZHOU Qiu-sheng1, PENG Zhi-hong1, QI Tian-gui1
(1. School of Metallurgy and Environment, Central South University, Changsha 410083, China;
2. Yunan Wenshan Aluminium Co., Ltd., Wenshan 663099, China)
Abstract: The mineralogy of aluminum dross and the reaction behavior of the active phase (Al and AlN) in water and sodium hydroxide solution were investigated by XRD and SEM-EDS (microanalysis). The results indicate that more Al and AlN occur in aluminum dross, and AlN content is more than Al content. Al exists alone as spherical particles or appears in Al-Si alloy. AlN can exist alone or co-exist with ��-Al2O3 in the shape of large particles or needle-like particles, respectively, corundum (��-Al2O3) appearance is irregular. NaCl occurs alone or appears together with other phases, Al or AlN reacts with water slowly. AlN is more active compared with Al in water. Moreover, the formation of aluminum hydroxide on Al particle limits the reaction of Al in water. However, Al or AlN quickly reacts with the concentrated NaOH solution with reaction rate of above 80% at 25 �� for 0.5 h, Al reacts more quickly as comparison with AlN in NaOH solution. Meanwhile, Si and SiO2 also react with the concentrated NaOH solution. In addition, elevating temperature promotes the reaction of AlN and Al in water or NaOH solution.
Key words: aluminum dross; aluminum; aluminum nitride; mineralogy; water; sodium hydroxide
Foundation item: Project(51604309) supported by the National Natural Science Foundation of China
Received date: 2017-08-24; Accepted date: 2018-01-05
Corresponding author: LIU Gui-hua; Tel: +86-731-88830453; E-mail: liugh303@163.com
(�༭ ����)
������Ŀ��������Ȼ��ѧ����������Ŀ(51604309)
�ո����ڣ�2017-08-24�������ڣ�2018-01-05
ͨ�����ߣ��������ڣ��绰��0731-88830453��E-mail��liugh303@163.com