基于空间模糊C均值与区域生长的腹部CT序列图像肾脏自动分割
王晓红,赵于前,廖苗,刘苗苗
(中南大学 地球科学与信息物理学院,湖南 长沙,410083)
摘要:针对腹部CT序列图像因相邻器官灰度相似以及部分容积效应等造成的肾脏分割困难问题,提出一种基于空间模糊C均值以及区域生长的腹部CT序列图像肾脏自动分割方法。首先应用经典阈值法以及形态学重构去除肋骨和脊椎,然后对图像各向异性扩散滤波,再利用空间模糊C均值对肾脏图像进行聚类。当相邻切片分割结果的相对面积变化率超出预定范围时,算法自动选择区域生长法对该图像进行重新分割,且区域生长法受空间模糊C均值算法的约束。最后,应用形态学滤波对分割结果进行处理。通过对CT序列图像进行肾脏分割试验,结果表明本文算法是可行和有效的。
关键词:CT序列;肾脏分割;各向异性扩散滤波;空间模糊C均值;区域生长
中图分类号:TP391.4 文献标志码:A 文章编号:1672-7207(2014)10-3463-07
Automated kidneys segmentation from abdominal CT scans based on spatial fuzzy C-means and region growing
WANG Xiaohong, ZHAO Yuqian, LIAO Miao, LIU Miaomiao
(School of Geosciences and Info-Physics, Central South University, Changsha 410083, China)
Abstract: Considering that the kidneys segmentation from abdominal computer tomography (CT) scans is a great challenge for image processing because of the gray level similarity of adjacent organs, partial volume effects and so on, a novel method was proposed based on the spatial fuzzy C-means and region growing to segment kidneys from CT scans automatically. Firstly, the classical threshold method and the morphological reconstruction were applied to remove spine and fibs. Then the anisotropic diffusion filter was used to smooth the images, followed by the spatial fuzzy C-means to classify pixels belonging to kidneys. When the change rate of kidneys region area between two adjacent slices exceeds a defined range, the proposed method switches automatically to segment kidneys by region growing, whose seeds were constrained by the spatial fuzzy C-means. Finally, the morphological filtering method was used to smooth the segmented results. The results show that the proposed method can segment kidneys from CT scans successfully and effectively.
Key words: CT scans; kidneys segmentation; anisotropic diffusion filter; spatial fuzzy C-means; region growing
腹部器官的分割在医学图像处理领域具有重要意义。由于腹部医学图像各器官的灰度相近,相邻器官之间具有连接性以及受部分容积效应的影响,腹部器官的自动分割成为医学图像分割中的难点。目前,国内外学者已经提出很多腹部器官分割方法,主要包含水平集方法[1-3]、神经网络[4-6]以及图割[7-8]等。文献[1]通过2次种子区域增长法来确定大致的肝脏轮廓初始区域,然后用水平集方法通过设定的迭代次数最终将肝脏的边缘收敛在最佳位置。文献[2]对引入先验知识的活动轮廓模型进行演化,对被遮挡的肝脏具有较好的分割效果。文献[3]首先对肝脏等医学图像进行模糊聚类,然后将聚类结果作为水平集函数的约束力,引导水平集函数的精确演化。文献[4]提出了一种基于灰度均值、标准差、不对称度等优化特征的人工神经网络识别方法,这些统计特征不能有效区分2个纹理或统计属性相近的器官及组织。文献[5]提出了一种基于多层感知器神经网络的肝脏图像分割算法,该算法首先计算肝脏CT图像的均值、方差以及距离变换,然后利用多层感知器神经网络实现肝脏分割。文献[6]结合迭代分水岭算法以及多层感知器神经网络对肝脏图像进行分割,首先利用形态学方法增强肝脏图像,计算并比较分水岭算法以及神经网络对肝脏图像特征提取结果,对分水岭算法参数进行调整,从而约束分水岭算法对肝脏图像进行准确分割,避免了分水岭迭代过程中出现的过分割问题。文献[7]提出了一种由阈值引导图割初始化的方法,该方法可以对几何形状复杂的肝脏进行自动分割。文献[8]利用图像边界以及局部区域信息构成全局最优化框架,从而指导图割方法对肝脏CT序列的分割过程。肾脏的形态以及功能状态对肾脏疾病的分析诊断具有重要的指导作用,对肾脏图像的准确分割与三维重建是某些肾脏疾病诊断与治疗的重要前提,如肾衰竭、肾移植等。文献[9]提出了一种基于非刚性图像配准的活动形状模型,该模型可以对肾脏图像进行较准确分割。文献[10]首先给出了目标物体的先验灰度模型,然后利用图割方法对肾脏图像进行分割。文献[11]对肾脏位置进行统计估计,然后利用自适应阈值方法去除非肾脏部分的器官或者组织,最后利用基于标记的区域生长法得到最终肾脏分割结果。该算法依赖于对肾脏位置的精确估计,且对与周围器官或组织灰度相近的肾脏分割准确率低。为此,本文作者研究基于空间模糊C均值与区域生长的CT序列图像肾脏自动分割方法。首先采用经典阈值法以及形态学重构去除肋骨和脊椎,然后对图像进行各向异性扩散滤波,再应用空间模糊C均值对肾脏图像进行聚类。当空间模糊C均值分割结果的相对面积变化率超出预定范围时,自动转为用区域生长算法进行重新分割。且区域生长算法同时受空间模糊C均值算法的约束,即由上一切片空间模糊C均值聚类分割结果来确定当前切片初始种子点位置,避免手动选择区域生长种子点的过程。最后,应用形态学滤波对分割结果进行后处理。
1 算法描述
1.1 预处理
具体算法流程如图1所示。为了减少CT序列图像中其他组织或器官对肾脏分割的影响,需要在预处理阶段去除脊椎和肋骨等组织。肾脏图像预处理见图2。首先,对CT切片(图2(a))进行灰度拉伸变换,并应用经典阈值法去除脂肪组织,然后采用行列映射,找到图像中非零像素点所在区域。腐蚀该区域,将区域外部的脊椎以及肋骨作为标记图像f。再对去除脂肪组织的图像r进行形态学重构,得到脊椎和肋骨图(图2(b))。去除脊椎和肋骨的切片如图2(c)所示。最后根据相邻切片空间连接信息,去除整个CT序列图像的脊椎和肋骨,具体步骤如下。
Step 1 创建结构元素s;
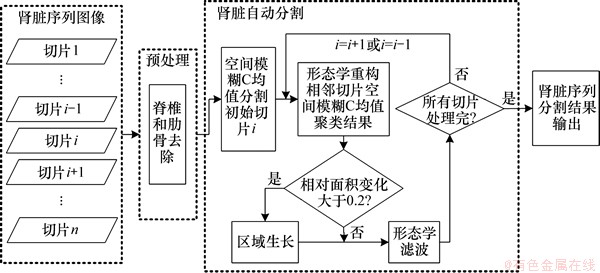
图1 本文算法流程图
Fig. 1 Flowchart of the proposed method

图2 肾脏图像预处理
Fig. 2 Preprocesses of kidney images
Step 2 初始化标记图像h1,令h1=f;
Step 3 重复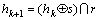 ,直到
,直到 为止(其中“
为止(其中“ ”为形态学膨胀算子)。
”为形态学膨胀算子)。
Step 4 定义下一切片标记图像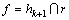 (其中r为下一切片去除脂肪组织的图像)。重复Step 2,Step 3和Step 4,直到所有切片分割完毕为止。
(其中r为下一切片去除脂肪组织的图像)。重复Step 2,Step 3和Step 4,直到所有切片分割完毕为止。
1.2 肾脏图像的模糊聚类分割
1.2.1 各向异性扩散滤波
为了平滑图像噪声并保护目标边缘信息,本文应用各向异性扩散滤波对CT序列图像进行处理。该方法最先由Perona等[12]提出,利用图像梯度信息进行边缘检测,对图像比较平坦的区域进行平滑滤波处理,同时保持图像边缘信息不受影响。各向异性扩散滤波基本方程为
 (1)
(1)
其中: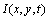 表示t时刻的图像的像素值;
表示t时刻的图像的像素值;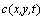 为扩散系数上非负递减函数,能够在每一迭代时刻对图像区域内部进行平滑处理,而在穿过区域边界位置时保护边缘。由于区域边界未知,本文应用
为扩散系数上非负递减函数,能够在每一迭代时刻对图像区域内部进行平滑处理,而在穿过区域边界位置时保护边缘。由于区域边界未知,本文应用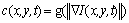 对边界点进行估计,且
对边界点进行估计,且
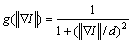 (2)
(2)
式中:g满足g(0)=1,且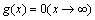 。在图像边缘处,梯度
。在图像边缘处,梯度 通常较大,
通常较大,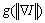 取得最小值,在边缘处对模型进行弱光滑处理;反之,则在图像区域内部进行滤波操作。本文设置参数d=30,且算法迭代5次。
取得最小值,在边缘处对模型进行弱光滑处理;反之,则在图像区域内部进行滤波操作。本文设置参数d=30,且算法迭代5次。
1.2.2 模糊聚类分割
模糊聚类分割在模式识别以及图像处理领域具有重要意义。传统的模糊C均值聚类方法根据图像特征点到聚类中心的距离特性,将图像N个特征点划分为C类(其中,C≤N)。令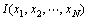 表示待分为C类的图像,xi为图像对应特征点。模糊C均值聚类算法将这N个数据分为C个模糊类,其过程通过最小化以下目标函数得到:
表示待分为C类的图像,xi为图像对应特征点。模糊C均值聚类算法将这N个数据分为C个模糊类,其过程通过最小化以下目标函数得到:
 (3)
(3)
其中:uni为像素点xi属于第n类的模糊隶属度;常数m为模糊权重指数;vn为第n类的聚类中心点。模糊隶属度uni表征了图像像素点与不同聚类中心vn的距离对应关系,其迭代计算公式分别为:
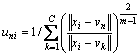 (4)
(4)
 (5)
(5)
一般的模糊C均值聚类算法缺少图像的空间邻域信息,即没有考虑图像相邻像素点之间的相关性。本文结合CT序列图像局部灰度特性,应用空间模糊C均值[16]实现肾脏的聚类分割,其模糊隶属度函数可改写为:
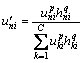 (6)
(6)
 (7)
(7)
其中:参数p和q分别控制uni和hni的数值贡献率,且本文设置类别数C为5。NB(xi)为中心点在xi的矩形窗口;hni表示xi属于类n的概率。空间模糊C均值聚类算法最终得到模糊隶属度矩阵 ,根据隶属度矩阵每列最大元素位置判断像素所属类别。
,根据隶属度矩阵每列最大元素位置判断像素所属类别。
在空间模糊C均值聚类肾脏序列图像之前,需要定位肾脏CT序列的初始分割图像,该图像要求满足:1) 肾脏区域面积较大;2) 肾脏与周围组织之间的边界相对清晰。图3所示为初始肾脏图片及其空间模糊C均值聚类分割结果,其中图3(a)所示为初始肾脏图像,图3(b)所示为空间模糊C均值聚类结果。采用区域标记法去除肝脏以及区域面积较小的组织,可得到肾脏分割区域。为了平滑分割结果的轮廓,本文应用形态学滤波操作进行后处理。图3(c)所示为初始肾脏切片的最终分割结果。在进行CT序列图像的肾脏分割时,首先将所得当前切片分割结果进行骨骼化操作,并且将其作为下一切片(上一切片)分割操作的标记图像,然后重构该切片空间模糊C均值聚类结果。重复此过程,直到分割完所有肾脏CT序列切片为止。

图3 初始肾脏图像分割结果
Fig. 3 Segmented results of initial kidneys images
1.3 区域生长分割
由于在CT序列图像中,相邻器官(组织)之间具有灰度相似性,空间模糊C均值会产生误分类现象。本文根据同一序列不同切片的相同器官所在区域具有连续性以及相似性这一特征,应用相对面积变化率Ta来指导算法的自动分割,即对被错误分类的图像应用区域生长法进行重新分割,同时在区域生长过程中,由空间模糊C均值聚类分割结果确定种子点的位置,从而避免了手动选择生长种子点的过程。相对面积变化率Ta的计算式为
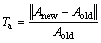 (8)
(8)
式中:Anew和Aold分别为当前切片和相邻上一切片肾脏分割结果的面积。位于CT序列肾脏开始以及结束位置的图像,肾脏区域面积变化较快,本文将这部分面积较小的肾脏区域忽略不计。本文Ta的取值范围为[0, 0.2]。图4(a)所示为某一CT序列中的肾脏图像,图4(b)所示为空间模糊C均值聚类分割结果。显然,算法将肝脏区域误分割为肾脏,其相对面积变化率为0.611 4,超出了Ta的取值范围,因此,认为该切片分割错误,转而采用区域生长法分割。
基于区域生长的分割方法利用图像的空间信息,将具有相似性质的像素点合并构成新的区域。该方法对每个待分割区域确定生长种子点,以种子像素点为中心检索其邻域像素点,根据生长准则将具有相似性质的像素点合并到种子像素所在区域。重复此过程,直到没有满足条件的像素点被包括进来为止。本文应用基于区域灰度差的区域生长法对CT序列图像的肾脏进行处理。首先,对原始肾脏图像求标准方差(见图5(a)),然后,对该标准方差图进行反变换。取相邻上一切片肾脏分割部分区域作为当前切片种子点所在位置,对当前肾脏切片的标准方差图应用区域生长算法。具体操作步骤如下。
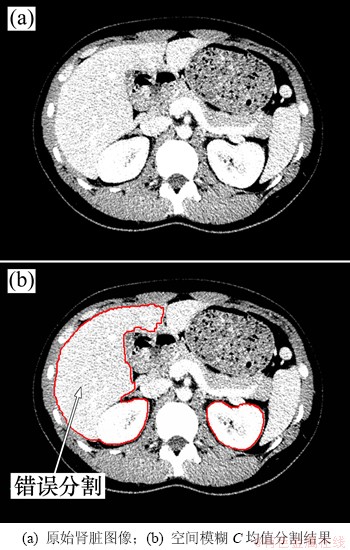
图4 空间模糊C均值聚类误分割结果
Fig. 4 Error segmentation by spatial fuzzy C-means
Step 1 确定初始种子点集合。将已分割好的相邻上一切片肾脏图像进行迭代形态学腐蚀运算(图5(b)),将2次迭代结果相减得到图5(c),将其作为当前肾脏切片种子点所在区域。
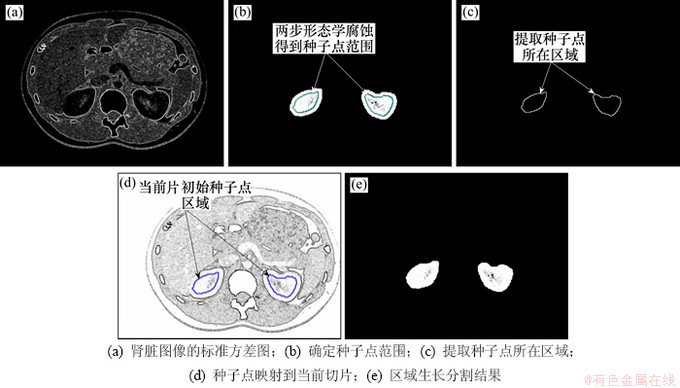
图5 区域生长分割结果
Fig. 5 Results of kidneys segmentation by region growing
Step 2 以确定的种子点(图5(d))为中心,将其8-邻域内的像素逐个与其所在区域的平均灰度进行比较,若灰度差 ,则将该点合并到种子点区域。
,则将该点合并到种子点区域。
Step 3 确定新生成的种子点区域。返回Step 2,直到种子点区域不再增加为止。区域生长最终结果如图5(e)所示。
2 实验及结果分析
为了验证算法的有效性,本文对某一腹部CT序列图像进行肾脏自动分割。当相邻2张切片肾脏分割结果的相对面积变化率Ta位于给定取值范围时,算法采用空间模糊C均值聚类方法提取目标区域;否则,算法根据相邻切片间肾脏连续性与灰度相似性关系自动选择区域生长法分割。图6所示为某一CT序列图像部分切片分割结果,其中,图6(a)~(c)所示分别为该序列第90,110和114片的原始CT图像;图6(d)~(f)所示分别为图6(a)~(c)的空间模糊C均值聚类结果;图6(g)~(i)所示分别为图6(a)~(c)的本文算法分割结果。从图6可以看出:空间模糊C均值聚类对于灰度相似且毗邻的组织或器官出现了误分类现象,而本文提出的算法可以克服空间模糊C均值聚类的不足,依据相邻切片聚类结果,指导区域生长过程,以得到准确的分割结果。
图7所示为本文算法对某一CT序列第105至116片的肾脏分割结果。根据序列图像之间的空间相关性,对当前切片分割结果进行形态学骨骼化操作,作为相邻下一切片的标记图像,然后,对该切片空间模糊C均值聚类后的图像进行形态学重构。当相邻2片肾脏的面积变化率Ta超出给定范围时,对相邻切片肾脏图像应用区域生长法重新分割。该方法根据相邻切片形态学迭代腐蚀结果定位当前切片肾脏图像的初始生长种子点,然后按照生长准则得到最终分割结果。由图7可知:本文算法对肾脏CT序列图像能够进行有效自动分割,且分割结果准确率高。
本文利用三维体绘制方法,将肾脏序列分割结果进行重建,图8所示为某一CT序列肾脏分割结果的三维重建结果。通过将肾脏分割实验进行三维可视化,可以直观地反映出肾脏的形状结构,从而辅助医生进行肾脏器官的疾病诊断与治疗,具有重要的临床应用价值。
为了进一步验证算法的分割性能,本文应用面积误差率(Rarea)[7]对分割结果进行评价。Rarea描述了算法分割面积(Ra)与手动分割面积(Rm)之间的差异,定义为
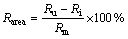 (9)
(9)
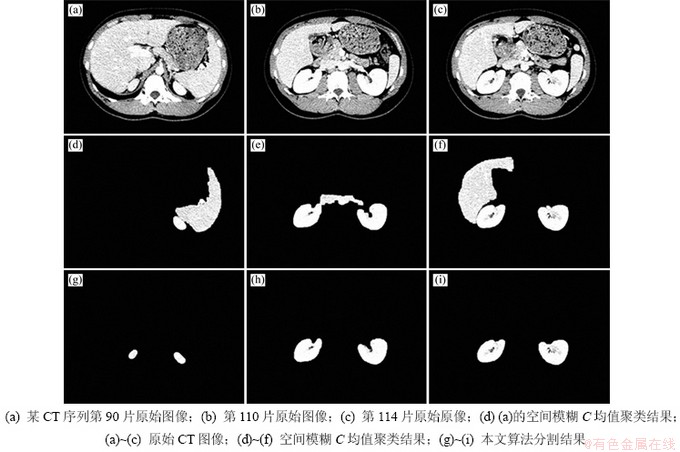
图6 空间模糊C均值聚类与本文算法分割比较
Fig. 6 Comparison of segmented results between spatial fuzzy C-means and the proposed method
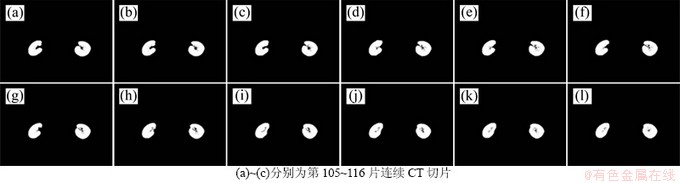
图7 某一序列连续CT切片的肾脏分割结果
Fig. 7 Segmented results of kidneys from some continuous CT slices from No.105 to No.116
式中: ;
; 。Rarea越小,表示算法分割效果越好。文献[5,11]以及本文算法对同一CT序列的分割结果见图9,其中,本文算法Rarea的范围为[0.036 0, 0.230 8]。从图9可以看出:肾脏序列中间部分的Rarea分布比较均匀,取值较小,这是因为这些位置的肾脏形状清晰,相邻切片之间的肾脏面积变化率相对较小。对于位于CT序列肾脏开始以及结束位置的图像,由于肾脏面积变化率较大,所以,Rarea也较高。表1所示为序列图像左、右肾的面积误差率,与文献[5,11]中的肾脏分割方法相比,本文算法的面积误差率较小,表明本文算法具有较好的分割性能。
。Rarea越小,表示算法分割效果越好。文献[5,11]以及本文算法对同一CT序列的分割结果见图9,其中,本文算法Rarea的范围为[0.036 0, 0.230 8]。从图9可以看出:肾脏序列中间部分的Rarea分布比较均匀,取值较小,这是因为这些位置的肾脏形状清晰,相邻切片之间的肾脏面积变化率相对较小。对于位于CT序列肾脏开始以及结束位置的图像,由于肾脏面积变化率较大,所以,Rarea也较高。表1所示为序列图像左、右肾的面积误差率,与文献[5,11]中的肾脏分割方法相比,本文算法的面积误差率较小,表明本文算法具有较好的分割性能。
表1 本文算法的面积误差率Rarea及标准方差
Table 1 Rarea and standard deviation of the proposed method
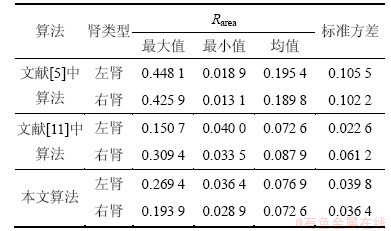

图8 肾脏序列分割结果的三维显示
Fig. 8 3D reconstruction of segmented kidneys from CT scan
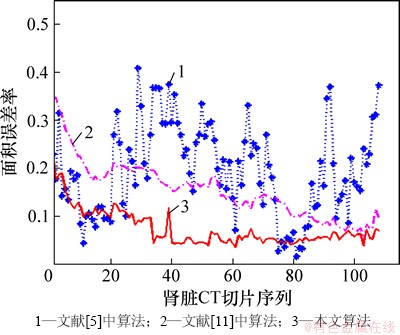
图9 本文算法与文献[5]和[11]中的面积误差率Rarea比较
Fig. 9 Comparison of Rarea obtained by proposed method in the paper and methods in Refs.[5] and [11]
3 结论
1) 研究了基于空间模糊C均值以及区域生长的CT序列图像肾脏自动分割方法。首先,采用经典阈值法以及形态学重构去除肋骨和脊椎。然后,对图像进行各向异性扩散滤波,应用空间模糊C均值对肾脏图像进行聚类。当空间模糊C均值分割结果的面积变化率超出预定范围时,算法自动转为区域生长法进行重新分割。最后,应用形态学滤波对分割结果进行后处理。
2) 本文算法对左肾和右肾的分割面积误差率最小值分别为0.036 4和0.028 9,且分割面积误差率具有较低的平均值和标准方差,证明了本文肾脏分割算法的可行性。
3) 运用空间模糊C均值算法对区域生长法进行约束,即用上一切片空间模糊C均值聚类分割结果来确定当前切片初始种子点位置,避免了手动选择区域生长种子点的过程,提高了算法的鲁棒性。
参考文献:
[1] Lee J, Kim N, Lee H, et al. Efficient liver segmentation using a level-set method with optimal detection of the initial liver boundary from level-set speed images[J]. Computer Methods and Programs in Biomedicine, 2007, 88(1): 26-38.
[2] 王小芳, 赵于前. 基于先验形状的CV模型肝脏CT图像分割[J]. 光电子・激光, 2010, 21(6): 953-956.
WANG Xiaofang, ZHAO Yuqian. Liver CT image segmentation based on prior shape CV model[J]. Journal of Optoelectronics・Laser, 2010, 21(6): 953-956.
[3] LI Bingnan, Chui C K, Chang S, et al. Integrating spatial fuzzy clustering with level set methods for automated medical image segmentation[J]. Computers in Biology and Medicine, 2011, 41(1): 1-10.
[4] WANG Shitong, FU Duan, XU Min, et al. Advanced fuzzy cellular neural network: Application to CT liver images[J]. Artificial Intelligence in Medicine, 2007, 39(1): 65-77.
[5] Selver M A, Kocaoglu A, Akyar H, et al. Patient oriented neural networks to overcome challenges of abdominal organ segmentation in CT Angiograph studies[C]//International Conference on Electrical and Electronics Engineering. Bursa, 2009: 177-181.
[6] Masoumi H, Behrad A, Pourmina M A, et al. Automatic liver segmentation in MRI images using an iterative watershed algorithm and artificial neural network[J]. Biomedical Signal Processing and Control, 2012, 7(5): 429-437.
[7] Massoptier L, Casciaro S. Fully automatic liver segmentation through graph-cut technique[C]//Proceedings of the 29th Annual International Conference of the IEEE EMBS. Lyon, France, 2007: 5243-5346.
[8] CHEN Yufei, WANG Zhicheng, HU Jinyong, et al. The domain knowledge based graph-cut model for liver CT segmentation[J]. Biomedical Signal Processing and Control, 2012, 7(6): 591-598.
[9] Spiegel M, Hahn D A, Daum V, et al. Segmentation of kidneys using a new active shape model generation technique based on non-rigid image registration[J]. Computerized Medical Imaging and Graphics, 2009, 33(1): 29-39.
[10] Shim H, Chang S, Tao C, et al. Semiautomated segmentation of kidney from high-resolution multidetector computed tomography images using a graph-cuts technique[J]. Journal of Computer Assisted Tomography, 2009, 33(6): 893-901.
[11] GAO Yan, WANG Boliang. An automatic segmentation of kidney in serial abdominal CT scans using region growing approach[J]. Journal of Donghua University, 2010, 27(2): 225-228.
[12] Perona P, Malik J. Scale-space and edge detection using anisotropic diffusion[J]. IEEE Transactions on Pattern Analysis and Machine Intelligence, 1990, 12(7): 629-639.
(编辑 陈灿华)
收稿日期:2013-10-02;修回日期:2013-12-23
基金项目(Foundation item):国家自然科学基金资助项目(61172184, 61379107);新世纪优秀人才支持计划(NCET-13-0603)资助项目;高等学校博士学科点专项科研基金(20130162110016)资助项目;湖南省科技基本建设(20131199)项目(Projects (61172184, 61379107) supported by the National Natural Science Foundation of China; Project (NCET-13-0603) supported by Program for New Century Excellent Talents in University; Project (20130162110016) supported by Specialized Research Fund for the Doctoral Program of Higher Education; Project (20131199) supported by Hunan Province Science and Technology Basic Construction)
通信作者:赵于前(1973-),男,湖南双峰人,教授,从事医学图像处理、模式识别与人工智能、信息安全等研究;电话:0731-88836362;E-mail:bme@csu.edu.cn