�κ�±ˮ�Ʊ���״������þ
��ϲ�ƣ�����壬��գ�ʯ����
(���ϴ�ѧ ұ���뻷��ѧԺ������ ��ɳ��410083)
ժҪ����±ˮŨ���ᾧ�õ���ˮ��þʯΪԭ�ϣ������������Ʊ���״������þ�������ð����Ʊ���ά״��ʽ�Ȼ�þ(Mg3Cl(OH)5��4H2O)ǰ���壬�ٽ�ǰ�������ռ�ת��Ϊ��״������þ��̽��Mg2+Ũ�ȡ���Ӧʱ�䡢�»�ʱ���ǰ����ɷֺ���ò��Ӱ�졣�ڼ�ʽ�Ȼ�þת��Ϊ������þ�Ĺ����У�̽�ַ�Ӧ�ܼ�������뷴Ӧ�¶ȶ�������þ��ò��Ӱ�졣�о����������ֻ��Mg2+Ũ�ȴ���3.0 mol/Lʱ���ܵõ���ʽ�Ȼ�þ��Mg2+Ũ��С��3.0 mol/Lʱֻ�ܵõ�������þ�����ŷ�Ӧʱ������ӣ�ǰ���岿��ת��Ϊ������þ�����ų»�ʱ����ӳ���ǰ����ᾧ�������ƣ����ӱ�����ӹ⻬����������8.3���ӵ�35.6���ܼ���ɶ�������þ����òӰ���������ڴ�ˮ��ϵ�У�������þ�ž����أ���״�����٣����Ҵ���ϵ�У�������þ��ɢ�Ժã�����⻬����״���Ӳ��ʸߡ����Ҵ���ϵ�У�40 �淴Ӧ1 h���õ������ȴ���25.0�����ȴ�99.8%���ϵİ�״������þ��
�ؼ��ʣ���ʽ�Ȼ�þ��ǰ���壻��״��������þ
��ͼ����ţ�TQ132.2 ���ױ�־�룺A ���±�ţ�1672-7207(2014)01-0025-08
Preparation of rod-like magnesium hydroxide from brine
YANG Xiyun, YU Peifeng, XU Hui, SHI Xichang
(School of Metallurgy and Environment, Central South University, Changsha 410083, China)
Abstract: Two-step method was adopted to prepare rod-like magnesium hydroxide using bischofite as raw material. The preparation process consists of the synthesis of a precursor called fibrous basic magnesium chloride (Mg3Cl(OH)5��4H2O) and the conversion of the resulting precursor to magnesium hydroxide. The effects of concentration of Mg2+, reaction temperature and aging time on the composition and shape of precursor were investigated. In the process of precursor conversion, the effects of solvent composition and reaction time on magnesium hydroxide were discussed. The results show that the basic magnesium chloride is prepared when the concentration of Mg2+ is more than 3.0 mol/L, otherwise only magnesium hydroxide is obtained. With the increase of the reaction time, basic magnesium chloride converts into magnesium hydroxide, but prolonging aging time is favorable to obtain smooth particles with aspect ratio increasing from 8.3 to 35.6. The solvent composition has a great influence on the morphology of magnesium hydroxide. The rod-like magnesium hydroxide is obtained by heating the alcohol-containing solution at 40 �� for 1 h. Its aspect ratio can reach more than 25.0 and purity can reach 99.8%.
Key words: basic magnesium chloride; precursor; rod-like; magnesium hydroxide
�ҹ���һ���κ��ֲ��϶�Ĺ��ң��κ����̲��ŷḻ�ļء��ơ�þ����Դ�����ຣ��̨���˶��κ�Ϊ�����������Ȼ��ء��Ȼ�þ�����ﵽ��7 000��t[1]���ء�����Դ�������ýϺã��������죬���κ�þ��Դ�Ŀ����������д��ڳ����Σ�ԭ���Բ�Ʒ�͵͵���Ʒ�࣬�ߵ������ܻ���Ʒ�٣��γ��˵Ͷ˲�Ʒ���ڡ��߶˲�Ʒ���ڵľ��档������þ��Ϊһ����ɫ��������ȼ����Ʒ��������ȼ�����̺����ȶ��ع��ܣ������ܵ����ǵ�������������þ��������ò���ߴ����Ӧ�������кܴ�Ӱ�죬����Ƭ״������þ��һ�����õĸ߷��Ӳ�����ȼ��[2-3]����ά״������þ������ǿ�߷��Ӳ��ϵ��ͳ�����ܡ���״������þ���Ʊ���״����þ��ǰ���壬��״����þ��һ�ָ߶˵ĵ��Ӳ�Ʒ����״���״������þ�������������ά���ϵ�����Ӧ��[4]����������κ�±ˮ�Ʊ�������ò��������þ��þ��Դ�ۺ����õ�һ����Ч;��������Ƭ״������þ���Ʊ����������ڶ࣬����״������þ���ױ������١���ǿ��[5]���Ȼ�þ�Ͱ�ˮΪԭ�ϣ�����ֱ�ӳ������Ʊ����˰�״����״��Ƭ״3�ֲ�ͬ��ò��������þ������ƽ��[6]̽�������Ӽ���������þ��ò��Ӱ�죬��ʮ����������ƺ�����Ϊ�������Ӽ��Ʊ����˰�״����״��Ƭ״��������þ����Щ���������Եõ���״������þ������Ҫ�ϸ�����¶Ⱥ����ϵμ��ٶȡ�Li��[7]�Խ���þ��ĩΪԭ�ϣ��Ҷ���Ϊ���Ӽ���180 ��ˮ�ȷ�Ӧ20 h�Ʊ�����������þ���װ���Li��[8]����ϡŨ������þ�Ͱ�ˮΪԭ�ϣ�����160 ��ˮ�Ⱥϳ��˰�״������þ����Щ������Ҫ���¸�ѹ���ɱ��ϸߣ��������ޡ�Ŀǰ������ά״��ʽ�Ȼ�þ��Ϊ�м��壬�پ��ܽ�-�����õ���״������þ�����߾����������Ʊ���״����þ���Ѿ���Ϊ�Ʊ�һάþϵ���ײ��ϵ���Ҫ;����Yang��[9-10]����MgO��MgCl2��6H2OΪԭ�ϣ�����ˮ�ȷ��ɹ��Ʊ�������ά״��ʽ�Ȼ�þ���÷�����Ҫ���ʡ����Ե�����þ�ͷ�������ˮ�Ȼ�þ��Ϊԭ���ϡ������˵�[11]�Ƚ�NaOH��MgCl2��Ӧ�õ�Ƭ״Mg(OH)2����Ƭ״Mg(OH)2��MgCl2��Ӧ�Ʊ���ʽ�Ȼ�þ��Ȼ��ʽ�Ȼ�þ��NaOH��Ӧ�õ���״������þ���ù��սϸ��������������Ʊ�Ƭ״������þ�����ƣ��ײ�����״�����������ˡ�����������������ȡ�ơ��ء���﮵�±ˮΪԭ�ϣ���Ũ���ᾧ�õ�ˮ��þʯ�����ð����Ʊ�����ά״��ʽ�Ȼ�þ��Ϊǰ���壬�ٽ�ǰ�����ɢ���ܽ��Ʊ�������þ���װ���ԭ�ϼ����ã�����������κ�±ˮþ��Դ����Ӧ���̶̣��ڳ��³�ѹ�¼��ɽ��У����˴��ģ������
1 ʵ��
1.1 ʵ�鷽��
1.1.1 ±ˮ����
��ȡ�ء���﮺���κ�±ˮ��þ����Ũ��Ϊ93.4 g/L���ܶ�Ϊ1.28 g/mL�����ȵ����ڣ�����Ũ�����ܶ�Ϊ1.43 g/mL��Ȼ����2~3 h�����ȹ��ˣ���ȴ�����£��ᾧ����ˮ��þʯ����ˮ��þʯ�����ܽ⣬�ٴμ��ȡ�Ũ�����ܶ�Ϊ1.43 g/mL����ȴ�����£����˵õ����νᾧ��Ʒ��
1.1.2 ��ʽ�Ȼ�þ�ĺϳ�
��Ũ��ˮ�����μӵ�һ��Ũ�ȵ�ˮ��þʯ��Һ�У����ư�ˮ���Ȼ�þĦ����Ϊһ��ֵ���ӱ߽��裬�μ������ƿ����ˮԡ�н��跴Ӧһ��ʱ�䣬Ȼ��»���Сʱ�γɼ�ʽ�Ȼ�þ��ϴ�ӣ����ˡ���Һ����һ����ˮ��þʯѭ�����á�
1.1.3 ������þ���Ʊ�
����ʽ�Ȼ�þ��ɢ��60 mL��ˮ�����Һ�У��ڽ����½�3.0 mol/L NaOHѸ�ٵμӵ���ʽ�Ȼ�þ�У�60 ���»�������1 h(��Ӧ��ʽ(1)��ʾ)�����ˣ�ϴ�ӣ���ɡ�
Mg3Cl(OH)5��4H2O+OH-=3Mg(OH)2+Cl-+4H2O (1)
1.2 ��ʽ�Ȼ�þ�γɻ���
����ˮ��þʯ��ˮ��Һ�з���ˮ�ⷴӦ(��ʽ(2)��(3)��ʾ)�����������������[Mg(OH)(H2O)5]+������H+��ʹ��Һ��������(pHԼΪ5.7)����ˮ�μӵ���Һ�У�������������Mg(OH)2��Mg(OH)2�������Ի����н���ˮ��(��Ӧ��ʽ(4)��(5)��ʾ)���õ�ˮ������[Mg(H2O)6]2+��[Mg(OH)(H2O)5]+������ˮ��������ɵĵ����������[Mg(OH)(H2O)5]+��ˮ������[Mg(H2O)6]2+��[Mg(OH)(H2O)5]+�����γ��������ֿ���ͨ������Mg2+�������γɾ��в�ȷ����ɵĶ�������(��ʽ(6)~(8)��ʾ)������Mg(OH)2���ܽ⣬��Щ��Ӧ�ֿ��Խ������У���һϵ�еĵ��롢ˮ��ͼ��ŷ�Ӧ������ʽ(9)��ʾ��ˮ����ᆳ�»�һ��ʱ�䣬��Һ�����γ��������������յõ��ᾧˮ�࣬�ᾧ������ʽ(10)��ʾ[12-13]��
���ü����ʽ�Ȼ�þʱ�������е�Cl-����OH-�û����ᾧˮҲ����ȥ������ʽ�Ȼ�þ����ò�����������������õ���״������þ(��Ӧ��ʽ(1)��ʾ)��
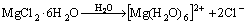 (2)
(2)
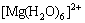

 (3)
(3)
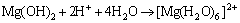 (4)
(4)
 (5)
(5)


 (6)
(6)


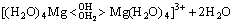 (7)
(7)
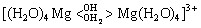

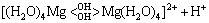 (8)
(8)
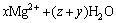

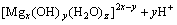 (9)
(9)


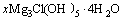 (10)
(10)
1.3 ����ķ��������
�����ձ���ѧD/max-2550 X�������Ǽ�������ʽ�Ȼ�þ��������þ�����࣬����ԴΪCu K�� (������=0.154 06 nm)��ʯīΪ��ɫ������ѹΪ40 kV���ܵ���Ϊ40 mA��ɨ�跶ΧΪ10��~80�㣻��JEOL��˾JSM 5600-LVɨ�������������Ʒ��ò������
2 ʵ����������
2.1 ±ˮ�Ʊ�ˮ��þʯ�����о�
2.1.1 ±ˮ�����ܶȶ�ˮ��þʯ������Ӱ��
����1.1.1�ڵ�ʵ�鷽������300 mL±ˮ����Ũ�����ܶȷֱ�Ϊ1.40��1.41��1.42��1.43��1.44��1.45 g/mLʱֹͣ�������ܷⲢ����120 �汣��2 h�����ȹ��˳�ȥ�������Һ����������Ȼ��ȴ��40 �棬�ᾧ�����ˣ���ɣ����ò�Ʒ�IJ�����ͼ1��ʾ��
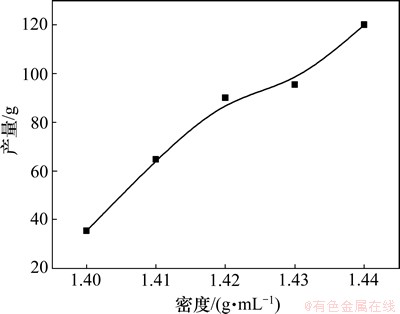
ͼ1 ±ˮ�����ܶȶԲ�����Ӱ��
Fig. 1 Influence of density of brine on yield
��ͼ1��֪������±ˮ�����ܶȵ�����ˮ��þʯ�IJ������������ܶȽ�Сʱ���Ȼ�þ�ﲻ�����ͻ��߹����ͶȽ�С���������Ȼ�þ���������������ܶȲ��������Ȼ�þ�Ĺ����Ͷ��������սᾧ�õ����Ȼ�þ����Խ�ࣻ��ʵ������з��֣��������ܶȴ���1.44 g/mL��ˮ��þʯ�����������뱣�³����������������Է��룬���Ҫ�ϸ���������յ�ʱ±ˮ���ܶȲ�����1.44 g/mL��
2.1.2 �ᾧ�����Բ�Ʒ���ȵ�Ӱ��
��һ�νᾧ��157.0 gˮ��þʯ�����ܽ⣬���Ƴ��Ȼ�þ����Ϊ40%�ı�����Һ�����ȵ����ڣ�Ũ�����Ȼ�þ����Ϊ43%����ȴ�ᾧ�õ����νᾧ��Ʒˮ��þʯ101.2 g����±±ˮ��һ�νᾧˮ��þʯ�Ͷ��νᾧˮ��þʯ������Ԫ�صı仯�������1��ʾ��
��1 ����Ԫ�غ���ICP�������
Table 1 ICP results of impurity elements in product
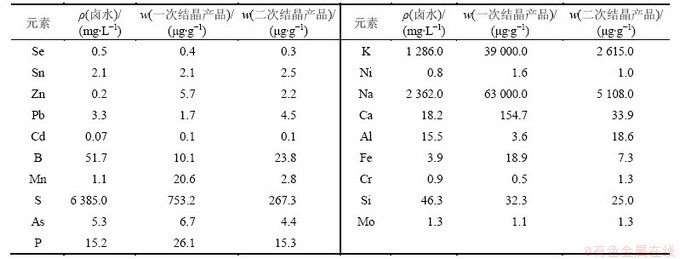
�ɱ�1��֪������һ�������ᾧ����Ʒ�е�K��Na��S������Ԫ�غ��������ؽ��ͣ���ȡ���νᾧ������Ԫ���ֽ�һ�����ͣ�ˮ��þʯ���ȿɴ�98%�������˺��������Ҫ��
2.2 ��ʽ�Ȼ�þ�Ʊ������о�
2.2.1 þ����Ũ�ȶԼ�ʽ�Ȼ�þ������ɵ�Ӱ��
�ֱ������Ȼ�þ��ҺŨ��Ϊ2.0��3.0��3.5��4.0��5.0 mol/L�����ư�ˮ���Ȼ�þĦ����(��ư�þ��)Ϊ1:5����30 ���·�Ӧ1.5 h��50 ���³»�48 h�����ò�Ʒ��XRD����ͼ2��ʾ��
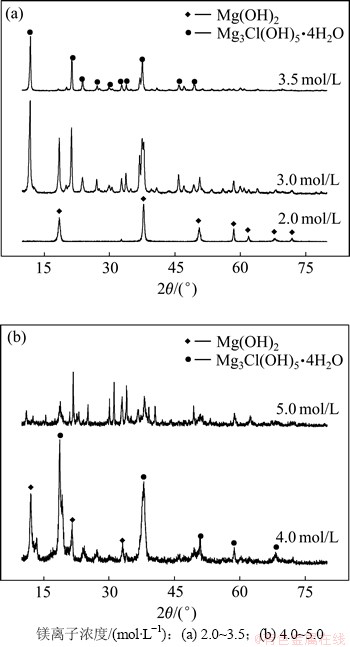
ͼ2 ��ͬþ����Ũ�����ü�ʽ�Ȼ�þXRD��
Fig. 2 XRD patterns of basic magnesium chloride obtained with different concentration of Mg2+
��ͼ2��֪����þ����Ũ��Ϊ2.0 mol/Lʱ���ò�Ʒȫ��Ϊ������þ��þ����Ũ������3.0 mol/Lʱ�����ò�Ʒ��Ϊ��ʽ�Ȼ�þ����������������þ����������þ����Ũ�ȵ�3.5 mol/Lʱ������ȫ��Ϊ��ʽ�Ȼ�þ(Mg3Cl(OH)5��4H2O)����þ����Ũ�ȴ���3.5 mol/Lʱ�����ò�Ʒ�������ǿ�ȱ�ͣ���Ʒ�к���δת����������þ��������������ij��֣���ʵ������з��֣�þ����Ũ��Խ���γ���������ʱ��Խ�̣������ɺ˽ᾧ�ٶ�ҲԽ�졣��MgO-MgCl2-H2O��ϵ��ƽ���ϵ��֪����ʽ�Ȼ�þֻ���ڸ�Ũ�ȵ��Ȼ�þ��Һ(����3.0 mol/L)�в����ȶ�����[14]��Lewis[15]�о���25 ��ʱ��Ũ��MgCl2��Һ��Mg2+��ˮ�⡣�о�������ֻ������Ũ�ȳ���ij����Ũ��(1.96 mol/L)ʱ���������ӵ�ˮ��Ż��γɶ����������������Ũ�ȵ��ڸü���Ũ��ʱ��ֻ���γɵ����������ܵõ�������������γ��������Ӷ��ò�����ʽ�Ȼ�þ���壬��˵�þ����Ũ�ȵ���3.0 mol/Lʱ�����γɴ���Mg(OH)2������
2.2.2 ��Ӧʱ��Լ�ʽ�Ȼ�þ������ɵ�Ӱ��
����þ����Ũ��Ϊ3.5 mol/L����þ��Ϊ1:5����30 ���·ֱ�Ӧ0.5��1.0��1.5��2.0��2.5 h��50 ���³»�48 h�����ò�Ʒ��XRD����ͼ3��ʾ��
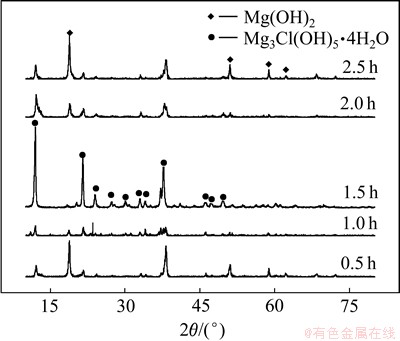
ͼ3 ��ͬ��Ӧʱ�����ò�Ʒ��XRD��
Fig. 3 XRD patterns of basic magnesium chloride obtained at different reaction time
��ͼ3��֪������Ӧʱ��Ϊ0.5 hʱ����Ʒ��ҪΪ������þ����Ӧʱ��Ϊ1.0 hʱ��������ҪΪ��ʽ�Ȼ�þ������������������þ����Ӧʱ��Ϊ1.5 hʱ����Ʒȫ��Ϊ��ʽ�Ȼ�þ����һ���ӳ���Ӧʱ�䣬��Ʒ���ֿ�ʼ����������þ������Ӧʱ��С��1.5 hʱ�����費��֣���������Ӳ��ܳ�ַ�ɢ��Mg(OH)2û����ȫˮ�⣬���뵽��Һ�ײ��������ڼ��ŷ�Ӧ(ʽ(6)~(8))����Ľ��У����»������δ��ȫ���뷴Ӧ��������þ����ʽ�Ȼ�þ�γɵij��ڣ�������Ԫ��ĵ��Dz��ȶ��ģ���Ҫ������ʱ��ľ��ó»�������Ӧʱ����� (����1.5 h)ʱ����ʱ����ҵĽ�����谭�������������ã����γɴ���������������������ֻ���ת��Ϊ������þ���Ȼ�þ��ˮ�е�ˮ���Լ�������þ�ĵ�����һ����ԽϿ�Ĺ��̣����õ��ĵ���������Լ�ˮ��������Ҫ�������ó»�24 h���ϲ��ܵõ���ʽ�Ȼ�þ���壬�෴�ڼ�Ľ�����ƻ��������γɡ�
2.2.3 �»�ʱ��Լ�ʽ�Ȼ�þ���༰��ò��Ӱ��
���ư�þ��Ϊ1:5��þ����Ũ��Ϊ3.5 mol/L��30 �淴Ӧ1.5 h���ֱ���50 ���³»�12��24��36��48 h�����ò�Ʒ��XRD����ͼ4��ʾ��SEM����ͼ5��ʾ��
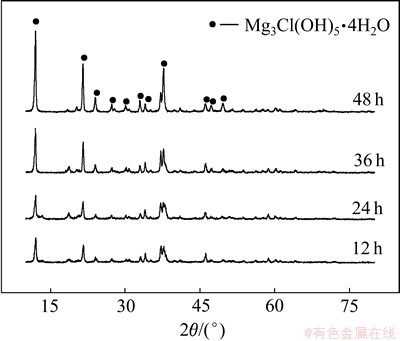
ͼ4 ��ͬ�»�ʱ�����ò�Ʒ��XRD��
Fig. 4 XRD patterns of basic magnesium chloride obtained at different aging time
��ͼ4��֪���»�ʱ�����12 hʱ������Ϊ��ʽ�Ȼ�þ�������ǿ�Ƚ���������ᾧ�����ƣ��»�ʱ�����24 hʱ�������ǿ�����ӣ���������������á���ͼ5��֪���»�ʱ��Ϊ12 hʱ(ͼ5(a))�����ﳤ���Ƚ�С(Լ8.3)������ۼ����ң��ᾧ�����ƣ��»�ʱ�����ӵ�24 hʱ(ͼ5(b))�����͵õ����Ը��ƣ��»�ʱ��Ϊ48 hʱ(ͼ5(d))�����������Ϻã�����⻬�������ȴ�35.0�������͵�[16-17]���о���Ҳ���֣��»�ʱ��Ϊ48 hʱ��Ʒ��ò�Ѿ��õ��ϴ���ơ�����Ҫ�����ڼ�ʽ�Ȼ�þ���γ���һ�������Ĺ��̣��ϳ��ij»�ʱ�����ʹ���������������ţ������γɶ��������ӣ�����һ�����������õ������ȴ�Ŀ���������ᾧ�������ƣ���ò�����ȡ�
2.3 ������þ�Ʊ����յ��о�
2.3.1 ��Ӧ�ܼ���ȶ�������þ��ò��Ӱ��
�����ܼ����Ҵ���������ֱ�Ϊ0��40%��60%��100%����ʽ�Ȼ�þŨ��Ϊ0.1 mol/L��NaOH���ʽ�Ȼ�þĦ����Ϊ2:1����60 ���·�Ӧ1 h�����ò�Ʒ��SEMͼ��ͼ6��ʾ��
��ͼ6��֪�������ô�ˮΪ��Ӧ�ܼ�ʱ�����ɵ�������þ����ֲ�(ͼ6(a))���������ң��ž������Ϊ���أ������ܼ����Ҵ��������������(��ͼ6(b)��ͼ6(c))���������ֲ��������ƣ���Ʒ�ķ�ɢ��Ҳ������ߣ�����Ӧ�ܼ�Ϊ���Ҵ�ʱ(��ͼ6(d))�����ͱ�ù�����ҲԽ�⻬�����룬����������С��������Ҳ�������ӡ�����Ҫ�������Ҵ��Ĵ��ڿ������Ƽ�ʽ�Ȼ�þˮ�⣬�ֿ��Խ���������þ�����ܣ������ž۳̶ȣ�����˲���ķ�ɢ���ܣ����Ʒ�Ӧ��ϵ�Ļ������Ӷ��õ�����⻬���������Ƶİ���������þ����·��[19]���Ʊ���ʽ�Ȼ�þ����ʱҲ���֣���ˮ�ȵ����������ڵõ�����⻬�ľ��塣Baranek��[20]Ӧ�����������ӻ�ѧ�������о���Mg(OH)2�Ľṹ����ʾ�˴��нᾧˮ�ļ�ʽþ�����ȴ�Ľ����и�������������þת�䡣

ͼ5 ��ͬ�»�ʱ�����ò�Ʒ��SEM��
Fig. 5 SEM images of basic magnesium chloride obtained at different aging time

ͼ6 ��ͬ�Ҵ������������������þ��SEM��
Fig. 6 SEM images of magnesium hydroxide obtained with different alcohol-H2O ratios
2.3.2 ��Ӧ�¶ȶ�������þ��ò��Ӱ��
���Ƽ�ʽ�Ȼ�þŨ��Ϊ0.1 mol/L���ܼ����Ҵ�60%��NaOH���ʽ�Ȼ�þĦ����Ϊ2:1���ֱ���30��40��50��60 ���·�Ӧ1.0 h�����ò�Ʒ��SEM����ͼ7��ͼ6(c)��ʾ��
��ͼ7��ͼ6(c)��֪������Ӧ�¶�Ϊ30 ��ʱ(ͼ7(a))�������������룬����������Դֲڣ�����Ӧ�¶����ߵ�40 ��ʱ(ͼ7(b))�����������ӹ⻬�����ӷֲ�Ҳ���Ӿ��ȣ���Ӧ�¶Ƚ�һ�����ߵ�50 �棬����С����������þ��������ò�������ң����¶����ߵ�60 ��ʱ(ͼ6(c))��������ø��Ӵֲڣ��������Ʊ���ʽ�Ȼ�þ�Ĺ����п�֪������Ӧ�¶ȴ���50 ��ʱ�������л���������ʽ�Ȼ�þ(Mg2Cl(OH)3��4H2O)�����¶���60 ��ʱ��ʽ�Ȼ�þ�г��ֲ�������״��������þ������ʽ�Ȼ�þ���·�ɢ���ܼ���ʱ���¶ȹ��ߣ���ʽ�Ȼ�þ����������ȷ����ı䣬������ת�������г���Ƭ״���̰��εȲ�������ò��������þ��

ͼ7 ��ͬת���¶�����������þ��ò��SEM��
Fig. 7 SEM images of magnesium hydroxide obtained at different reaction temperature
2.4 ��ͬþԴ����������þ���ȶԱ�
����1.1.2��1.1.3�ڵ�ʵ�鷽�����ֱ����±ˮһ�νᾧ�����νᾧ���õ���ˮ��þʯ�ͷ�������ˮ�Ȼ�þ��Ϊԭ���Ʊ���ʽ�Ȼ�þ����ת��Ϊ������þ(�ֱ����A��B��C��ʾ)������������þ��Ʒ��ICPȫ�������2��ʾ��
��2 ������þICPȫ�������
Table 2 ICP results of Mg(OH)2 ��g/g
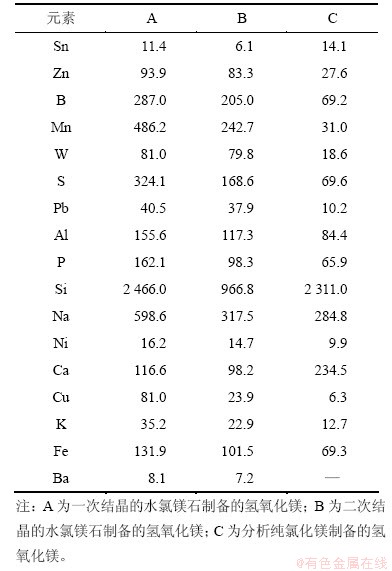
�ɱ�2��֪�����νᾧ��ˮ��þʯ���Ʊ���������þ���ʺ������Ե���һ�νᾧ��ˮ��þʯ���Ʊ���������þ�����ʺ���������EDTA�ζ����ⶨһ��ˮ��þʯ����������þ������98.0%���ϣ����ö��νᾧˮ��þʯ���Ʊ���������þ����Ϊ99.8%���ϣ����Է�������ˮ�Ȼ�þΪԭ�ϵõ���������þ����һ���������Զ��νᾧ����ˮ��þʯΪԭ�����Ʊ��İ�״������þ��������ߴ���Ҫ��
3 ����
(1) ��±ˮ�����õ���ˮ��þʯ�Ͱ�ˮΪԭ���Ʊ�������ά״��ʽ�Ȼ�þǰ���壬��ǰ�����ɢ�ܽ⣬�μ�����������Һ�Ʊ����˰�״������þ��
(2) ±ˮ�����ܶȶ�ˮ��þʯ�����нϴ�Ӱ�죬�����ܶ�Խ����Խ�࣬Ϊ��ʹ�������ڹ��ˣ������ܶȲ��˳���1.44 g/mL���ᾧ������ˮ��þʯ����Ӱ���������������νᾧˮ��þʯ���ȼ��ɴ�98%��������������Ҫ��
(3) þ����Ũ�ȶ�ǰ�����ʽ�Ȼ�þ�ijɷ�����ò�нϴ��Ӱ�졣ֻ���ڴ���3.0 mol/L���Ȼ�þ��Һ�в��ܵõ���ʽ�Ȼ�þ���Ȼ�þŨ�ȵ���3.0 mol/Lֻ�ܵõ�������þ��
(4) ��Ӧʱ��Բ������ɵ�Ӱ���������ϳ���϶̵ķ�Ӧʱ�䶼����ɲ�Ʒ�г���������þ�Լ�������̬�ļ�ʽ�Ȼ�þ���»�ʱ��ﵽ12 hʱ�Ѿ��γɼ�ʽ�Ȼ�þ���壬��ֻ�г»�ʱ�����24 hʱ���õ��ļ�ʽ�Ȼ�þ��������Ϊ�Ʊ�������þ��ǰ���塣
(5) �Լ�ʽ�Ȼ�þΪǰ���壬����NaOH����ת�����ܼ����Ҵ���ռ�����Ϊ60%����40 ���·�Ӧ1.0 h���õ����ȸߡ������ȴ���25.0�İ�״������þ���䴿�ȿɴ�99%���ϡ�
�ο����ף�
[1] ������. �κ�ˮ��þʯ��ȡ��ϸ��ȼ��������þ���о�[D]. ��ɳ: ���ϴ�ѧұ���ѧ�빤��ѧԺ, 2004: 1-68.
DENG Xinrong. Study on preparation of ultra-fine flame retardant magnesium hydroxide by salt lake bischofite[D]. Changsha: Central South University. School of Metallurgical Science and Engineering, 2004: 1-68.
[2] DING Yi, ZHANG Guangtao, WU Hao, et al. Nanoscale magnesium hydroxide and magnesium oxide powders: Control over size, shape, and structure via hydrothermal synthesis[J]. Chemistry of Materials,2001,13(2): 435-440.
[3] L Jianping, QIU Longzhen, QU Baojun, et al. Controlled synthesis of magnesium hydroxide nanoparticles with different morphological structures and related properties in flame retardant ethylene�Cvinyl acetate blends[J]. Nanotechnology, 2004, 10(15): 1576-1581.
Jianping, QIU Longzhen, QU Baojun, et al. Controlled synthesis of magnesium hydroxide nanoparticles with different morphological structures and related properties in flame retardant ethylene�Cvinyl acetate blends[J]. Nanotechnology, 2004, 10(15): 1576-1581.
[4] WANG Peipei, LI Caihong, GONG Haiyan, et al. Morphology control and growth mechanism of magnesium hydroxide nanoparticles via a simple wet precipitation method[J]. Ceramics International, 2011, 37: 3365-3370.
[5] ��ǿ, ������. ������þ��ò�����Ʊ�[J]. ������ҵ�Ļ�, 2007, 10(3): 90-91.
WU Qiang, WANG Xiangtian. Preparation and shape control of magnesium hydroxide[J]. Oriental Enterprise Culture, 2007, 10(3): 90-91.
[6] ����ƽ, ��ѹ��, �Ա���. ��ͬ��ò����������þ�Ŀɿغϳɼ���Ӧ��[C]// ȫ�����������ײ��Ϻͼ���Ӧ�û������ļ�. �Ͼ�, 2003: 172-175.
L Jianping, QIU Longzhen, ZHAI Baojun. Controllable synthesis and application of different morphologies nanometer magnesium hydroxide[C]// Proceeding of third Chinese Nanomaterials and Technology Application Conference. Nanjing, 2003: 172-175.
Jianping, QIU Longzhen, ZHAI Baojun. Controllable synthesis and application of different morphologies nanometer magnesium hydroxide[C]// Proceeding of third Chinese Nanomaterials and Technology Application Conference. Nanjing, 2003: 172-175.
[7] Li Y, Sui M, Ding Y, et al. Preparation of Mg(OH)2 nanorods[J]. Advanced Materials, 2000, 12(11): 818-821.
[8] Li Y, Jing Z, Xiao M S, et al. Formation of rod-like Mg(OH)2 nanocrystallites under hydrothermal conditions and the conversion to MgO nanorods by thermal dehydration[J]. Materials Chemistry and Physics, 2002, 76(2): 119-122.
[9] Yang Z J, Cingarapu S, Klabunde K J. Synthesis of magnesium oxychloride nanorods with controllable morphology and their transformation to magnesium hydroxide nanorods via treatment with sodium hydroxide[J]. Journal of Sol-Gel Science and Technology, 2010, 53(2): 359-365.
[10] ������. þϵ���װ��ĺϳɹ����о�[D]. ����: ����������ѧ����ѧԺ, 2006: 30-50.
FAN Fangrong. Synthesis of magnesium serial nanorods[D]. Dalian: Dalian University of Technology. School of Chemical Engineering, 2006: 30-50.
[11] ������, �½���, ���ƻ�, ��. ��״������þ�ĺϳ�[J]. ����ѧѧ��, 2010, 26(1): 8-12.
LI Zhenxing, CHEN Jianming, SONG Yunhua, et al. Rod-like magnesium hydroxide preparation[J]. Chinese J Inorg Chem, 2010, 26(1): 8-12.
[12] �����, ����. þˮ��ĸ��Լ���Ʒ����ʵ�ü���[M]. ����: ��ѧ��ҵ������, 2006: 150-250.
YAN Zhen-jia, HE Yan-jun. The practical technology of magnesia cement modification and production[M]. Beijing: chemical Industry Press,2006: 150-250.
[13] Pye C C, Rudolph W W, An A B, et al. Initio and Raman investigation of magnesium(��) hydration[J]. Journal of Physical Chemistry A, 1998, 102: 9933-9943.
[14] Bilinski H, Matkovic B, Mazuranic C, et a1. The formation of magnesium oxychloride phases in the systems MgO-MgCl2-H2O and NaOH-MgCl2-H2O[J]. Journal of the American Ceramic Society, 1984, 67(4): 266-269.
[15] Lewis D. Studies on the hydrolysis of metal ions: The hydrolysis of magnesium in chloride self-medium[J]. Acta Chemica Scandinavica, 1963, 45(17): 1891-1894.
[16] ������, ������. ��ʽ�Ȼ�þ���װ����Ʊ��ͱ���[J]. ���ϻ���, 2010, 27(7): 29-32.
WANG Baohe, L Xiaoming. Preparation and characterization of basic magnesium chloride nanorods[J]. Henan Chemical Industry, 2010, 27(7): 29-32.
Xiaoming. Preparation and characterization of basic magnesium chloride nanorods[J]. Henan Chemical Industry, 2010, 27(7): 29-32.
[17] ������, ����, ��ά, ��. �Ʊ����ն���ά״��ʽ�Ȼ�þ�����Ӱ��[J]. ��Ե����, 2004, 37(2): 32-35.
REN Qingli, LIU Bin, CHEN Wei, et al. Effect of the preparation technics on korshuskite whisker[J]. Insulating Materials, 2004, 37(2): 32-35.
[18] Jeevanandam P, Mulukutla R S, Yang Z, et al. Nanocrystals to nanorods: A precursor approach for the synthesis of magnesium hydroxide nanorods from magnesium oxychloride nanorods starting from nanocrystalline magnesium oxide[J]. Chemistry of Materials, 2007, 19(22): 5395-5403.
[19] ��·, ��ѩ��, Ҧ־ͨ, ��. ��ʽ�Ȼ�þ��������֦����ϩ������ۺϷ�Ӧ���о�[J]. ������ѧ��, 2009, 24(4): 859-863.
ZHANG Lu, CHEN Xuegang, YAO Zhitong, et al. Study on the radical grafting polymerization of MMT onto basic magnesium chloride whisker surface[J]. Journal of Inorganic Materials, 2009, 24(4): 859-863.
[20] Baranek P, Lichanot A, Orlando R, et al. Structural and vibrational properties of solid Mg(OH)2 and Ca(OH)2: Performances of various Hamiltonians[J]. Chemical Physics Letters, 2001, 340(3/4): 362-369.
(�༭ ����ƽ)
�ո����ڣ�2012-12-13�������ڣ�2013-01-15
������Ŀ������ר�����ϴ�ѧǰ���о��ƻ��ص���Ŀ(2010QZZD003)
ͨ�����ߣ���ϲ��(1974-)��Ů�������۶��ˣ���ʿ�����ڣ������κ�±ˮ��Դ�о����绰��0731-88830869��E-mail: xiyun.yang@yahoo.com