正极自支撑的聚合物电解质的制备
胡拥军1, 2, 陈白珍1, 袁 艳1, 徐 徽1, 石西昌1
(1. 中南大学 冶金科学与工程学院, 湖南 长沙,410083;
2. 湖南城市学院 化学与环境工程系,湖南 益阳,413049)
摘 要: 以N,N-二甲基甲酰胺为溶剂, 聚偏氟乙烯-六氟丙烯为聚合物基质, 采用直接挥发溶剂法制备正极自支撑的聚合物电解质, 并以锂为负极制备LiCoO2聚合物电池. 用扫描电子显微镜和循环伏安实验对聚合物电解质进行表征, 用红外光谱分析了电解质微孔的形成机理, 并对聚合物电池的充放电性能和界面阻抗进行测试。 结果表明: 直接挥发溶剂制得的聚合物电解质孔穴丰富, 电化学稳定窗口达5.5 V. 采用正极自支撑电解质可改善材料的力学性能, 降低电池的界面阻抗; 制备的聚合物电池界面性质稳定, 循环40次后容量保持率为97.5%, 0.5C和1C倍率放电分别能保持0.1C放电容量的97.8%和95.7%.
关键词: 聚合物电解质; 锂离子电池; 交流阻抗; 界面行为; 聚偏氟乙烯-六氟丙烯
中图分类号:TM912 文献标识码:A 文章编号:1672-7207(2007)02-0256-06
Preparation of polymer electrolyte supported by cathode electrode
HU Yong-jun1, 2, CHEN Bai-zhen1, YUAN Yan1, XU Hui1, SHI Xi-chang1
(1. School of Metallurgical Science and Engineering, Central South University, Changsha 410083, China;
2. Department of Chemistry, Hunan City University, Yiyang 413049, China)
Abstract: A poly(vinylidene) fluoride-hexafluoropropylene electrolyte supported by the cathode electrode was prepared by evaporating the solvent of dimethyl formamide, and polymer lithium-ion batteries were assembled by using lithium foil as anode and LiCoO2 as cathode material. Polymer membrane was characterized by scanning electron microscopy and cyclic voltammetry test, the formation mechanism of micropore was discussed by infrared spectroscopy, and the polymer battery’s electrochemical properties and resistance were tested by charge-discharge experiment and A.C. impedance. The results show that this polymer membrane has rich micropore and its electrochemical stability window reaches 5.5 V. The polymer electrolyte supported by cathode electrode has excellent mechanical property and can reduce the interfacial impedance of polymer battery. Polymer lithium battery keeps a stable interfacial property, and its capacity retention is 97.5% after 40 cycles. The discharge capacities of 0.5 C and 1C are 97.8% and 95.7% of the discharge capacity of 0.1 C, respectively.
Key words: polymer electrolyte; lithium battery; A.C. impedance; interfacial behavior; poly(vinylidene) fluoride- hexafluoropropylene
聚合物电池具有质量比能量高、无漏液危险和可任意形状化等特点,深受人们关注。要实现聚合物电池的产业化,必须了解好聚合物电解质的力学性 能,并保证制备的聚合物电池具有良好的循环性能和倍率放电能力[1-4]。
制备聚合物电解质最常用的材料是PVDF-HFP(聚偏氟乙烯-六氟丙烯),方法有3种:一是增塑萃取工艺[5],原理是利用抽提步骤萃取出事先混合在聚合物膜中的增塑剂而造孔成膜,此工艺要处理大量有机增塑剂,存在安全问题,电池成本也较高;二是相转移法,即在聚合物溶液中加入非溶剂,利用溶剂和非溶剂的挥发速度差异来造孔[6-8],与增塑萃取工艺相比,此法简化了制膜工序,但由于引入了非溶剂,故要求严格的温湿度条件以控制溶剂的挥发,重现性不好,实验时易导致微孔膜制备失败[9];第3种方法操作简单,仅通过在聚合物溶液中掺入有机或无机材料,利用掺杂剂和聚合物对溶剂的作用力不同来直接造 孔[9-11],存在的弊端是制备的聚合物膜脆性大,同时还会引入杂质。
本实验以正极片作机械支撑,用单一的聚合物溶液经直接挥发溶剂,一步获得牢固附着于正极上的聚合物电解质微孔膜。与其他方法相比,本工艺不使用任何掺杂剂、不采用抽提步骤、也不使用非溶剂,制备简单,获得的聚合物膜孔穴丰富;而且由于聚合物电解质膜是直接制备于正极表面,因此,聚合物膜能随正极片一起卷绕,不脱落,难断裂,可满足电池的卷绕式生产工艺;电解质与正极接触紧密,电池阻抗降低,界面性质稳定,循环性能和倍率放电能力优良。
1 实 验
以LiCoO2(湖南瑞翔公司)为正极,与粘结剂和导电剂混匀,用N-甲基吡咯烷酮调成浆料后涂于铝箔上干燥成正极片备用。按一定配比将PVDF-HFP(Elf Atochem, Kynar 2801)溶于DMF(N,N-二甲基甲酰胺),将溶液直接浇于正极片上流动延展成膜,在空气气氛下挥发至膜成白色,再经80 ℃真空干燥6 h即得牢固附着于正极上的聚合物电解质膜。在充满氩气的手套箱中将此正极自支撑的聚合物膜浸取含质量比为1?1?1 的EC/DEC/DMC的1 mol?L-1 LiPF6溶液,以锂为负极制成2032型聚合物电池。
聚合物电解质表面形貌用JSM-6360LV型扫描电子显微镜检测,红外光谱用WQF-310傅里叶变换红外光谱仪测量,范围为400~4 000 cm-1,分辨率为2 cm-1。电解质膜吸液率=(W-W0) /W0×100%。其中W0和W分别为聚合物吸收电解液前后的质量。离子电导率(σ)通过交流阻抗实验测试,σ=D/(S×R)。其中:D为聚合物电解质膜的厚度;S为膜的面积;R为通过对不锈钢/聚合物/不锈钢阻塞电池的阻抗实验测得的溶液本体阻抗。电解质电化学稳定窗口用循环伏安法测量,扫描速度为2 mV?s-1,电池交流阻抗测试频率范围为105~0.01 Hz,电压振幅为5 mV,循环伏安和交流阻抗均在Chi660B 电化学工作站上进行。电池充放电用Neware电池检测系统测试,电压起止范围为2.75~ 4.20 V。
2 结果与讨论
2.1 聚合物电解质的性质
图1所示是制备的聚合物微孔膜的SEM照片,其中图1(b)所示是未用正极支撑的微孔膜SEM照片,该聚合物膜同样用直接挥发溶剂法在玻璃板上制备。

(a)―正极自支撑膜; (b)―非正极支撑膜
图1 聚合物膜SEM照片
Fig.1 SEM images of different polymer membranes
比较图1(a)和(b)可发现:不管有无正极支撑,采用挥发溶剂法制得的PVDF-HFP聚合物微孔膜结构相同:孔穴丰富,呈网络结构,孔径在5~15 μm之间,分布较为均匀,且孔穴相互交织,微孔网络深及膜内部。这种结构利于储藏电解液和离子传导。此外,采用正极自支撑的聚合物膜经多次卷绕和折叠至铝箔断裂也不脱落。这说明聚合物膜已牢固粘附于正极上,而且,由于有集流体铝箔支撑,正极自支撑的聚合物膜可操作性好,能满足电池的卷绕式生产工艺。同样用挥发溶剂法制备的非正极支撑膜以及用增塑萃取工艺或相转移制得的PVDF-HFP聚合物膜因为力学强度有限,卷绕时易断裂。用挥发溶剂法制得的2种聚合物微孔膜吸液率均在260%左右。另外,实验还发现溶剂种类及聚合物溶液的挥发温度对膜的形貌影响很大,溶剂沸点太低或挥发温度过高都会导致膜的微孔减少,吸液率降低,甚至出现致密膜。
聚合物电解质要用于锂离子电池,其电化学稳定窗口必须达到4.5 V。为此,将吸收了电解液的聚合物膜夹于锂和不锈钢工作电极间,通过循环伏安实验测量电流随电压的响应曲线。从图2所示第1次扫描结果可知:聚合物电解质从1.5 V往0 V扫描时的响应电流很小,从第2次扫描开始在1.5~0 V之间出现的逐渐增强的电流,这可能是聚合物在高电压下被氧化后产物的还原峰;而在-0.5 V和回扫至+0.5 V左右出现的2个峰则分别是锂在不锈钢上的沉积和溶解 峰[12];之后,从0.5 V一直到5.5 V,电流都几乎为0,超过5.5 V后电流开始明显增加,说明聚合物膜开始氧化分解。因此,PVDF-HFP聚合物电解质的电化学稳定窗口达到5.5 V,可满足锂离子电池的应用要求。
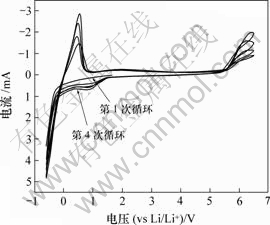
图2 锂/电解质/不锈钢电池的循环伏安曲线
Fig.2 Cyclic voltammogram of stainless/electrolyte/Li cell
聚合物电解质要用于锂离子电池,其室温离子电导率必须达到10-3 S/cm。为此,将不含正极的聚合物电解质夹于两不锈钢电极之间,用交流阻抗技术测量了室温下阻塞电池的阻抗谱(图3)。用螺旋千分尺测量出所用膜厚为0.018 cm,计算出聚合物表面积为1.42 cm2,因此,聚合物电解质的室温离子电导率为1.56 mS?cm-1。聚合物膜丰富的孔穴能储藏大量电解液,相互贯通的微孔有利于离子传导,这是该聚合物电解质室温离子电导率高的主要原因。
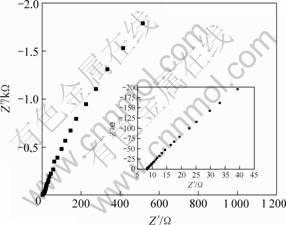
图3 不锈钢/电解质/不锈钢阻塞电池的阻抗图谱
Fig.3 Impedance spectrum of blocking cell
2.2 聚合物微孔膜形成机理的红外光谱
为了探讨直接挥发溶剂法制备聚合物微孔膜的机理,对聚合物微孔膜进行了红外光谱研究。
图4中谱线(a)所示是DMF的红外吸收光谱。由图可见,1 689~1 657 cm-1处的峰是C=O的红外振动峰。1 350~1 000 cm-1之间的峰是分子中C―N的伸缩振动峰。图4中谱线(c)中1 350~1 000 cm-1间出现的几个峰对应PVDF-HFP的C―F吸收带[13]。图4中谱线(b)所示是PVDF-HFP的DMF溶液的红外吸收谱。
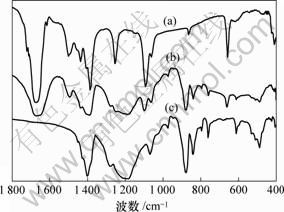
(a)―DMF; (b)―PVDF-HFP /DMF; (c)―PVDF-HFP
图4 聚合物及其溶剂的红外吸收光谱
Fig. 4 FTIR spectra of polymer and its solvent
经对比可知:DMF在加入PVDF-HFP后,其C=O的振动峰红移至1 649 cm-1,并明显宽化;1 257 cm-1处的吸收峰则淹没在PVDF-HFP的C―F吸收带中,而原1 095 cm-1处对应C―N的伸缩振动峰已蓝移至 1 101 cm-1,其他如650 cm-1处C―H键吸收峰也明显削弱。光谱的变化能反映两者间存在相互作用力,其原因可能是:DMF中л电子可沿O=C―N离域,加入PVDF-HFP后,由于DMF中的CH3与F存在非典型氢键,从而引发超共轭效应,使C=O红移和C―N键蓝移,表现出的宏观结果则是PVDF-HFP与DMF分子间的物理作用力增强,溶剂沸点升高,挥发速度减慢。
根据上述分析可推断:在聚合物膜的制备过程中,开始时大量存在的DMF挥发较快,溶液迅速分相进入亚稳态区域,形成PVDF-HFP富相和贫相,富相中的聚合物由于缺乏溶剂而沉淀成为微孔膜的骨架。此时聚合物骨架之间仍包容有含DMF的PVDF-HFP贫相,而贫相中的溶剂由于与PVDF-HFP的相互作用,沸点相对较高,挥发速度较慢。当加热挥发这部分溶剂后,原贫相位置就形成孔穴,贫相中的PVDF-HFP就附着在骨架上形成微晶,从而产生网络化的微孔。实验结果也表明:成膜刚开始时DMF挥发较快,但当形成了膜的骨架后,剩余的溶剂则较难挥发。
2.3 聚合物电池的循环性能
图5所示是分别用正极自支撑和非自支撑的PVDF-HFP聚合物电解质制备的电池在0.1C倍率充放电时的循环性能。由图可知:自支撑电解质制备的聚合物电池正极材料首次放电容量为141 mA?h?g-1,40次循环后容量仍保持在137.5 mA?h?g-1,容量保持率为97.5%,循环性能优良;而用未支撑的电解质制备的电池首次放电容量为140 mA?h?g-1,40次循环后容量衰减5%左右。
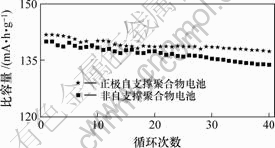
图5 聚合物电池的循环性能
Fig.5 Cycling performance of polymer cells
2.4 聚合物电池的EIS分析
电池性能与其阻抗关系密切。图6所示为聚合物电池首次充满电后的EIS图谱。阻抗图在实轴上的截距是电池的溶液阻抗Rb,高频半圆体现的是界面阻抗Rin,中频半圆体现的是电荷传递阻抗Rct[14]。对于聚合物电池,界面阻抗包括SEI膜阻抗和聚合物电解质与电极之间的接触阻抗。电解质对电极接触越紧,润湿越好,界面阻抗就越小。电荷传递阻抗反映的是锂离子从外界迁移嵌入正极晶格的阻力,正极材料的种类和晶格的粉化等对Rct影响较大。同时,界面阻抗也会影响其变化:Rin大,必然使电池极化增加,正极中的锂难以完全脱出[14-15],因而,正极晶格中锂的空位就越少,锂离子嵌入正极越困难,Rct也就随之变大。
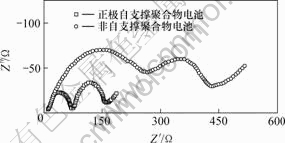
图6 聚合物电池的阻抗图谱
Fig. 6 Impedance spectrum of polymer cells
由图6可知:非支撑型电解质制备的电池界面阻抗达260 Ω,而正极自支撑的电解质制备的电池界面阻抗只有60 Ω。这显然是因为该聚合物电解质与电极接触牢固,因而其界面阻抗不到前者的1/4。
图7所示是2种电池循环过程中各阻抗的变化情况。图中两电池的溶液阻抗都很小,且基本无变化,但两者的Rin和Rct变化趋势却不同。用非支撑型电解质制备的电池界面阻抗增加快,其电荷传递阻抗也随之增加;而用正极自支撑电解质制备的电池两阻抗变化均较小。这说明其电池的界面性质较稳定,其原因可能是:电解质与正极接触牢固,不易脱落,同时还能有效减少电解液的流失,因而循环时电解质对电极接触和润湿好。正是由于该电池阻抗小,界面性质稳定,因此,电池的充放电循环性能优良。
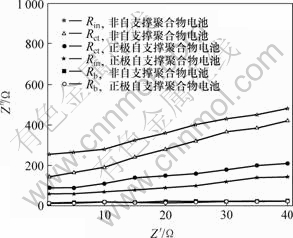
图7 循环过程中电池的阻抗变化
Fig.7 Change of resistance of batteries during cycling
2.5 聚合物电池的倍率放电性能
用聚合物电解质制备的锂离子电池不仅要求循环性能好,而且还要具有较强的倍率放电能力。图8所示是聚合物电池的不同倍率放电性能。由图8可知:用正极自支撑电解质制备的电池在较高倍率放电时电压下降很小;0.5C倍率放电容量为138 mA?h?g-1,1C放电容量为135 mA?h?g-1,0.5C和1C放电时分别能保持0.1C放电容量的97.8%和95.7%,比文献[4, 16]报道的其他聚合物电池的倍率放电性能明显要好。聚合物电解质孔穴丰富,吸收电解液能力强,制备的聚合物电池界面阻抗小是电池倍率放电性能优良的主要原因。非支撑型电解质制备的聚合物电池阻抗较大,放电时电池极化大,因此,容量和放电电压都有所降低。这种现象在较高倍率放电时尤为突出。
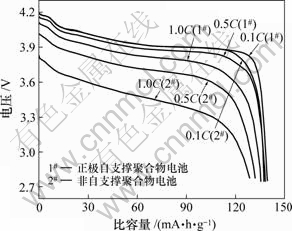
图8 聚合物电池的倍率放电性能
Fig.8 Rate performance of polymer cells
电池的循环性能和倍率放电能力表明:采用直接挥发溶剂法制备正极自支撑的聚合物电解质是可行的。
3 结 论
a. 以DMF为溶剂,PVDF-HFP为聚合物基质,采用挥发溶剂法将聚合物电解质直接制备于正极上,可获得孔穴丰富的聚合物电解质膜,吸收电解液后室温离子电导率为1.56 mS?cm-1。
b. 正极自支撑的聚合物电解质可牢固粘附于正极片上,能卷绕而不易断裂。用其制备的聚合物锂离子电池界面阻抗为60 Ω,仅为用非支撑型聚合物电解质制备的电池界面阻抗的23%,且循环过程中界面性质稳定。
c. 聚合物电池0.1C倍率循环40次后容量保持率为97.5%,0.5C和1C放电时分别能保持0.1C放电容量的97.8%和95.7%。
参考文献:
[1] Zhang S S, Ervin M H, Xu K, et al. Microporous P(AN-MMA) membrane as a separator of rechargeable lithium battery[J]. Electrochimica Acta, 2004, 49(20): 3339-3345.
[2] Song M K, Kim Y T, Cho J Y, et al. Composite polymer electrolytes reinforced by non-woven fabrics[J]. Journal of Power Sources, 2004, 125(1): 10-16.
[3] Wang M K, Qi L, Zhao F, et al. A novel comb-like copolymer based polymer electrolyte for Li batteries[J]. Journal of Power Sources, 2005, 139(1): 223-229.
[4] Wang Z L, Tang Z Y. Characterization of the polymer electrolyte based on the blend of PVDF-HFP and PVP for lithium battery[J]. Materials Chemistry and Physics, 2003, 82(1): 16-20.
[5] Song J Y, Wang Y Y, Wang C C. Review of gel-type polymer electrolytes for lithium batteries[J]. Journal of Power Sources, 1999, 77(1): 183-197.
[6] Zhang S S, Xu K, Foster D L, et al. Microporous gel electrolyte Li-ion battery[J]. Journal of Power Sources, 2004, 125(1): 114-118.
[7] 赵 毅, 王 涛, 徐 帆, 等. 以水作相分离造孔剂制备P(VDF-HFP)/PMMA聚合物电解质膜[J]. 高等学校化学学报, 2004, 25(5): 922-925.
ZHAO Yi, WANG Tao, XU Fan, et al. Preparation of P(VDF-HFP)/PMMA blend polymer electrolyte membrane with water as material for phase separation and pore producer)[J]. Chemical Journal of Chinese Universities, 2004, 25(5): 922-925.
[8] 任旭梅, 顾 辉, 陈立泉, 等. 新型锂离子电池聚合物电解质的制备[J]. 高等学校化学学报, 2002, 23(7): 1383-1385.
REN Xu-mei, GU Hui, CHEN Li-quan, et al. Preparation of polymer electrolyte for lithium-ion battery[J]. Chemical Journal of Chinese Universities, 2002, 23(7): 1383-1385.
[9] 陈作锋, 姜艳霞, 庄全超, 等. 一种新型微孔聚合物电解质的制备与表征[J]. 科学通报, 2005, 50(7): 638-642.
CHEN Zuo-feng, JIANG Yan-xia, ZHUANG Quan-chao, et al. Preparation and characterization of a new microporous polymer electrolyte[J]. Chinese Science Bulletin, 2005, 50(7): 638-642.
[10] 陈作锋, 姜艳霞, 庄全超, 等. MCM-41介孔分子筛掺杂的微孔聚合物电解质的制备与表征[J]. 电化学, 2005, 11(2): 162-166.
CHEN Zuo-feng, JIANG Yan-xia, ZHUANG Quan-chao),et al. Preparation and characterization in MCMB-41/PVDF-HFP composite microporous polymer electrolyte for Li-oin battery[J]. Electrochemistry, 2005, 11(2): 162-166.
[11] Xi J Y, Tang X Z. Enhanced Lithium ion transference number and ionic conductivity of composite polymer electrolyte doped with organic-inorganic hybrid P123@SBA-15[J]. Chemical Physics Letters, 2004, 400(1): 68-73.
[12] Michael M S, Prebaharan S R S. Rechargeable lithium battery employing a new ambient temperature hybrid polymer electrolyte based on PVK+PVDF-HFP(copolymer)[J]. Journal of Power Sources, 2004, 136(2/3): 408-415.
[13] 徐寿昌. 有机化学[M]. 北京: 高等教育出版社, 1981: 89-91.
XU Shou-chang. Organic Chemistry[M]. Beijing: Higher Education Press, 1981: 89-91.
[14] Kum K S, Song M K, Kim Y T, et al. The effect of mixed salts in gel-coated polymer electrolyte for advanced lithium battery[J]. Electrochimica Acta, 2004, 50(1): 285-288.
[15] 张 森, 史鹏飞. 新型聚合物锂离子蓄电池的性能和失效机理[J]. 电源技术, 2004, 128(4): 206-230.
ZHANG Sen, SHI Peng-fei. Performance characteristics and failure mechanism of a new type polymer lithium battery[J]. Chinese Journal of Power Sources, 2004, 128(4): 206-230.
[16] Lee J Y, Kang Y K, Suh D H, et al. Ionic conductivity and electrochemical properties of cross-linked poly[siloxane- g-oligo(ethylene oxide)] gel-type polymer electrolyte[J]. Electrochimica Acta, 2004, 50(1): 351-356.
收稿日期:2006-05-25
基金项目:国家高技术研究发展计划资助项目(2003AA32X010)
作者简介:胡拥军(1968-),男,湖南益阳人,博士研究生;主要从事锂离子电池研究
通讯作者:胡拥军,博士生;电话:0731-8876621;E-mail: hyjwsg@163.com