
DOI: 10.11817/j.issn.1672-7207.2020.12.011
废旧三元锂离子电池正极还原焙烧回收Li的研究
严康,熊正阳,刘志楼,徐志峰,王瑞祥,聂华平
(江西理工大学 绿色冶金与过程强化研究所,江西 赣州,341000)
摘要:对废旧锂离子电池正极料还原焙烧回收Li的工艺、还原焙烧过程中Li还原产物及其形态变化行为进行研究。采用控制变量法,通过单因素实验研究焙烧过程中焙烧温度、焙烧时间、还原剂用量对Li氢化浸出的影响。采用X线衍射仪、扫描电镜-能谱(SEM-EDS)对还原焙烧产物物相及形貌进行表征,通过Factsage软件计算焙烧过程热力学,研究还原焙烧过程中Li还原产物在不同温度下的存在形式以及不同形式的存在条件。研究结果表明:当焙烧温度为650 °C,焙烧时间为3 h,含碳量(即碳质量分数)为20%时,Li的浸出率最高,达90.33%;随着焙烧温度从500 °C提高到750 °C,Li2CO3及低价有价金属稳定区呈现出先变大后减小的趋势;高温、长时间焙烧对于Li2CO3生成有抑制作用;当含碳量低于10%时,增加含碳量对还原反应影响较大,当含碳量高于10%时,增加含碳量对还原反应影响较小。
关键词:Li回收;还原焙烧;热力学;浸出率
中图分类号:X24 文献标志码:A 开放科学(资源服务)标识码(OSID)
文章编号:1672-7207(2020)12-3367-12
Study on recycling Li of waste lithium ion batteries by reduction roasting
YAN Kang, XIONG Zhengyang, LIU Zhilou, XU Zhifeng, WANG Ruixiang, NIE Huaping
(Institute of Green Metallurgy and Process Intensification, Jiangxi University of Science and Technology,Ganzhou 341000, China)
Abstract: The technology of recovering Li from waste lithium ion positive electrode by reduction roasting and the change of Li reduction products and their morphology during reduction roasting were studied. The influences of calcination temperature, calcination time and reducing agent amount on Li hydrogenation leaching were studied by using the control variable method and single factor experiment. X-ray diffractometer and SEM-EDS were used to characterize the materials during the reduction roasting, and then the thermodynamics of the roasting process was calculated by Factsage software to comprehensively explain the existence forms of Li reduced products at different temperatures and the existence conditions of different forms during the reduction roasting. The results show that when the roasting temperature is 650 ℃, the roasting time is 3 h and the carbon mass fraction is 20%, the leaching rate of Li reaches 90.33%. With the increase of calcination temperature from 500 ℃ to 750 ℃, the formation difficulty of Li2CO3 and the stable area of low-priced valuable metal increases. Roasting at high temperature for a long time has inhibitory effect on the formation of Li2CO3 when the carbon content is lower than 10%, but increasing the carbon content has greater impact on the reduction reaction, and the carbon content is less affected when the carbon content is higher than 10%.
Key words: lithium recycling; reduction roasting; thermodynamics; leaching rate
近年来,锂离子电池(lithium ion batteries, LIBs)使用量持续增高,预计到2025年,废旧LIBs的报废量将达到97.7 GW・h,若大量报废的LIBs得不到合理处理,将对环境产生巨大危害[1-5]。LIBs中含有Ni,Co,Mn和Li等多种有价金属,回收LIBs对于解决环境污染以及金属资源相对匮乏问题都具有重大意义[6-7]。目前,对于废旧LIBs正极材料的主要回收方法有湿法冶金、火法冶金、湿法-火法联合冶金[8-14],其中湿法冶金应用最广泛。MESHRAM等[15]以H2SO4为浸出剂,NaHSO3为还原剂,在368 K下浸出正极活性材料(nickel cobalt manganese,NCM),Li浸出率可达96.7%。采用此方法可得到较高的Li浸出率,但浸出尾液难以处理,且Li和其他有价金属较难分离,回收率难以保证。LI等[16]使用H2O2和柠檬酸对NCM进行浸出,通过溶胶-凝胶法合成的新型NCM电化学性能优异,可实现有价金属高效利用,但有机酸浸出后废水难以处理且处理成本偏高,难以实现工业化应用。由于正极材料结构稳定,采用常规湿法回收废旧LIBs中有价金属时,需要添加H2O2和NaHSO3等还原剂[17-18]才能实现有价金属浸出。后续分离Ni,Co和Mn所使用的沉淀法存在流程长、操作复杂等缺点,使用萃取法分离有价金属存在损失率大等缺点[19]。鉴于常规湿法所存在的诸多问题[20-21],一些研究者提出了更加环保且经济的回收方法,如:LI等[22]使用石墨和LiCoO2在1 000 °C下无氧焙烧,经过磁选回收Co,Li和石墨,Li回收率达98%,此法绿色环保且在应用过程中不引入杂质,但Li2CO3在水中溶解度很低,湿法磁选时需要大量浸出液,且焙烧温度高,容易烧结,使得回收产物纯度偏低。HU等[23]将LiNixCoyMn1-x-yO2与褐煤在650 ℃下无氧焙烧后,对焙烧渣进行碳酸水浸,质量分数为84.7%的Li被选择性浸出,浸出渣使用H2SO4浸出,Ni,Co和Mn回收率高达99%。人们虽然研究了相应的浸出条件,Li浸出率较高,但仍不能满足高效回收Li的要求。目前,人们对焙烧过程中的有价金属行为和热力学研究较少,不能很好地解释Li浸出率不够高以及在焙烧过程中Li富集形态变化的原因。为此,本文作者提出使用电解废阴极和LIBs正极料还原焙烧水浸回收Li,对焙烧过程进行进一步研究,对焙烧过程中Li以及其他有价金属行为进行表征和解释,并且通过热力学计算,进一步揭示还原焙烧水浸提锂机理,以期为废旧锂离子电池中锂的回收提供新思路。
1 实验
1.1 实验原料
本实验所使用原料为赣州某电子厂废旧锂离子电池经过预处理之后的正极活性材料。还原剂(含碳量(即碳质量分数)为90.7%)为赣州某电解厂电解废阴极破碎后粉料,NCM化学成分质量分数见表1。为确定NCM组成,对其进行XRD表征,结果见图1。
表1 锂离子电池正极活性材料成分质量分数
Table 1 Composition mass fraction of positive active materials of lithium ion battery %
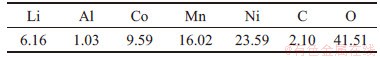
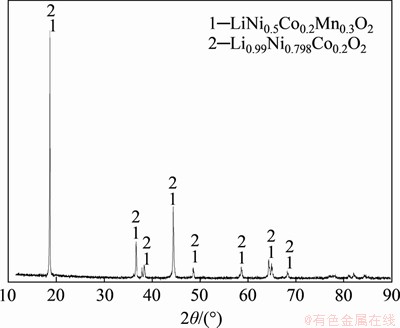
图1 预处理后正极活性材料XRD图谱
Fig. 1 XRD pattern of positive electrode active material after pretreatment
由表1可知:三元活性材料的主要物质为镍、钴、锰、锂、氧,在预处理之后仍然存在1.03%(质量分数,下同)的Al以及2.10%的碳杂质。从三元配比来看,正极活性材料为高镍低钴中锰型NCM523。由图1可见:原料中的成分为LiNi0.5Co0.2Mn0.3O2以及Li0.99Ni0.798Co0.2O2,联合表1中原料各元素质量分数可知正极料中主要成分为LiNi0.5Co0.2Mn0.3O2。
1.2 实验方法
1.2.1 热力学分析方法
采用Factsage软件绘制不同温度下Li-Co-C-O系、Li-Ni-C-O系、Li-Mn-C-O系热力学稳定区域图。根据不同温度下Li-Me-C-O系各热力学稳定区域随温度的变化,探讨Li以及其他有价金属在还原焙烧过程中物相及存在形态的变化规律。
1.2.2 实验过程
将粒度低于0.075 mm的正极活性粉料与粒度低于0.075 mm的废阴极粉料混合,依次改变焙烧温度、焙烧时间、焙烧料碳含碳量对NCM进行还原焙烧得到烧后料,将焙烧后料磨至统一粒度进行水浸,在水浸过程中保持浸出条件一致,考察不同焙烧因素对水浸提Li的影响。通过Li浸出率确定最优还原焙烧条件。水浸氢化反应原理为
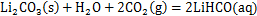 (1)
(1)
Li浸出率计算方程式如下:
 (2)
(2)
式中: 为Li浸出率,%;
为Li浸出率,%; 为焙烧产物中Li质量分数,%;
为焙烧产物中Li质量分数,%; 为焙烧产物质量,g;
为焙烧产物质量,g; 为浸出液中Li质量浓度,g/L;
为浸出液中Li质量浓度,g/L;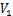 为浸出液体积,mL。
为浸出液体积,mL。
1.3 分析与测试
采用电感耦合等离子体原子发射光谱(ICAP7400,美国Thermo公司)检测焙烧后料及浸出液中锂的质量浓度。采用X线衍射仪(MiniFlex600,日本Rigaku公司,铜靶)分析还原焙烧产物物相组成,采用扫描式电子显微镜-能谱仪(FEI-Prisma-E,美国Thermo公司)分析还原焙烧产物微观形貌及元素组成。
2 结果与讨论
2.1 Li还原焙烧过程热力学研究
NCM焙烧过程中存在多种还原反应及还原产物,先对焙烧过程理论热力学进行研究,这对后续实验条件的设计以及结果、表征、分析解释具有较大参考意义。Li-Co-C-O系下不同温度的热力学稳定区域图如图2所示(其中, 和
和 分别为理论反应环境中的O2分压和CO分压)。
分别为理论反应环境中的O2分压和CO分压)。
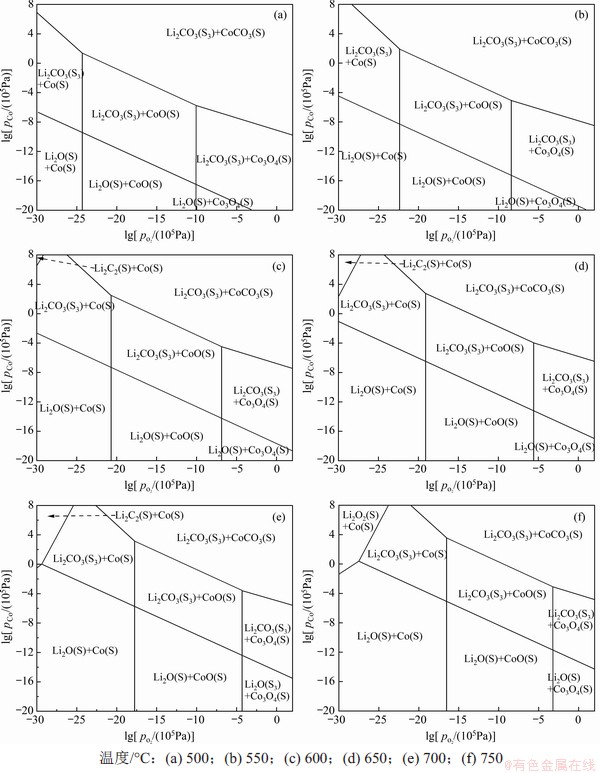
图2 Li-Co-C-O系热力学稳定区域图
Fig. 2 Thermodynamic stability diagrams of Li-Co-C-O system
从图2可见:当温度从500 ℃上升至650 ℃时,Li2CO3和Co低价氧化物及单质的稳定区域面积不断变大;当温度超过650 ℃时,Li2CO3和Co低价氧化物及单质的稳定区域面积开始逐渐变小,这说明在650 ℃之前,高焙烧温度有利于Li2CO3生成,当温度超过650 ℃时,Li2CO3稳定区域面积变小;继续升高焙烧温度对Li2CO3生成有抑制作用,在高温焙烧下主要产物为Li2CO3及Co单质或低价Co氧化物。
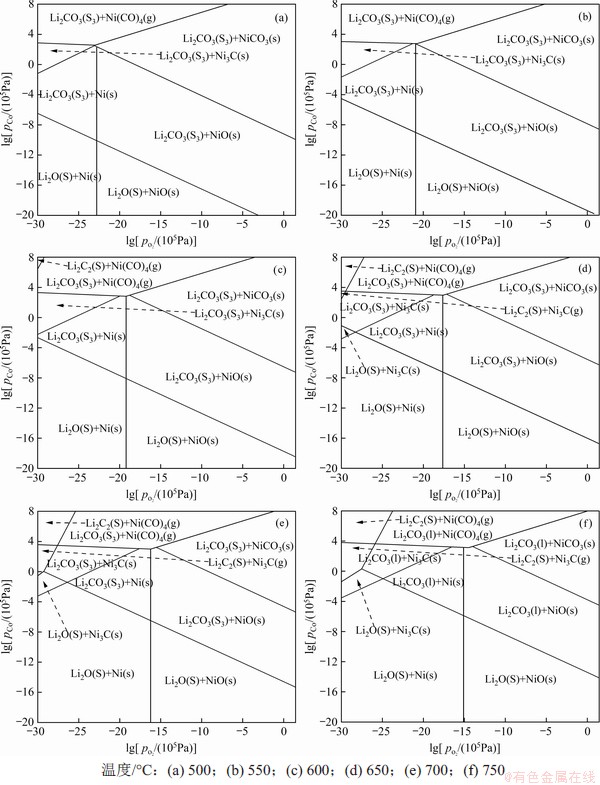
图3 Li-Ni-C-O系热力学稳定区域图
Fig. 3 Thermodynamic stability diagram of Li-Ni-C-O system
在不同温度下,Li-Ni-C-O系热力学稳定区域图如图3所示。从图3可见:当焙烧温度由500 ℃升高至600 ℃时,Li2CO3稳定区域面积呈现出增大趋势;当焙烧温度由650 ℃升高至750 ℃时,Li2CO3热力学稳定区域面积不断变小,Li2CO3生成难度增大;在整个升温过程中,Ni及NiO稳定区域总体向右偏移,说明随温度升高,Ni的生成趋势变强,还原产物中Ni质量分数逐渐增高;在750 ℃时,Li2CO3从固相转变为液相,说明温度在升高至700 ℃后可能存在烧结现象,从而改变Li2CO3和Ni与NiO的结合形态,进而影响Li的浸出率。
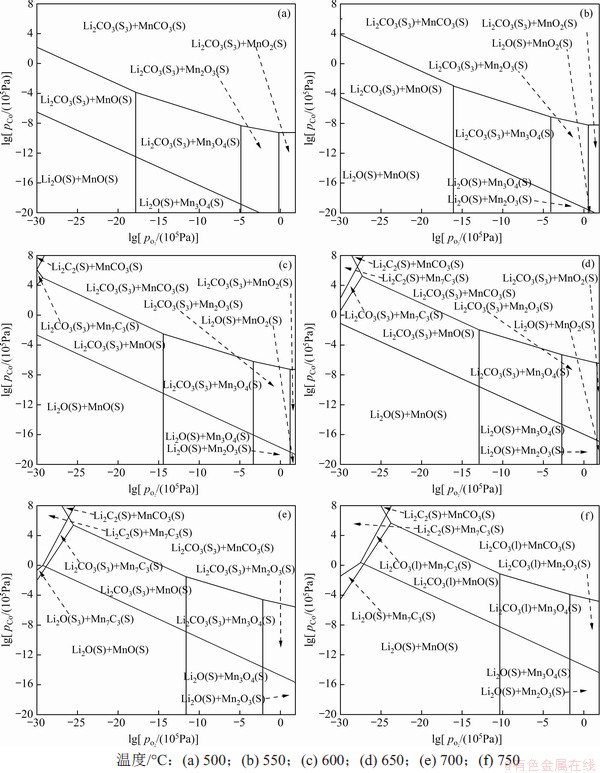
图4 Li-Mn-C-O系热力学稳定区域图
Fig. 4 Thermodynamic stability diagram of Li-Mn-C-O system
在不同温度下,Li-Mn-C-O系热力学稳定区域图如图4所示。由图4可见:当焙烧温度由500 ℃升高至750 ℃时,Li2CO3热力学稳定区域面积呈现出先增大后减小的趋势,其稳定区域面积在600 ℃至650 ℃之间达到最大,继续升高温度,Li2CO3稳定区面积变小,生成受到抑制。MnO热力学稳定区域面积随温度升高持续增大,说明焙烧温度升高,Mn的存在形态会逐渐变为MnO形式,并且在700 ℃升至750 ℃过程中,Li2CO3物态由固相变为液相,说明Li2CO3在此过程中发生熔化,可能导致烧结现象严重,从而改变Li2CO3和MnO的结合形态,进而影响Li的浸出率。
2.2 还原焙烧实验
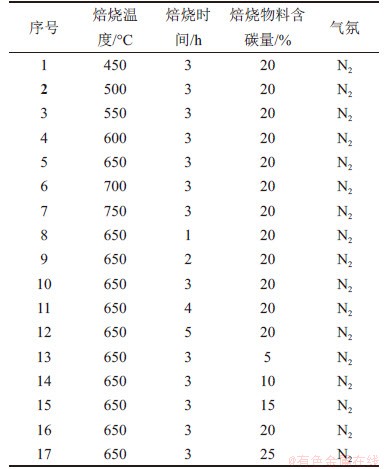
在水浸前,先将正极粉料与废阴极粉料混合,进行还原焙烧实验,分别控制焙烧温度为550~750 ℃,焙烧时间为1~5 h,焙烧物料含碳量为5%~25%,在常压N2气氛下还原焙烧。实验条件如表2所示。
表2 焙烧实验条件
Table 2 Experimental conditions of roasting
2.3 水浸提锂实验
继还原焙烧得到还原产物后,将焙烧产物研磨至粒度为0.075 mm进行水浸实验,水浸条件如下:浸出液固比为15:1,浸出时间为90 min,浸出温度为10 ℃,CO2通入速率为800 mL/min,机械搅拌为400 r/min。
2.3.1 焙烧温度对水浸提锂的影响
保持焙烧时间3 h,焙烧料含碳量20%不变,考察不同焙烧温度(550,600,650,700和750 ℃)对水浸提锂的影响,结果如图5所示。由图5可见:随着焙烧温度不断增高,Li浸出率呈现先升高后降低的变化规律;当焙烧温度为650 ℃时, 浸出率最高,达90.33%。这可能是由于在650 ℃前,还原反应充分发生,导致Li2CO3生成量增加;而在650 ℃后,焙烧产物过分还原Li2CO3,产生烧结现象,与其他低价金属氧化物或单质结合方式发生变化。实验结果与热力学分析结果基本一致。
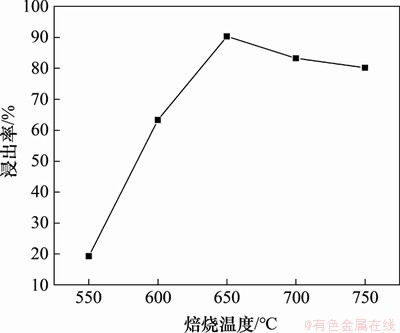
图5 不同焙烧温度下的Li碳化浸出率
Fig. 5 Li carbonization leaching rate at different roasting temperatures
2.3.2 焙烧时间对水浸提锂的影响
保持焙烧温度为650 ℃,含碳量20%不变,考察不同焙烧时间(1,2,3,4和5 h)对水浸提锂的影响,结果如图6所示。从图6可见:随着焙烧时间延长,Li浸出率呈现出先上升后下降的趋势,在焙烧时间为3 h时,达到最高值90.33%。其原因可能是在1~3 h过程中还原反应不充分,Li2CO3生成量呈上升趋势,在3 h后还原反应过度,部分Li2CO3与低价有价金属氧化物结合方式发生改变。
2.3.3 焙烧料含碳量对水浸提锂的影响
保持焙烧温度为650 °C,焙烧时间为3 h不变,考察焙烧料不同含碳量(5%,10%,15%,20%和25%)对水浸提锂的影响,结果如图7所示。从图7可见:随着焙烧料含碳量增加,Li浸出率呈现先上升后逐渐平缓的变化趋势;在焙烧料含碳量达到10%时,Li浸出率达到88.52%;随着碳含量的继续增加,Li浸出率上升幅度很小。其原因可能是在碳含量低于10%时,添加还原剂使得还原焙烧反应更加充分,Li2CO3生成量不断增加;在还原剂添加达到10%左右时,还原反应基本完成,继续添加还原剂对还原反应影响很小。
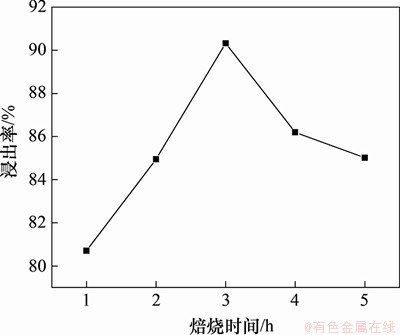
图6 不同烧结时间下的Li碳化浸出率
Fig. 6 Li carbonization leaching rate under different roasting time
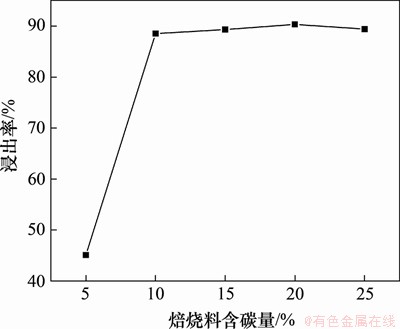
图7 物料含碳量不同时的Li碳化浸出率
Fig. 7 Li carbonization leaching rate under different carbon mass fractions
2.4 焙烧物料表征
2.4.1 焙烧产物XRD表征
通过不同焙烧条件下单因素实验得到如下最优焙烧条件:焙烧温度为650 ℃,焙烧时间为3 h,焙烧料含碳量为20%。在此条件下,水浸提锂的浸出率可达90.33%。为了进一步探究焙烧过程中的物相变化,对不同焙烧条件下的焙烧后料进行XRD检测分析。
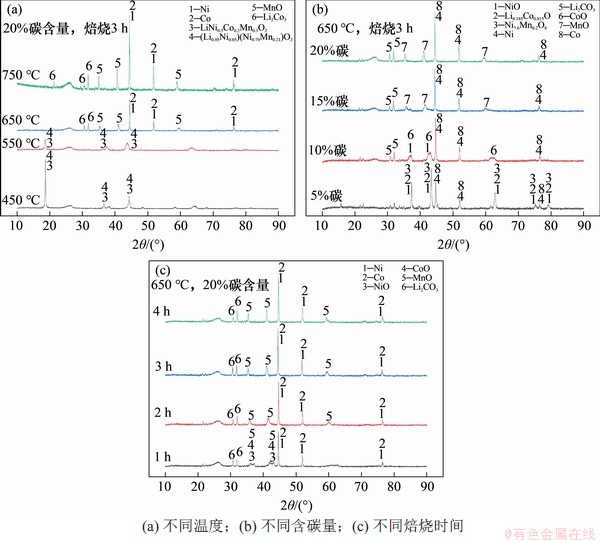
图8 不同条件因素下焙烧产物XRD图
Fig. 8 XRD patterns of roasted products under different conditions
不同温度下焙烧产物XRD图如图8(a)所示。从图8(a)可见:在焙烧温度为450 ℃时,主要焙烧产物为三元正极材LiNi0.5Co0.2Mn0.3O2,这说明在此温度下,还原反应并未发生,且三元材料的物相也没有发生变化;当温度上升至550 ℃时,三元物相的峰强大幅度减弱,但并未有其他物质衍射峰产生,这说明在此温度下,三元结构发生变化,但并未发生还原反应生成还原产物;在650 ℃焙烧温度下,三元物相峰完全消失,并且出现了Li2CO3,Ni,Co以及MnO峰,说明三元正极料发生了还原反应,Ni和Co的氧化物被大量还原为单质,Mn的高价氧化物被还原成二价的氧化亚锰;Li大量生成相应的Li2CO3,为水浸提锂提供了依据;当温度达到750 ℃时,整体峰值和650 ℃焙烧产物峰值相比差距不大,金属单质峰强度变大,Li2CO3峰仍然存在但峰型和强度发生了变化,这可能是其存在形式和生成量发生了改变,说明在750 ℃焙烧条件下,还原产物焙烧充分,烧结明显,晶型变得更好,同时也使得部分Li2CO3与其他有价金属结合更紧密,增加了浸出难度,导致温度进一步升高时浸出率下降。这与热力学计算结果基本一致。
不同含碳量焙烧产物XRD研究结果如图8(b)所示。从图8(b)可见:在含碳量为5%时,三元物质峰消失,还原反应发生,Li0.185Co0.815O,Ni7.6Mn0.2O8和NiO峰出现,说明三价Ni和Co以及高价态的Mn被初步还原为二价Ni,Co和Mn氧化物并且与Li氧化物结合。还原焙烧不充分,大量Li并未生成Li2CO3,因此,Li浸出率并不高;在含碳量为10%时,Li0.185Co0.815O,Ni7.6Mn0.2O8和NiO峰大幅度减小,Ni和Co单质衍射峰增强,Li2CO3峰明显出现,说明还原反应进一步发生,低价态的Ni和Co氧化物被进一步还原为单质Ni和Co,Li2CO3大量生成。可见:从含碳量为15%和20%的焙烧产物物相看,二者衍射峰与10%含碳量焙烧产物的衍射峰相比变化并不明显,区别主要在于NiO和CoO衍射峰消失,以及MnO,Ni和Co的衍射峰强稍微变高。因此,继续添加还原剂用量对Li2CO3浸出影响很小。
在不同焙烧时间条件下,产物XRD研究结果如图8(c)所示。从图8(c)可见:当焙烧时间为1 h时,还原反应明显发生,Li2CO3峰出现,NiO和CoO峰微弱,同时,MnO峰刚刚出现,说明NiO和CoO的结构已被破坏,并进一步向单质方向还原,MnO开始生成;从2 h和3 h的峰型看,Li2CO3峰强进一步增大,而其他物质衍射峰变化较小,说明在此过程中,还原产物Li2CO3生成量变多,同时,Li2CO3浸出率上升也表现出一致性;4 h的峰相较于2 h和3 h的峰,单质以及MnO峰强度更高,说明还原反应更加充分,但Li2CO3峰发生了微小变化,其原因可能是,在充分焙烧情况下,Li2CO3和其他有价金属的结合发生了新的变化,或者是还原反应发生过度,Li的存在形式从Li2CO3向其他形式发生了转变,这仍需进一步研究。
2.4.2 焙烧产物SEM-EDS分析
对2.2节中部分还原焙烧产物进行SEM-EDS表征,分析不同焙烧条件下有价金属行为。在温度为650 ℃、含碳量为20%、时间为1 h的焙烧条件下,焙烧产物SEM-EDS如图9所示。从图9可见:在此焙烧条件下,三元结构完全被破坏,形貌呈现出不规则簇状堆叠在一起,整体附着在大块废阴极碳上;点1的EDS元素分析结果表现出Ni和Co质量分数高、Mn质量分数低的分布规律,O质量分数为19.35%,说明簇状区域有价金属的主要存在形态为Ni和Co低价氧化物。联立图6中该条件下Li浸出率80.7%以及图8(c)中Ni和Co单质峰可知,仍存在少量单质Ni和Co以及部分Li2CO3。
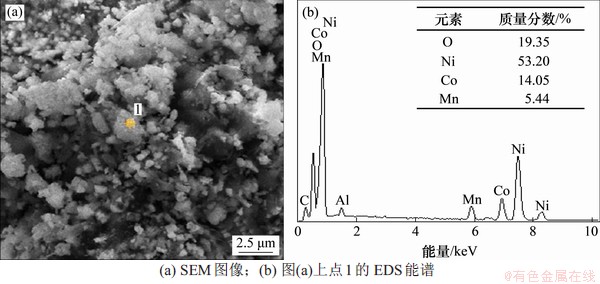
图9 在温度为650°C、含碳量为20%、时间为1 h时焙烧产物的SEM-EDS
Fig. 9 SEM-EDS of roasted products at 650 °C and 20% carbon mass fraction for 1 h

图10 在温度为650°C、含碳量为20%、时间为3 h时焙烧产物的SEM-EDS
Fig. 10 SEM-EDS of roasted products at 650 °C and 20% carbon mass fraction for 3 h
在温度为650 ℃、含碳量为20%、时间为3 h的焙烧条件下,焙烧产物SEM-EDS如图10所示。从图10可见:在温度为650 ℃、含碳量为20%时,焙烧3 h与焙烧1 h相比,其簇状区域堆叠变少,呈现出部分规则六面体型,整体也趋向于向规则型转变。通过点1的EDS元素分布可以看出,在规则的六面体上几乎全部都是Ni和Co,仅含2.22% O,说明规则区域为Ni和Co单质富集区Li2CO3质量分数较低。联立图8(a)及其余簇状区域的变化趋势分析可知,簇状区域多数应为未形成较好晶型的Ni和Co单质以及部分Mn氧化物。该条件下Li浸出率90.7%(见图5)可以推测在这些区域中,Li2CO3质量分数应该较高,与其对应产物的XRD物相也一致。
在温度为450 ℃、含碳量为20%、焙烧时间为3 h的焙烧条件下,焙烧产物SEM-EDS如图11所示。从图11可见:在此焙烧条件下,焙烧产物形貌依旧呈现出三元材料的规则球形。通过对球形上点1的EDS分析结果可知,其Ni,Co,Mn及O的质量分数分别与焙烧前三元正极料NCM523中Ni,Co,Mn和O的质量分数大致相同,说明在450 ℃下还原反应并未发生,且反应物形貌也并未发生改变,没有Li2CO3生成,因此,在温度低于450 ℃时,Li水浸氢化反应不能发生,表现出Li浸出率低。

图11 在温度为450°C、含碳量为20%、焙烧时间为3 h时焙烧产物的SEM-EDS
Fig. 11 SEM-EDS of roasted products at 450 °C and 20% carbon content for 3 h
在温度为650 ℃、含碳量为5%、焙烧时间为3 h的焙烧条件下,焙烧产物SEM-EDS如图12所示。从图12可见:在该条件下焙烧后,三元材料结构被破坏,焙烧产物形貌呈现出大小不规则圆球形以及团聚堆叠亮色区域。对图12(a)中亮、暗球形区域进行EDS检测发现,不规则暗色球形区域元素分布呈现出Ni和Co质量分数较高、Mn质量分数较低的现象,且O质量分数只有15.67%,说明此区域主要物质为Ni和Co低价氧化物。联立图7中该条件下Li浸出率45%以及图8(b)中存在的Li2CO3,Ni和Co衍射峰可知,其中存在部分Li2CO3,Ni和Co单质以及少量Mn氧化物;亮色堆叠区域元素分布与三元材料的一致性说明不规则的堆叠区域是结构被破坏但还未发生还原反应的三元物质。
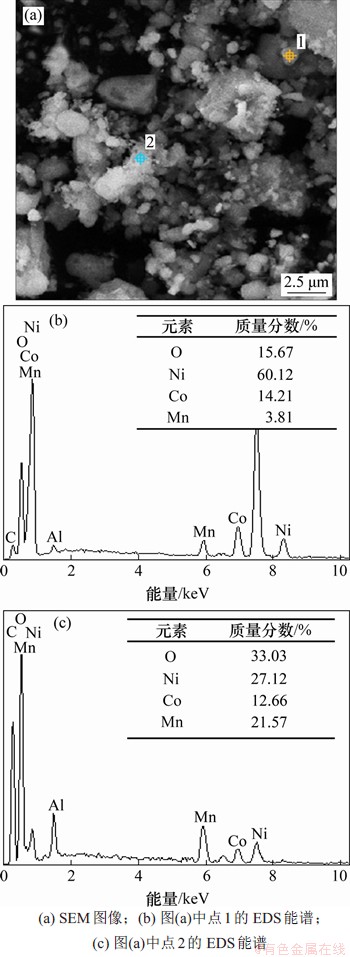
图12 在温度为650°C、含碳量为5%、焙烧时间为3 h时的焙烧产物SEM-EDS
Fig. 12 SEM-EDS of roasted products at 650 °C with 5% carbon mass fraction for 3 h
通过对不同焙烧条件下还原焙烧产物的SEM-EDS能谱进行分析可知:当焙烧温度低于450 ℃时,还原反应不能发生,NCM形态结构未发生改变。根据低含碳量与高含碳量对比、1 h焙烧与3 h焙烧对比可知:在低含碳量和焙烧时间较短情况下,还原反应发生不充分,有Li2CO3生成,但生成量较低,且有价金属还原产物主要为低价氧化物。在还原反应发生完全的条件下,Li2CO3生成量达到最高,其他有价金属还原产物主要为单质及少量低价氧化物。
3 结论
1) 在温度为650 ℃、焙烧时间为3 h、焙烧料含碳量为20%时,水浸过程Li浸出率最高,可达90.33%,且其余有价金属几乎不进入溶液中,达到较好的提Li效果。
2) 当焙烧温度低于450 ℃时,还原反应无法发生,三元活性材料结构完整。当焙烧温度高于600 ℃时,还原反应明显发生,Li2CO3在600~650 ℃时生成量增多;当焙烧温度高于650 ℃时,Li2CO3烧结明显,与Ni和Co单质结合力加强,浸出难度增大,浸出率下降。焙烧1 h时。还原反应明显;当焙烧时间达到3 h时,Li2CO3浸出率下降;当焙烧料碳含量低于10%时,增加还原剂用量对还原产物物相影响明显;当焙烧料碳含量高于10%时,继续增加还原剂用量对还原产物影响较小。
3) Li2CO3生成的稳定区域面积在500~750 ℃内随温度升高呈现出先增大后减小趋势;在700~750 ℃时,Li2CO3发生烧结现象,从而改变Li2CO3与其他有价金属单质或低价氧化物的结合方式,进而增加Li浸出难度。若得到尽可能多的Li2CO3及Ni,Co和MnO,则需控制焙烧温度在600~650 ℃之间。
参考文献:
[1] 黎华玲, 陈永珍, 宋文吉, 等. 湿法回收退役三元锂离子电池有价金属的研究进展[J]. 化工进展, 2019, 38(2): 921-932.
LI Hualing, CHEN Yongzhen, SONG Wenji, et al. Research progress on the recovery of valuable metals in retired LiNixCoyMnzO2 batteries by wet process[J]. Chemical Industry and Engineering Progress, 2019, 38(2): 921-932.
[2] SONG Yunfeng, ZHAO Zhongwei. Recovery of lithium from spent lithium-ion batteries using precipitation and electrodialysis techniques[J]. Separation and Purification Technology, 2018, 206(2): 335-342.
[3] 张英杰, 宁培超, 杨轩, 等. 废旧三元锂离子电池回收技术研究新进展[J]. 化工进展, 2019, 39(7): 2828-2840.
ZHANG Yingjie, NING Peichao, YANG Xuan, et al. New research progress on recycling technology of spent ternary lithiumion battery[J]. Chemical Industry and Engineering Progress, 2019, 39(7): 2828-2840.
[4] CONTESTABILE M, PANERO S, SCROSATI B. A laboratory-scale lithium-ion battery recycling process[J]. Journal of Power Sources, 2001, 92(1): 65-69.
[5] NATARAJAN S, ARAVINDAN V. Burgeoning prospects of spent lithium-ion batteries in multifarious applications[J]. Advanced Energy Materials, 2018, 8(33): 1-16.
[6] GRATZ E APELIAN D, ZOU Haiyang. A novel method to recycle mixed cathode materials for lithium ion batteries[J]. Green Chemistry, 2013, 15(5): 1183-1191.
[7] JO C H, MYUNG S T. Efficient recycling of valuable resources from discarded lithium-ion batteries[J]. Journal of Power Sources, 2019, 426: 259-265.
[8] SHIN S M, KIM N H, SOHN J S, et al. Development of a metal recovery process from Li-ion battery wastes[J]. Hydrometallurgy, 2005, 79(3/4): 172-181.
[9] YANG Li, XI Guoxi, XI Yuebin. Recovery of Co, Mn, Ni, and Li from spent lithium ion batteries for the preparation of LiNixCoyMnzO2 cathode materials[J]. Ceramics International, 2015, 41(9): 11498-11503.
[10] HANISCH C, HASELRIEDER W, KWADE A. Recovery of active materials from spent lithium-ion electrodes and electrode production rejects[C]// Glocalized Solutions for Sustainability in Manufacturing. Braunschweig, Germany, 2011: 85-89.
[11] HOU Peiyu, ZHANG Lianqi, ZHOU Enlou, et al. Recovery and heat treatment of the Li(Ni(1/3)Co(1/3)Mn(1/3))O2 cathode scrap material for lithium ion battery[J]. Journal of Power Sources, 2013, 232: 348-352.
[12] 张永禄, 尹飞, 揭晓武, 等. 碱循环浸出法分离废旧锂离子电池中铝的研究[J]. 有色金属(冶炼部分), 2018(12): 22-26.
ZHANG Yonglu, YIN Fei, JIE Xiaowu, et al. Study on removal of aluminum from spent lithium-ion batteries by alkali recycling leaching process[J]. Nonferrous Metals(Extractive Metallurgy), 2018(12): 22-26.
[13] LI Jinhui, LI Xinhai, HU Qiyang, et al. Study of extraction and purification of Ni, Co and Mn from spent battery material[J]. Hydrometallurgy, 2009, 99(1/2): 7-12.
[14] 陈亮, 唐新村, 张阳, 等. 从废旧锂离子电池中分离回收钴镍锰[J]. 中国有色金属学报, 2011, 21(5): 1192-1198.
CHEN Liang, TANG Xincun, ZHANG Yang, et al. Separation and recovery of Ni, Co and Mn from spent lithium-ion batteries[J]. The Chinese Journal of Nonferrous Metals, 2011, 21(5): 1192-1198.
[15] MESHRAM P, PANDEY B D, MANKHAND T R. Hydrometallurgical processing of spent lithium ion batteries (LIBs) in the presence of a reducing agent with emphasis on kinetics of leaching[J]. Chemical Engineering Journal, 2015, 281: 418-427.
[16] LI Li, BIAN Yifan, ZHANG Xiaoxiao, et al. Process for recycling mixed-cathode materials from spent lithium-ion batteries and kinetics of leaching[J]. Waste Management, 2018, 71: 362-371.
[17] YAO Lu, FENG Yong, XI Guoxi. A new method for the synthesis of LiNi1/3Co1/3Mn1/3O2 from waste lithium ion batteries[J]. RSC Advances, 2015, 55(5): 44107-44114.
[18] 朱显峰, 赵瑞瑞, 常毅, 等. 废旧锂离子电池三元正极材料酸浸研究[J]. 电池, 2017, 47(2): 105-108.
ZHU Xianfeng, ZHAO Ruirui, CHANG Yi, et al. Study on the acid leaching of ternary anode materials in spent Li-ion battery[J]. Battery Bimonthly, 2017, 47(2): 105-108.
[19] CHEN Xiangping, ZHOU Tao, KONG Jiangrong, et al. Separation and recovery of metal values from leach liquor of waste lithium nickel cobalt manganese oxide based cathodes[J]. Separation and Purification Technology, 2015, 141(2B): 76-83.
[20] LI Li, ZHANG Xiaoxiao, CHEN Renjie, et al. Synthesis and electrochemical performance of cathode material Li1.2Co0.13Ni0.13Mn0.54O2 from spent lithium-ion batteries[J]. Journal of Power Sources, 2014, 249: 28-34.
[21] 高岩, 李金辉, 李鹏举, 等. 由电池废料制备镍钴锰三元正极材料性能研究[J]. 电源技术, 2013, 37(6): 934-936.
GAO Yan, LI Jinhui, LI Pengju, et al. Research of NixCoyMnz material performance prepared from spent battery[J]. Chinese Journal of Power Sources, 2013, 37(6): 934-936.
[22] LI Jia, WANG Guangxu, XU Zhenming. Environmentally-friendly oxygen-free roasting/wet magnetic separation technology for in situ recycling cobalt, lithium carbonate and graphite from spent LiCoO2/graphite lithium batteries[J]. Journal of Hazardous Materials, 2016, 302: 97-104.
[23] HU Juntao, ZHANG Jialiang, LI Hongxu, et al. A promising approach for the recovery of high value-added metals from spent lithium-ion batteries[J]. Journal of Power Sources, 2017, 351: 192-199.
(编辑 陈灿华)
收稿日期: 2020 -07 -30; 修回日期: 2020 -09 -22
基金项目(Foundation item):国家自然科学基金资助项目(51904124) (Project(51904124) supported by the National Natural Science Foundation of China)
通信作者:聂华平,硕士,教授,从事复杂金属二次固废高效资源化等研究;E-mail: ntpben@163.com