PRGD/PDLLA/��-TCP/NGF�������ܵ��Ʊ��������⽵������
������1��������2�������2��������2
(1. �人������ѧҽԺ������ �人��430070��
2. �人������ѧ ��������빤���о����ģ����� �人��430070)
ժ Ҫ�����ۺ���-RGD���Ľ�֦��(����-�ǻ�����L-�����ᣬPRGD)���(D,L-���ᣬPDLLA)����-��������(��-TCP)������������(NGF)�����Ʊ�������PRGD/PDLLA/��-TCP/NGF���ϵ��ܲ�����37������Ỻ����Һ�н��н������飬�о�֧�ܲ��������⽵���������Է����������������������pHֵ������ò�ı仯��NGF���ͷŹ��ɡ��о����������NGF���ͷ�����30 d�ڿ��Դﵽ�յ�����֯�Ĺ��ܣ������-TCP�����Բ����к;������PRGD�����������ԣ���Ч���ڽ�����ʵ�pHֵ��ʹ��ά�������ԡ� ����PRGD��NGF�ɴٽ�����Ĥ�Ľ��⣬PRGD/PDLLA/��-TCP/NGF���ϲ��ϱȾ�������и��õĽ������ܡ�
�ؼ��ʣ�RGD���Ľ�֦����(D,L-����)����-�������ƣ����������ӣ����ܣ�����
��ͼ����ţ�R318.08 ���ױ�ʶ�룺A ���±�ţ�1672-7207(2009)02-0406-05
Preparation and degradation performance of PRGD/PDLLA/��-TCP/NGF composite nerve conduit
WANG Yong-hong1, DAI Hong-lian2, YAN Qiong-jiao2, LI Shi-pu2
(1. Hospital of Wuhan University of Technology, Wuhan 430070, China;
2. Biomedical Materials and Engineering Research Center, Wuhan University of Technology, Wuhan 430070, China)
Abstract: The PRGD/PDLLA/��-TCP/NGF composite nerve conduits were prepared by solvent evaporation method using poly {(lactic acid)�Cco-[(glycolic acid)-alt-(L-lysine)]}(PRGD), poly (D,L-lactide)(PDLLA), ��-tricalcium(��-TCP) and nerve growth factor(NGF). The degradation performance of composite nerve conduits were studied by observing the variation of pH value of degradation medium and relative molecular mass, mass loss ratio, NGF releasing quantity and microstructure of the composite. The results show that the releasing quantity of NGF can achieve the function inducing nerve tissue growth within 30 d; ��-TCP can neutralize the acidity produced by degradation of PDLLA and PRGD, availably adjusts pH value of degradation medium to keep at neuter. Adding PRGD and ��-TCP can promote the composite to degrade, hence, PRGD/PDLLA/��-TCP/NGF composite has better biodegradation than PDLLA.
Key words: RGD-polypeptide grafting; poly (D,L-lactide); ��-tricalcium; nerve growth factor; nerve conduit; degradation
��Χ���������ٴ��������²��Լ�������������һֱ����ѧ������������⡣Ŀǰ���������������ƿ����オ����˹��������ٽ���Χ��������������( PDLLA)�������õ����������ԺͿɽ��������ԣ��ѱ�����ʳƷ��ҩƷ������(FDA)�������������ܣ��������併�����ƫ���ԣ�������Ǹ�Ⱦ����֢����ϸ�����Բȱ��ϸ��ʶ���źţ�������ѩ��ϸ������ͻ��Ǩ�ƣ����Ѵﵽ��������ֲ����Ч��[1-5]�����������������ϸ����ʶ���ź�(��RGD����)���������������ԣ�ͨ������ʶ��ͼ����ת������ֱ�Ӵ̼����ﷴӦ��������ϸ����ճ������ֳ���ֻ���Ǩ��[6-7]����Χ�����������ָܻ���ṹ������Ҫ�����ָܻ���о����˶����ܡ�ʵ�ֹ�����������Ҫ���ʵ������������ʵ����������������ӣ���������ԪӪ���ʹٽ����յ���������ά�����������������������ǵ����������Ĺؼ�����֮һ[8-10]����һ���棬��-��������(��-TCP) Ҳ��һ�־����������������Ե�������Բ��ϣ����к�ǿ����ˮ�Ժ�һ���ļ��ԣ��п����ֲ�������IJ���[11]����ˣ����о��Ʊ���RGD���Ľ�֦��(�ǻ�����-L-������-����)(PRGD)��������PDLLA����-TCP������������(NGF)�������ڷ��Ӽ��ֲ��ϵ��ۺ����ƣ�Ϊ��Χ�����ṩ����ĵ��ܲ��ϣ���̽��PRGD/PDLLA/��-TCP/NGF���������ܵĽ������ܼ�NGF���ͷŹ��ɡ�
1 ʵ ��
1.1 PRGD/PDLLA/��-TCP/NGF���������ܵ��Ʊ�
��N��-�����ʻ�-L-���������������Ϊ��ʼԭ�ϣ��ϳɵ���3S-[4-(�����ʻ�����)����]-����-2,5-��ͪ�����õ�����������ۺ����ɾ�(����-�ǻ�����-N��-�����ʻ�-L-������)���پ�������������ʻ��Ƶþ�(����-�ǻ�����-L-������)�����ͨ��L-������IJఱ���������RGD���Ƶ�һ�����;ۺ��TRGD���Ľ�֦��(����-�ǻ�����-L-������)������������Ϊ�ܼ����ֱ����Ũ��Ϊ85%����Է�������Ϊ10��104~15��104�ľ����ᣬŨ��Ϊ10%��PRGD��Ũ��Ϊ5%��ƽ������С��500 nm�Ħ�-TCP�Լ������������ӣ�����������ɢ���������裬�����ܼ��ӷ����Ʊ�PRGD/PDLLA/��-TCP/NGF���ϳ�Ĥ(���Ϊ0.2 mm)������ո��������ء���Ĥ��ʵ��Ҫ�������Ƶ�ģ�߳ɹܣ������ھ�Ϊ2 mm������Ϊ14 mm�����Ϊ0.2 mm��������ͬ�ķ����Ʊ�PDLLA��PRGD/ PDLLA��PRGD/PDLLA/��-TCP���ܡ�
1.2 ���ϲ�����NGF���ͷ�����
��5��PRGD/PDLLA/��-TCP/NGF����Ĥ�����ֱܷ������3.0 mL���Ỻ����Һ�У���ڣ�����37 �����ҡ�������������ٶ�Ϊ60 r/min����Ԥ��ʱ���ռ���Һ��Ӧ��ø�������������ⶨ��[12]�Խ���Һ����NGF�����ⶨ��ʵ���õ��Լ��������人��ʿ�����﹤������˾�ṩ��С��NGF ELISA kit�������õı�ƷΪС��2.5S NGF������1500��ø����(Finland, Thermo Labsystems)�ⶨ450 nm���Ĺ��ܶ�(Optical density)[13]��
1.3 ����ʵ��
�����Ʊ���PDLLA��PRGD/PDLLA��PRGD/ PDLLA/��-TCP��PRGD/PDLLA/��-TCP/NGF��4��Ĥ���ϸ���Ϊ5�飬���������أ������ʼ����m1��Ͷ���ڲ���ƿ�У�����������Ỻ����Һ(pH=7.4��0.2)����37 ����½��⡣���ò��������ʵķ������н���ʵ�顣�Ӳ��Ϸ���PBS��Һ1 h��ʼ��ÿ�ܲⶨ2�ν���Һ��pHֵ���ⶨ14 d��Ȼ��ÿ7 d�ⶨ1�Σ��ⶨ70 d���۲콵��Һ��pHֵ�ı仯��
�ڵ�14��28��42��56��70��84 dʱ���ӽ���Һ��ȡ��������ϣ�������ˮ��ϴ������ֽ��ȥ����ˮ�֣�����ո���������ȷ£�����Water 2690D��������ɫ���Dzⶨ�ؾ���Է���������
�ֱ��ڲ�ͬ��ʱ���(14��28��42��56��70��84 d)���ӽ���Һ��ȡ�����ϣ�������ˮ��ϴ����ֽ��ȥ����ˮ�֣���ո��������أ�������m2��������ʧ��(Mass loss��ML) Ϊ��ML=(m1-m2)/m1���������84 d�ĵ��ܲ�����ո�������ձ������JSM-5610LV��ɨ���������(SEM)����20 kV�¹۲�����ò��
2 ���������
ʵ�ֹ���������ȡ����3������Ҫ�أ���Ԫ����Ĵ�����״̬����ͻ�������ʺͰ��������������ԡ����߾������������ӵĵ��أ���ˣ���ȱ��λ�ϳ�ʱ��ά��NGF���ͷŷdz���Ҫ��NGF�����ͷ�����ͼ1��ʾ���ɼ��� PRGD/PDLLA/��-TCP/ NGF����Ĥ�͵��ܵ�NGF�ͷŹ��ɻ���һ�£�NGF���Գ����ͷ�����30 d��NGF���ͷ�����ǰ3 d���� 1 d���ͷ����ﵽ370.6 ��g/L��NGF�������ͺ��ͷ�������С���ڵ�7~24 d֮��ÿ����ͷ����ȶ���1.5 ��g/L���ҡ������ڵ�30 d�ͷŵ�NGF���ܱ������������ϵͣ�ԼΪ0.15 ��g/L���о�������NGF������Ũ�ȴﵽ0.1 ��g/L���ɴ̼�PC-12����ͻ[14-15]����30 d��NGF���ͷ������Դﵽ�յ�����֯�� ���ܡ�
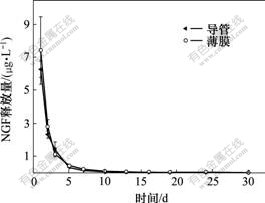
ͼ1 NGF�����ͷ���
Fig.1 Release mass of NGF in vitro
���ܲ����ڽ�������е�pHֵ�仯��ͼ2��ʾ���ɼ���ǰ14 d���в��ϵĽ���pHֵ�������½��������½�����������С��Է���������PRGD����Ѹ�ٽ��⣬ʹ����Һ��pHֵ�����½�����PDLLA�ڽ�������еĿ�������������Ҳ�ᵼ��pHֵ�½���PRGD/ PDLLA���������������pHֵһֱ�½�����PRGD/ PDLLA/��-TCP��PRGD/PDLLA/��-TCP/NGF�ڽ�������У�pHֵ����������pHֵ�½���PRGD/PDLLA��PDLLA���½��ٶ�����������ڦ�-TCP�ܽ��������ļ��Բ������к�PDLLA������������ԡ���4�ֲ����ڽ�����ڣ�pHֵ������ά��ϸ�����������Ի�����
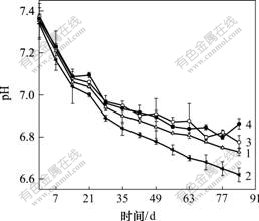
1��PDLLA; 2��PRGD/PDLLA;
3��PRGD/PDLLA/��-TCP; 4��PRGD/PDLLA/��-TCP/NGF
ͼ2 ���ܲ����ڽ�������н������pHֵ�ı仯
Fig.2 Relationship between pH value of medium and degradation time
���ܲ����ڽ���������ؾ���Է��������ı仯��ͼ3��ʾ���ɼ�����PDLLA ���ܺ��ϵ��ܵĽ��ⶼ����Ϊ�ȿ�������ڽ����ǰ14 d����������еľ�������ؾ���Է������������½��������� 70 d���ؾ���Է��������½��ٶ���С�������ڽ������ڣ����Ͻ��뵽PBS��Һ�к����ȷ������Dz�����ˮ��H2O������ɢ�������ڲ���PDLLA�������ȶ��ѣ�ʹPDLLA����ӿ죬����Է�����������Ƚ��ͣ��������������������̣����ܱ�ˮ��IJ�λ���٣�����Է������������ٶȼ�����PDLLA�Ļ�ѧ�ṹ���������仯��������H2O�����룬PDLLA���ɳڣ���Է��������ϴ�ľ��������Ѹ��ˮ�⣬���ҷ�������ÿ�����������ܱ�ˮ����ѣ��ͷų���COOH��pH ֵ��ʼ�½�������ˮ����λ�����࣬������Խ������ˮ��IJ�λҲ��Խ�࣬ˮ������Ҳ�����ͷų��ġ�COOHҲ���࣬�����Ž�����ϵ��H+ Ũ�ȵ��������������ǿ����2��ЧӦ��ͬ���½��ʾ����ή�����pHֵ��������Է�������Ҳ����Ƚ��ͣ����ԣ��ڿ�ʼ�ν���죬����ΪPDLLA�ı���ˮ�⡣���Ž���Ľ��У�����Է����������ͣ�����Ҫ��С��Է��������ķ��ӽ������£����ǣ������ٶȼ�С����һ���棬���ڦ�-TCP������PDLLA���ʼ��ϴ���ȱ��, ˮ���ӽ�������ɢ��������ڲ�, ʹ���ϲ�����PDLLA �����ٶȱȴ�PDLLA�Ľ����ٶȿ죬��ͬһʱ�ڣ�PDLLA��Է����������PRGD/PDLLA/��-TCP��PRGD/ PDLLA/��-TCP/NGF����Է���������֮��PRGD/ PDLLA����Է���������С����ͼ2��֪��������ʵ�pH ֵ�½��ٶȱ�PDLLA����Է��������½��ٶ�С��˵��PDLLA �������Ķ���(����)������ģ����ǽ���һ��ʼ�Ͳ���������ˮ����Է���������С���������ʣ���-TCP�Խ��ⷴӦ����û��Ӱ�죬�����ϲ����е�PDLLA�Ľ������ʾ��ȴ�PDLLA�Ĵ�
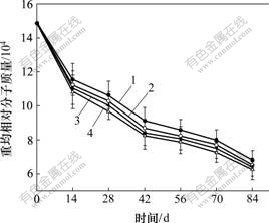
1��PDLLA; 2��PRGD/PDLLA/��-TCP;
3��PRGD/PDLLA/��-TCP/NGF; 4��PRGD/PDLLA
ͼ3 ���ܲ����ڽ���������ؾ���Է��������ı仯
Fig.3 Variation of relative molecule mass of materials with degradation time
���ۺ��オ�һ���̶�ʱ���併��������ڽ�������У�ʹ�ۺ�����ϵ���������١����ܲ����ڽ�������е�������ʧ�ʼ�ͼ4��ͼ4��������4�ֲ�����ǰ56 d������ʧ�ϴ�56 d��������ʧ����ƽ�������Ի������ӡ�����ͬ��ʱ��㣬PDLLA��������ʧ��С��PRGD/PDLLA/��-TCP��PRGD/PDLLA/��-TCP/ NGF��������ʧ��֮��PRGD/PDLLA��������ʧ�����������С��Է���������PRGDѸ�ٽ���¸��ϲ��ϵ��������٣���ʹ������ʵ�pHֵ�½����ٽ��˸��ϲ��ϵ����彵�⣬����-TCP�����Ի����еĽ����ٶȽ�С��������pHֵ�½��ٽ���-TCP�Ľ��⣬��Ҳ�ᵼ�¸��ϲ���������ʧ�ʱȴ�PDLLA�ĸߡ�
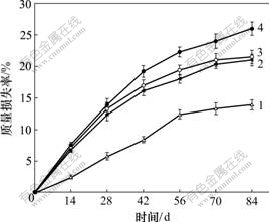
1��PDLLA; 2��PRDG/PDLLA/��-TCP;
3��PRGD/PDLLA/��-TCP/NGF; 4��PRGD/PDLLA
ͼ4 ���ܲ����ڽ�������е�������ʧ��
Fig.4 Mass loss of materials with degradation time
ͼ5��ʾ���ܾ���84 d�������в�ͬ�̶ȵĽ��⡣��PDLLA �ܺ�PRGD/PDLLA/��-TCP/NGF���ϵ���84 d����Ƚ��⣬���ϳ��ִ����ס���PDLLA����������Ա�PRGD/PDLLA/��-TCP/NGF���ϲ��ϵ�С���ҷֲ������ȡ��ɴ˿ɼ���PRGD/PDLLA/ ��-TCP/NGF���ϲ��ϵĽ����ٶ����Աȴ�PDLLA�Ľ����ٶȿ졣��������PRGD�ͦ�-TCP�Ľ��⣬NGF���ͷ��Լ���-TCP��PDLLA ���ʼ�Ľ��ȱ�ݵ��¸ý���PDLLA���ٽ��⡣
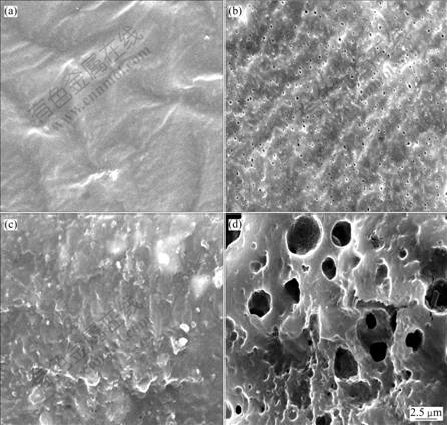
(a) PDLLA(����ǰ)��(b) PDLLA(����84 d)��(c) ���ϵ���(����ǰ)��(d) ���ϵ���(����84 d)
ͼ5 PDLLA���ܺ�PRGD/PDLLA/��-TCP/NGF���ϵ��ܽ���ǰ���SEM������ò
Fig.5 Scanning electron microscope (SEM) images of surface morphology of PDLLA conduit and PRGD/PDLLA/��-TCP/NGF composite conduit before and after degradation
���⣬PDLLA�Ľ����������������̬����ѧ��
�ɡ��ṹ����Է������������ϳߴ硢����������ʵȡ�Grizzi��[16]���ֱ�Ĥ����ĩ�����������������併���ٶ�ҪС�ܶࡣ���ڲ���Խ���������������Ŀ�����Խ�ͣ������Դ����ٽ���ЧӦС��������˵����PDLLA ���ܺ��ϵ������⽵��84 d����ҺpHֵ��Ȼ���ͣ����Գ������ԣ����뵼�ܲ��ϵĹܱڱ�(0.2 mm)���ڽ�������У����Դ����ò������ԣ������ٶ����С�йء�
PRGD/PDLLA/��-TCP/NGF���ϲ��ϵĽ�����PGRD��PDLLA����-TCP��NGF���ۺ����ã������С��Է���������PRGDѸ�ٽ��⣬���½�����ʵ�pHֵ�½���Ҳ�ٽ���PDLLA���⣻Ȼ��PDLLA�ı��彵�⣬����pHֵ�����½�������Է�����������Ƚ��ͣ����Ⲣ����ʹPDLLA��������PBS�У����ϵ�������ʧ�����ͺ�ЧӦ����ˣ�PRGD/PDLLA/ ��-TCP/NGF���ϲ����ڽ����������Ȼ���������ͣ������νṹ�ڽ������(0~84 d)���Ա����������ڸø��ϲ����У����ڱ���ֲ�����ˮ�Ե�NGF���ɴٽ�H2O��������ϱ�����ɢ����ˣ�NGF������ٽ��˲��ϵĽ��⡣��-TCP�����Խ����е��ܽ�Ⱥܵͣ���PRGD��PDLLA�Ľ���ʹ��ϵ�������Ӷ��ٽ��˦�-TCP�Ľ��⣬���併��������һ�����к����ã���Ч������PRGD��PDLLA�����������ԣ�����˸��ϵ��ܵ����������ԡ�
��������ɽ������ܣ����ϵĽ����ٶ���һ���dz���Ҫ��ָ�ꡣ���Ϊ10 mm����������Ҫ2~3���£���ˣ�Ҫ����������Ӧά��3���µ�֧�����ú�����������ա����о�������PRGD/ PDLLA/��-TCP/NGF���ϵ��ܾ�84 d�Ľ������Ȼ��Է�������������½���������ʧ�ʴﵽ21.4%�����ϱ���Ҳ�����˴����ף�������������Ȼ�������������е��ԡ��ɴ˿ɼ���PRGD/PDLLA/��-TCP/NGF�������ܲ������нϺõ����オ�����ܣ�ͬʱ���ﵽ�����ڼ��֧�ֹ��ܡ�
3 �� ��
a. ͨ��L-������IJఱ���������RGD�ϳ������;ۺ���PRGD��������PDLLA����-TCP��NGF���ϣ������ܼ��ӷ����Ʊ������͵�PRGD/PDLLA/ ��-TCP/NGF�������ܡ�
b. PRGD/PDLLA/��-TCP/NGF����������NGF���ͷ���������30 d�ڱ���Դﵽ�յ�����֯�Ĺ��ܡ�
c. ��-TCP���Բ����к;����ᡢPRGD���������������Բ����Ч���ڽ�����ʵ�pHֵ��ʹ��ά�������ԡ� ����PRGD��NGF�ɴٽ�����Ĥ�Ľ��⣬PRGD/PDLLA/��-TCP/NGF���ϲ��ϱ�PDLLA���и��õ����オ�����ܡ�
�ο����ף�
[1] Evans G R, Brandt K, Widmer M S, et al. In vivo evaluation of poly l-lactic acid porous conduits for peripheral nerve regeneration[J]. Biomaterials, 1999, 20(12): 1109-1115.
[2] Hudson T W, Evans G R, Schmidt C E. Engineering strategies for peripheral nerve repair[J]. Clin Plast Surg, 1999, 26(4): 617-628.
[3] Belkas J S, Shoichet M S, Midha R. Axonal guidance channels in peripheral nerve regeneration[J]. Oper Tech Orthop, 2004, 14(3): 190-198.
[4] MeekM F, Robinson P H, Stokroos I, et al. Electronmicroscopical evaluation of short-term nerve regeneration through a thin-walled biodegradable poly (DLLA-��-CL) nerve guide filled with modified denatured muscle tissue[J]. Biomaterials, 2001, 22(10): 1177-1185.
[5] Evans G R, Brandt K, Katz S, et al. Bioactive poly(L-lactic acid) conduits seeded with Schwann cells for peripheral nerve regeneration[J]. Biomaterials, 2002, 23(3): 841-848.
[6] Tessmar J, Mikos A, Gopferich A. The use of poly(ethylene glycol)-block-poly(lactic acid) derived copolymers for the rapid creation of biomimetic surfaces[J]. Biomaterials, 2003, 24(24): 4475-4486.
[7] Quirk R A, Chan W C, Davies M C, et al. Poly(L-lysine)-GRGDS as a biomimetic surface modifier for poly(lactic acid)[J]. Biomaterials, 2001, 22(8): 865-872.
[8] Verreck G, Chun I, Li Y, et al. Preparation and physicochemical characterization of biodegradable nerve guides containing the nerve growth agent sabeluzole[J]. Biomaterials, 2005, 26(11): 1307-1315.
[9] Johnson E O, Zoubos A B, Soucacos P N. Regeneration and repair of peripheral nerves[J]. Injury, 2005, 36(4): S24-S29.
[10] Brunello N, Reynolds M, Wrathall J R, et al. Increased nerve growth factor receptor mRNA in contused rat spinal cord[J]. Neurosci Lett, 1990, 118(2): 238-240.
[11] Dai H, Li S, Yan Y, et al. The osteogenesis process of tricalcium phosphate ceramics in vivo[J]. Transactions of Nonferrous Metals Society of China, 2003, 13(1): 65-68.
[12] Xia Y X, Ikeda T, Xia X Y,et al. Differential neurotrophin levels in cerebrospinal fluid and their changes during development in newborn rat[J]. Neuroscience Letters, 2000, 25(3): 220-222.
[13] Thoene H, Edgar D. Neurotophic factors[J]. Science, 1985, 229(4710): 238-242.
[14] Darling T L, Shooter E M. Methods for preparation and assay of nerve growth factor[C]//Barnes D W, Sinbasku D A. Cell Culture Methods for Molecular and Cellular Biology. New York: Alan R Liss Inc, 1984: 79-93.
[15] Varon S, Nomura J, Shooter E M. The isolation of the mouse nerve growth factor protein in a high molecular weight form[J]. Biochemistry, 1967, 6(7): 2202-2209.
[16] Grizzi I, Garreau H, Li S, et al. Hydrolytic degradation of devices based on Poly(D,L-lactic acid) size dependence[J]. Biomaterials, 1995, 16(4): 305-311.
�ո����ڣ�2008-11-16�������ڣ�2009-01-20
������Ŀ�����ҡ�973���ص�����о���չ�ƻ�������Ŀ(G2005CB623905)
ͨ�����ߣ�������(1946-)���У����������ˣ����ڣ���ʿ����ʦ����������ҽ�ò��ϵ��о��뿪�����绰��027-87216470��E-mail: lishipu46@126.com