���±�ţ�1004-0609(2012)06-1812-09
�������������Һ������ϳɼ��������Ӧ��
����������־ΰ�����Ƚ����� �ݣ����ƻᣬ������
(ɽ��������ѧ ��ѧ����ѧԺ���Ͳ� 255049)
ժ Ҫ�������������ϳɷ����Ʊ��������������Һ�壬������������ѧ���ܣ���������Ϊ�����Ӧ�������ĵ������ͨ���ⶨѭ���������ߡ���ʱ���������Լ���������̽������2AlCl3/[EMIM]Br����Һ���еĵ������������������ͭ�����Ͻ������ĺ��λ��������������ò�Լ��ṹ���Էֱ���SEM��XRD���б���������������������������Һ����������ϳ�����ͨ���ϳ���ȣ���������˷�Ӧʱ�䣬����˲�Ʒ���ܣ����ĵ����Ϊ����Ķ���ѧ��Ϊ���������̷ǵ�������ɢ���ƶ��Ǹ��ӵĶ���ѧ���Ʋ��裻���ڲ�ͬ��λ�µij�������·�Ϊ3�ֵ�����ò�����Ը�����ò������ԭ���������з�����
�ؼ��ʣ����ϳɣ���������������Ũ���
��ͼ����ţ�O646 ���� ���ױ�־�룺A
Microwave synthesis of bromo-chloroaluminate ionic liquid and its application in aluminium electrodeposition
ZHANG Li-peng, GE Zhi-wei, YU Xian-jin, WANG Jie, DONG Yun-hui, ZHAO Zeng-dian
(School of Chemical Engineering, Shandong University of Technology, Zibo 255049, China)
Abstract: A new microwave synthesis method was proposed to prepare bromo-chloroaluminate ionic liquid. The physical and chemical characteristics of this ionic liquid were tested and the ionic liquid was used as the electrolyte in aluminium electrodeposition. Electrochemical techniques of cyclicvoltammetry, chronoamperometry and polarization curve (tafel) were used to investigate the mechanism of aluminium electrodeposition from 2AlCl3/[EMIM]Br ionic liquid. Constant potential electrodepositon of aluminium was conducted on the copper substrates at room temperature and the qualitative analysis of the deposits was performed using SEM and XRD, respectively. The results indicate that the reaction time of the new microwave synthesis of bromo-chloroaluminate is drastically reduced, comparing with that of the conventional methods, and the properties of chloroaluminate ionic liquid are improved. Aluminium electrodeposition from this ionic liquid is not a simple linear diffusion controlled process, but a quasi-reversible process with complex kinetic limitations. The aluminium deposits obtained at different potentials are mainly about three typical morphologies and the reason for the three typical morphologies and their characteristics are analyzed.
Key words: microwave synthesis; electrodeposition; activation polarization; concentration polarization
���ǵؿ��д��������Ľ���Ԫ��֮һ�������������ȡ����硢���ᡢװ�����ܺõ��ŵ㱻�㷺Ӧ���ڽ������ϵı�����������Ʋ���Ʊ������ܶ࣬��Ҫ���Ƚ�[1-2]������Ϳ[3]�����������[4]�������[5-8]�����е�����Ʊ��õ��������ܵ����Ʋ㣬����Ϊ��һ����Ϊ��Ч�ķ�����Ȼ������һ�ּ�Ϊ���õĽ� �����������λ����ĵ�λ������ʹ����ˮ��Һ�е�������Խ��С�Ŀǰ��������Ʊ����Ʋ���Ҫ���л��ܼ�[9]����������ϵ�н���[10-11]����Ȼ�л��ܼ�������ϵӦ�����磬����Ҳ��Գ��죬����Һ���Ƹ��ӣ����Һ��ȼ����Һ���ܲ��ȶ����Ʋ������ݵ�ȱ������Լ����㷺Ӧ�á��������ε绯ѧ���ۺͼ����ķ�չ, ���ε�����Ʊ����Ʋ�Ҳ�õ��������о���Ȼ�����εĸ�ʴ�Խ�ǿ���Ե���豸��Ҫ��Ҳ�ߣ���֮���ڻ�����Ⱦ����Դ�����ʵ͵�ȱ�㣬�䳤�ڴ��ģӦ���ܵ�������[12]��
��1914��WALDEN[13]���ֵ�һ������Һ��[EtNH3][NO3]��������������Һ��Ķ���һֱ������������������Һ�屻��Ϊ�ǵ�һ������Һ�塣Ŀǰ������Һ��Ŀ�����Կ���ʵ�����ض����ܣ��ѹ㷺Ӧ�õ������л��ϳɡ����롢����ѭ�������Լ����ײ��ϵ��������[14-17]����������Һ���Ѿ���������ķ�չ���̣�����û��һ������Һ���ܳ�Խ����������Һ������������������Խ��[18-20]������������Һ�嵼���ʸߡ��ܽ���ǿ������Ч�ֲ��л��ܼ������ε������ȱ�㡣HURLEY��[21-22]�״��о����廯�һ�����������ε����ԣ�������ɹ�Ӧ�õ����ĵ�������У��������ĵ��������δ����ϸ�о�����1951�� �𣬶�����������Һ�������ĵ�������о�һֱ��������[6, 23-26]��
����������������Һ���г������˸����������Ʋ㣬��������������Һ��ij����Ʊ�������Ҫ�����ķ�Ӧʱ�䣬������Ҫ�������ܼ����ܵõ��ϸߵIJ��ʡ��������ϳɽ�֮��ͳ�ĺϳɷ����ܴ�����̷�Ӧʱ�䣬�ѹ㷺Ӧ��������Һ��ĺϳɵ���[27]��������ͨ�����ڲ��ܾ�ȷ���Ʒ�Ӧ�¶ȣ������·�Ӧ����Ĺ�������[28]������������Ӧ�з�Ӧ��Ĺ��������ڼ��ٷ�Ӧ���ʵ�ͬʱҲ����ʹ�������¶ȹ��߶��ѽ�[29]��LAW��[30]����ˮ��Ϊ���������ͼͨ����װ��װ������������⣬Ȼ������������Һ��ķ�Ӧ����к�ǿ����ˮ�ԣ��ڳ��ڷ�Ӧ���н��и÷�Ӧ���ѵõ����ʲ�Ʒ[31]��
���������ڿɿ��µ��ܱշ�Ӧ���н����������������Һ������ϳɣ��о�������Һ����������Բ���һ��̽������������������Ӧ�á�
1 ʵ��
1.1 ����Һ��ĺϳɼ��ﻯ���ܲ���
����Ħ���ļ����������������ܱյķ�Ӧ���У��������Ӻ�����������ϳ���(Milestone microwave lab station, Italy)�ϳ��м���[EMIM]Br���м����ø���Ҷ�任���������(Nicolet 5700)���б���������ˮ��ɫ����״���Ȼ����������뵽�м����У���ʱ�ļ����ٶȲ��˹����Է�ֹ��������¶ȹ��߶��ѽ⡣Ϊ�˸��õ��о��乤ҵӦ��ǰ�����м��弰�ϳɵ��������������Һ������贿����Ϊ�˼����м���ĺϳɲ��ʣ������²�������м�����ᴿ�����Ƚ��м����������棬Ȼ������������������侲���ؽᾧ���㵹���ܼ�����˷�������2~3�κ���80 ������ո���24 h�����Ϻϳɼ��ᴿ�������ڱ��������н���(Mikrouna)�����Ʊ����������������Һ����۵��Լ�������ת���¶��ɲ�ʽɨ��������(������DSC Q100����������)��ã��ܶȲ��ñ���ƿ���������¶�ѡ����ԡ����(DF101S, Gongyi)����������������ʾ�ȼƲⶨ(NDJ-8S���Ϻ�����)���絼���ɵ絼���Dzⶨ(DDS-307, �Ϻ�����)��
1.2 �绯ѧ����
ѭ����������ʱ�����Լ��������ߵIJ�����ʹ��IM6e(ZAHNER, Elektrik���¹�����) �绯ѧ����վ������Ƭ(1.0 cm��1.0 cm)��ͭƬ(0.25 cm��0.25 cm)�ʹ������ֱ���Ϊ�Ե缫�������缫�Ͳαȵ缫���缫��ǰ�ڴ�����Ϊ��Ҫ�����ȵ缫���ò�ͬĿ����ɰֽ�Ӵ�С���⣬Ȼ������������ĥ����������ϴ4 min��Ȼ������������ֱ�Ϊ25%����(98%)��70%����(85%)��5%����(52.5%)�Ļ����Һ�н���10 min����[26]����ϴ�缫�ķǹ�����Ϳ�ϻ�����֬�����������ˮ��ϴ��������ո�����(DZG-6050���Ϻ�ɭ������)������á����Һѡ��2AlCl3/[EMIM]Br����������ౣ����1 cm ���ң������Ͳαȵ缫֮��ľ���С��1 mm��
1.3 ���ĵ����
���ĺ��λ����ʵ����CHI�绯ѧ����վ(�Ϻ����й�)�Ͻ��С�ʵ��������缫��ϵ����Ƭ (1.0 cm��1.0 cm)Ϊ������ͭƬ (1.0 cm��0.5 cm) Ϊ������������Ϊ�αȵ缫���缫��ǰ�ڴ�����1.2������һ������λ��Χѡ����-0.25~ -1.27 V������������֮��ľ���Ϊ1 cm��2AlCl3/[EMIM]Br��Ϊ����ʣ�����ʱ��Ϊ22 min�������ʵ�����֮��������ˮ�Ҵ���ϴ������Ȼ����������ˮ��ϴ������������ֱ���ɨ���������(SEM��FEI-Sirion 200)��X����������(XRD, D8 advance, bruker/axs)���б�����
2 ���������
2.1 �������������Һ�������
��������f�ε��Ʊ������ǵ��͵ļ�炙���Ӧ��Ҳ��һ������Ҫ��SN2��ȡ����Ӧ�������ܼ��Ը÷�Ӧ��Ӱ��ܴ���ǿ���ϳɹ����У�Ϊ�˱��������ܼ������Գ�ȥ��������Һ��Ĵ�������Ӱ�죬ͨ��ֻʹ��������±����(һ��Ħ������10%~20%)���з�Ӧ[28, 32]���ɿ��µ����ϳ�ʵ������У�������������Բ������û��������Ӱ�죬������ 1���С�
���ϳ�[EMIM]Br���¶�ʱ������ͼ��ͼ1��ʾ����ͼ1���Կ������ڷ�Ӧ30 s��Ӧ���¶���ƫ������趨���ߣ�����Ҫ�Ƿ�Ӧ����ȵ��µġ�BAGHURST��MINGOS[33]�����ڳ�ѹ����Ӧ�����У���Ӧ����¶�ͨ���ᳬ����е�13~26 �棬���״��о��˹�������Է�Ӧ��Ӱ�졣�ڱ�ʵ���У������¶����߲���δ���뷴Ӧ��������Ѹ�����������࣬���ܼ��ڲ����������չ�����������ݵ����˷�Ӧ����ȡ��������¶ȿ���ϵͳ�ܼ�ʱ���¶�ƫ�룬ͨ������ͼ�С����ʹ�÷�Ӧ���������ڽ�������90 s������趨���߷dz��Ǻ�, �ܺõؽ��������Һ��ϳ��еķ�Ӧ����ȵ����⡣
����������Һ�����������ȡ�����Ȼ����ĺ� ��[21, 34-35]��AlCl3/[EMIM]Br����Һ���з�Ӧ����Ҫ����[EMIM]Br:A1Cl3 ��ʽ���ϣ��������ʽ�������淴Ӧʽ��ʾ��
m[EMIM]+Br-+nAlCl3 n[EMIM]+AlCl3Br-+
n[EMIM]+AlCl3Br-+
(m-n)[EMIM]+Br- (n/m��1) (1)
m[EMIM]+Br-+nAlCl3 (2m-n)[EMIM]+AlCl3Br-+
(2m-n)[EMIM]+AlCl3Br-+
(n-m)[EMIM]+Al2Cl6Br- (1��n/m��2) (2)
����Al2Cl6Br-Ϊ·��˹�ᣬ�����ĵ����ֻ������������������Һ���н���[18, 34-36]������2AlCl3/ [EMIM]Br����Һ�������ĵ������Ӧ����ʽΪ
4Al2Cl6Br-+3e��Al+3AlCl4-+4AlCl3Br- (3)

ͼ1 [EMIM]Br����Ӧ�����е��¶ȡ�ʱ������
Fig. 1 Temperature��time curve for synthesis of [EMIM]Br ionic liquids
2AlCl3/[EMIM]Br���ﻯ�������Ȼ�����Ħ�������Ĺ�ϵ��ͼ2��ʾ����ͼ2(a)���Կ������������۵���Ȼ�����Ħ�������������Ըı䣬��������õĻ������۵�ͨ��������һ�����ʺ����ĸı�����Ըı䡣���Ȼ���Ħ������������33%��ʱ���¶���Լ9 ���ʱ����ֵ�һ����͵���ͼ�е�1��ʾ�������Ȼ����ļ������ӣ��������۵㿪ʼ���������Ȼ���Ħ������Ϊ50%ʱ�۵�����52 �棻���������Ȼ����ĺ��������Ȼ���Ħ������ԼΪ66.7% �¶��ٴγ�����Сֵ(ԼΪ-96 ��)����ͼ�е�2��ʾ��������Сֵ�ij��ֱ�����ʱ���¶Ⱥ��п������ڸ�Ħ������������Һ��IJ������¶�[37]�����Ȼ�������������ϵȴû���������ԣ���ҲΪ����������Һ���������µĹ㷺Ӧ���ṩ�˿��ܡ�ͼ2������b��c��d�ֱ��Ӧ���������������Һ����ȡ��絼�ʺ��ܶ����Ȼ���Ħ�������ı仯���ߣ����Կ�����Щ���Բ�����Һ���������źܴ��ϵ��ͼ2������a��b��d���Ȼ���Ħ������Ϊ66.7%ʱ�����ֳ����������ԣ�Ψ������c���ֳ�����Һ�����Ȼ���Ħ������Ϊ66.7%ʱ�ĵ����Ե����Ȼ���Ħ������Ϊ50%ʱ�ĵ����ԣ�������Ǽ����Ըߵ�[EMIM]+��AlCl3Br-��[EMIM]+��Al2Cl6Br-ȡ�������µĽ������������������Һ�������ɱ������������Ȼ���Ħ������Ϊ54%~70%����������۵�������Ȼ���Ħ������Ϊ66.7%������ˣ��ۺ��������������Һ����ﻯ���ʣ�ѡ���Ȼ���Ħ������Ϊ66.7%������Һ����Ϊ�о�����
��1 �ڲ�ͬ��������������Һ������ϳ�
Table 1 Microwave synthesis of ionic liquids under different conditions
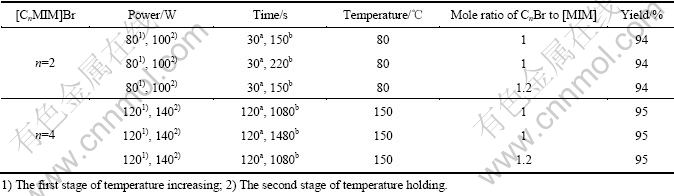

ͼ2 AlCl3/[EMIM]Br ����Һ�����������
Fig.2 Properties of AlCl3/[EMIM]Br ionic liquid
2.2 ���������
2.2.1 ѭ���������߷���
2AlCl3/[EMIM]Br����Һ����ɨ���λ��Χ(-1.5~2.0 V)�����ѭ������������ͼ3(a)��ʾ����ԭ��b��Ӧ�ŷ�Ӧ����ʽ(3)�����ij�������ԭ��b���a����ֱ��Ӧ��AlR4- (RΪCl����Br)����Ļ�ԭ�����������ŵ�λ����ɨ����ԭ��a�ij������Ӧ������������ܽ⡣��ɨ���λ��Χ������-1.0~1.5 Vʱ(��ͼ3(b)��ʾ)������Ա���AlR4-�����������ԭ��Ӧ��ͬʱ���ij����������һ���������ij��ֱ��������ij��������У���Ҫһ���ܴ�Ĺ���λ����ʵ����ᾧ�ɺ˼�����ͼ3(b)�����Կ���������ɨ�����ʵIJ������ӣ�ѭ���������߱��ֳ�����ķ��λ������岻�����ƺ������岻�ϸ��Ʊ�����2AlCl3/[EMIM]Br �����ĵ��������ѧΪ������Ϊ����ͼ3�ɼ��������ܶ�����������a֮��������˽Ͽ��Ķۻ�ƽ̨���������������������������Һ���еĶۻ����¡�

ͼ3 ������2AlCl3/[EMIM]Br��ͭ�缫�ϵ�ѭ����������
Fig. 3 Voltammogram recorded on Cu substrate in 2AlCl3/ [EMIM]Br ionic liquid at room temperature: (a) Scanning rate of 50 mV/s, potential range of -1.5~2.0 V; (b) Voltammogram obtained at different sweeping rates with scanning potential range of -1.0~1.5 V
��ͼ4��ʾ�����������ܶ�(jp)��ɨ���ٶ�ƽ�������������Թ�ϵ����������ɨ�����ʵIJ������ӣ������ȴ��ƫ��ֱ�ߣ����Կ������������̷ǵ�������ɢ���ƶ��ǰ����ŵ�ɴ��ݻ��������ݿ��Ƶĸ��Ӷ���ѧ���Ʋ��裬����LAI��[38]���о�����һ�¡�
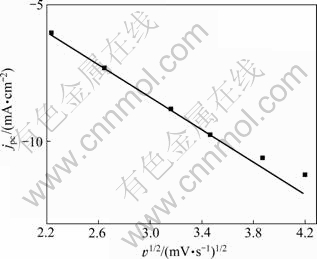
ͼ4 ������2AlCl3/[EMIM]Br�����������ܶȺ�ɨ���ٶ�ƽ�����Ĺ�ϵ
Fig. 4 Relationship between cathodic peak current density (jpc) and square root of scanning rate (��) in 2AlCl3/[EMIM]Br ionic liquid at room temperature
2.2.2 ��̬���߷���
Ŀǰ�����ܶ�����������Һ�������ĵ���������о��϶�[23, 25-26]�����Ƕ��䷴Ӧ����ѧ���Ʋ����Բ�����������������еļ�ʱ����������ͼ5��ʾ����ͼ5�ɼ�����ʱ�������ߴ��·�Ϊ3����������1�е�����Ѹ��������Ҫ�����������Ļ�������������̶ȸ�����λ�кܴ��ϵ��ͨ������λԽ�����Ӧ�Ļ�����̶�Խ������2ʵ���˵��������ӵ���С�Ĺ��ɣ���������С�Ҷ��ݣ����Ź���λ���������ƻ�����ԣ�������ǻ������Ũ�����ͬ�����µĽ��������3�е�������ʱ������Ӷ����Ͳ������ں㶨�����ŷ�Ӧ�ļ������У�Ũ�����Ϊ��Ҫ�Ŀ��Ʋ��衣��������3��Ũ����ķ����кܶ��ֽ��ͣ�KAMAVARAM��[39]��Ϊ���������ۻ��йأ��������������γ���һ�㲻�����谭�������ܽ⣬���Һ�з�Ӧ��������εò�����ʱ���������Բ�����Ũ�����
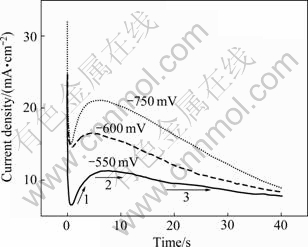
ͼ5 ������2AlCl3/[EMIM]Br�в�ͬ��λ�����������ʱ����̬����ͼ
Fig. 5 Current density��time transients curves obtained in 2AlCl3/[EMIM]Br ionic liquid with different potentials at room temperature
2.2.3 �������߷���
��������(Tafel)��ͼ6��ʾ������ʽ(4)
 (4)
(4)
ʽ�У� Ϊ��������λ��V��jΪ���������ܶȣ�mA/cm2��RΪĦ�����峣����8.314 J/(mol��K)��TΪ����ѧ�¶ȣ�K��j0Ϊ���������ܶȣ�mA/cm2��acΪ������ɴ���ϵ����nΪת�Ƶ�������FΪ�����ڳ�����96 485 C/mol��
Ϊ��������λ��V��jΪ���������ܶȣ�mA/cm2��RΪĦ�����峣����8.314 J/(mol��K)��TΪ����ѧ�¶ȣ�K��j0Ϊ���������ܶȣ�mA/cm2��acΪ������ɴ���ϵ����nΪת�Ƶ�������FΪ�����ڳ�����96 485 C/mol��
������֧ǿ���(ab��)����������ϣ��ɸ���б�ʿɼ���������ĵ�ɴ���ϵ��ԼΪ0.2�����������ܶ� (j0)����ͨ������֧������֧ǿ�����ֱ�߲������������㣬�ɽ����������ͨ��ʽ(4)����õ����ܶ�ԼΪ10.2 mA/cm2����Ҳ��һ����֤����������������Һ���г���Ϊ������Ϊ������֧��������cd��ͬѭ���������߷�����(��ͼ3)���ֵĶۻ�ƽ̨һ���������������������ۻ����������缫������������Һ���еĶۻ���������û�к�ȷ�Ľ��ͣ�HOLLECK��GINER[40]��Ϊ��AlCl3������ϵ�����缫�Ķۻ�ԭ�����£��������������ܶȵIJ������ӣ����缫�ϸ����˲��ܵĹ�̬�β㣬�����谭�����������ܽ⡣���ֽ���Ҳ���������缫������������Һ���жۻ����������ʱ����������(��ͼ5)����3��Ũ�������ܺ��Ǻϡ�

ͼ6 ������2AlCl3/[EMIM]Br�ļ�������ͼ
Fig. 6 Polarization curve of 2AlCl3/[EMIM]Br ionic liquid at room temperature
2.3 ������������
ͼ7��ʾΪ��ͬ��������µõ������������SEM��ͼ7���Կ���������������Ҫ��3�ֵ��͵���ò���ڽϵ͵Ĺ���λ������(-0.25~-0.45 V)�����Ʋ���Ҫ�ǿ���״�ᾧ���Ʋ�������ܣ��������ܺá��ڸ�����Χ�ڣ����������Ҫ�ܵ��������Ӱ�죬��ʱ�缫����ķ�Ӧ��dz����㣬�ܹ���ֵ��ڷ�Ӧ������е��ӽ�����Al�����ڷ�Ӧ����õ����Ӻ�����ɾ������ĵ���ԭ�ӣ�Ȼ��ԭ�ӽ������ž������Ŀ�λ��̨��������͵ĵط�����Ǩ�ƣ����վ����ɾ����һ���֡����������ڸ�����Ƚϸ��㣬Alԭ���ڽ����ϵ�Ǩ���ٶȾ��ȣ����Գ����ı�����̬�Ϻã���ͼ7�в�ͼa��b��c��ʾ���������¸����ڵõ���ͼ8(a)��ʾ�Ĺ������������㡣
�������������λ(-0.56~-0.88 V)��������������Գ��ֳ�����������β�״�ṹ���ڸ������ڣ����ij��������ܵ������Ӱ��ͬʱ���ܵ�Ũ�����Ӱ�졣���ڹ���λ���Ӽӿ��˻�ѧ��Ӧ�ٶȣ���λʱ������ɢ���缫��������ʵ�����ʼ�������㻯ѧ��Ӧ���ĵ�������ϵ�п�ʼ������Ũ������ڻ������Ũ�����ͬ�����£�Alԭ��Ǩ����ɢ���ٶȱ�ò����ȣ�����ԭ���Կ���˳�ž�������̨�ײ�״��������ͼ7�в�ͼd��e��f ��ʾ�����������õ�ͼ8(b)��ʾ���������㣬�ó�����Ĺ����̶����� �½���
������λ����-1.05 Vʱ���������㿪ʼ�������Եķ��ͽṹ���Ʋ�Ҳ��ø������ȡ� �����ͽṹ����������������ɢ�͵�ɺ�֮�⣬Ũ��������ǵ���������������Ҫԭ������λ������ȫŨ�����ʱ�������������Ķۻ������˵��Һ�������ڵ缫��Ӧ�����Ũ�ȼ��٣������������������Ӱ���С����ʱ��������������̬�ͻ���ֳ������Եķ��νṹ����ͼ 7�в�ͼg��h��i��ʾ��Ũ����̶ȵ����ӼӾ��������������IJ������ԣ������ֳ�ͼ8(c)��ʾ�İ���ɫ�ֲڱ��档

ͼ7 ��ͬ��������µ�����������ò�Լ����Ӧ�ĸ������ɵĵ����ܶȡ���λ����ͼ
Fig. 7 Curves for aluminum electrodeposition at different potentials at room temperature with corresponding morphology of aluminum deposits marked on curve

ͼ8 ��ͬ�������������������������Ƭ
Fig. 8 Digital photos of Al deposits with different potentials: (a) -0.25~-0.45 V; (b) -0.56~-0.88 V; (c) Bellow -1.05 V
ͼ9��ʾΪ����3�ֵ�����ò�ij������XRD�ס���ͼ9���Կ�������������Ҫ����(111)��(200)����������������(111)�淽��ȡ����ǿ��3����ò֮��IJ�ͬ��Ҫ������������ǿ�ȺͿ����ϣ�����״���������ڴ��ڻ�������������������������������������Ӷ�����Ϊ(111)����ķ������ǿ����ߡ�����Ũ����ļӾ磬�����㿪ʼ�����˷��νṹ�����IJ�����Ȼ�ܻ�����������������������������������ṹ�IJ������Ժͱ���ȱ�ݵ����������ǿ�Ƚ��ͺ������Ŀ�����

ͼ9 ����3�ֵ�����ò�����������XRD���Լ������ı���Ƭ
Fig. 9 XRD patterns of Al deposits that having three typical morphologies and standard data (ICDD) of pure Al
3 ����
1) �������������ϳ��������������Һ�壬��Ӧʱ��̣��ﻯ����������
2) ����(2AlCl3/[EMIM]Br) ����Һ���еĵ��������ѧΪ���棬ͬʱ��������Ϊ�ǵ�������ɢ���ƣ����Ǹ��Ӷ���ѧ���Ʋ��衣
3) �����������¿ɷ�Ϊ3�ֵ�����ò���ֱ�Ϊ����״�������μ����ͽṹ�������β�״�ṹ�ͷ��ͽṹ�ij�������Ҫ�ǵ缫�IJ�ͬ������ʽ��ɵģ�Ũ��������������ͽṹ��ò�����������ڱ���ṹ�IJ��죬��ͬ��ò�ij�����XRD�����ǿ�ȺͿ��Ȳ�ͬ��
REFERENCES
[1] WANG D, SHI Z. Aluminizing and oxidation treatment of 1Cr18Ni9 stainless steel[J]. Applied Surface Science, 2004, 227(1/4): 255-260.
[2] WANG D, SHI Z, ZOU L. A liquid aluminum corrosion resistance surface on steel substrate[J]. Applied Surface Science, 2003, 214(1/4): 304-311.
[3] PAREDES R S C, AMICO S C, D'OLIVEIRA A S C M. The effect of roughness and pre-heating of the substrate on the morphology of aluminium coatings deposited by thermal spraying[J]. Surface and Coatings Technology, 2006, 200(9): 3049-3055.
[4] BOOGAARD A, VAN DEN BROEK J J. Crystallisation and electrical resistivity of sputter-deposited aluminium-germanium alloy films[J]. Thin Solid Films, 2001, 401(1/2): 1-6.
[5] CAPORALI S, FOSSATI A, BARDI U. Oxidative post- treatments for enhanced corrosion resistance of aluminium electrodeposited from ionic liquids[J]. Corrosion Science, 2010, 52(1): 235-241.
[6] BARCHI L, BARDI U, CAPORALI S, FANTINI M, SCRIVANI A. Electroplated bright aluminium coatings for anticorrosion and decorative purposes[J]. Progress in Organic Coatings, 2010, 67(2): 146-151.
[7] LI B, CHEN Y, YAN L, MA J. Pulse current electrodeposition of Al from an AlCl3-EMIC ionic liquid containing NdCl3[J]. Electrochemistry, 2010, 78(6): 523-525.
[8] LI B, FAN C, CHEN Y, LOU J, YAN L. Pulse current electrodeposition of Al from an AlCl3-EMIC ionic liquid[J]. Electrochimica Acta, 2011, 56(16): 5478-5482.
[9] ZIEGLER K, LEHMKUHL H. Die elektrolytische abscheidung von aluminium aus organischen komplexverbindungen[J]. Zeitschrift fur Anorganische und Allgemeine Chemie, 1956, 283(1/6): 414-424. (in German)
[10] UEDA M, KIGAWA H, OHTSUKA T. Co-deposition of Al-Cr-Ni alloys using constant potential and potential pulse techniques in AlCl3-NaCl-KCl molten salt[J]. Electrochimica Acta, 2007, 52(7): 2515-2519.
[11] JAFARIAN M, MAHJANI M G, GOBAL F, DANAEE I. Effect of potential on the early stage of nucleation and growth during aluminum electrocrystallization from molten salt (AlCl3-NaCl- KCl)[J]. Journal of Electroanalytical Chemistry, 2006, 588(2): 190-196.
[12] SIMKA W, PUSZCZYK D, NAWRAT G. Electrodeposition of metals from non-aqueous solutions[J]. Electrochimica Acta, 2009, 54(23): 5307-5319.
[13] WALDEN P. Molecular weights and electrical conductivity of several fused salts[J]. Bull Russian Acad Imper Sci St Petersburg, 1914, 8(6): 405-422. (in Russian)
[14] �� ��, �����, ��ά��, ��Ϫ��, ������, Ѧ ��, ���г�, ��־��. ϡɢ������������Һ���о�(��): InCl3/BPC��ϵ[J]. ��ѧѧ��, 2002, 60(10): 1811-1816.
TIAN Peng, YANG Jia-zhen, XU Wei-guo, SONG Xi-ming, LIU Jian-guo, XUE Hong, LIU Shang-chang, LIANG Zhi-de. Studies on room temperature ionic liquid containing rarely scattered metals (��): The system of InCl3/BPC[J]. Acta Chimica Sinica, 2002, 60(10): 1811-1816.
[15] �ΰ, ���ַ�, �Ĵ���. �廯п-����Һ�帴�ϴ���ϵ��Ч���ϳɻ�״̼����[J]. �ߵ�ѧУ��ѧѧ��, 2005, 26(2): 343-345.
LI Fu-wei, XIA Lin-fei, XIA Chun-gu. Synthesis of cycilc carbonates catalyzed by ionic liquid mediated ZnBr2 catalytic system[J]. Chem J Chinese Universities, 2005, 26(2): 343-345.
[16] �����, �� һ, ��Ӣ��, ������, ̷־��. ��������Һ��绯ѧ�ȶ��Ե��о�[J]. �ߵȻ�ѧѧ��, 2004, 25(9): 1733-1735.
YANG Jia-zhen, JIN Yi, CAO Ying-hua, SUN Li-xian, TAN Zhi-cheng. Studies on electrochemical stability of room temperature ionic liquids[J]. Chemical Research in Chinese Universities, 2004, 25(9): 1733-1735.
[17] ������, �� ��, �����, �� ��. ZnCl2-EMIC����Һ���е����п[J]. �й���ɫ����ѧ��, 2008, 18(6): 1135-1142.
MA Jun-de, LI Bing, YAN Ling-guang, CHEN Yan. Electrodeposition of zinc from zinc chloride-1-ethyl-3- methylimidazolium chloride molten salt[J]. The Chinese Journal of Nonferrous Metals, 2008, 18(6): 1135-1142.
[18] ENDRES F, MACFARLANE D, ABBOTT A. Electrodeposition from Ionic liquids[M]. John Wiley & Sons. Inc., 2008: 84-126.
[19] ABBOTT A, MCKENZIE K. Application of ionic liquids to the electrodeposition of metals[J]. Physical Chemistry Chemical Physics, 2006, 8(37): 4265-4279.
[20] TSUDA T, HUSSEY C. Electrochemical applications of room-temperature ionic liquids[J]. Electrochemical Society Interface, 2007, 16(1): 42-49.
[21] HURLEY F H, THOMAS P. WIER J. Electrodeposition of metals from fused quaternary ammonium salts[J]. Journal of the Electrochemical Society, 1951, 98(5): 203-206.
[22] HURLEY F H, THOMAS P. WIER J. The electrodeposition of aluminum from nonaqueous solutions at room temperature[J]. Journal of the Electrochemical Society, 1951, 98(5): 207-212.
[23] YUE G, ZHANG S, ZHU Y, LU X, LI S, LI Z. A promising method for electrodeposition of aluminium on stainless steel in ionic liquid[J]. AICHE Journal, 2009, 55(3): 783-796.
[24] CHANG J K, CHEN S Y, TSAI W T, DENG M J, SUN I W. Electrodeposition of aluminum on magnesium alloy in aluminum chloride (AlCl3)-1-ethyl-3-methylimidazolium chloride (EMIC) ionic liquid and its corrosion behavior[J]. Electrochemistry Communications, 2007, 9(7): 1602-1606.
[25] JIANG T, CHOLLIER BRYM M J, DUB G, LASIA A, BRISARD G M. Electrodeposition of aluminium from ionic liquids (Part ��): Studies on the electrodeposition of aluminum from aluminum chloride (AlCl3)-trimethylphenylammonium chloride (TMPAC) ionic liquids[J]. Surface and Coatings Technology, 2006, 201(1/2): 10-18.
[26] ١ ��, �����, �� ÷, �����. ��������Һ��BMIAlCl4������ѧ����[J]. ������ѧѧ��, 2006, 22(1): 71-75.
TONG Jing, ZHANG Qing-guo, HONG Mei, YANG Jia-zhen. Thermodynamic properties of ionic liquid BMIAlCl4[J]. Acta Physico-Chimica Sinica, 2006, 22(1): 71-75.
[27] CRAVOTTO G, BOFFA L, L'EV QUE J, ESTAGER J, DRAYE M, BONRATH W. A speedy one-pot synthesis of second- generation ionic liquids under ultrasound and/or microwave irradiation[J]. Australian Journal of Chemistry, 2007, 60(12): 946-950.
[28] DEETLEFS M, SEDDON K. Improved preparations of ionic liquids using microwave irradiation[J]. Green Chemistry, 2003, 5(2): 181-186.
[29] DE LA HOZ A, DIAZ-ORTIZ A, MORENO A. Microwaves in organic synthesis. Thermal and non-thermal microwave effects[J]. Chemical Society Reviews, 2005, 34(2): 164-178.
[30] LAW M, WONG K, CHAN T. Solvent-free route to ionic liquid precursors using a water-moderated microwave process[J]. Green Chemistry, 2002, 4(4): 328-330.
[31] KHADILKAR B M, REBEIRO G L. Microwave-assisted synthesis of room-temperature ionic liquid precursor in closed vessel[J]. Organic Process Research & Development, 2002, 6(6): 826-828.
[32] EARLE M J, GORDON C M, PLECHKOVA N V, SEDDON K R, WELTON T. Decolorization of ionic liquids for spectroscopy[J]. Analytical Chemistry, 2006, 79(2): 758-764.
[33] BAGHURST D R, MINGOS D M P. Superheating effects associated with microwave dielectric heating[J]. Journal of the Chemical Society, Chemical Communications, 1992(9): 674-677.
[34] ZHAO Y, VANDERNOOT T J. Electrodeposition of aluminium from nonaqueous organic electrolytic systems and room temperature molten salts[J]. Electrochimica Acta, 1997, 42(1): 3-13.
[35] WELTON T. Room-temperature ionic liquids: Solvents for synthesis and catalysis[J]. Chemical Reviews, 1999, 99(8): 2071-2084.
[36] GALINSKI M, LEWANDOWSKI A, STEPNIAK I. Ionic liquids as electrolytes[J]. Electrochimica Acta, 2006, 51(26): 5567-5580.
[37] FANNIN A A, FLOREANI D A, KING L A, LANDERS J S, PIERSMA B J, STECH D J, VAUGHN R L, WILKES J S, WILLIAMS J L. Properties of 1,3-dialkylimidazolium chloride-aluminum chloride ionic liquids. 2. Phase transitions, densities, electrical conductivities, and viscosities[J]. The Journal of Physical Chemistry, 1984, 88(12): 2614-2621.
[38] LAI P K, SKYLLAS-KAZACOS M. Electrodeposition of aluminium in aluminium chloride/1-methyl-3-ethylimidazolium chloride[J]. Journal of Electroanalytical Chemistry, 1988, 248(2): 431-440.
[39] KAMAVARAM V, MANTHA D, REDDY R G. Recycling of aluminum metal matrix composite using ionic liquids:: Effect of process variables on current efficiency and deposit characteristics[J]. Electrochimica Acta, 2005, 50(16/17): 3286-3295.
[40] HOLLECK G L, GINER J. The aluminum electrode in AlCl3-alkali-halide melts[J]. Journal of the Electrochemical Society, 1972, 119(9): 1161-1166.
(�༭ ��ѧ��)
������Ŀ��������Ȼ��ѧ����������Ŀ(51054003��50374045)��ɽ��ʡ��Ȼ��ѧ����������Ŀ(Y2007F60��ZR2011BL005)��ɽ��ʡ�ߵ�ѧУ�Ƽ��ƻ�������Ŀ(J09LB59)��ɽ��ʡ�������ѧ�ҿ��н�������������Ŀ(BS2009NJ007)���Ͳ��п�ѧ������չ�ƻ�������Ŀ(2008)
�ո����ڣ�2011-04-12�������ڣ�2012-03-01
ͨ�����ߣ����Ƚ������ڣ���ʿ���绰��18253376831��E-mail: hgxyzlp@sdut.edu.cn