Sn-Cu薄膜的沉积行为及其微观形貌分析
胡炜1,2,谭澄宇1,崔航1,郑子樵1,贺甜1
(1. 中南大学 有色金属材料科学与工程教育部重点实验室,湖南 长沙,410083;
2. 三一重工股份有限公司,湖南 长沙,410100)
摘要:利用电沉积法,在酸性镀液中制得Sn-Cu薄膜,采用扫描电子显微镜(SEM)及能谱仪(EDS)研究镀液中主盐浓度、电镀工艺条件及添加剂对薄膜形貌的影响,并借助循环伏安曲线研究不同条件对Sn-Cu沉积行为的影响。研究结果表明:镀液中主盐浓度的增大促进了Sn-Cu的还原沉积;添加剂的引入对金属离子具有较强的螯合作用,限制了镀液中自由金属离子的浓度,使得合金沉积电位负移;此外,镀液中Sn2+浓度变化对镀层晶粒粒度影响较大,改变Cu2+浓度对镀层的平整度影响较大;电流密度增加、温度降低及加入添加剂,都能细化镀层晶粒。
关键词:电沉积;可焊性镀层;Sn-Cu薄膜;循环伏安
中图分类号:TQ172.84 文献标志码:A 文章编号:1672-7207(2011)04-0940-07
Analysis of Sn-Cu films deposition behaviors and micromorphologies
HU Wei1, 2, TAN Cheng-yu 1, CUI Hang1, ZHENG Zi-qiao1, HE Tian1
(1. Educational Key Laboratory of Non-ferrous Metal Materials Science and Engineering,
Central South University, Changsha 410083, China;
2. SANY Heavy Industry Co.Ltd, Changsha 410100, China)
Abstract: Sn-Cu films were prepared by electrodeposition. The effect of the concentrations of main salts, the process conditions and additives on the morphologies of Sn-Cu films were investigated by scanning electron microscopy (SEM) and energy disperse spectroscopy (EDS), and the effect of various conditions on electrodeposition of Sn-Cu was investigated by cyclic voltammetry (CV). The results indicate that the increase of main salts concentrations promotes Sn-Cu reduction deposition. The addition of additives holds metal ions in chelation, restricts the concentration of free metal ions and the deposition potential of Sn-Cu turns to negative direction. The concentration of Sn2+ has influence mainly on the grain size, while the concentration of Cu2+ has influence mainly on the planeness of the deposits. The increase of the current density, or the decrease of the bath temperature or the addition of additives can accelerate the growth of fine grains in the deposits.
Key words: electrodeposition; solderable coating; Sn-Cu film; cyclic voltammetry
电子产品中使用的印刷电路板和贴片元件表面通常需要电镀可焊性镀层来实现二者的互联。Sn-Pb合金镀层是传统电子电镀中广泛使用的可焊性镀层[1],但是,废旧电子产品中的铅对环境造成严重的污染。在欧盟WEEE指令和RoHS 指令中,铅已经被明确禁止在电子产品中使用[2],我国也于2007-03-01正式施行《电子信息产品污染控制管理办法》,规定对电子信息产品中含有铅等多种有毒有害物质应限制或禁止使用;因此,需要开发无铅可焊性镀层以实现电子封装行业的可持续发展。由于Sn-Cu合金镀层的综合性能较好, Sn-Cu合金镀层成为最有发展前途的可焊性镀层之一,其特点主要表现为低毒、沉积速度快、可焊性好、成本较低,并且还具有在波峰焊接过程中不污染焊料等优点[3-7]。Sn-Cu合金镀层钎料既适宜于表面贴装的再流焊,也适用于接插型的波峰焊,是最具研究和应用价值的Sn系镀层体系。Okada等[8]研究表明:0.1%~0.2% Sn-Cu合金具有很强的抗锡须生长能力,即使在高温下也有很好的可焊性。日本上村工业公司开发的Soft Alloy GTC220 型电镀液很好地抑制了晶须的产生,具备电镀作业性良好和成本低廉等优点。电镀和电化学薄膜生长都是以电化学沉积为基础的,在工业生产和技术发展需要的强烈推动下,金属电沉积的研究一直受到人们广泛关注。近20年来,人们做了大量单组分金属如锌、铜、银等的电沉积实验,主要是研究生长环境如电压、浓度、液层厚度等对沉积物形貌的影响[9-11]。一般认为,生长界面各向异性的变化是枝晶-分形花样转变的主要因素。这种各向异性的变化可能来自于液层中离子浓度的随机分布、生长界面上杂质等所引起的界面不稳定性[12-13]。Winand[14]认为:镀层的晶粒粒径和表面形貌受阴极离子异常吸附的影响,吸附处吸附力决定了晶体生长受阻的程度;并认为晶体生长过程与沉积过电位有关,高过电位下沉积速率变得很快,促使更多的晶核形成,晶粒得以细化;反之,在低过电位下,沉积速率慢,晶粒有充分的时间长大而形成粗大晶粒。这就是过电位原理。这些结果表明:电沉积因素对镀层微观形貌的影响起着至关重要的作用,而镀层的微观形貌影响着镀层的使用性能。在此,本文作者利用电化学方法探讨Sn-Cu的沉积行为,并利用微观结构控制原理研究镀液中主盐浓度、电镀工艺条件及添加剂对镀层微观形貌的影响,以便为制得晶粒细小、表面平整的Sn-Cu薄膜提供理论基础。
1 实验方法
1.1 电沉积实验
实验采用酸性柠檬酸-硫酸盐镀液体系。镀液组成为:20~50 g/L 硫酸亚锡,0.4~1.2 g/L 硫酸铜,1 g/L 对苯二酚,60 g/L 柠檬酸,100~120 g/L 硫酸,2 g/L 明胶,0.8 g/L β-萘酚,0.04 g/L 硫脲。采用纯锡板作阳极,镀液温度控制在(25±1) ℃,使用WYJ 型直流稳流电源进行电镀,电流密度为2 A・dm-2。使用经热处理的光亮紫铜片为阴极。
电镀工艺流程为:铜片→乙醇除油→蒸馏水洗→10%稀硫酸除氧化膜→蒸馏水洗→磷酸擦拭活化表面→电镀Sn-Cu合金→蒸馏水洗→干燥。
利用Qunta200型环境扫描电镜及其附带的电子能谱观察合金镀层的微观表面形貌,并对镀层成分进行分析,电压为25 kV。在以下研究中,每次改变上述镀液组成和工艺操作条件中的1个参数,其他参数均不变。
1.2 循环伏安测试
实验采用CHI660C型电化学工作站(上海辰华)分别对不同条件下的Sn-Cu镀液体系进行循环伏安测试,研究不同条件对Sn-Cu合金共沉积的影响;所有测试都采用三电极体系,以玻碳电极为工作电极,辅助电极采用大面积光亮铂片,232型饱和甘汞电极为参比电极;扫描速度为100 mV/s,溶液温度控制在 (25±1) ℃。
2 结果与讨论
2.1 循环伏安分析
玻碳电极上不同主盐浓度酸性镀液中的循环伏安曲线如图1所示。从图1可以看出:不同主盐浓度时的循环伏安曲线具有相似的变化规律,但随着镀液中Cu2+或Sn2+质量浓度的增大,负向扫描时,还原电流的起峰电位正移,此时,电流增大对应着Sn-Cu合金沉积开始;同时,随着金属离子质量浓度的增大,还原阴极电流也有所提高。正向扫描时,随着主盐质量浓度的增大,氧化电流峰所对应的电位也有向正移的趋势,同时,氧化峰的峰值电流随着主盐质量浓度的增大而增大。对比图1(a)和(b)可以看出:Sn2+质量浓度的改变比Cu2+质量浓度改变所引起的曲线的变化更加明显。这可能是由于当Sn2+质量浓度过低时,离子的迁移速度会低于离子在阴极上放电的速度,出现扩散控制的现象,增大了电极表面的极化率;而当Sn2+质量浓度增大时,镀液中的离子浓度也相应增大,从而降低了电荷的转移电阻,放电金属离子向阴极表面扩散的速度加快,阴极极化降低,使得Sn-Cu合金的沉积电位正移,如图1(a)所示。
从图1(b)可见:随镀液中Cu2+质量浓度的增大,Sn的沉积电位正移。这可能是由于金属在异相基底上沉积时,晶体结构不匹配而导致沉积电位通常比同种金属的电位高。当溶液中不含Cu2+时,Sn在玻碳基底上沉积,由于Sn和玻碳的晶格不匹配,在其上沉积,需要较高的能量,沉积电位较负;而当溶液中含Cu2+时,由于Cu2+的沉积电位较正,优先在玻碳电极上析出,而Sn在Cu层上沉积形核。由于Cu和Sn的晶体结构都是FCC,而且晶格参数相近,因而Sn在Cu上沉积所需要的能量较低,沉积电位正移;随着镀液中Cu2+质量浓度的增大,阴极电流密度增大,表明Cu的沉积量较多,玻碳电极上被Cu覆盖的面积增大,致使Sn的沉积电位逐渐正移。
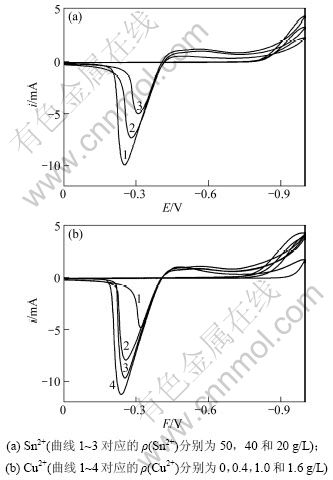
图1 不同主盐浓度的循环伏安曲线
Fig.1 Cyclic voltametry for Sn-Cu alloy system in various main salts concentrations
图2所示为不同添加剂存在时Sn-Cu合金镀液体系中的循环伏安曲线。从图2可以看出:当镀液中分别加入硫脲、柠檬酸时,负向扫描电流峰的起始电位逐渐负移,并且其峰值电流逐渐降低。这可能是由于少量的硫脲吸附在电极表面阻碍了金属离子的还原沉积;此外,据报道[15],硫脲与镀液中Cu2+形成较强螯合物,使其沉积电位大大负移;而与Sn2+形成很弱的螯合物,基本没有改变Sn的沉积电位,促使Sn和Cu共沉积;而加入柠檬酸则对金属离子具有较强的络合作用,使镀液中自由金属离子浓度大大降低,电极表面还原反应速率也随之降低。

图2 不同添加剂的循环伏安曲线
Fig.2 Cyclic voltametry for Sn-Cu alloy system in various additives
2.2 主盐质量浓度的影响
2.2.1 Sn2+质量浓度的影响
图3所示为镀液中Sn2+质量浓度从20 g/L变化到50 g/L时所得的镀层微观形貌。从宏观表面上可以看出:镀层从半光亮渐变为光亮,再变为半光亮并有少量麻点。这可能是由于当Sn2+质量浓度过低时,离子的迁移速度会低于离子在阴极上放电的速度,出现扩散控制的现象,放电离子容易在突出部位沉积,形成较大的晶粒,见图3(a);当Sn2+质量浓度过高时,放电金属离子向阴极表面扩散的速度加快,阴极极化程度降低,结晶又变得比较粗大,如图3(b)所示。
2.2.2 Cu2+质量浓度的影响
图4所示为不同Cu2+质量浓度时所得镀层的SEM像。从图4可见:当Cu2+质量浓度为0.4 g/L时,可得到半光亮的镀层;而当Cu2+质量浓度为1.6 g/L时,镀层变暗。改变Cu2+质量浓度,所得镀层的结晶程度变化不大。这是由于镀层铜的质量浓度较低,其对合金的结晶影响程度亦较小。但是,Cu2+质量浓度过高或过低,镀层都不太平整。当Cu2+质量浓度较低时(图4(a)),镀层出现较多的针孔;当Cu2+质量浓度较高时(图4(c)),镀层变暗。这可能是由于Cu2+与能催化析氢反应的消耗性整平添加剂类似,适量质量浓度的Cu2+在阴极还原过程中起到了整平镀层的作用。由于Cu2+消耗速度受电极表面附近液层中扩散传质速度的限制,当Cu2+质量浓度适当时,其扩散到达电极表面的速度恰好阻化了突出部分的生长,而剩余部分不足以深入凹处阻止凹陷部分的生长,所以,表面比较平整,如图4(b)所示。而当Cu2+质量浓度过高或过低时,都不能起到整平的作用;当镀液中Cu2+的质量浓度超过一定值后,电沉积得到的镀层为黑色粉末状。这主要是由于Sn-Cu合金的沉积属于正则共沉积,铜是电势较正的金属,容易在阴极优先析出;当Cu2+在镀液中的质量浓度过高时,沉积速度过快,导致结晶粗大,形成粉末状的镀层。因此,为了得到符合要求的镀层,需要严格控制铜离子在镀液中的质量浓度为0.8~1.0 g/L,这也是电镀工艺控制的关键。
2.3 电镀工艺的影响
电沉积金属的表面形态和结构主要取决于电沉积的条件。图5所示为不同工艺条件下所得Sn-Cu合金镀层的SEM像。从图5可见:电流密度对镀层表观状态的影响很大;电势对金属表面自由能的影响和表面存在阴离子的特性吸附,也会导致电结晶的形态和结构发生变化;当电流密度为1 A・dm-2时,镀层表面不光亮,呈灰暗色,有少量的突起,表面不平整;而当电流密度为5 A・dm-2时(如图5(a)所示),镀层结晶十分粗大,且存在很多空洞。这是由于电流密度过低时,沉积过电位很小,晶核形成小于成长速度,只有少数晶核长大。随着电流密度的增大,沉积过电位增加,晶核形成速率加快,镀层结晶细致。当电流密度过高时,接近极限电流密度时,电沉积过程主要为扩散控制,阴极附近放电金属离子贫乏,金属离子易在棱角和突出部位放电,出现结瘤或枝状结晶,因而形成疏松的粗大晶粒[16]。此外,随着电流密度的增大,沉积过电位达到析氢电位,阴极表面发生了大量的析氢反应,使电极表面出现较多的针孔。综合考虑各因素,电流密度为2 A・dm-2时可得到晶粒细小、表面平整的镀层。

图3 Sn2+质量浓度不同时Sn-Cu 合金镀层的SEM像
Fig.3 SEM images of Sn-Cu alloy with various Sn2+ mass concentrations

图4 Cu2+质量浓度不同时Sn-Cu 合金镀层的SEM像
Fig.4 SEM images of Sn-Cu alloy with various Cu2+ concentrations

图5 不同工艺条件下Sn-Cu 合金镀层的SEM像
Fig.5 SEM images of Sn-Cu alloy electrodeposited at different process conditions
镀液温度是控制表面形貌重要因素之一。镀液温度高,往往导致镀层表面不平整性加剧。图5(b)所示是温度为40 ℃时得到的镀层表面形貌。从图5(b)可以看出:镀层晶粒粗大,粒度不一,表面上有白色条纹。这是由于镀液温度升高,不仅增大了离子的扩散速度,导致浓差极化降低,而且较高的温度使放电离子具有更大的活化能,电化学极化也降低。上述2方面因素引起阴极极化降低,促使了粗晶镀层的形成[16]。尽管升高温度可以增加盐类的溶解度,提高镀液分散能力,提高镀层的沉积速率,同时也提高阴极电流效率。但对于酸性镀液体系,镀液温度升高,降低了添加剂对金属离子的螯合作用,从而使镀层中铜的含量迅速增大;此外,镀液温度升高,镀液中的Sn2+极易被氧化成Sn4+,而使溶液变浑浊。因此,镀液温度控制在室温附近比较合适。
电镀时间对镀层表面形貌的影响主要表现为镀层厚度的影响。图5(c)所示为电镀50 min时镀层的表面形貌,可以看到镀层表面凹凸不平,晶粒呈较大的纤维状。一般认为表面粗糙度随着镀层厚度的增加而增大。电镀开始前,阴极表面上的镀液成分与镀液的本体成分相同。当衬底上施加电位后,紧靠阴极表面的金属离子立即被阴极上的电子所还原,形成晶粒细致的金属膜层而均匀地覆盖在衬底表面。同时,由于放电诱导,紧靠衬底表面处形成了一层金属-离子匮乏层(MIDL)。在衬底表面上,MIDL厚度是变化的,厚度取决于放电进行的程度,MIDL厚度的变化直接影响到后续的金属沉积效果。金属离子的放电过程显然没有保持均匀,在衬底的突起点(凸点)优先发生放电。凸点上的增强放电诱生出热量,进而增强该处阴离子供给和阳离子发射而促进电极反应进程,更多离子在这些促进点形成沉积,促成了厚度的局域性增长。而在凹点处,由于金属离子匮乏,没有明显放电发生,镀层的生长收到抑制。金属离子的局域化放电随着时间加剧,进一步促成表面粗糙化;而当电镀时间过短时,镀层沉积速度较慢,镀层较薄,表面形状趋于基体表面形状。综合考虑各因素,电镀时间为20 min比较合适。
2.4 添加剂的影响
图6所示为Sn-Cu合金镀层的微观形貌,图7所示为Sn-Cu合金镀层的EDS结果。从图6(a)可见:无添加剂时,镀层表面疏松,不平整,有大量孔洞,并且无添加剂时,镀液中的Sn2+极易被氧化成Sn4+而使镀液变混浊。而单独加硫脲或柠檬酸时,镀层表面仍有大量缺陷,见图6(b)和(c)。从图6(d)可见:柠檬酸和硫脲的加入使镀层表面变得平整、均匀,晶粒细小呈半圆状,粒径为3~5 μm。从图7(a)可见:白色结晶物为锡的氧化产物,同时晶核周围有大量晶须生长。分析图7(b)可知:硫脲的加入明显降低了镀层中通的含量,使镀层中铜的含量维持在共晶点附近(0.5%~2.0%)。
从图6和图7可以看出柠檬酸和硫脲对合金镀层微观形貌及成分的影响。由于金属表面不均匀,金属沉积速度较大的晶面同时也是添加剂分子优先吸收的位置,柠檬酸和硫脲对Sn2+和Cu2+的螯合作用限制了镀液中自由金属离子的浓度,对锡铜共沉积有阻碍作用,本来电沉积速度较大的铜受到的阻碍作用也比较明显,结果使电极表面不同位置上的生长速度趋于一致,这也就阻止了单向生长而形成的粗晶和树枝状镀层出现,从而细化了镀层晶粒,提高了镀层表面质 量[17]。

图6 Sn-Cu合金镀层的表面形貌
Fig.6 Microstructures of Sn-Cu alloy coatings

图7 Sn-Cu合金镀层的EDS结果
Fig.7 EDS results of Sn-Cu alloy coatings
3 结论
(1) 镀液中主盐质量浓度的增大使Sn-Cu沉积电位正移,促进了Sn-Cu还原沉积;由于添加剂对金属离子具有较强的螯合作用,限制了镀液中自由金属离子的浓度,阻碍了Sn-Cu的还原沉积;引入添加剂,使Sn-Cu沉积电位负移。
(2) Sn2+质量浓度对镀层晶核的生长有较大的影响,Sn2+质量浓度过高或过低都会使镀层晶粒粗大化;而Cu2+质量浓度对镀层平整致密性影响较大,Cu2+质量浓度过高或过低都会使镀层变得不平整;Cu2+质量浓度过高还会导致形成黑色粉末状镀层。
(3) 在本实验条件下,电流密度增加、温度降低、电镀时间减小及添加剂的引入都能增大阴极极化程度,得到结晶细致(粒径为3~5 μm)、表面平整的合金镀层,但电流密度过高(>5 A/dm2)、温度过低(<15 ℃)或过高(>30 ℃)及电镀时间过短(<5 min),都会形成粗大的结晶或使镀层表面不平整。
参考文献:
[1] 庄瑞舫. 电镀锡和可焊性锡合金发展概况[J]. 电镀与涂饰, 2000, 19(2): 38-43.
ZHUANG Rui-fang. Review of tin and solderable tin alloy electroplating[J]. Electroplating and Finishing, 2000, 19(2): 38-43.
[2] Davis B. Changing the rules RoHS directive on hazardous substances[J]. Environmental Engineering, 2006, 19(2): 21-23.
[3] 邓正平, 温青. 锡及锡合金可焊性镀层电镀工艺[J]. 电镀与精饰, 2006, 28(5): 33-38.
DENG Zheng-ping, WEN Qing. Electroplating technology for tin and tin alloy solderable coating[J]. Plating and Finishing, 2006, 28(5): 33-38.
[4] 杜长华, 陈方, 杜云飞. Sn-Cu和Sn-Ag-Cu 系无铅钎料的钎焊特性研究[J]. 电子元件与材料, 2004, 28(11): 34-36.
DU Chang-hua, CHEN Fang, DU Yun-fei. Investigation for solderability of Sn-Cu and Sn-Ag-Cu lead-free solders[J]. Electronic Components & Materials, 2004, 28(11): 34-36.
[5] Lu M H, Hsieh K C. Sn-Cu intermetallic grain morphology related to Sn layer thickness[J]. Journal of Electronic Materials, 2007, 36(11): 1448-1454.
[6] Wu C M, Huang M L. Creep behavior of eutectic Sn-Cu lead-free solder alloy[J]. Journal of Electronic Materials, 2002, 31(5): 442-448.
[7] Williams M E, Moon K W, Boettinger W J, et al. Hillock and whisker growth on Sn and SnCu electrodeposition a substrate not forming interfacial intermetallic compounds[J]. Journal of Electronic Materials, 2007, 36(7): 214-219.
[8] Okada Y, Harada H, Saka K. Tin-copper alloy plated wire: Japan, 2000-087204[P]. 1998-09-17.
[9] Matsushita M, Sano M, Havakawa Y, et al. Fractal structure of zinc metal leaves growth by electrodeposition[J]. Physics Review Letters, 1984, 53(3): 286-289.
[10] Hibbert D B, Melrose J R. Copper electrodeposition in paper support[J]. Physical Review A, 1988, 38(2): 1036-1048.
[11] Compton R G, Waller A M. An ac impedance study of fractal geometry of silver films electrodeposited within polymer matrix[J]. Journal of Applied Electrochemistry, 1990, 20(1): 23-25.
[12] Oberholtzer F, Barkev D, Wu Q. Kinetic selection of morphology and growth velocity in electrochemical deposition[J]. Physics Review E, 1998, 57(6): 6955-6961.
[13] Kuhn A, Argoul F. Revisited experimental analysis of morphological changes in thin-layer electrodeposition[J]. Journal of Electroanalytical Chemistry, 1994, 371(1/2): 93-100.
[14] Winand R. Electrodeposition of metals and alloys: New results and perspectives[J]. Electrochimica Acta, 1994, 39(8/9): 1091-1105.
[15] Jorgensen C K. Inorganic complexes[M]. London: Academic Press, 1963: 142.
[16] 安茂忠. 电镀理论与技术[M]. 哈尔滨: 哈尔滨工业大学出版社, 2004: 68-73.
AN Mao-zhong. Theory and technology of electroplating[M]. Harbin: Harbin Institute of Technology Press, 2004: 68-73.
[17] 方景礼. 电镀添加剂理论与应用[M]. 北京: 国防工业出版社, 2006: 224-235.
FANG Jing-li. Theory and application of electroplating additives[M]. Beijing: National Defense Industry Press, 2006: 224-235.
(编辑 陈灿华)
收稿日期:2009-12-05;修回日期:2010-04-02
基金项目:民口配套项目(MKPT-98-106)
通信作者:谭澄宇(1963-),男,湖南长沙人,博士,教授,从事材料及材料表面研究;电话:0731-88830270;E-mail:tanchengyu@yahoo.com.cn