海水中锰的流动注射-分光光度分析
冯思超,陈志刚,袁东星
(厦门大学 海洋与环境学院,福建 厦门,361005)
摘要:基于锰与PAN试剂(1-(2-吡啶基偶氮)-2-萘酚)形成红色螯合物的反应,采用流动注射与分光光度检测器联用,使用Labview语言编程对联用装置进行控制,通过对实验条件进行优化,建立了海水中锰的流动注射-分光光度分析方法。以超纯水为基底,检测限浓度为14 nmol/L,线性范围为0.02~2.00 μmol/L。对Zn,Cu,Ni和Fe等多种金属对锰检测信号的干扰进行考察。由于目前缺乏无锰海水作为工作曲线试样溶液的基底和流动注射的载流,海水测定的检测限和线性范围尚有待进一步确认。研究结果表明:本方法具有操作简单、分析速度快、线性范围宽等优点,可应用于海水样品中锰的现场测定。
关键词:锰;海水;流动注射分析;PAN
中图分类号:P734.4 文献标志码:A 文章编号:1672-7207(2011)S2-0176-05
Flow injection-spectrophotometry analysis of manganese in seawater samples
FENG Si-chao, CHEN Zhi-gang, YUAN Dong-xing
(College of Oceanography and Environmental Science, Xiamen University, Xiamen 361005, China)
Abstract: A flow injection analysis (FIA) method coupled with spectrophotometry detection utilizing the complex reaction between 1-(2-pyridylazo)-2-naphthol and manganese was developed for the determination of dissolved manganese in seawater. A program written in labview was used to control the detecting system. A method detection limit (MDL) 14 nmol/L and linear range 0.020―2.000 μmol/L were obtained in ultra pure water matrix and possible interferences from Zn, Cu, Ni, Fe were also investigated. Because of the lack of low-Mn seawater as the matrix solution of the calibration curve and the FIA carrier, the MDL and linear range of the seawater detection still needs further confirmed. The results show that this method is easy to operate, fast and with wider linear range, and can be applied as on-field analytical technique for dissolved manganese in seawater.
Key words: manganese; seawater; flow injection analysis; PAN
海洋化学的焦点之一是海洋中锰的生物地球化学循环。锰是海洋生物必需的营养元素之一,海底热液中锰的高度富集和氧化较慢的性质,使之可以作为热液羽状流的良好示踪剂。在海水环境中,锰的稳定形态是Mn(Ⅱ),主要以Mn2+或MnCl+形式存在[1],颗粒态锰含量很低。光降解使颗粒态MnO2转化为Mn2+,因此,表层海水(0~100 m)中的锰都以溶解态形式存在,而深层(500~4000 m)有80%锰是以溶解态存在 的[2]。目前测定海水中锰的方法主要有:石墨炉原子吸收光谱法(GFAAS)[3]、电感耦合等离子体-原子发射光谱法(ICP-AES)[4]、电感耦合等离子体-质谱法(ICP- MS)法[5]、样品预富集-化学发光法[6]、催化动力学分光光度法[7]等。GFAAS,ICP-AES和ICP-MS等方法可靠性高,但仪器昂贵,不适于船上现场应用,不能满足示踪海底热液羽状流等研究对锰现场测定的要求。样品预富集-化学发光法、催化动力学分光光度法虽然可以应用于现场,但操作复杂,受干扰因素多,对实验环境和实验人员操作要求高。Chin等[8]基于锰与PAN试剂(1-(2-吡啶基偶氮)-2-萘酚)形成红色螯合物的反应,建立了海水中锰的流动注射-分光光度分析法,并将其运用于海底热液区溶解态锰的现场测定。Statham等[9]基于此建立了近岸海水中锰的原位分析系统,该法具有操作简单、分析速度快、线性范围宽等优点;可实现海水中锰的现场测定,有一定的原位测定应用前景。本研究参照该方法,采用流动注射处理化学反应,与分光光度检测器联用,使用Labview语言编程对联用装置进行控制,通过对实验条件进行优化,建立了测定海水中锰的流动注射-分光光度分析方法。
1 材料和方法
1.1 实验试剂
(1) 0.1 mol/L NaOH溶液:0.4 g NaOH(GR上海山海工学团实验二厂生产)溶于100 mL超纯水。
(2) H3BO3缓冲溶液:0.618 g H3BO3(ACS德国Merck公司生产)加入至100 mL 0.1 mol/L NaOH溶液中。
(3) PAN混合试剂:0.05 g PAN(ACS德国Merck公司生产),5 mL Triton X-100(LG美国Sigma-Aldrich公司生产)加超纯水定容至50 mL,于80 ℃下磁力搅拌8 h至PAN完全溶解,加入100 mL H3BO3缓冲溶液并定容至250 mL。冷却后加入66 mg注射用甲磺酸去铁胺Desferal(瑞士Novartis公司生产)。混合溶液的pH为10左右。
(4) Mn标准使用液(20 μmol/L):110 μL Mn标准储备液(1000 g/L Mn2+,在质量分数为1%的HNO3溶液中,美国Sigma-Aldrich公司生产)加超纯水稀释至100 mL。
(5) 载流:建立、优化方法时使用超纯水作为载流,测定海水加标工作曲线时使用南海表层海水作为载流。
1.2 实验仪器和装置
实验仪器为:流动注射分析仪(北京吉天仪器有限公司制造);六通阀(美国VICI Valco公司制造);2 cm自制流通池;USB2000+微型光纤光谱仪(美国Ocean Optics公司制造);LS-1-LL光源(美国Ocean Optics公司制造);Millipore Simplicity 超纯水系统(美国Millipore公司制造);泵管为硅橡胶管(14#,内径为1.6 mm,壁厚为1.6 mm,保定兰格恒流泵有限公司制造);连接管路为聚四氟乙烯管(PTFE,外径1/16,内径0.75 mm,美国VICI Valco 公司制造)。
实验装置的流路图如图1所示,运行程序如表1所示。
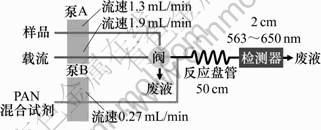
图1 实验装置流路图
Fig.1 Experimental device flow circuit diagram
表1 实验运行程序
Table 1 Program of experimental

1.3 实验方法
按图1所示连接流路,样品溶液充满进样环,载流推动样品溶液流出定量环,与显色剂(PAN 混合试剂)混合,在反应盘管(50 cm)中发生显色反应,流经检测器后排出系统。检测信号(波长为563 nm和650 nm)以Absorbance值输入计算机记录。实验装置中六通阀的控制及信号的采集、记录均由利用Labview语言编制的程序自行完成。
工作曲线的绘制:在数个高密度聚乙烯(HDPE)瓶中依次加入0,0.038,0.075,0.125,0.312和0.625 mL的20 μmol/L Mn标准使用液,用超纯水定容至25 mL。所得溶液Mn浓度依次为0,0.030,0.060,0.100,0.250和0.500 μmol/L。制作海水加标工作曲线时,用海水代替超纯水定容。所得溶液按上述步骤进行测定。
2 实验结果与讨论
2.1 测定波长的选择和信号的记录
对含10 μmol/L Mn的超纯水加标溶液进行吸收光谱的测定,结果如图2所示。从图2可见:PAN-Mn螯合物在563 nm处有最大吸收,PAN试剂(空白)和PAN-Mn螯合物在650 nm处均无吸收。故选用563 nm作为检测波长,650 nm作为参比波长,测定结果以563 nm处吸光值减去650 nm处吸光值给出,以校正微小气泡及其他不可控因素对检测信号的影响。采用流动注射技术,有别于传统的先显色、再比色的分光光度法,样品的检测信号以信号峰的形式出现,在检测信号达到最大值(峰值)时记录瞬时吸收值。
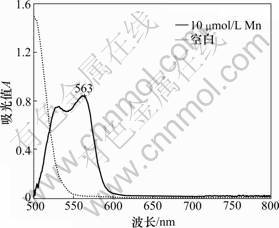
图2 PAN-Mn螯合物的吸收光谱图
Fig.2 Spectrum of PAN-Mn complex
2.2 测定参数的优化
对各实验参数进行了优化。参数包括:定量环长度、反应盘管长度、PAN混合试剂中PAN的浓度及pH、泵速等。参数优化实验中,以含2 μmol/L Mn 的超纯水加标试样作为测试样,以未添加Desferal的PAN混合试剂为显色剂,所有样品均平行测定3次,以平均值±标准偏差表示测定结果。充分考虑灵敏度、信号峰形、分析速度等因素,对结果进行评价。
2.2.1 定量环长度对信号的影响
定量环的长度决定进样体积,考察了其对检测信号的影响,结果如图3所示。从图3可见:随着定量环长度增大,进样体积增大,检测信号随之增大,但分析速度降低。综合考虑灵敏度和分析速度,选择定量环长度为100 cm,此时的进样体积为0.44 mL。
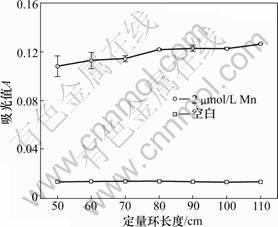
图3 n=3时定量环长度对信号的影响
Fig.3 Effect of length of sampling loop on signal when n=3
2.2.2 反应盘管长度对信号的影响
反应盘管的长度决定了样品与显色剂的反应时间以及反应产物的扩散程度,其对检测信号的影响如图4所示。从图4可见:反应盘管增长,检测信号下降。推测原因为Mn与PAN的反应迅速,反应盘管增长,增加了反应产物在盘管中的扩散,使得检测信号下降。选择反应盘管的长度为0.5 m。
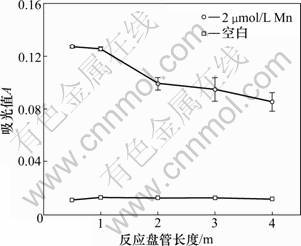
图4 n=3时反应盘管对信号的影响
Fig.4 Effect of length of reaction coil on signal when n=3
2.2.3 PAN混合试剂中PAN浓度对信号的影响
PAN混合试剂中PAN的浓度对检测信号的影响如图5所示。从图5可见:随着PAN浓度的增大,检测信号增强;同时,空白信号升高,综合考虑灵敏度和精确度,选择PAN浓度为0.8 mmol/L。
2.2.4 PAN混合试剂pH对信号的影响
在泵速确定即PAN混合试剂浓度确定后,PAN混合试剂的pH可影响反应的进行,进而影响检测信号。对此参数的考察结果如图6所示。从图6可见:PAN混合试剂的pH在9.00~10.50之间对检测信号和空白信号的影响不大;当pH低于9.00时,检测信号明显降低;当pH高于10.50时,检测信号增大,同时空白吸光值明显增大。为使本方法具有较宽的适用范围,使检测信号具有更好的稳定性,选择PAN混合试剂的pH为10.30,此试剂在加入Desferal后pH在10左右。
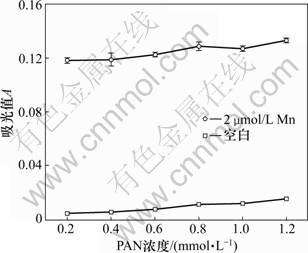
图5 n=3时PAN混合试剂中PAN浓度对信号的影响
Fig.5 Effect of concentration of PAN on signal when n=3
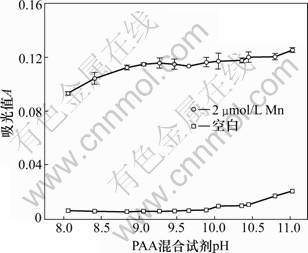
图6 n=3时PAN混合试剂pH对信号的影响
Fig.6 Effect of pH of PAN mixed reagent on signal when n=3
2.2.5 泵速的影响
本实验装置采用了双泵,其各自的泵速决定反应盘管中显色反应时的样品、载流与显色剂的混合比例,进而对参与反应的显色剂有效浓度、反应所处的pH等产生影响。实验对泵速进行优化,最后确定泵A速度为30 r/min,泵B速度为6 r/min。此时各路流速分别为:样品,1.3 mL/min;载流,1.9 mL/min;PAN混合试剂,0.27 mL/min。
2.3 方法的线性范围、检测限、平行性和重复性
应用上述流路及优化的参数,以超纯水为基底,测定0.020~2.000 μmol/L浓度范围内的Mn标准试样,试样的吸光度与Mn浓度成正比,回归方程为:A=0.063 5c+0.012 0 (测定次数n=8, R2=0.998 3)。式中:A为吸光值;c为浓度,μmol/L。本方法的线性范围为0.020~2.000 μmol/L。
方法检测限(Method detection limit, LMD)参照文献[10]确立,用一定浓度的标准试样,平行测定n(≥4)次,据LMD=DS×tf,0.01(单边)=DS×tf,0.01(双边)计算LMD。式中:DS为标准偏差,加标浓度须≤5LMD。在超纯水中加标20 nmol/L,平行测定9次,结果见图7。计算得本方法的检测限为14 nmol/L,5LMD为70 nmol/L,高于加标浓度20 nmol/L。因此,计算所得的方法检测限有效。
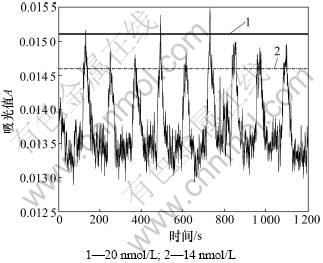
图7 方法检测限实验的信号(Mn浓度为20 nmol/L)
Fig.7 MDL signal for Mn (spiked at 20 nmol/L)
在最佳实验条件下,对2.000 μmol/L Mn试样分别连续测定9次,得相对标准偏差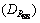 为1.07%,说明本方法具有很好的平行性。在最佳实验条件下,对2.000 μmol/L Mn试样在不同天里测定8次,相对标准偏差
为1.07%,说明本方法具有很好的平行性。在最佳实验条件下,对2.000 μmol/L Mn试样在不同天里测定8次,相对标准偏差 为2.89%,说明本方法具有良好的重复性。
为2.89%,说明本方法具有良好的重复性。
2.4 其他金属的干扰
PAN作为一种金属螯合剂,可以与多种金属反应生成螯合物。根据文献[8],选取Zn,Cu,Ni和Fe等金属进行干扰实验。绘制Zn,Cu,Ni,Fe与PAN形成的螯合物的吸收光谱,如图8所示。各金属加标浓度为10 μmol/L,光谱绘制方法与PAN-Mn螯合物吸收光谱的绘制方法相同。
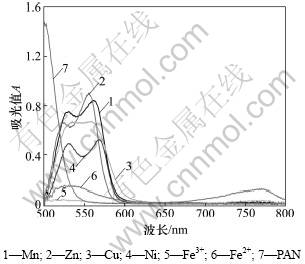
图8 PAN与Mn, Zn, Cu, Ni和Fe形成的螯合物的吸收光谱图
Fig.8 Spectra of complex of PAN with Mn, Zn, Cu, Ni and Fe
由图8可以看出:Zn,Cu和Ni在563 nm处均有较强吸收。但在天然海区,Zn,Cu和Ni大部分以有机络合物的形式存在,对Mn的测定干扰不超过10%[8]。Fe虽然在563 nm处吸收较弱,但在热液区含量很高而且具有广泛的污染来源,可对Mn的检测产生干扰。因此,本方法采用在PAN混合试剂中加入注射用甲磺酸去铁胺Desferal,使之与Fe形成螯合物,以消除Fe对检测的干扰。PAN混合试剂中的Desferal在实验室条件下可以稳定3 d,可以通过含Fe质控样吸收光谱中700~800 nm处信号(PAN-Fe在此处有吸收)的明显增强来指示其失效。
2.5 方法的应用
本实验曾尝试使用超纯水做载流,直接进行海水样品的测定,结果发现:Schlieren效应(在流动注射分析中,当样品与载流的盐度不同时,两者界面上的折射率差异将产生检测干扰信号)严重影响检测信号,无法进行定量。又尝试使用本实验室保存的南海表层海水样品作为载流,以消除Schlieren效应,其作为载流的吸光值超过0.1(以超纯水做载流的吸光值为0.01),加入注射用甲磺酸去铁胺后,吸光值下降近50%,说明其中Fe含量很高,该海水在保存和运输过程中可能受到了污染。由于缺少更好的无锰海水,还是选择该南海表层海水作为流动注射的载流和基底,进行基底加标工作曲线的制作,加标范围为0.06~1.00 μmol/L,以检测信号减去空白信号的值为纵坐标,加标浓度为横坐标,与超纯水加标工作曲线进行斜率的比较,结果如图9所示。可见:海水加标工作曲线的斜率为超纯水加标曲线斜率的近2倍,可能与该海水的复杂组成有关。
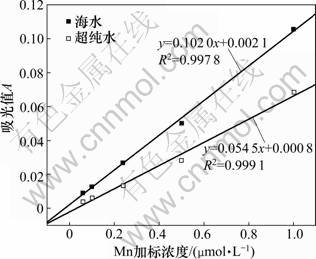
图9 n=3时海水和超纯水加标工作曲线
Fig.9 Calibration curves in seawater and ultra pure water when n=3
3 结论
本方法具有操作简单、分析速度快、线性范围宽等优点。在海洋现场,可取表层海水视为无锰海水作为载流。该方法可应用于较深层海水样品中锰的现场测定,尤其适用在海底热液区附近测定锰、示踪热液羽状流。
参考文献:
[1] Bruland K W. Trace elements in sea-water[M]. Riley J P, Chester R, eds. Chemical Oceanography. London: Academic Press, 1983: 157-220.
[2] Glasby G P. Manganese: Predominant role of nodules and crusts (2nd ed)[M]. Schulz H D, Zabel M, eds. Marine Geochemistry. Berlin: Springer-Verlag, 2006: 371-427.
[3] Klinkhammegr P M, Bender P. The distribution of manganese in the Pacific Ocean[J]. Earth and Planetary Science Letters, 1980, 46(3): 361-384.
[4] Berman S S, McLaren J W, Willie S N. Simultaneous determination of five trace metals in seawater by inductively coupled plasma atomic emission spectrometry with ultrasonic nebulization[J]. Analytical Chemistry, 1980, 488(52): 488-492.
[5] Beck N G, Franks R P, Bruland K W. Analysis for Cd, Cu, Ni, Zn, and Mn in estuarine water by inductively coupled plasma mass spectrometry coupled with an automated flow injection system[J]. Analytica Chimica Acta, 2002, 455(1): 11-22.
[6] Doi T, Obata H, Maruo M. Shipboard analysis of picomolar levels of manganese in seawater by chelating resin concentration and chemiluminescence detection[J]. Analytical and Bioanalytical Chemistry, 2004, 378(5): 1288-1293.
[7] 王尊本, 郑朱梓, 董清木. 近岸海水中痕量锰的催化动力学分光光度法测定[J]. 厦门大学学报: 自然科学版, 1991, 30(3): 336-338.
WANG Zun-ben, ZHENG Zhu-zi, DONG Qing-mu. Catalytic kinetic spectrophotometric determination of trace manganese in coastal sea water[J]. Journal of Xiamen University: Natural Science, 1991, 30(3): 336-338.
[8] Chin C S, Johnson K S, Coale K H. Spectrophotometric determination of dissolved manganese in natural waters with 1-(2-pyridylazo)-2-naphthol: Application to analysis in situ in hydrothermal plumes[J]. Marine Chemistry, 1992, 37(1-2): 65-82.
[9] Statham P J, Connelly D P, German C R, et al. Mapping the 3D spatial distribution of dissolved manganese in coastal waters using an in situ analyser and the autonomous underwater vehicle autosub[J]. Underwater Technology, 2003, 25(3): 129-134.
[10] Berger W, Mccarty H, Smith R K. Environmental laboratory data evaluation[M]. Douglasville, GA, the United States: Genium Publishing Corporation, 1996: 2-11.
(编辑 邓履翔)
收稿日期:2011-06-15;修回日期:2011-07-15
基金项目:中国大洋协会国际海底区域研究开发“十一五”项目(DYXM-115-02-1-12)
通信作者:袁东星(1955-),女,福建厦门人,教授,博士生导师,从事环境化学、分析化学和分离科学研究;电话:0592-2184820;E-mail: yuandx@xmu.edu.cn