
DOI: 10.11817/j.issn.1672-7207.2021.05.006
磁性蟹壳碳吸附材料对溶液中孔雀石绿吸附性能研究
江晨浩1,王杰1,龚亮2,沈康1,雷鸣3,唐谊平1
(1. 浙江工业大学 材料科学与工程学院,浙江 杭州,310014;
2. 浙江工业大学 实验室与资产管理处,浙江 杭州,310014;
3. 湖南农业大学 资源环境学院,湖南 长沙,410128)
摘要:对废弃蟹壳进行活化和碳化处理,采用共沉淀的方法将Fe3O4附载到蟹壳炭上,制备磁性蟹壳活性炭(MAC),并探究其对染料孔雀石绿(MG)的吸附性能和机理。研究结果表明:MAC去除水溶液中的MG时具有1 876.58 mg/g的最大吸附容量,实验结果与Langmuir吸附等温模型和准二级动力学模型拟合结果高度吻合。MAC的高吸附容量主要归因于活化过程创造的大量微米级孔洞以及蟹壳本身去除碳酸盐后的生物结构,提供了充足的活性位点。磁性分离回收后,MAC可以用无水乙醇脱附再生。经过5次MG吸附脱附循环,MAC保持84.6%的高吸附率。对于废弃物的二次利用和实际的废水处理而言,MAC具有高吸附效率和快速磁分离性能,是一种极具前景的生物质可回收吸附剂。
关键词:磁性;蟹壳;孔雀石绿(MG);循环再生
中图分类号:X788 文献标志码:A
文章编号:1672-7207(2021)05-1446-10
Adsorption properties of magnetic crab shell-derived adsorption material for malachite green in solution
JIANG Chenhao1,WANG Jie1, GONG Liang2, SHEN Kang1, LEI Ming3, TANG Yiping1
(1. College of Materials Science and Engineering, Zhejiang University of Technology, Hangzhou 310014, China;
2. Laboratory and Assets Management Department, Zhejiang University of Technology, Hangzhou 310014, China;
3. College of Resource and Environment, Hunan Agricultural University, Changsha 410128, China)
Abstract: The magnetic crab shell activated carbon(MAC) was prepared by co-precipitation method of loading Fe3O4 onto the crab shells that had been activated and carbonized. The adsorption performance and mechanism were explored by a series of experiments. The results show that MAC is used to remove MG cationic dyes in aqueous solution, which has a maximum adsorption capacity of 1 876.58 mg/g. The experimental data is highly consistent with the Langmuir adsorption isotherm model and the quasi-second-order kinetic model. The high adsorption capacity of MAC is mainly due to the large number of micro-scale pores created by the activation process and the biological structure of the crab shell itself after the removal of carbonate, which provides sufficient active sites. After magnetic separation and recovery, MAC can be desorbed and regenerated with absolute ethanol. After five cycles of MG adsorption and desorption, MAC maintains a high adsorption rate of 84.6%. This kind of biomass material with high adsorption efficiency and rapid magnetic separation is a very promising recyclable adsorbent for the secondary utilization of waste and actual wastewater treatment.
Key words: magnetic; crab shell; malachite green; recycling
来自纺织品、纸张、印刷、化妆品、皮革等行业的染料废水不仅对环境造成严重破坏,对人类的健康也构成了极大的威胁[1-2]。在过去的几十年中,已经开发了化学沉淀法、离子交换法、电解法、置换法、反渗透法、吸附法等方法来去除废水中的染料[3]。其中,吸附法因其操作简便、成本低廉、去除时间短、去除率高而备受关注,是最有发展前途的技术之一[4]。碳材料具有廉价、可持续来源、稳定性和易于工程化等优势成为目前主流的染料去除吸附剂,主要包括活性炭、碳纳米管、石墨烯、生物炭、生物质衍生碳材料和纤维素等[5]。其中甲壳类废弃物,如蟹壳,是一种天然具有纳米结构的有机/无机复合物,由蛋白质、几丁质和碳酸盐组成[6]。蟹壳本身拥有较多的碳含量,且自身拥有一定的多孔结构,是一种优良的生物炭前驱体。另外,蟹壳中的碳酸盐占据了一定的空间,利用酸将碳酸盐除去后可以进一步增加生物炭的孔洞结构,这使得蟹壳制备多孔碳材料具有独特的优势。目前,这种生物质及其衍生物(如甲壳素和壳聚糖)已被用作染料去除的生物吸附剂[7-9]。然而,吸附后难以分离以及再生速率低降低了该材料的使用寿命。
本文作者将蟹壳高温碳化后用酸去除残留的无机碳酸盐,然后借助KOH高温活化,形成蟹壳活性炭(AC),然后用共沉淀的方法将Fe3O4附载到蟹壳活性炭上,制成磁性蟹壳活性炭(MAC),并将其作为吸附剂用作孔雀石绿(MG)的吸附,研究接触时间、染料溶度、溶液pH、溶液温度等对吸附行为的影响,最后用吸附动力学和热力学模型拟合MG在2种多孔碳上的吸附行为,讨论其吸附机理。
1 实验
1.1 实验材料
实验材料为NaOH、HCl、KOH、FeCl3、FeCl2・4H2O、氨水、氯化钠、乙醇、孔雀石绿草酸盐等,购买自阿拉丁试剂有限公司,均为分析纯(AR)。所有试剂均未经进一步纯化。
1.2 磁性蟹壳活性炭的制备
将蟹壳充分清洗,去除表面残留的油渍和残留的蟹肉。将蟹壳放入质量分数为20%的NaOH溶液中,在100 ℃下碱煮2 h去除蛋白质,然后在60 ℃的恒温干燥箱中充分干燥12 h。将烘干的蟹壳用研钵磨碎,过孔径74 μm的筛网,储存在干燥处备用。
将上述蟹壳放入管式炉中,在N2的保护下,以5 ℃/min的升温速率从室温升到600 ℃,保温2 h后随炉冷却,然后将碳化后的粉末转移到0.5 mol/L的HCl中,反应30 min以去除蟹壳中的CaCO3。用去离子水将样品洗涤至中性,然后在80 ℃恒温干燥箱中充分干燥12 h。将样品和KOH以质量比(m(C):m(KOH))1:4均匀混合研磨,然后在N2的保护下,以5 ℃/min的升温速率从室温升到800 ℃,保温1.5 h,随炉冷却。用浓度为1 mol/L的HCl溶液洗涤高温活化后残留的KOH,再用去离子水将样品洗涤至中性,在80 ℃恒温干燥箱中充分干燥12 h,即得到蟹壳活性炭(AC)。
在干净的烧杯中加入100 mL去离子水、0.55 g FeCl3和0.35 g FeCl2・4H2O,加入2 mL浓盐酸,搅拌至溶解。再将1 g蟹壳活性炭(AC)加入上述溶液中,持续搅拌20 min,将溶液温度升高到75 ℃保证Fe离子可以充分进入活性炭的孔隙中,再将溶液温度从75 ℃降到40 ℃,保持搅拌的情况下向混合液中加入4 mL浓氨水,继续在40 ℃恒温水浴中搅拌30 min,用磁场将溶液中的固体和液体分离,并用去离子水和无水乙醇反复洗涤,最后在60 ℃恒温干燥箱中充分干燥12 h,即得到磁性蟹壳活性炭(MAC)。
1.3 材料表征
采用美国FEI公司生产的FEI Nano SEM450型场发射扫描电子显微镜(FESEM)表征样品的微观结构及元素组成,加速电压为10~20 kV。样品的物相分析采用荷兰帕纳科公司的X′Pert Pro型X射线衍射仪,测试的靶材为Cu靶(波长为1.546×10-10 m),扫描范围2θ=10°~80°。采用美国的Micromeritics ASAP 2020型氮气吸脱仪在77 K下测试样品的比表面积和孔径分布。采用PE Lambda750紫外/可见/近红外分光光度计测试617 nm处的吸光度,以此确定溶液中孔雀石绿(MG)染料的质量浓度。
1.4 吸附实验
配制质量浓度1 000 mg/L的标准MG溶液,稀释得到实验中所需的质量浓度。吸附实验在指定温度的水浴中进行,转速为120 r/min。在100 mL质量浓度为25~100 mg/L的MG溶液中加入AC和MAC,在指定温度搅拌12 h,离心分离吸附剂和溶液。采用紫外可见近红外扫描分光光度计测定吸附前后溶液中MG的质量浓度。平衡吸附容量计算公式如下:
 (1)
(1)
式中:qe为平衡吸附容量,mg/g;ρ0为MG的初始质量浓度,mg/L;ρe为吸附平衡时溶液中MG的质量浓度,mg/L;V为溶液的体积,mL;m为吸附剂的质量,mg。
吸附剂对MG的去除率R按下式计算:
 (2)
(2)
通过调节0.1 mol/L的HCl和NaOH溶液的比例得到实验所需pH,取0.1 g MAC,然后加入50 mL NaCl溶液,在20 °C的恒温条件下震荡24 h,采用盐添加法测量MAC的零电荷点(PZC),测量最终的pH。
1.5 磁性蟹壳活性炭的循环再生实验
将0.1 g MAC与2 L质量浓度为100 mg/L的MG溶液混合,在20 ℃下恒温震荡24 h达到平衡,然后借助磁场分离收集吸附饱和的MAC并在60 ℃恒温干燥24 h。采用无水乙醇洗涤吸附饱和的MAC,震荡洗涤2 h后重新借助磁场分离收集MAC,再用无水乙醇洗涤震荡,反复洗涤数次,直到乙醇为无色,烘干之后MAC即再生完成,将脱附完全的MAC再次进行吸附实验,共循环5次。
2 结果与讨论
2.1 磁性蟹壳活性炭的微观结构表征
图1所示为MAC制备过程不同阶段的SEM照片。从图1(a)可知:碳化后蟹壳表面呈现出凹凸不平的多孔状;当去除碳化后残留的碳酸盐后(图1(b)),样品表面呈现出数百纳米和几微米的孔洞结构,丰富了样品的比表面积;经过KOH高温活化后(图1(c)),样品表面出现了更多的微米级孔洞,同时,碳表面呈现出更加小的纳米结构,这是因为KOH高温与碳反应,从而在碳表面产生了纳米级的孔洞,反应剧烈的部分产生了局部微孔的结构,这大大增加了比表面积,增加了吸附的有效活性位点[10]。从图1(d)可见:样品表面仍然呈现出多孔结构。采用EDS对MAC进行元素分析可知:Fe3O4已成功负载到了蟹壳活性炭孔隙内部。
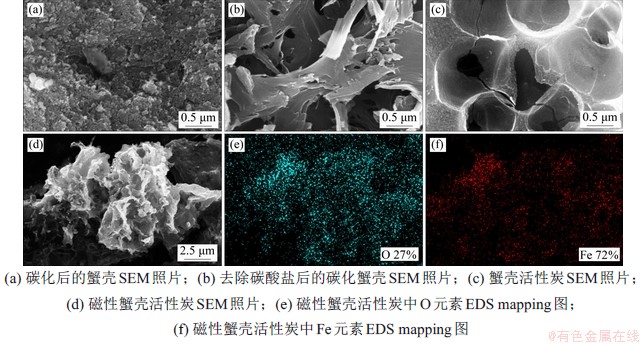
图1 MAC制备过程不同阶段的SEM照片以及EDS mapping图
Fig. 1 SEM images at different stages of MAC preparation process and EDS mapping images
2.2 磁性蟹壳活性炭的物相表征
制备的蟹壳活性炭(AC)和磁性蟹壳活性炭(MAC)的X射线衍射分析结果如图2所示。从图2可知:AC试样在2θ=25°附近有1个较宽的非晶馒头峰,表明AC为无定型碳。由于蟹壳活性炭的存在,MAC试样表现出与AC类似的趋势。MAC试样在2θ=30.1°,35.4°,43.1°,56.9°和62.5°处出现明显的特征峰,分别对应Fe3O4的(220),(311),(400),(511)以及(440)晶面(JCPDS, No.19-0629)[11]。可见,MAC是Fe3O4和蟹壳活性炭的复合材料。
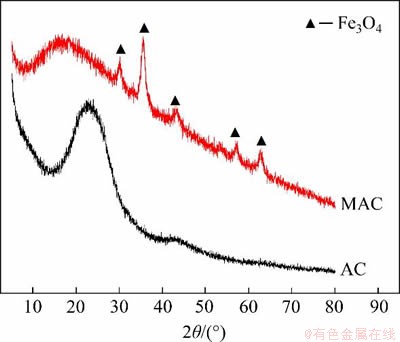
图2 AC和MAC的XRD图谱
Fig. 2 XRD patterns of AC and MAC
2.3 磁性蟹壳活性炭的N2吸附-脱附分析
图3所示为去除碳酸盐之后的蟹壳碳(CC)、蟹壳活性炭(AC)和磁性蟹壳活性炭(MAC)的比表面积和孔径分布。从图3(a)可见:CC的N2脱吸附曲线为具有H3滞后环的IV型曲线,表明了CC中存在介孔结构[12]。AC的N2脱吸附曲线为I型曲线,表明AC的结构以KOH高温活化产生的微孔为主。MAC的N2脱吸附曲线在相对压力p/p0为0~0.6之间表现出I型曲线和非常小的H3滞后环的IV型曲线,说明MAC结构中存在微孔结构和少量的介孔结构。从图3(b)可见:CC孔径主要分布在4.5 nm和20 nm左右,这2种尺寸的介孔结构是去除碳酸盐之后产生的孔洞。AC孔径分布在2 nm以下,主要由KOH高温活化产生的微孔组成。MAC孔径分布也在2 nm以下,但是在9 nm处有1个较弱的峰,证明介孔结构的存在,这些介孔结构可能是Fe3O4和活性炭之间的孔隙而产生的额外介孔。对比3种样品的比表面积和孔体积,CC的比表面积和孔体积分别为303.11 m2/g和0.82 cm3/g,AC的比表面积和孔体积分别为2 023.90 m2/g和1.27 cm3/g,MAC的比表面积和孔体积分别为1 231.49 m2/g和0.83 cm3/g。CC通过KOH高温活化之后转变成AC,比表面积和孔体积都大大增加,AC负载Fe3O4后,Fe3O4占据了活性炭内部的孔洞,又增加了整体的质量,导致比表面积和孔体积下降。
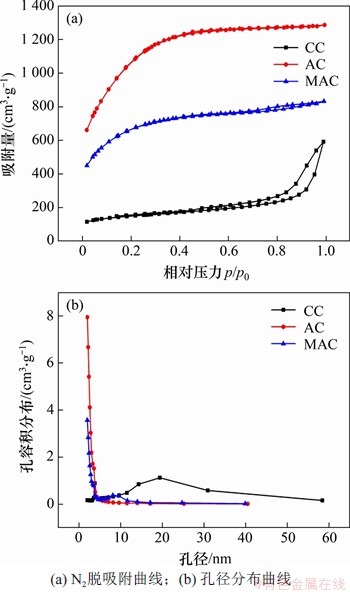
图3 CC,AC和MAC的N2脱吸附曲线和孔径分布曲线
Fig. 3 Nitrogen adsorption-desorption isotherms and pore size distribution curves of CC, AC and MAC
2.4 磁性蟹壳活性炭对MG吸附性能
2.4.1 接触时间和初始浓度的影响
图4(a)所示为AC和MAC在相同MG初始质量浓度下的吸附量qt随时间变化的曲线。可见:2种吸附剂均在180 min左右达到吸附平衡,前期吸附容量增加较快,吸附速率随着吸附的进行逐渐降低,AC的吸附容量要略高于MAC的吸附容量,这是因为附载Fe3O4后,Fe3O4占据了原有的孔隙,导致MAC的比表面积小于AC的比表面积,并且Fe3O4对MG不具有吸附效果,从而MAC单位质量的吸附位点也比AC的小,导致总体吸附容量有略微下降。由于磁性功能的存在,无论是吸附剂使用后的回收难易度,还是吸附剂的回收率,MAC的表现要明显优于AC。图4(b)显示了MAC在初始MG质量浓度从75 mg/L到150 mg/L时吸附量随时间变化的曲线。随着初始质量浓度的升高,MAC的吸附容量也逐渐升高,这是因为高的初始质量浓度可以提供更高的驱动力[13]。在293 K下,溶液初始质量浓度为100 mg/L时,MG最大吸附容量为1 876.58 mg/g,去除率为93.83%。但是随着初始质量浓度的升高,MG的去除率下降,其主要原因是MG过多,超过了MAC的吸附容量,导致残留在溶液中的MG增多。
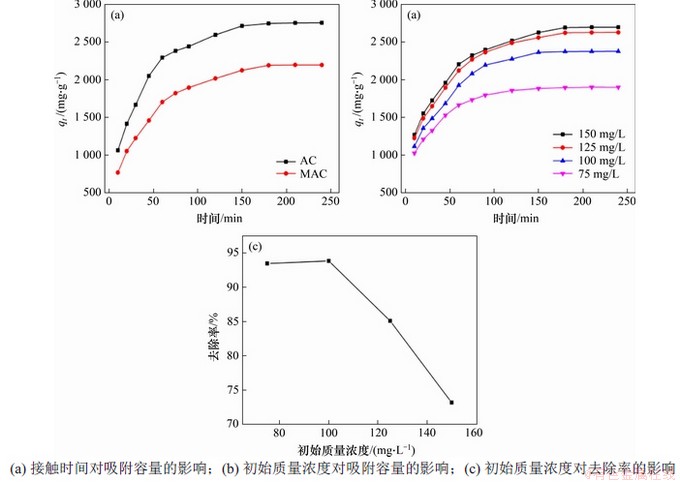
图4 接触时间、初始质量浓度对吸附容量和去除率的影响
Fig. 4 Effects of contact time and initial concentration on adsorption capacity and removal rate
2.4.2 pH的影响
染料分子的电离程度和吸附剂表面的电荷会随着溶液pH的变化而有所不同,这将严重影响吸附过程。因此,研究pH对吸附性能的影响至关重要。吸附剂表面的电荷受到零电荷点(PZC)的影响,当溶液pH大于零电荷点pH时,吸附剂表面带正电荷;当溶液pH小于零电荷点pH时,吸附剂表面带负点;当溶液pH等于零电荷点pH时,吸附剂表面则不带电荷。图5所示为MAC的零电荷点和初始pH对MAC吸附MG性能的影响。图中,pHs为标准pH,pHf为零电荷点pH。从图5(a)可见:MAC的零电荷点为6.3。从图5(b)可见:当溶液初始pH低于4时,吸附容量明显降低,这是由于MG在酸性较强的环境下和质子竞争吸附剂上的活性位点,并且在pH小于4时吸附剂表面带正电荷,MG与吸附剂发生静电排斥从而降低吸附容量[14]。当pH从4逐渐增大到7,吸附容量逐渐增加,这是因为溶液中的质子数随着pH增加不断减少,MG与质子的竞争作用减少,同时吸附剂表面的正电荷减少,逐步转化为带负电荷,这使得MG在吸附剂上的吸附容量逐渐增加,当pH为7时达到最大吸附容量2 315.94 mg/g。当pH大于7时,吸附容量又逐渐下降,这可能是由于MG与溶液中的OH-结合,导致了带负电荷吸附剂上的活性位点和发生了竞争作用,从而使吸附容量降低[15]。
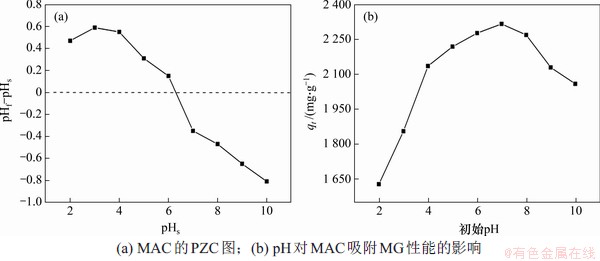
图5 MAC的零点电荷及pH对MAC吸附MG性能的影响
Fig. 5 PZC curve of MAC and effect of pH on adsorption capacity of MG by MAC
2.4.3 温度的影响
图6所示为初始质量浓度为150 mg/L时不同温度下MAC对MG的吸附容量变化曲线。可见:当温度从20 ℃升高到60 ℃,MG的吸附容量从2 196.67 mg/g增加到了2 641.17 mg/g。说明升高温度有利于为MG分子穿过液固相边界层提供更高的驱动力,同时也可以为MG分子和活性位点结合提供必要的能量[16]。
2.4.4 磁性蟹壳活性炭的吸附动力学
准一级动力学模型和准二级动力学模型可以分别用如下方程表示:
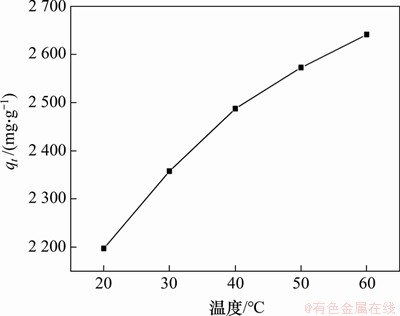
图6 不同温度下MAC对MG吸附容量的曲线
Fig. 6 Adsorption of MG by MAC at different temperatures
 (3)
(3)
 (4)
(4)
式中:qt为吸附剂在t时刻的MG吸附容量,mg/g;k1为准一级动力学吸附常数,min-1;k2为准二级动力学吸附常数,g・mg-1・min-1。
在t=0时,初始吸附速率v0可以通过以下公式计算:
 (5)
(5)
MAC在4种MG质量浓度下的准一级动力学模型和准二级动力学模型线性拟合结果如图7所示,拟合参数如表1所示。从表1可见:在4种浓度下,准二级动力学的拟合相关系数R2均比准一级动力学的大,且准二级动力学的qe更加接近实验结果,说明准二级动力学可以更好地描述MG在MAC上的吸附过程。随着MG初始质量浓度从75 mg/L增加到150 mg/L,MAC的初始吸附速率v0从59.91 mg/(g・min)增加到91.32 mg/(g・min),证明高浓度的MG可以提供高的驱动力来加快吸附速率[17]。
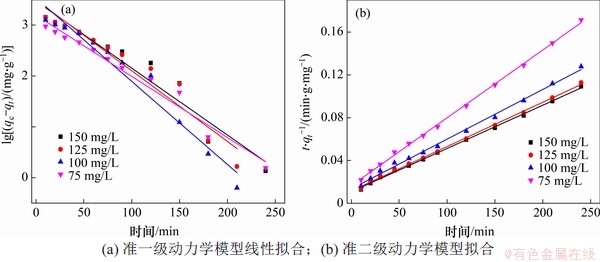
图7 MAC在不同MG质量浓度下动力学模型线性拟合曲线
Fig. 7 Linear fitting of kinetic models of MAC in different concentration of MG
表1 MAC在不同MG质量浓度下的准一级动力学和准二级动力学模型线性拟合参数
Table 1 Pseudo-first-order dynamics model and pseudo-second-order dynamic model fitting parameters of MAC in different concentration of MG

图8所示为MAC在MG初始质量浓度为125 mg/L的溶液中吸附动力学数据Weber-Morris扩散模型线性分段拟合的结果。可见:第一阶段线性拟合的R2为0.998,第二阶段线性拟合的R2为0.972。线性拟合结果较好,说明Weber-Morris扩散模型可以较好地描述MG在MAC上的吸附过程,第一段直线过程表示表面扩散,第二段直线表示粒内扩散,第三段直线为平衡阶段[18]。第一阶段的kdi最大,为191.12 mg/(g・min1/2),表明表面扩散是吸附速率的主要控制步骤。3段直线都不经过坐标原点,表明吸附过程较为复杂,并不是受到单一过程控制。
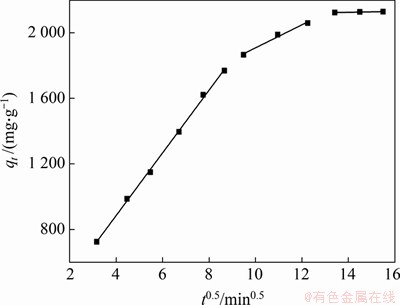
图8 MAC的粒内扩散模型方程拟合结果
Fig. 8 Intra-particle diffusion model of MAC
2.4.5 磁性蟹壳活性炭的吸附等温线
MAC在不同温度下的吸附等温线及其Langmuir模型和Freundlich模型线性拟合结果如图9所示,拟合结果的相关参数见表2。可见:在不同温度下,Langmuir模型线性拟合的R2均高于Freundlich模型线性拟合的R2,并且Langmuir模型线性拟合的qm与实验结果非常接近,这表明Langmuir模型可以更好地描述MG在MAC上的吸附等温线,MG在MAC上的吸附是均匀单层吸附。不同温度下的吸附等温线RL都在0~1的范围内,表明MG在MAC上的吸附是可行的,在该条件下,吸附过程容易进行[19]。

图9 MAC在不同温度下的吸附等温线及其Langmuir模型和Freundlich模型线性拟合结果
Fig.9 Adsorption isotherms of MAC at different temperatures and its Langmuir model and Freundlich model linear fitting curves
表2 MAC在不同温度下吸附等温线的Langmuir模型和Freundlich模型线性拟合参数结果
Table 2 Langmuir model and Freundlich model fitting parameters of adsorption isotherm for MAC at different temperatures

表3 热力学参数计算值
Table 3 Calculation data of thermodynamic parameters of MAC

2.4.6 磁性蟹壳活性炭的吸附热力学
热力学参数计算结果如表3所示。随着温度从293 K升高到333 K,吉布斯自由能的变化 从-3.377 kJ/mol变为-5 kJ/mol,这表明温度升高有利于MAC提升吸附性能。焓的变化
从-3.377 kJ/mol变为-5 kJ/mol,这表明温度升高有利于MAC提升吸附性能。焓的变化 为42.32 kJ/mol,表明MG在MAC上的吸附是一个吸热过程,熵的变化
为42.32 kJ/mol,表明MG在MAC上的吸附是一个吸热过程,熵的变化 为177.69 J/(K・mol),表明吸附过程是一个熵增加的过程[20]。
为177.69 J/(K・mol),表明吸附过程是一个熵增加的过程[20]。
2.4.7 磁性蟹壳活性炭的循环再生实验
MAC具有磁性,可以通过磁场轻易地从吸附后的废液中分离,图10所示为模拟磁场分离吸附剂和溶液的照片。可见,利用磁场可以简单高效地回收吸附剂,进行二次循环使用,大大提高了吸附剂的回收利用率,降低了吸附成本。用无水乙醇可以有效对吸附MG后的MAC进行脱附。循环5次后,MAC仍然保持了1 587.65 mg/g的吸附容量,与第一次相比吸附容量仅降低了15.4%,吸附剂循环使用性较好,可以进行多次高效的MG去除,是一种良好的吸附剂。

图10 MAC磁场分离吸附剂和溶液照片及循环吸附性能
Fig. 10 Photo of simulated magnetic field separation of adsorbent and solution and cycle adsorption performance of MAC
3 结论
1) 制备的磁性蟹壳活性炭具有1 231.49 m2/g的比表面积。MG在MAC上的吸附量在pH为7时最大,并且随着MG初始浓度和温度的增加,MAC对MG的吸附容量也增加。在293 K的温度下,溶液初始浓度为100 mg/L时,MG最大吸附容量为1 876.58 mg/g,去除率为93.83%。
2) MAC对MG的吸附过程具有吸热和自发吸附过程,可以用Langmuir吸附等温模型和准二级动力学模型很好地拟合。
3) MAC经过5次吸脱附循环后吸附容量保持在1 587.65 mg/g,与第一次吸附相比,仅下降了15.4%,具有很好的循环使用能力。
参考文献:
[1] SIYAL A A, SHAMSUDDIN M R, KHAN M I, et al. A review on geopolymers as emerging materials for the adsorption of heavy metals and dyes[J]. Journal of Environmental Management, 2018, 224: 327-339.
[2] MEERBERGEN K, WILLEMS K A, DEWIL R, et al. Isolation and screening of bacterial isolates from wastewater treatment plants to decolorize azo dyes[J]. Journal of Bioscience and Bioengineering, 2018, 125(4): 448-456.
[3] KATHERESAN V, KANSEDO J, LAU S Y. Efficiency of various recent wastewater dye removal methods: a review[J]. Journal of Environmental Chemical Engineering, 2018, 6(4): 4676-4697.
[4] RANGABHASHIYAM S, BALASUBRAMANIAN P. The potential of lignocellulosic biomass precursors for biochar production: performance, mechanism and wastewater application―A review[J]. Industrial Crops and Products, 2019, 128: 405-423.
[5] DAI Yingjie, ZHANG Naixin, XING Chuanming, et al. The adsorption, regeneration and engineering applications of biochar for removal organic pollutants: a review[J]. Chemosphere, 2019, 223: 12-27.
[6] DAI Lichun, ZHU Wenkun, HE Li, et al. Calcium- rich biochar from crab shell: an unexpected super adsorbent for dye removal[J]. Bioresource Technology, 2018, 267: 510-516.
[7] GAO Yuan, XU Shiping, YUE Qinyan, et al. Chemical preparation of crab shell-based activated carbon with superior adsorption performance for dye removal from wastewater[J]. Journal of the Taiwan Institute of Chemical Engineers, 2016, 61: 327-335.
[8] JEON C. Removal of Cr(VI) from aqueous solution using amine-impregnated crab shells in the batch process[J]. Journal of Industrial and Engineering Chemistry, 2019, 77: 111-117.
[9] CHEN Tao, DENG Shubo, WANG Bin, et al. CO2 adsorption on crab shell derived activated carbons: contribution of micropores and nitrogen-containing groups[J]. RSC Advances, 2015, 5(60): 48323-48330.
[10] YAMASHITA A, YOSHIDA T, HIDAKA A, et al. Preparation of activated carbons with high specific surface areas using lignin and crab shells, and their use in methane adsorption[J]. Carbon, 2015, 93: 1080.
[11] NI Shibing, SUN Xiaolei, WANG Xinghui, et al. Low temperature synthesis of Fe3O4 micro-spheres and its microwave absorption properties[J]. Materials Chemistry and Physics, 2010, 124(1): 353-358.
[12] LIN K S, DEHVARI K, LIU Y J, et al. Synthesis and characterization of porous zero-valent iron nanoparticles for remediation of chromium-contaminated wastewater[J]. Journal of Nanoscience and Nanotechnology, 2013, 13(4): 2675-2681.
[13] WANG Jie, HOU Guangya, WU Liankui, et al. A novel adsorbent of three-dimensional ordered macro/mesoporous carbon for removal of malachite green dye[J]. Journal of Central South University, 2020, 27(2): 388-402.
[14] BAYRAMOGLU G, ARICA M Y. Adsorption of Congo Red dye by native amine and carboxyl modified biomass of Funalia trogii: isotherms, kinetics and thermodynamics mechanisms[J]. Korean Journal of Chemical Engineering, 2018, 35(6): 1303-1311.
[15] ALTINTIG E, ONARAN M, SARI A, et al. Preparation, characterization and evaluation of bio-based magnetic activated carbon for effective adsorption of malachite green from aqueous solution[J]. Materials Chemistry and Physics, 2018, 220: 313-321.
[16] SEPULVEDA L A, SANTANA C C. Effect of solution temperature, pH and ionic strength on dye adsorption onto magellanic peat[J]. Environmental Technology, 2013, 34(8): 967-977.
[17] PURI C, SUMANA G. Highly effective adsorption of crystal violet dye from contaminated water using graphene oxide intercalated montmorillonite nanocomposite[J]. Applied Clay Science, 2018, 166: 102-112.
[18] SINGH S, SIDHU G K, SINGH H. Removal of methylene blue dye using activated carbon prepared from biowaste precursor[J]. Indian Chemical Engineer, 2019, 61(1): 28-39.
[19] WANG Shu, NING Huiming, HU Ning, et al. Preparation and characterization of graphene oxide/silk fibroin hybrid aerogel for dye and heavy metal adsorption[J]. Composites Part B: Engineering, 2019, 163: 716-722.
[20] XIONG Shuiying, QIU Muqing, SONG Jiangping, et al. Adsorption isotherm and equilibrium process of dye wastewater onto camphor sawdust[J]. Nature Environment and Pollution Technology, 2016, 15(2): 689-692.
(编辑 赵俊)
收稿日期: 2020 -06 -28; 修回日期: 2020 -10 -18
基金项目(Foundation item):国家自然科学基金资助项目(U1802254,51871201);浙江省自然科学基金资助项目(LY18E040003) (Projects(U1802254, 51871201) supported by the National Natural Science Foundation of China; Project(LY18E040003) supported by Zhejiang Provincial Natural Science Foundation)
通信作者:唐谊平,博士,教授,从事吸附材料和新能源材料研究;E-mail: tangyiping@zjut.edu.cn
引用格式: 江晨浩, 王杰, 龚亮, 等. 磁性蟹壳碳吸附材料对溶液中孔雀石绿吸附性能研究[J]. 中南大学学报(自然科学版), 2021, 52(5): 1446-1455.
Citation: JIANG Chenhao, WANG Jie, GONG Liang, et al. Adsorption properties of magnetic crab shell-derived adsorption material for malachite green in solution[J]. Journal of Central South University(Science and Technology), 2021, 52(5): 1446-1455.