中等嗜热菌浸出黄铜矿的温度影响规律及种群组成分析
温建康1,徐金光2,陈勃伟1,武彪1,姚国成1, 3,刘美林1,王淀佐1, 4
(1. 北京有色金属研究总院 生物冶金国家工程实验室,北京,100088;
2. 中国瑞林工程技术有限公司,江西 南昌,330002;
3. 北京科技大学 土木与环境工程学院,北京,100083;
4. 中国工程院,北京,100088)
摘要:在不同温度条件下进行浸出实验。研究结果表明:中等嗜热菌在12~55 ℃时可保持浸矿活性,其最适生长温度为45~50 ℃,温度达到60 ℃时初始阶段还保持一定活性,但几天后菌浓度逐渐降低,种群比例发生较大变化;克隆文库分析表明:45 ℃和60 ℃条件下浸矿细菌主要为Leptospirillum ferriphilum,Acidithiobacillus caldus,Sulfobacillus thermotolerans和Acidosphaera rubrifaciens,其中Leptospirillum ferriphilum菌所占比例较大,是浸矿过程中的优势菌种。60 ℃条件下浸出过程中还存在古生菌Ferroplasma cupricumulans,古生菌可以利用其他浸矿菌产生的有机物为能源生长。它们之间对浸出所起的作用是相辅相成的,可共同促进黄铜矿的溶解。
关键词:细菌浸出;黄铜矿;中等嗜热菌;克隆文库
中图分类号:TF18 文献标志码:A 文章编号:1672-7207(2012)01-0001-07
Temperature influence on chalcopyrite bioleaching by moderate thermophile bacteria and microbial population analysis
WEN Jian-kang1, XU Jin-guang2, CHEN Bo-wei1, WU Biao1, YAO Guo-cheng1, 3,
LIU Mei-lin1, WANG Dian-zuo1, 4
(1. National Engineering Laboratory of Biohydrometallurgy, General Research Institute for Nonferrous Metals,
Beijing 100088, China;
2. China Nerin Engineering Co., Ltd., Nanchang 330002, China;
3. School of Civil and Environmental Engineering, University of Science & Technology Beijing, Beijing 100083, China;
4. Chinese Academy of Engineering, Beijing 100088, China)
Abstract: Bioleaching of chalcopyrite with moderate thermophilic bacteria was conducted at different temperatures. The results show that the moderate thermophiles can present bioleaching ability at 12-55 ℃ during leaching process. The optimum growth temperature is 45-50℃. When the temperature reaches 60 ℃, moderate thermophiles can maintain activity in the initial stage, but after a few days the bacteria concentration reduces gradually. 16S rDNA clone library reveals that the composition of moderate thermophiles at 45 ℃ and 60 ℃ are mainly Leptospirillum ferriphilum, Acidithiobacillus caldus, Sulfobacillus thermotolerans and Acidosphaera rubrifaciens. Leptospirillum ferriphilum is the dominant bacteria at the both temperatures, and archaea Ferroplasma cupricumulans are found at 60 ℃, which can use organic substances produced by other bacteria as energy source. It is suggested that these bacteria can supplement each other during bioleaching, thus facilitating the dissolution of chalcopyrite.
Key words: bioleaching; chalcopyrite; moderate thermophile; clone library
中国铜矿资源中大部分为硫化铜矿,而其中原生硫化铜矿,即黄铜矿又占很大比例。随着开采品位的不断下降,低品位铜矿采用传统选冶工艺已逐渐不适用,生物冶金技术以其工艺流程短、投资省、生产成本低及环保等诸多优势已逐步得到工业应用[1],但目前采用常温浸矿菌处理黄铜矿难以达到理想的铜浸出效果。研究表明极端嗜热菌对黄铜矿具有较好的浸出效果[2],但由于极端嗜热菌工业放大培养难和高温状态下气液传输的难度要求较高,实现工业应用还没有取得重大突破。中等嗜热菌对黄铜矿的浸出效果较常温菌具有很大优势,浸出速度快、浸出率高[3-4];低品位硫化铜矿的细菌堆浸过程中,堆的内部温度一般可以达到40~50 ℃,正好是中等嗜热菌的最佳生长温度条件,相对极端嗜热菌来说更容易实现工业上的应用。目前,针对中等嗜热菌浸出黄铜矿的实验室研究较 多[5-7],但鲜见关于实现工业应用和产业化应用的文献报道。温度是影响浸矿细菌生长和繁殖的最重要因素之一[8]。在一定温度范围内,微生物的代谢活动与生长繁殖随温度的上升而增加,温度上升到一定程度,开始对机体产生不利影响,如果温度继续升高,细胞功能会急剧下降,以至死亡。各种浸矿细菌有其能进行生长的最低温度、生长速率最大的最适温度和热变性破坏反应占主导的最高温度[9]。一般认为,在最低温度和最高温度时,细菌生长速率可视为零;在最适温度时,生长速率最大。当温度向最适温度升高时,每升高10 ℃,生长速率约增加1倍;当温度高于最适温度时,生长速率降低,并可能发生热死亡。因此,探明中等嗜热菌浸出黄铜矿的温度影响因素和浸矿过程微生物种群组成,对提高黄铜矿微生物浸矿效率具有重要意义。本文作者研究温度对中等嗜热菌浸出黄铜矿过程中的影响规律,并采用16S rDNA克隆文库分析中等嗜热菌在不同温度条件下浸矿过程中的优势浸矿菌的组成,考察45 ℃和60 ℃条件下浸矿细菌的优势菌以及它们之间对黄铜矿浸出过程中所起的 作用。
1 实验
1.1 矿样
试验矿样来自江西德兴铜矿的黄铜矿浮选精矿,含有的主要矿物是黄铜矿,其次是辉铜矿、斑铜矿及脉石矿物,另有少量黄铁矿。矿样的矿物组成见表1,化学元素分析结果见表2。
表1 实验矿样的矿物组成(质量分数)
Table 1 Mineralogical composition of ore %

表2 实验矿样的化学成分(质量分数)
Table 2 Chemical composition of ore %

1.2 菌种
实验用菌种为本实验室所保存的中等嗜热菌混合菌,该混合菌种的原始菌采集自云南墨江镍矿生物堆浸厂和江西德兴铜矿废石堆浸矿区,最适生长温度为45~55 ℃,适宜pH范围1.0~2.2,生物显微镜下观察其形态主要包括长杆状、短杆状和螺旋状,长为1.0~3.0 μm,可氧化Fe2+、硫化矿及单质硫。培养条件为9K培养基,组成为:3.0 g/L (NH4) 2SO4,0.1 g/L KCl,0.5 g/L K2HPO4,0.5 g/L MgSO4和0.01 g/L Ca(NO3)2。
1.3 试验方法
1.3.1 摇瓶浸出
在250 mL锥形瓶中加入90 mL的无铁9K培养基和10 mL的接种液,并加入2 g粒度小于30 μm的黄铜矿精矿,用稀硫酸溶液调pH至1.75。分别在12,33,45和70 ℃的摇床上培养,摇床转速160 r/min,每隔一段时间测定培养液中pH、氧化还原电位和Cu2+浓度。
1.3.2 搅拌浸出
黄铜矿搅拌浸出反应器如图1所示。采用镀膜(聚四氟)不锈钢制成,总体积为3 L。反应器装有在线检测pH和氧化还原电位的装置,同时也可充气。浸出过程中矿浆固液比为1%,矿物粒度D90=74 μm,搅拌转速为160 r/min。初始细菌浓度为1.08×107 mL-1、空气流量0.1 m3/h,浸出过程中每天间隔一定时间用灭菌水补充蒸发水至定量,每隔24 h测定溶液pH及氧化还原电位(VORP)并取样分析Cu2+浓度。
1.4 浸矿过程种群分析方法
1.4.1 DNA提取与纯化
浸出结束后取45 ℃和60 ℃条件下浸出液各300 mL,参考Oved等的方法提取DNA[10]。具体步骤为: 在12 000 r/min离心2 min。离心后的沉淀加入1.5 mL灭菌离心管,用超纯水清洗2次;加入1.0 mL pH 8.0 TE溶液,100 μL 10%PVP,100 μL 20%SDS,465~600 μm灭菌玻璃珠0.6 g;振荡器匀浆5 min;12 000 r/min离心1 min,上清转移至干净离心管,加入1/10体积的3 mol/L冰冷乙醇钠,冰上放置10 min;12 000 r/min离心5 min,上清转移至干净离心管,加入1 mL冰冷异丙醇,沉淀,冰上放置30 min;12 000 r/min离心10 min,用70%乙醇洗沉淀,50 μL TE溶解。粗提DNA采用Wizard DNA Clean-Up System Kit(Promega,USA)纯化,- 20 ℃保存。

图1 黄铜矿生物搅拌浸出反应器示意图
Fig.1 Schematic diagram of stirred tank bioreactor for bioleaching of chalcopyrite
1.4.2 16S rDNA片段的扩增和克隆文库的构建
用于扩增细菌和古细菌的正向引物分别为27F和21F,反向引物均为1492R扩增[11]。反应体系:5倍缓冲液10 μL,Mg2+(25 mmol/L) 3 μL,dNTP(10 mmol/L) 1μL,27F(50 μmol/L) 0.5 μL,1492R(50 μmol/L) 0.5 μL,DNA 1 μL,Promega Flexi GoTaq酶(5 U/μL) 0.25 μL,补灭菌去离子水至50 μL。反应条件:94 ℃变性2 min;再接95 ℃,45 s;54 ℃,45 s;72 ℃,1 min;循环30次;最后于72 ℃延伸10 min。扩增产物以1.0%的琼脂糖凝胶电泳后,用Wizard SV Gel and PCR Clean-Up System(Promega, USA)回收。用Promega的pGEM T Easy Vector与扩增的16S rDNA片段连接后,转到大肠杆菌DH5α(北京博大泰克)感受态细胞中,经蓝白斑筛选获得阳性克隆子,建立16S rDNA克隆文库,克隆文库通过Ampr平板保藏。
1.4.3 16S rDNA克隆文库序列测定和系统发育分析及多样性指数分析
挑取白色克隆后,送上海生工生物工程技术服务有限公司进行DNA序列测定。获得的序列采用Clustal X进行序列比对[12],通过RDP(Ribosomal Database Project)的CHIMERA_CHECK version 2.7将嵌合体序列排除。利用DOTUR软件[13]对测得的序列划分OTU,种群结构多样性指数分析采用SPADE软件[14]。利用BLAST软件从GenBank数据库中搜索相关菌株的16S rRNA 基因序列。用MEGA4 软件[15]进行多序列对位排列,并采用MEGA4软件包中的Kimura 2-Parameter Distance模型及Neighbor-Joining法构建系统发育树。
1.5 检测方法
细菌计数采用血球计数板在生物相差显微镜下观察。pH和氧化还原电位(VORP)采用PC-350型控制器在线测量。溶氧浓度采用Mettler Toledo 4050e型溶氧仪和SmeR型记录仪在线测量和记录。
2 结果和讨论
2.1 温度对中等嗜热菌浸出黄铜矿的影响
为初步考察温度对中等嗜热菌浸出黄铜矿的影响,通过摇瓶试验进行12,33,45和70 ℃条件下的浸出试验,图2所示为浸出过程中的pH和VORP随时间的变化曲线,图3所示为铜浸出率随时间的变化曲线。可见:浸出过程中浸矿细菌的活性决定了浸出速率的高低。在12 ℃条件下铜浸出速率很低,浸出25 d,铜浸出率只有10%左右,在33 ℃条件下,浸出速率明显升高,但是在浸出进行7 d后,浸出速率开始下降并一直维持在较低水平,最终浸出率为30%左右;相比12 ℃和33 ℃ 2个温度水平,在45 ℃时为中等嗜热菌的最适生长温度,在该温度水平下铜浸出速率最高,在浸出进行12 d时,铜浸出率即可达到35%,之后铜浸出速率有所下降,此时细菌浓度检测结果表明也是下降的,但是溶液pH和氧化还原电位一直维持在适宜范围,这种现象的可能原因是生成的黄钾铁矾造成的钝化膜阻碍了浸出的持续进行[16],最终铜浸出率为42%;温度升高到70 ℃时,浸出过程中pH亦呈先升高后降低的变化规律,但氧化还原电位一直维持在最低水平上,浸出速率较低,浸出过程中在该温度水平下细菌浓度一直很低。
为进一步考察温度对中等嗜热菌浸出黄铜矿的影响,研究了40,55和60 ℃条件下黄铜矿的搅拌浸出,结果如图4~6所示。从图4~6可以看出:40 ℃时细菌可以正常生长,铜浸出率随细菌浓度增加而升高,pH维持在1.5至2.00之间,浸出液的氧化还原电位在浸出进行9 d后升高到540 mV,期间铜浸出速率一直维持在高水平,浸出进行12 d铜浸出率为20%,较45 ℃条件下铜的浸出速率要慢;55 ℃条件下,浸出过程中氧化还原电位一直维持在420 mV以下,pH先升高后缓慢下降,细菌生长速率逐步提高,并能保持较好活性,说明浸矿用中等嗜热菌可以在该温度水平下良好生长,但需要一段适应期,经过驯化后可以保持较好的生长和浸矿活性;60 ℃条件下,接种后细菌浓度逐渐下降,浸出进行8 d后细菌浓度维持在1.0× 106 mL-1左右,但是铜浸出速率仍然保持在较高水平,表明浸矿用中等嗜热菌群耐高温能力较弱,但菌群中却存在能在60 ℃条件下存活并具有较强浸矿能力的某类浸矿菌[17],同时在浸矿温度40~60 ℃之间,温度升高有利于加快铜的浸出进行。

图2 不同温度条件下浸出过程中pH和ORP的变化
Fig.2 Changes of pH and ORP with time at different temperatures

图3 不同温度条件下浸出过程中铜浸出率的变化
Fig.3 Changes of copper leaching rate with time at different temperatures
2.2 中等嗜热菌浸矿过程种群组成克隆文库分析结果
前面在进行不同温度条件下采用中等嗜热菌浸出黄铜矿精矿的摇瓶浸出和搅拌浸出中发现,不是在中等嗜热菌的最佳生长温度45~55 ℃,而是在60 ℃的高温条件下,铜浸出速率仍然保持在较高水平。为了解在黄铜矿浸出过程中起作用的细菌种类,试验中采用16S rDNA克隆文库分析45 ℃和60 ℃条件下中等嗜热菌的组成。表3所示为45 ℃和60 ℃样品中微生物种群的多样性指数。从表3可以看出:微生物种群的多样性不高,45 ℃和60 ℃下OTU(Operational taxonomic unit, 操作分类单元)数目分别为4和5。从估计样品覆盖率可以看出覆盖度较高。因此,所得数据能够较好地反映浸出过程中的微生物种群的多样性。

图4 40 ℃条件下搅拌浸出结果
Fig.4 Stirred tank bioleaching result at 40 ℃
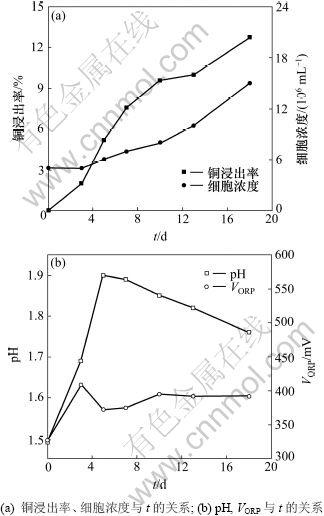
图5 55 ℃条件下搅拌浸出结果
Fig.5 Stirred tank bioleaching result at 55 ℃

图6 60 ℃条件下搅拌浸出结果
Fig.6 Stirred tank bioleaching result at 60 ℃
将每个OTU的代表序列与Genbank中的16S rDNA数据比对,确定每个OTUs最相似的种,将相同的种归为一类,确定不同种在种群中所占的比例,并做圆饼图,如图7和8所示。可见:45 ℃和60 ℃条件下中等嗜热菌的组成主要为Leptospirillum ferriphilum,Acidithiobacillus caldus,Sulfobacillus thermotolerans和Acidosphaera rubrifaciens,其所占比例在45 ℃时分别为60%,16%,14%和10%,在60 ℃时分别为40%,30%,24%和6%。
表3 45 ℃和60 ℃样品中微生物种群的多样性指数
Table 3 Microbial population diversity index at 45 ℃ and 60 ℃
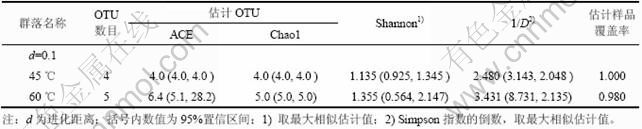
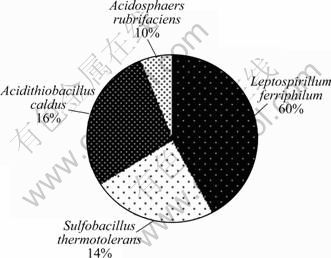
图7 45 ℃时浸出黄铜矿的中等嗜热菌种群组成
Fig.7 Composition of moderate thermophiles at 45 ℃
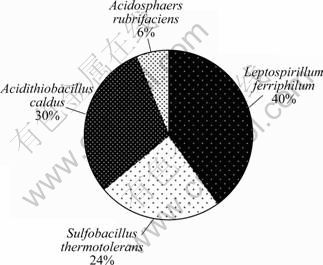
图8 60 ℃时浸出黄铜矿的中等嗜热菌种群组成
Fig.8 Composition of moderate thermophiles at 60 ℃
另外,针对45 ℃和60 ℃条件下搅拌浸出过程中所含的古生菌进行类似的分析,结果表明在45 ℃时未发现有古生菌存在,而在60 ℃时全部为Ferroplasma cupricumulans。
从中等嗜热菌在45 ℃和60 ℃下的种群组成结构可以看出:浸出过程中浸出液的优势菌均为Leptospirillum ferriphilum,在浸出黄铜矿的过程中,主要作用为不断将溶解出来的Fe2+氧化成Fe3+。此外还存在较大比例的Acidithiobacillus caldus,该菌为中等嗜热菌,其最佳生长温度为45 ℃,可氧化还原态硫,不能氧化Fe2+,是黄铜矿浸出过程中还原态硫的主要氧化者。Sulfobacillus thermotolerans能够以Fe2+、元素硫、还原态硫作为其能源基质,可氧化黄铜矿浸出过程中产生的多硫化物中间介质,最适温度为40 ℃,但是能够耐受较高的温度。另外浸出液中亦发现不少的Acidosphaera rubrifaciens,该菌为异养菌,不能氧化铁,也不能氧化硫,在系统中的作用主要是消耗自养菌产生的有机物,消除有机物对自养菌的抑制作用。
60 ℃时存在的古生菌Ferroplasma cupricumulans,细胞形状不固定,缺少细胞壁,抗剪切力能力差,不能耐受搅拌浸出过程中的高矿浆浓度,只能以Fe2+为唯一能源,以无机碳为唯一碳源。
总的来说,在黄铜矿浸出过程中,Sulfobacillus thermotolerans和Leptospirillum ferriphilum可共同对溶液中的Fe2+进行氧化,产生的Fe3+又对黄铜矿进行氧化,矿物表面生成的S膜和还原态的多硫化物又可以作为At. caldus的能源物质被氧化,使得浸矿菌和Fe3+可以更好地与矿物接触,促进浸出反应的进行。Acidosphaera rubrifaciens以及60 ℃时存在的古生菌Ferroplasma cupricumulans,能以其他浸矿细菌提供的有机物为能源,另外Ferroplasma cupricumulans也可氧化溶液中的Fe2+,促进Fe3+浓度升高,从而加快黄铜矿的浸出。可以说上述菌种的存在对浸出所起的作用是相辅相成的,它们共同促进黄铜矿中铜的浸出。
3 结论
(1) 在12 ℃时中等嗜热菌可以适应生长,但铜浸出速率很低;33 ℃时浸出速率有所加快,说明随着温度升高浸矿菌生长活性也升高,从而提高了浸出效率;45 ℃为浸矿菌最适生长温度,此时铜浸出速率最高;温度升高到70 ℃时,氧化还原电位一直维持在低水平,浸出过程中基本未发现有浸矿菌存在,中等嗜热菌在70 ℃时不能够存活。
(2) 40 ℃搅拌浸出时,中等嗜热菌可以正常生长,铜浸出率随细菌浓度增加而升高,期间铜浸出速率一直维持在较高水平;55 ℃时中等嗜热菌可良好生长,但延滞期长,经过驯化后可以保持较好的生长和较高的浸矿活性;温度升至60 ℃时,浸出速度仍然较快,但细菌浓度较低,浸矿菌群中的部分类属菌已失活。
(3) 45 ℃和60 ℃条件下中等嗜热菌组成主要为Leptospirillum ferriphilum,Acidithiobacillus caldus,Sulfobacillus thermotolerans和Acidosphaera rubrifaciens。在黄铜矿浸出过程中,Sulfobacillus thermotoleran和Leptospirillum ferriphilum可共同对溶液中的Fe2+进行氧化,Acidthiobacillus caldus氧化矿物表面生成的S膜和还原态的多硫化物,促进浸出反应的进行。60 ℃时存在的古生菌Ferroplasma cupricumulans可以利用其它浸矿细菌产生的有机物为能源生长,同时氧化溶液中的Fe2+为Fe3+,保持浸矿过程中高水平的氧化还原电位。它们之间对浸出所起的作用是相辅相成的,可共同促进黄铜矿的溶解。
参考文献:
[1] Brierley C L, Brierley T A. Copper bioleaching: State-of- the-art[C]//Young S K, Dreisinger D B, Hackl R P, et al. Proceedings of the Copper99-Cober99 International Conference, Vol.Ⅳ―Hydrometallurgy of Copper. Warrendale, Pennsylvania: The Minerals, Metals & Materials Society, 1999: 59-68.
[2] Petersen J, Dixon D G. Thermophilic heap leaching of a chalcopyrite concentrate[J]. Minerals Engineering, 2002, 15: 777-785.
[3] 舒荣波, 阮仁满, 温建康. 黄铜矿生物浸出中钝化现象研究进展[J]. 稀有金属, 2006, 30(3): 395-400.
SHU Rong-bo, RUAN Ren-man, WEN Jian-kang. Review on passivation of chalcopyrite during bioleaching process[J]. Chinese Journal of Rare Metals, 2006, 30(3): 395-400.
[4] Sladen P J V. The Mintek/Bactech copper bioleach process[C]// Proceedings of Alta 1998 Copper Hydrometallurgy Forum and Sulphides Symposium. Victoria: Alta Metallurgical Services, 1998: 13-23.
[5] 邓敬石, 阮仁满, 温建康, 等. 中等嗜热菌浸出硫化矿的研究现状及展望[J]. 矿产综合利用, 2002, 24(2): 33-38.
DENG Jing-shi, RUAN Ren-man, WEN Jian-kang, et al. Present situation and prospects in bioleaching of sulphides by moderate thermophiles[J]. Multipurpose Utilization of Mineral Resources, 2002, 24(2): 33-38.
[6] Rohwerder T, Gehrke T, Kinzler K, et al. Bioleaching review part A: Progress in bioleaching: fundamentals and mechanisms of bacterial metal sulfide oxidation[J]. Applied Microbiology and Biotechnology, 2003, 63(3): 239-248.
[7] Donati E, Curutchet G, Pogliani C, et al. Bioleaching of covellite using pure and mixed cultures of Thiobacillus ferrooxidans and Thiobacillus thiooxidans[J]. Process Biochemistry, 1996, 31(2): 129-134.
[8] 杨显万, 沈庆峰, 郭玉霞. 微生物湿法冶金[M]. 北京: 冶金工业出版社, 2003: 65-163.
YANG Xian-wan, SHEN Qing-feng, GUO Yu-xia. Microbial hydrometallurgy[M]. Beijing: Metallurgical Industry Press, 2003: 65-163.
[9] 温建康, 姚国成, 陈勃伟, 等. 温度对浸矿微生物活性及浸出速率的影响研究[J]. 北京科技大学学报, 2009, 31(3): 295-299.
WEN Jian-kang, YAO Guo-cheng, CHEN Bo-wei, et al. Effect of temperature on the activity of mineral-bioleaching microorganisms and the bioleaching rate of copper[J]. Journal of University of Science and Technology Beijing, 2009, 31(3): 295-299.
[10] Oved T, Shaviv A, Goldrath T, et al. Influence of effluent irrigation on community composition and function of ammonia- oxidizing bacteria in soil[J]. Applied and Environmental Microbiology, 2001, 67(8): 3426-3433.
[11] Weisburg W G, Barns S M, Pelletier D A, et al. 16S ribosomal DNA amplification for phylogenetic study[J]. Journal of Bacteriology, 1991, 173(2): 697-703.
[12] Thompson J D, Gibson T J, Plewniak F. The ClustalX windows interface: Flexible strategies for multiple sequence alignment aided by quality analysis tools[J]. Nucleic Acids Research, 1997, 24: 4876-4882.
[13] Schloss P D, Handelsman J. Introducing DOTUR: A computer program for defining operational taxonomic units and estimating species richness[J]. Applied and Environmental Microbiology, 2005, 71(3): 1501-1506.
[14] Chao A, Shen T J. Program SPADE (Species Prediction and Diversity Estimation). Program and user’s guide[EB/OL]. [2009-02-13]. http://chao.stat.nthu.edu.tw.
[15] Schloss P D, Handelsman J. Introducing SONS, a tool for operational taxonomic unit-based comparisons of microbial community memberships and structures[J]. Applied and Environmental Microbiology, 2006, 72(10): 6773-6779.
[16] Wichlacz P L, Thompson D L. The effect of heterotrophic acidophilic bacteria on the leaching of cobalt by Thiobacillus ferrooxidans[C]//Norris P R, Kelly D P. Biohydrometallurgy, Proceedings of the International Symposium 1987. Kew, United Kingdom: Science and Technology Letters, 1988: 77-86.
[17] Third K A, Ruwish C R, Watling H R. The role of iron-oxidzing bacteria in stimulation or inhibition of chalcopyrite bioleaching[J]. Hydrometallurgy, 2000, 57: 225-233.
(编辑 杨幼平)
收稿日期:2011-01-19;修回日期:2011-03-21
基金项目:国家高技术研究发展计划(“863”计划)项目(2007AA060900);国家自然科学基金重点资助项目(50934002);国家科技支撑计划项目(2006BAB02A08)
通信作者:温建康(1966-),男,广西陆川人,教授级高级工程师,从事矿物加工、生物冶金技术研究;电话:010-82241313;E-mail: kang3412@126.com