���±�ţ�1004-0609(2011)03-0687-07
������ȡ��YORS��ȡZn(��)-NH3�������ϵ�е�п
�� ��, �� ��, ������, ������, ��ʤ��, �����, ��ʤ��
(���ϴ�ѧ ұ���ѧ�빤��ѧԺ����ɳ410083)
ժ Ҫ��Ϊ��Ч�ظ�����Ʒλ����п��Һ�е�п���ӣ�ʹ��������ȡ��2-������-3-����-���������-ʮ�������(YORS)��Zn(��)-NH3�������ϵ����ȡп���о�������������л������50%YORS+45%H(ϡ�ͼ�)+5%P(���Ӽ�)�����V(A)/V(O) =2?1���¶�298.15 K����ʱ��5 min���ܰ�Ũ��2 mol/L��ˮ���ʼpH 9~11�����������£�п��ƽ����ȡ�ʴ�97%���ϣ������Dex=41.74������ȡ�������л�����к������������������õ���ȡ�����ͺ���ķ��ӽṹ����֤ʵ��п����ȡ��������ȡ���еĦ�-��ͪ������̬Zn2+������������NH3δ����ȡ��
�ؼ��ʣ�����п��Zn(��)-NH3��ϵ���ܼ���ȡ��2-������-3-����-���������-ʮ�������
��ͼ����ţ�TF804.2���� ���ױ�־�룺A
Solvent extraction of zinc from Zn(��)-NH3 complex system by new extractant YORS
HE Jing, HUANG Ling, CHEN Yong-ming, TANG Mo-tang,
JIN Sheng-ming, FENG Rui-zhu, WU Sheng-nan
(School of Metallurgical Science and Engineering, Central South University, Changsha 410083, China)
Abstract: In order to enrich the zinc concentration in ammoniacal leaching solution of low grade of zinc oxide ores, 2-acetyl-3-oxo-dithiobutyric acid-myristyl ester, a new extractant, named as YORS, was used to extract zinc ion from Zn(II)-NH3 solutions. The results show that the average extraction ratio of zinc is larger than 97% and the distribution ratio of zinc can reach 41.74 under the following optimum conditions: organic phase composition 50%YORS+45%H (diluent)+5%P (additive), phase ratio V(A)/V(O) =2:1, temperature 298.15 K, agitation time 5 min, total ammonium concentration 2 mol/L, initial pH value 9~11. YORS extractant and loaded organic phase was characterized by FTIR and UV spectra to determine their molecular structures, respectively. It is demonstrated that the ��-diketone of YORS reacts with free bivalent zinc ion to form coordination compound during zinc solvent extraction, but zinc ammine complexes are not co-extracted.
Key words: zinc oxide ores; Zn(��)-NH3 system; solvent extraction; 2-acetyl-3-oxo-dithiobutyric acid-myristyl ester
������п����Դ������ƶ��������п��ȷǴ�ͳ��п��Դ�����ܵ���ע�����ӡ��ҹ�����п����Դ�ḻ�������п�ʯ���顢���ʺ����ߡ�����ĥ����ɸ��ӵĹ��ԣ�ѡ���ո��ӣ�ҩ��������ѡ��ָ��ͣ�п�Ļ�����Ϊ68%~78%������п����ƷλҲ����35%~40%����Si��Ca��Mg��Fe�����ʺ����ϸ�[1-4]��Ŀǰ������п���ұ���������л�ԭ�ӷ�����������������Ͱ�������3�ࡣ��ԭ�ӷ��������ʺ���Ʒλ����10%�����������ܺĸߡ��̳��ࡢ������Ⱦ���ؼ�п�����ʵͣ�����������������ѡ���Բ��ĸߺ;����������ѵ����⡣��ˣ�����������п���յõ��㷺���Ӻ������о�[5-12]��������Ϊ�о�����������Ʒλ����п���ǽ���ҹ�п��Դ��ȱ��ʵ�ֿɳ�����չ��һ����Ҫ;����
ʵ�ְ���������Ʒλ����п��ҵ��Ӧ�õĹؼ����ڴ�Zn(��)-NH3�������Һ����Ч����ȡ����п��ͬʱʵ�ֽ���������������������пԭ��Ʒλ�ͣ�����Һ��п����Ũ�Ȳ������������յ�Ҫ���ܼ���ȡ�Ǹ��������п����Ũ�ȵ���Ч�ֶ�֮һ��ALGUACIL��[13-15]��RAO��[16]��MICKLER��[17]��SENGUPTA��[18]��FU��[19]��OLIVA��[20]�о����æ�-˫ͪ������(��LIX54��LIX84I��Hostarex DK-16)��NH3-(NH4)2SO4��Һ����ȡп�����������п����ȡ��ͨ������̬Zn2+�������-˫ͪ�����γ�������[Zn(NH3)i]2+ (i=1~4)�����ȴ������ȡ����ˣ�п����ȡ����Ҳ��ʵ�ְ��Խ�����������������Һֱ�ӷ��ذ����������л���������ᷴ�͵õ���Ũ������п��Һ��ͨ����ͳ������ɵõ���п������ʹ��������-˫ͪ����ȡ��ʱ��п����ȡ�ʿ�ʼ����ˮ���ʼpHֵ�����������ߣ���pH=7.5~8.0ʱ��п����ȡ�ʴﵽ���ֵ���ֲ����½�������п���Խ���Һ�ij�ʼpHֵһ��Ϊ10~12��п�İ��Խ������ܼ���ȡ����ֱ��ƥ�䣬�������ӵ��ڽ���ҺpHֵ�Ĺ���OLIVA��[20]ʹ��1-����-3-�ǻ�-4-ʮ�������������� ��-5-������ͪ��NH3-(NH4)2SO4��Һ����ȡп���ڽϿ���pHֵ��Χ��(pH=8~12) ��п�ʾ���95%���ң�Ӧ�ø���ȡ����ʵ�ְ��Խ������ܼ���ȡ���Ż��νӣ����������ȡ����pHֵ��ϵ�Լ����������µ���ȡ��Ũ�ȶԷ���ȵ�Ӱ������˳������о���Ϊ�ˣ�����������һ��������ͪ�������������������Ϊԭ�ϣ��ϳ�һ�ָ�Ч��������ȡ������2-������-3-����-���������-ʮ����������о���ȡ��ϵ��ˮ����ɡ���ȡ��Ũ�ȡ��¶ȡ���ʱ�����ȶ���п�ʵ�Ӱ�죻���ú�������������������ȡ�������л���ķ��ӽṹ���б�������ʾ����ȡ����Zn(��)-NH3�������Һ����ȡп�Ļ�����
1 ʵ��
1.1 ԭ�ϼ��Լ�
Zn(��)-NH3�����ˮ��Һ���÷���������п����ˮ�ֱ�������李��Ȼ�炙�̼������ƶ��ɣ�п��Ũ��ԼΪ0.09 mol/L��������ȡ������������ͪ������̼�����ʮ����Ϊԭ�Ϻϳɵ�2-������-3-����-���������-ʮ�������(YORS)���仯ѧ�ṹʽ���Ц�-˫ͪ�ṹ����ͼ1��ʾ����������������ڱ�1��ͨ�����´���ʵ��������п��������Ϊ19.932 g/L��
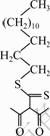
ͼ1 ������ȡ��2-������-3-����-���������-ʮ��������ķ��ӽṹ
Fig.1 Molecular structure of new extractant 2-acetyl-3-oxo- dithiobutyric acid-myristyl ester
1.2 ʵ�鷽��
��һ�����л��������ȡ������ȡ��YORS��ϡ�ͼ�H�����������Ӽ�P��������п���������һ���������£�������Zn(��)-NH3�������Һһ��������η�Һ©�������ں���ˮԡ�����н��е�������ȡ���ﵽ��Ӧʱ���ȡ����Һ©������2 min�����������롣����Һ����EDTA�ζ�����WFX-210��ԭ�����շֹ��ȼƷ�������п������������п�ʣ������л����������ȡ��YORS��ֱ����Nicolet 6700��FTIR�����Ǻ�Shimadzu UV-2450����ֹ��ȼƽ��вⶨ��
��1 ������ȡ��2-������-3-����-���������-ʮ�����������������
Table 1 Physical properties of new extractant 2-acetyl-3-oxo- dithiobutyric acid-myristyl ester

2 ����ԭ��
������ȡ��YORS���Ц�-˫ͪ�ṹ���������칹Ϊϩ��ʽ����OH���е�H�ɺͽ������ӻ���������������ȡ����Zn(��)-NH3�������ϵ��ȡп�ķ�Ӧ��ʽ(1)��ʾ��
 (1)
(1)
����ȡ��Ӧ�ﵽ��ѧƽ��ʱ����ƽ�ⳣ��Kex�ɱ�ʾ
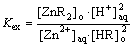 (2)
(2)
 ˮ����ͬʱ����Zn2+��NH3��OH-����Ϸ�Ӧ�Լ���H2O��ˮ�Ϸ�Ӧ�����������غ㶨�ɣ�ˮ����п����Ũ��[Zn]TΪ
ˮ����ͬʱ����Zn2+��NH3��OH-����Ϸ�Ӧ�Լ���H2O��ˮ�Ϸ�Ӧ�����������غ㶨�ɣ�ˮ����п����Ũ��[Zn]TΪ
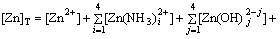
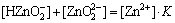 (3)
(3)
���ݷ����Dex�Ķ��壬��
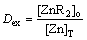 (4)
(4)
��ʽ(3)����ʽ(4)��
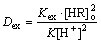 (5)
(5)
ʽ�У�[HR]o��[ZnR2]o�ֱ�Ϊ�л�������ȡ�����ͺ����Ũ�ȣ�[Zn2+]aq��[H+]�ֱ�Ϊˮ��������Zn2+��H+���ӵ�Ũ�ȣ�[Zn]TΪˮ����п����Ũ�ȣ�KΪ��ˮ�������ص�ϵ������ˮ����ɲ���ʱ��KΪ������
��ʽ(5)��֪��ˮ����ɡ���ȡ��Ũ�Ⱥ��¶ȵ����ؾ�Ӱ��п����ȡ��
3 ���������
3.1 ��ȡ��������
3.1.1 ��ȡ��ϵ��ѡ��
�����V(A)/V(O)=1:1���¶�Ϊ298.15 K����ʱ��Ϊ10 min���ܰ�Ũ��Ϊ2 mol/L��ˮ���ʼpHֵΪ9�������£����첻ͬ��ȡ��ϵ����ȡ��Ũ�ȶ���п���̵�Ӱ�죬�����ͼ2��ʾ�����������3����ȡ��ϵ���ֳ����Ƶ���п���ɣ�����п�ʾ������л�����YORSŨ�ȵ����Ӷ�������������Zn(��)-NH3- (NH4)2SO4-H2O��ϵ����п�ʵ������ٶ���죬��Zn(��)-NH3-(NH4)2CO3-H2O��ϵ����п������������������Zn(��)-NH3-(NH4)2SO4-H2O��ϵ�У���[YORS]o=50%ʱ����п�ʸߴ�87.1%������������ϵ��Ҫ�ﵽ��ͬ����п�ʣ���[YORS]o��80%���ɴ˿�֪��������ȡ��YORS��Zn(��)-NH3-(NH4)2SO4-H2O��ϵ����п��Ч����ѣ�������ȡ����������ڸ��������ϵ���С�
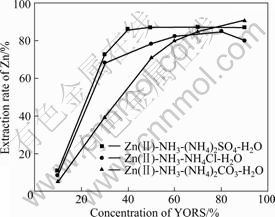
ͼ2 ��ͬ��ȡ��ϵ����ȡ��Ũ�ȶ���п�ʵ�Ӱ��
Fig.2 Effect of concentration of extrant in different extraction systems on extraction rate of zinc
3.1.2 ˮ����ɵ�Ӱ��
���л������Ϊ50%YORS+45%H+5%P�����V(A)/V(O)=1:1���¶�Ϊ298.15 K����ʱ��Ϊ10 min�������£�����ˮ�����ܰ�Ũ���Լ�ˮ���ʼpHֵ����п���̵�Ӱ�죬����ֱ���ͼ3��4��ʾ��

ͼ3 �ܰ�Ũ�ȶ���п�ʵ�Ӱ��
Fig.3 Effect of total ammonia concentration on extraction rate of zinc
��ͼ3��֪�����ܰ�Ũ��Ϊ2~3 mol/Lʱ�ڣ���п�ʽԿ�ά����90%���ϣ������ܰ�Ũ�ȼ�������ʱ��п����ȡ�ʿ�ʼ�����½����������ڵ��ܰ�Ũ������ʱ��ˮ�������백Ũ��Ҳ�����ӣ�ʹ��п����ȡ�����Dex������С���ɴ�ȷ������ܰ�Ũ��Ϊ2 mol/L��
��ͼ4��֪����ˮ���ʼpHֵΪ9~11ʱ����п�ʾ���ά����90%���ң���ˮ���ʼpHֵ����8ʱ������ȡ���е�C=S��������ȡ���̷������Ѷ��ֽ⣬�Ӷ�Ӱ����п����������ʼpHֵ����11ʱ��ˮ��������NH3Ũ������ͬ������п����ȡ�����Dex���ͣ�������п����ȡ���ɴ˿�֪��ˮ���ʼpHֵ������9~11��Ϊ���ˡ�
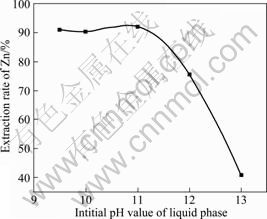
ͼ4 ˮ���ʼpHֵ����п�ʵ�Ӱ��
Fig.4 Effect of initial pH value on extraction rate of zinc
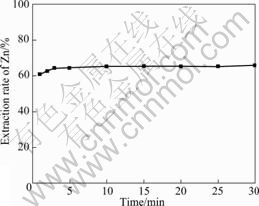
ͼ5 ��ʱ�����п�ʵ�Ӱ��
Fig.5 Effect of agitation time on extraction rate of zinc
3.1.3 ��ʱ���Ӱ��
���л������Ϊ25%YORS+70 %H+ 5%P�����V(A)/V(O)=1:1���¶�Ϊ298.15 K���ܰ�Ũ��Ϊ2 mol/L��ˮ���ʼpHֵΪ 9�������£�������ʱ�����п���̵�Ӱ�죬������ͼ5��ʾ����ͼ5��֪��п����ȡ��Ӧ�dz�Ѹ�٣�5 min����п�ʼ��ɴﵽ64.28%���˺�����ӳ���ʱ�䣬��п�ʻ������ֺ㶨���ɴ�ȷ�������ʱ��Ϊ5 min��
3.1.4 ��ȡ��Ũ�ȵ�Ӱ��
�����V(A)/V(O)=1:1���¶�Ϊ298.15 K����ʱ��Ϊ5 min���ܰ�Ũ��Ϊ2 mol/L��ˮ���ʼpHֵΪ 9�������£�������ȡ��Ũ�ȶ���п���̵�Ӱ�죬������ͼ6��ʾ����Dex�ı���ʽ��֪��������ȡ����Ũ�ȣ��ɴ�����п��ȡ�ķ���ȡ���Ҳ��ͼ5�еõ�����֤�����л�������ȡ��YORS��Ũ����10%���ӵ�50%ʱ����п����֮��10.06%������90%���˺����������ȡ��YORS��Ũ�ȣ��л�����Ȳ������ӣ����ഫ�ʺͷ������ѣ���п���½�����ˣ�ѡȡ��ȡ��YORS�����Ũ��Ϊ50%��

ͼ6 ��ȡ��Ũ�ȶ���п�ʵ�Ӱ��
Fig.6 Effect of extractant concentration on extraction rate of zinc
3.1.5 �¶ȵ�Ӱ��
���л������Ϊ50%YORS+45%H+5%P�����V(A)/V(O)=1:1�� ��ʱ��Ϊ5 min���ܰ�Ũ��Ϊ2 mol/L��ˮ���ʼpH ֵΪ9�������£������¶ȶ���п���̵�Ӱ�죬������ͼ7��ʾ����ͼ7��֪�����¶ȸ���303 Kʱ����п�������¶ȵ���߶����Ͻ��ͣ�����Ҫ����ΪYORS��п����ȡ��Ӧ���ڷ��ȷ�Ӧ���¶ȵ���ߵ�����ȡƽ�ⳣ��Kex�ͷ����Dex���Ͻ��ͣ����¶ȹ���ʱ���л����Ⱥܴ����ഫ�ʺͷ������ѣ�Ҳ��������п��Ӧ�Ľ��У��ɴ�ȷ����ȡ�¶�Ϊ298.15 K��
3.1.6 ��ȵ�Ӱ��
���л������Ϊ50%YORS+45%H+5%P���¶�Ϊ298.15 K����ʱ��Ϊ5 min���ܰ�Ũ��Ϊ2 mol/L��ˮ���ʼpHֵΪ9�������£�������ȶ���п���� ��Ӱ�죬������ͼ8��ʾ����ͼ8��֪�������

ͼ7 �¶ȶ���п�ʵ�Ӱ��
Fig.7 Effect of temperature on extraction rate of zinc

ͼ8 ��ȶ���п�ʵ�Ӱ��
Fig.8 Effect of phase ratio V(A)/V(O) on extraction rate of zinc
V(A)/V(O)��5:1�仯��2:1ʱ����п����25.80%����������87.10%���˺����������V(A)/V(O)����п��������������������пŨ�ȵĸ������ɴ�ȷ��������V(A)/V(O)=2:1��
3.2 ��������
�������������о������ȷ����ȡ��YORS��Zn(��)-NH3�������ϵ��ȡп����������Ϊ���л������50%YORS +45%H+5%P�����V(A)/V(O)=2:1���¶�298.15 K����ʱ��5 min���ܰ�Ũ��2 mol/L��ˮ���ʼpHֵ9~11���ڴ��Ż������£�����4���ظ���п���飬�������2���С��ɱ�2��֪��п��ƽ����ȡ�ʸ���97%��ƽ�������Dex��ߴ�41.74��
3.3 �ͺ���Ľṹ
��ͬ��ȡ��ϵ�и����л������ȡ��YORS��FTIR��UV-Vis�ֱ���ͼ9��10��ʾ��
��2 ����������
Table 2 Results of Zn solvent extraction by YORS extractant under optimum conditions

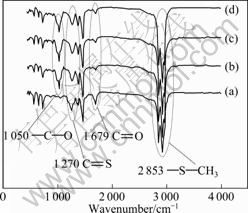
ͼ9 ��ȡ�������л����FTIR��
Fig.9 FTIR spectra of extractant and load organic phase: (a) Extractant; (b) Zn(��)-NH3-(NH4)2SO4-H2O; (c) Zn(��)- NH3-NH4Cl-H2O; (d) Zn(��)-NH3-(NH4)2CO3-H2O
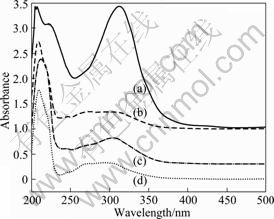
ͼ10 ��ȡ�������л����UV��
Fig.10 UV-Vis spectra of extractant and load organic phase: (a) Extractant; (b) Zn(��)-NH3-(NH4)2CO3-H2O; (c) Zn(��)- NH3-NH4Cl-H2O; (d) Zn(��)-NH3-( NH4)2SO4-H2O
��ͼ9��֪����п��Ӧǰ����ȡ��YORS�ķ��ӽṹ�仯�������л������ȡ����FTIR���϶�����3�������壺��1 270 cm-1����ΪC=S�������壬��1 679 cm-1����ΪC=O�������壬2 853 cm-1������Ϊ��S��CH2���������塣�����л�����1 050 cm-1������һ��ǿ���շ壬���ݹ�����[21-22]����ȷ����Ϊ��C��O���������塣�������ȡ�����У���-˫ͪ�ṹ�ѻ����칹Ϊϩ��ʽ��NH3�����������645��1 145��1 596��3 220��3 350 cm-1������NH3�ļ����������δ�ڸ����л����FTIR���г��֣��ɴ˿�֪����ȡ������NH3δ����ȡ��
��ͼ10��֪����ȡ��YORS���ͺ������
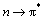 ��ԾǨ���ʷ�ֵ��
��ԾǨ���ʷ�ֵ��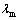 ��208 nm��315 nm����
��208 nm��315 nm����
�����л�����222 nm�������շ���ʧ����ΪC=O�����˶��ѣ�315 nm���ķ�ֵ���������������������ȡ����п�γ���������ԭ�ӵŶԵ��Ӳ���Ǩ�����¡�
3����ȡ��ϵ�ĺ������������������һ�£�˵����ȡ��ϵ�е�CO32-��Cl-��SO42-δ����ȡ��������Ӧ�����������о����������[23]�ķ�������ȡ��YORS��п���ͺ���Ľṹ��ͼ11��ʾ��

ͼ11 �ͺ���ķ��ӽṹ
Fig.11 Molecular structure of extracted species
4 ����
1) ������ȡ��2-������-3-����-���������-ʮ����������Ц�-˫ͪ�ṹ����п���Ӿ��к�ǿ���������ã��ɴ�Zn(��)-NH3-NH4+-H2O��ϵ����ȡ����̬Zn2+���ӣ�������ȡNH3��
2) ��ȡ��Ũ�ȡ��ܰ�Ũ�ȡ�ˮ���ʼpHֵ�����V(A)/V(O)���¶ȵ����ض���п����Ӱ�����������л������Ϊ50%YORS+45%H+5%P�����V(A)/V(O)= 2:1���¶�Ϊ298.15 K����ʱ��Ϊ5 min���ܰ�Ũ��Ϊ2 mol/L��ˮ���ʼpHֵΪ9~11�����������£�п��ƽ����ȡ�ʴ�97.59%��ƽ�������Dex=41.74��
3) ���ݺ�����������������ȷ����п����ȡ�����У���-˫ͪ�ṹ�����칹Ϊϩ��ʽ��OH���е�H�ɺ�����̬Zn2+���ӻ�����������
REFERENCES
[1] �� ��, ������, ��ռ��, �����, κ ��. ����п�������о���״[J]. ��ұ, 2009, 18(2): 57-63.
LI Yong, WANG Ji-kun, REN Zhan-yu, LI Cun-xiong, WEI Chang. Development of treatment on zinc oxide ore[J]. Mining and Metallurgy, 2009, 18(2): 57-63.
[2] ë����, ������, �� ��, �Ų�ѧ. ����п��ѡ��״���о���չ[J]. ���������ѡ��, 2007, 44(4): 4-6.
MAO Su-rong, YANG Xiao-jun, HE Jian, ZHANG Cai-xue. Present situation and development of the flotation of oxidized zinc ore[J]. Metallic Ore Dressing Abroad, 2007, 44(4): 4-6.
[3] ������, ������. ����п��ѡ��״��ǰ��[J]. ���������ѡ��, 2002, 39(7): 17-19.
LIU Rong-rong, LIU Shu-ming. Present situation and prospect the flotation of oxidized zinc ore[J]. Metallic Ore Dressing Abroad, 2002, 39(7): 17-19.
[4] ������, �½���, �� ��, ������. ����ij����п��ѡ�����о�[J]. ��ұ����, 2009, 29(4): 28-32.
LI Yu-qiong, CHEN Jian-hua, CHEN Ye, LONG Qiu-rong. Study on the flotation of zinc oxide ore in Tibet[J]. Mining and Metallurgical Engineering, 2009, 29(4): 28-32.
[5] HARVEY T G. The hydrometallurgical extraction of zinc by ammonium carbonate: A review of the Schnabel process[J]. Mineral Processing and Extractive Metallurgy Review, 2006, 27(4): 231-279.
[6] MOGHADDAM J, SARRAF-MAMOORY R, YAMINI Y, ABDOLLAHY M. Determination of the optimum conditions for the leaching of nonsulfide zinc ores (high-SiO2) in ammonium carbonate media[J]. Industrial and Engineering Chemistry Research, 2005, 44(24): 8952-8958.
[7] YIN Zhou-lan, DING Zhi-ying, HU Hui-ping, LIU Kui, CHEN Qi-yuan. Dissolution of zinc silicate (hemimorphite) with ammonia�Cammonium chloride solution[J]. Hydrometallurgy, 2010, 103(1/4): 215-220.
[8] MENG X H, KENNETH H N. The principles and applications of ammonia leaching of metals: A review[J]. Mineral Processing and Extractive Metallurgy Review, 1996, 16(1): 23-61.
[9] RABAH M A, EL-SAYED A S. Recovery of zinc and some of its valuables salts from secondary resources and wastes[J]. Hydrometallurgy, 1995, 37(1): 23-32.
[10] ������, ������, �� ά, ������, ���ĺ�. NH3-NH4Cl-H2O��ϵ������Ʒλ����п����ȡ��п[J]. ���̹���ѧ��, 2008, 8(S): 219-222.
WANG Rui-xiang, TANG Mo-tang, LIU Wei, YANG Sheng-hai, ZHANG Wen-hai. Leaching of low grade zinc oxide ore in NH3-NH4Cl-H2O system for production of electrolytic zinc[J]. The Chinese Journal of Process Engineering, 2008, 8(S): 219-222.
[11] WANG Rui-xiang, TANG Mo-tang, YANG Sheng-hai, ZHANG Wen-hai, TANG Chao-bo, HE Jing, YANG Jian-guang. Leaching kinetics of low grade zinc oxide ore in NH3-NH4Cl-H2O system[J]. Journal of Central South University of Technology, 2008, 15(5): 679-683.
[12] �°���, ����ΰ, ��ϣ��, �� ˫, ������, ����. ����п���ۺ�������״��չ��[J]. ��ұ����, 2008, 28(6): 62-66.
CHEN Ai-liang, ZHAO Zhong-wei, JIA Xi-jun, LONG Shuang, HUO Guang-sheng, LI Hong-gui. Comprehensive utilization status and expectation of zinc oxide ores[J]. Mining and Metallurgical Engineering, 2008, 28(6): 62-66.
[13] ALGUACIL F J, COBO A. Extraction of zinc from ammoniacal/ammonium sulphate solutions by LIX54 [J]. Journal of Chemical Technology and Biotechnology, 1998, 71(2): 162-166.
[14] ALGUACIL F J, MARTINEZ S. Solvent extraction equilibrium of zinc(��) from ammonium chloride medium by CYANEX 923 in solvesso 100[J]. Journal of Chemical Engineering of Japan, 2001, 34(11): 1439-1442.
[15] ALGUACIL F J, ALONSO M. The effect of ammonium sulphate and ammonia on the liquid-liquid extraction of zinc using LIX 54[J]. Hydrometallurgy, 1999, 53(2): 203-209.
[16] RAO K S, SAHOO P K, JENA P K. Extraction of zinc from ammoniacal solutions by hostarex DK-16[J]. Hydrometallurgy, 1992, 31(1/2): 91-100.
[17] MICKLER W, REICH A, UHLEMANN E, BART H J. Extraction of zinc with long-chain beta-diketones and 4-acyl-5-pyrazolones[J]. Separation Science and Technology, 1995, 30(12): 2585-2592.
[18] SENGUPTA B, BHAKHAR M S, SENGUPTA R. Extraction of zinc and copper-zinc mixtures from ammoniacal solutions into emulsion liquid membranes using LIX 84I[J]. Hydrometallurgy, 2009, 99(1/2): 25-32.
[19] FU Weng, CHEN Qi-yuan, WU Qian, HU Hui-ping, BAI Lan. Solvent extraction of zinc from ammoniacal/ammonium chloride solutions by a sterically hindered ��-diketone and it mixture with tri-n-octylphosphine oxide[J]. Hydrometallurgy, 2010, 100(3/4): 116-121.
[20] OLIVA A, MOLINARI A, Z?NIG F. Studies on the liquid-liquid extraction of nickel (��), zinc(��), cadmium (��), mercury(��), and lead(��) with 1-phenyl-3-hydroxy-4-dodecyldithio carboxylate-5-pyrazolone[J]. Microchim Acta, 2002, 140: 201-203.
[21] ������. ��������������Ӧ��[M]. ����: ��ѧ������, 2006: 42-43, 57.
LI Min-zan. Spectral technique and its application[M]. Beijing: Science Press, 2006: 42-43, 57.
[22] �� �, ����ľ�������ݶ���. �����ۺϽ���ָ��[M]. ����: ��ѧ��ҵ������, 2008: 22, 27-28.
WANG Yao, A LI MU JIANG��BaiDoull. Spectrum analysis and instruction[M]. Beijing: Chemical Industry Press, 2008: 22, 27-28.
[23] MARCHETTI F, PETTINARI C, PETTINARI R. Acylpyrazolone ligands: Synthesis, structures, metal coordination chemistry and applications[J]. Coordination Chemistry Reviews, 2005, 249(24): 2909-2945.
(�༭ ����Ƽ)
������Ŀ�����ҡ�ʮһ�塱�Ƽ�֧�żƻ�������Ŀ(2006BA02B04-4-2)��������Ȼ����������Ŀ(50674104)
�ո����ڣ�2010-04-08�������ڣ�2010-07-27
ͨ�����ߣ��� ���������ڣ��绰��0731-88830470��E-mail��he6213@163.com