文章编号:1004-0609(2007)01-0166-06
均匀沉淀法制备片状结构α-Ni(OH)2
张文魁,黄 娜,黄 辉,甘永平
(浙江工业大学 化工与材料学院,杭州 310014)
摘 要:采用均匀沉淀法制备20%Al取代的α-Ni(OH)2,研究表面活性剂、镍盐浓度、pH值等因素对α-Ni(OH)2微结构和电化学性能的影响。结果表明:控制合适的合成条件,可以获得片厚约为10~20 nm、具有片状微观结构的α-Ni(OH)2粉末;采用CoO作为添加剂时,优化条件下合成的α-Ni(OH)2的放电容量接近390 mA?h/g;与β-Ni(OH)2相比,合成的片状α-Ni(OH)2具有充电电压低、放电电压高及放电容量大的特点。循环伏安测试表明,α-Ni(OH)2电极具有更好的可逆性。
关键词:α-Ni(OH)2;片状结构;均匀沉淀法;电化学性能
中图分类号:TM 911 文献标识码:A
Preparation of flaky α-Ni(OH)2 by coprecipitation method
ZHANG Wen-kui, HUANG Na, HUANG Hui, GAN Yong-ping
(College of Chemical Engineering and Material Science, Zhejiang University of Technology, Hangzhou 310014, China)
Abstract: 20% Al-substituted α-Ni(OH)2 was synthesized by a co-precipitation method, and the effects of surfactants, Ni2+ concentration and pH value on the microstructure and electrochemical properties of the as-prepared α-Ni(OH)2 were investigated. The results show that a special flaky α-Ni(OH)2 with thickness of 10~20 nm can be obtained under the optimum conditions. The discharge capacity of the as-prepared α-Ni(OH)2 powder approximates to 390 mA?h/g using CoO as additive. Compared with β-Ni(OH)2, the as-synthesized flaky α-Ni(OH)2 has the lower charge potential pleateau, higher diacharge potential pleateau and larger discharge capacity. The results of cyclic voltammogram measurements also show that the as-synthesized α-Ni(OH)2 has better electrochemical reversibility.
Key words: α-Ni(OH)2; flaky structure; coprecipitation method; electrochemical properties
Ni(OH)2有α-Ni(OH)2和β-Ni(OH)2两种形态,目前商用β-Ni(OH)2的电化学容量已接近理论容量,提高潜力有限。α-Ni(OH)2/γ-NiOOH在充放电过程 中,a/g 转变过程的电子转移数大于1(γ-NiOOH中Ni的平均价态为3.67,而β-NiOOH中Ni的平均价态为2.90[1]),因此α-Ni(OH)2作为镍电极活性物质,可获得更高的放电容量,但是一般条件下制备的α-Ni(OH)2在强碱中不稳定,很容易在充放电过程中转变为β-Ni(OH)2。近年的研究发现[2-4],在α-Ni(OH)2的晶格中引入三价或二价金属阳离子替代镍离子,可获得一种稳定的水滑石型双氢氧化合物(LDH)。作为掺杂的金属离子,其半径不能太大,在强碱中要能稳定存 在,同时还要保证结构层内有足够的剩余电荷,因此替代镍离子使α-Ni(OH)2相稳定的金属离子主要有Al3+[2-7]、Zn2+[8-9]、Fe3+[10-11]、Mn2+[12]和Co2+[13]等。由于Al3+的半径适宜,在强碱中不会发生价态的变 化,同时价格便宜,对环境污染小,自身的相对原子量小,有利于增大整体物质的质量比能量,因此是制备稳定α-Ni(OH)2的有效替代元素。
实验证明[2-7],Al代α-Ni(OH)2具有放电容量高、大电流放电性能好、内阻和电化学反应电阻小、以及过充时电极不发生膨胀的优点。因此开发高性能、低成本的Al代α-Ni(OH)2替代β-Ni(OH)2作为镍系电池正极活性物质,具有良好的应用前景。
本文作者采用均匀沉淀法制备Al取代的α-Ni(OH)2,研究反应条件对产物的微观结构及电化学性能影响,探索Al取代α-Ni(OH)2的优化合成工艺条件。通过研究发现,在合适的制备条件下,可以得到表面呈特殊片状结构的α-Ni(OH)2,该结构的Al代α-Ni(OH)2具有良好的电化学活性和放电容量。
1 实验
1.1 Al取代α-Ni(OH)2的制备和表征
配制0.3~1.5 mol/L 的Ni(NO3)2・6H2O和0.075~0.375 mol/L的Al(NO3)3・18H2O水或乙醇水溶液,尿素溶液的浓度为4.5 mol/L。根据以前的研究结果[2-3],本实验中Al掺杂量定为20%,因此选择Ni2+与Al3+的摩尔比为4?1,镍盐与尿素的摩尔浓度比为1?6。
首先在三口烧瓶中加入溶液总体积1%的TX-100(OP乳化剂),然后将镍盐溶液和尿素溶液用滴液漏斗并流滴入三口烧瓶中,流速控制在0.5 mL/min,同时快速强烈搅拌,反应温度用水浴锅控制在80~90 ℃。在反应过程中用0.5 mol/L 的KOH溶液调节反应溶液的pH值,反应结束后,将溶液进行超声波分散,离心分离出氢氧化镍样品,用蒸馏水和无水乙醇各洗涤2~3遍,然后在100 ℃下烘干,得到粉末状样品。按照文献[14]的条件,实验中对比测试用的β-Ni(OH)2采用沉淀法在实验室合成。
XRD分析采用D/MAX-3B型X射线衍射仪,Cu Kα单色器(λ=0.154 18 nm),连续扫描,扫描速度8(?)/ min,扫描范围3?~ 70?,工作电压40 kV。表面形貌分析在Hitachis-4700Ⅱ型扫描电子显微镜上进行。
1.2 电极制备和电化学性能测试
将制备的α-Ni(OH)2与5%的石墨粉或CoO粉末混合均匀,加入少量PTFE(60%)和蒸馏水,混合均匀后,涂刮到2 cm×2 cm×1.4 mm的泡沫镍中,在60 ℃下烘干后,刮掉表面的浮粉,然后辊压成0.7 mm厚的电极。制备好的电极进行电化学性能测试前,先在6 mol/L 的KOH溶液中浸泡20 h。
电化学性能测试采用三电极体系,研究电极为氢氧化镍电极,辅助电极为泡沫镍,Hg/HgO为参比电极,电解液为6.0 mol/L KOH。电化学性能的检测在BS-9390二次电池性能检测装置(广州擎天实业有限公司生产)上进行,循环伏安测试采用CHI660B电化学工作站(上海辰华仪器公司)。测试电极的充放电和循环特性时,充放电倍率均为0.2C,充电时间为6 h,放电截止电位为0 V ( vs Hg/HgO),各放电电极的容量均相对于样品质量。
2 结果与讨论
2.1 不同制备条件对α-Ni(OH)2的电化学性能的影响
2.1.1 表面活性剂和溶剂的影响
图1所示为水溶液中添加1%(体积比)TX-100对α-Ni(OH)2放电性能的影响。如图所示,添加少量TX-100后合成的α-Ni(OH)2,放电电压变化不大,但放电容量显著增加,表明溶液中添加表面活性剂可提高α-Ni(OH)2的电化学性能。
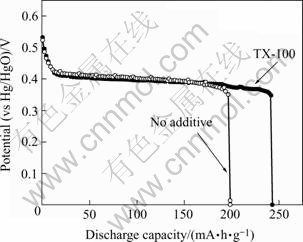
图1 添加1%的表面活性剂TX-100对α-Ni(OH)2放电曲线的影响
Fig.1 Effect of surfactant TX-100 on discharge curve of α-Ni(OH)2 electrode (c(Ni2+)=0.7 mol/L, pH≈8)
α-Ni(OH)2的合成通常是在水溶液中进行,其形貌和大小与制备条件有关。在沉淀过程中,溶液表面张力的改变对氢氧化镍的晶核形成和长大有明显的影响,从而改变氢氧化镍的微观形貌[14]。图2所示为在不同浓度乙醇溶液中合成的α-Ni(OH)2的放电曲线。与水溶液中合成的样品相比,采用乙醇水溶液制备的α-Ni(OH)2放电容量明显增加,其中在30%乙醇溶液中制备的α-Ni(OH)2放电容量最大,放电平台电压也最高,表明采用乙醇溶液合成α-Ni(OH)2的电化学性能较好。
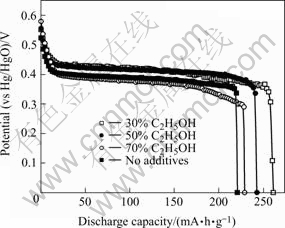
图2 乙醇溶液浓度对α-Ni(OH)2电极放电曲线的影响
Fig.2 Effect of ethanol concentration on discharge curves for α-Ni(OH)2 (1% TX-100, pH≈8)
2.1.2 镍盐浓度的影响
图3所示为镍盐浓度对α-Ni(OH)2的放电容量 和放电平台电压的影响,合成时采用30%乙醇水溶液,其中含有1%(体积比)TX-100表面活性剂。合成过程中,溶液的pH值控制在8~9左右。如图所示,随着镍盐浓度的增加,α-Ni(OH)2的放电容量逐渐增加,当浓度为0.7 mol/L 时放电容量最高,在261 mA・h/g左右,随后随着镍盐浓度的进一步增加,放电容量则快速下降。镍盐浓度对α-Ni(OH)2的放电平台电压也有明显的影响,放电电压随着镍盐浓度的增加先缓慢增加,约0.7 mol/L时放电电压达到极大值,随后逐渐下降;当镍盐浓度超过1 mol/L后,放电平台又随着镍盐浓度的增加而逐渐增加,放电平台出现在0.30~ 0.45 V之间。
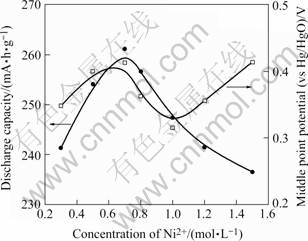
图3 镍盐浓度对放电容量和放电平台电压的影响
Fig.3 Effects of Ni2+ concentration on discharge capacity and discharge potential
2.1.3 pH值的影响
研究表明[15],合成时不同pH值对合成的α-Ni(OH)2的堆积密度、比容量、粒径大小和形貌有一定影响,从而对其放电容量也有一定影响。一般来 说,随着制备时溶液pH值的升高,α-Ni(OH)2放电容量增加。pH值较低时,制备的活性物质利用率低,容量也不高,同时由于电解液渗透困难,会引起局部电流密度过大,导致充电不均,加剧电极的变形和膨 胀,降低电极的循环寿命。但pH超过一定值后,由于α-Ni(OH)2颗粒平均粒径小、内孔体积小、堆积密度低、电极的比容量也不高,要使α-Ni(OH)2的堆积密度与活性都得到提高,必须选择一个合适的反应pH值。本研究发现,pH值为10时,所得的α-Ni(OH)2电极的放电电压和放电容量远高于pH为8时制得的α-Ni(OH)2(图4)。
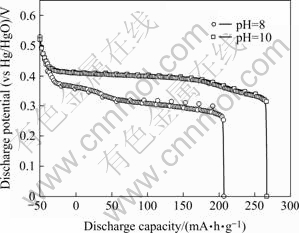
图4 不同pH时制备的α-Ni(OH)2电极的放电曲线
Fig.4 Discharge curves of α-Ni(OH)2 synthesized at different pH values (c(Ni2+)=0.7 mol/L, 30% ethanol solution)
2.2 优化条件下制备的α-Ni(OH)2的电化学性能
通过对Al代α-Ni(OH)2合成条件的优化,可以获得综合电化学性能较好的α-Ni(OH)2样品。本实验中,溶剂为30%乙醇水溶液,镍盐浓度为0.7 mol/L,尿素溶液的浓度为4.2 mol/L,表面活性剂为溶液总体积的1%。反应过程中将镍盐溶液和尿素溶液流速控制在0.5 mL/min,同时快速强烈搅拌,反应温度控制在80~90 ℃。在该条件下,可以得到电化学性能较好的α-Ni(OH)2样品。
图5所示为优化条件下制备的α-Ni(OH)2和β-Ni(OH)2样品电极的充放电曲线。前面的电化学性能测试过程中,电极的添加剂均为石墨粉,本实验还比较了电极中添加5%CoO时的充放电性能。从图中可以看出,采用石墨添加剂时,α-Ni(OH)2电极的最高放电容量为320 mA・h/g;但采用CoO为添加剂时,制备的α-Ni(OH)2电极的放电容量可达到390 mA・h/g。同时Al取代α-Ni(OH)2的充电电压比β-Ni(OH)2低 50 mV左右,而平均放电电压比β-Ni(OH)2高100 mV左右。
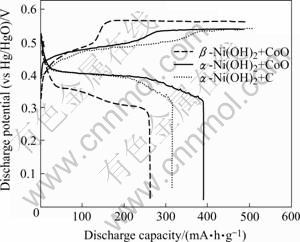
图5 Al取代的α-Ni(OH)2和实验室合成的β-Ni(OH)2样品的充放电曲线
Fig.5 Charge/discharge curves for Al-substituted α-Ni(OH)2 and β-Ni(OH)2 electrode
图6所示为Al取代α-Ni(OH)2及β-Ni(OH)2电极的循环曲线。从图6可以看出,循环初期,随着循环次数的增加,α-Ni(OH)2和β-Ni(OH)2电极的放电容量均逐渐增加,约10次左右达到高放电容量;随着循环次数的进一步增加,电极的放电容量逐渐降低,其中,β-Ni(OH)2电极的容量衰退速度明显比Al取代α-Ni(OH)2要快。经过100次循环,β-Ni(OH)2电极的容量衰退了76.4%,而Al取代α-Ni(OH)2电极衰退了10.5%,表明Al取代α-Ni(OH)2的循环性能明显优于β-Ni(OH)2。
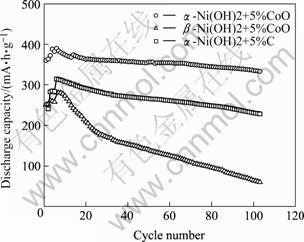
图6 Al取代α-Ni(OH)2和β-Ni(OH)2样品电极的循环性能
Fig.6 Cycling curves for Al-substituted α-Ni(OH)2 and β-Ni(OH)2 electrode (Charge/discharge current: 0.2C, charge time: 6 h, discharge cut-off potential: 0 V
本实验中合成的Al取代α-Ni(OH)2的理论容量约为487.4 mA・h/g,其中20%(摩尔分数)Ni被Al取代,因此其中Ni含量明显低于β-Ni(OH)2。在充放电反应过程中,如果β-Ni(OH)2的电子转移数假设为1,则Al取代α-Ni(OH)2的电子转移数为1.686 5。
图7所示为优化条件下制备的α-Ni(OH)2的循 环伏安曲线。如图所示,α-Ni(OH)2的Δφp为0.287 V,而β-Ni(OH)2的Δφp为0.498 6 V,这表明Al取代α-Ni(OH)2的可逆性比β-Ni(OH)2好,循环转变过程中α-Ni(OH)2的镍原子交换的电子要比β-Ni(OH)2中的多,也表明α-Ni(OH)2比β-Ni(OH)2有更高的放电容量。同时,α-Ni(OH)2的氧化和还原峰电流分别为 0.826 7 A和0.741 2 A,β-Ni(OH)2的氧化和还原峰电流分别为0.215 5 A和0.189 2 A,这表明α-Ni(OH)2具有更高的电化学活性。
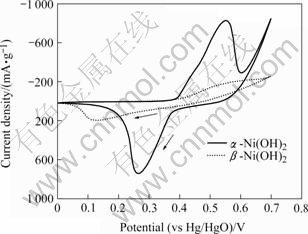
图7 优化条件下制备的α-Ni(OH)2样品的循环伏安曲线(扫描速度为0.1 mV/s)
Fig.7 Cyclic voltamagram of α-Ni(OH)2 sample synthesized under optimum conditions (scan rate: 0.1 mV/s)
2.3 XRD和SEM分析
图8所示为优化条件下制备的Al代α-Ni(OH)2样品的XRD衍射图,表明本研究合成的样品具有典型的α-Ni(OH)2结构,其(003)晶面的晶间距为0.789 38 nm,与文献[14]的数据一致。XRD谱上未发现Al的衍射峰,同时结合文献[15]中的研究结果,说明 Al以固溶态存在于α-Ni(OH)2的晶格中。图中曲线2所示为α-Ni(OH)2在6 mol/L KOH溶液中老化7 d后的XRD谱,与曲线1的特征峰基本一致,表明本实验制备的Al取代α-Ni(OH)2在强碱介质中能稳定存在。
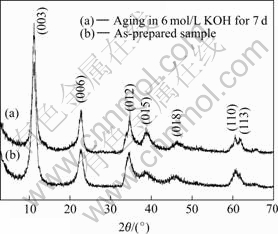
图8 优化条件下制备的α-Ni(OH)2样品的XRD图谱
Fig.8 XRD patterns for α-Ni(OH)2 sample synthesized under optimum conditions
图9所示为优化条件下合成的α-Ni(OH)2样品的SEM照片。如图所示,放大倍率较小时,α-Ni(OH)2呈不规则的类球形,颗粒有团聚的现象。高放大倍数下,样品表面微观结构呈特殊的片状,片与片之间相互交联,形成具有类蜂窝的结构,片厚度约为10~20 nm,微观结构比较特殊。文献[2-16]报道,一般的α-Ni(OH)2具有类球形或无定形结构,与本实验得到的片状结构微观形态差别甚大,初步分析可能是由于本实验合成α-Ni(OH)2时采用乙醇水溶液代替纯水溶液,同时在其中加入表面活性剂,改变了溶液的表面张力和溶质的溶解度,从而对α-Ni(OH)2的结晶过程产生影响,使α-Ni(OH)2的结晶过程产生明显的择优取向生长所致。
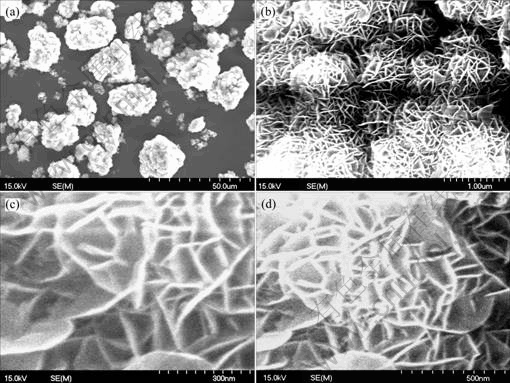
图9 优化条件下制备的α-Ni(OH)2样品的SEM像
Fig.9 SEM images for α-Ni(OH)2 sample synthesized under optimum conditions
由于制备的α-Ni(OH)2样品表面具有特殊的微观片状结构,这类结构与常规的球形或类球形结构相 比,质量相同时具有大得多的比表面积,因此其电化学反应活性和高倍率放电性能明显得到改善,这与循环伏安的研究结果一致。由于α-Ni(OH)2具有较大的比表面积,颗粒之间的导电性差,采用CoO作为导电剂时,在电极化成过程中会形成高效的导电网络,添加效果要好于石墨导电剂,因此不同添加剂对放电容量会造成显著的影响。
3 结论
1) 采用均匀沉淀法制备Al代α-Ni(OH)2时,表面活性剂、溶剂、镍盐浓度、pH值等因素对α-Ni(OH)2的电化学性能具有明显的影响,控制好各影响因素,可获得性能良好的α-Ni(OH)2。
2) 在合适的合成条件下,可以获得具有特殊表面片状结构的α-Ni(OH)2,片厚约为10~20 nm,采用CoO作为电极添加剂,其放电容量接近390 mA?h/g,充放电循环性能优良,经过100次循环后,容量保持率仍达到90%左右。与β-Ni(OH)2相比,充电电压低50 mV左右,平均放电电压高100 mV,具有良好的电化学性能。
3) 循环伏安研究表明,本研究合成的特殊片状结构α-Ni(OH)2电极具有很高的电化学活性,同时电化学可逆性良好。
REFERENCES
[1] Singh D. Characteristics and effects of γ-NiOOH on cell performance and a method to quantify it in nickel electrode[J]. J Electrochem Soc, 1998, 145(1): 116-119.
[2] Kamath P V, Dixit M, Indira M. Stabilized α-Ni(OH)2 as electrode material for alkaline secondary cells[J]. J Electrochem. Soc, 1994, 141(11): 2956-2959.
[3] Indira L, Dixit M, Kamath P V. Electrosynthesis of layered double hydroxides of nickel with trivalent cations[J]. J Power Sources, 1994, 52: 93.
[4] Kumar V G, Unichandraiah N M, Kamath P V. On the performance of stabilized α-nickel hydroxide as a nickel-positive electrode in alkaline storage batteries[J]. J Power Sources, 1995, 56: 111.
[5] Sugimoto A, Ishida S, Hanawa K. Preparation and characterization of Ni/Al-layered double hydroxide[J]. J Electrochem Soc, 1999, 146(4): 1251-1255.
[6] Zhao Y L, Wang J M, Chen H, Pan T, Zhang J Q, Cao C N. Different additives-substituted α-nickel hydroxide prepared by urea decomposition[J]. Electrochimica Acta, 2004, 50: 91-98.
[7] Liu B, Wang X Y, Yuan H T, Zhang Y S, Song D Y, Zhou Z X. Physical and electrochemical characteristics of aluminum (Ⅰ): Substituted nickel hydroxide [J]. J Appl Electrochem, 1999, 29(7): 855-860.
[8] Ezhov B B, Malandin O G. Structure modification and change of electrochemical activity of nickel hydroxides [J]. J Electrochem Soc, 1991, 138(4): 885-889.
[9] Dixit M, Kamath P V, Gopalakrishnan J. Zinc-substituted α-nickel hydroxide as an electrode material for alkaline secondary cells[J]. J Electrochem Soc, 1999, 146(1): 79-82.
[10] Demourgues-Guerlou L, Delmas C. Structure and properties of precipitated nickel-iron hydroxides[J]. J Power Sources, 1993, 45: 281-289.
[11] Demourgues-Guerlou L, Delmas C. Effect of iron on the electrochemical properties of the nickel hydroxide electrode[J]. J Electrochem Soc, 1994, 141(3): 713-717.
[12] Demourgues-Guerlou L, Delmas C. Electrochemical behavior of the manganese-substituted nickel hydroxides[J]. J Electrochem Soc, 1996, 143(2): 561-566.
[13] Audemer A, Delahaye A, Farhi R, Sac-Epee N, Tarascon M. Electrochemical and raman studies of beta-type nickel hydroxides Ni1-xCox(OH)2 electrode materials[J]. J Electrochem Soc, 1997, 144(8): 2614-2620.
[14] 姜长印,万春荣,张泉荣,章金基. 高密度高活性球形氢氧化镍的制备与性能控制[J]. 电源技术,1997, 21(6): 243-247.
JIANG Chang-yin, WAN Chun-rong, ZHANG Quan-rong, ZHANG Jing-ji. Preparation of the high-density, high-activity, and spherical nickel hydroxide and its performance control[J]. Chinese Journal of Power Sources, 1997, 21(6): 243-247.
[15] 肖慧明,王建明,陈 惠,潘 滔,张鉴清. Al取代α-Ni(OH)2的有机溶剂法合成及其电化学性能[J]. 功能材料,2003, 34(5): 553-555.
XIAO Hui-ming, WANG Jian-ming, CHEN Hui, PAN Tiao, ZHANG Jian-qing. Structure and electrochemical performancec of Al and Zn co-substituted α-Ni(OH)2[J]. Functional Materials, 2003, 34(5): 553-555.
[16] 陈昌国,文 莉,余丹梅. 制备工艺条件对Ni(OH)2粒度和电化学性能的影响[J]. 电源技术,2004, 28(9): 558-561.
CHEN Chang-guo, WEN Li, YU Dan-mei. Effect of preparing conditions on granularity and electrochemical performance of Ni(OH)2[J]. Chinese Journal of Power Sources, 2004, 28(9): 558-561.
基金项目:国家高技术研究发展计划资助项目(2003AA302420)
收稿日期:2005-10-08;修订日期:2006-07-26
通讯作者:张文魁, 博士, 教授; 电话: 0571-88320394; E-mail: echem@zjut.edu.cn
(编辑 龙怀中)