酸性矿山废水中锌铁锰的分离及回收
郑雅杰1, 2,彭映林1, 2,乐红春1,李长虹2
(1. 中南大学 冶金科学与工程学院,湖南 长沙,410083;
2. 中南大学 云浮研究院,广东 云浮,527300)
摘要:采用机械活化硫精矿吸附,氧化沉淀以及氢氧化钠沉淀处理酸性矿山废水,使废水中锌、铁、锰得到分离与回收。当酸性矿山废水pH为1.83,锌、铁和锰质量浓度分别为150,2 900和315 mg/L时,在10 L酸性矿山废水中加入活化硫精矿975 g,反应20 min后,锌残留质量浓度为1.33 mg/L,锌去除率达到99.08%。废水经除锌后,取10 L废水,当废水pH为6.92,空气流量为500 mL/min,反应时间为2.5 h时,铁和锰残留质量浓度分别为97.96和290.55 mg/L,铁、锰去除率分别为98.28%和18.45%。XRD分析表明:氧化沉淀渣为Fe3O4和α-FeOOH,渣中铁含量为52.73%;废水经除铁后用氢氧化钠溶液调节pH至11.01,反应时间为30 min时,废水中锰残留质量浓度为1.15 mg/L,所得锰渣锰含量达到34.47%;除锰废水经硫酸调节pH为7后达GB 8978―1996排放标准。
关键词:酸性矿山废水;硫精矿;锌;铁;锰
中图分类号:X703.1 文献标志码:A 文章编号:1672-7207(2011)07-1858-07
Separation and recovery of Zn, Fe and Mn in acid mine drainage
ZHENG Ya-jie1, 2, PENG Ying-lin1, 2, LE Hong-chun1, LI Chang-hong2
(1. School of Metallurgical Science and Engineering, Central South University, Changsha 410083, China;
2. Yunfu institute, Central South University, Yunfu 527300, China)
Abstract: Separation and recovery of Zn, Fe and Mn from acid mine drainage was researched by applying absorption with mechanically activated pyrite, oxidation-precipitation and sodium hydroxide neutralization. The mass concentration of residual Zn is 1.33 mg/L, and the removal rate of Zn is up to 99.08% when pH of the acid mine drainage is 1.83, the mass concentrations of Zn, total iron and Mn are 150, 2 900 and 315 mg/L, respectively, the dosage of activated pyrite is 975 g in 10 L wastewater, reaction time is 20 min. In 10 L wastewater after removing Zn, the residual Fe and Mn are 97.96 mg/L and 290.55 mg/L, respectively, and the removal rates of Fe and Mn are 98.28% and 18.45%, respectively when pH of the wastewater is 6.92, airflow is 500 mL/min, reaction time is 2.5 h. X-ray diffraction (XRD) analysis shows that the products of oxidation-precipitation are Fe3O4 and α-FeOOH, in which the content of Fe is 52.73%. Then the residual Mn is 1.15 mg/L, and the Mn content in the sediment is 34.47% when pH of the wastewater is adjusted to about 11.01 with sodium hydroxide solution, and reaction time is 30 min. The effluent quality can meet the Chinese standards of wastewater discharge (GB 8978―1996) after pH of the Mn removing wastewater is adjusted to 7 with sulfuric acid.
Key words: acid mine drainage; pyrite; Zn; Fe; Mn
天然硫铁矿在细菌及氧气作用下被氧化而产生酸性矿山废水,酸性矿山废水水量大,pH低,含铁高,且含有多种重金属离子,其中多数重金属离子的含量超过了废水的排放标准,如果直接排放,将对水体产生严重污染,破坏生态环境,危害人类健康[1-3]。据报道处理这类废水的主要方法有中和沉淀法[4]、铁氧体沉淀法[5]、吸附法[6]、湿地法[7]、微生物法[8]等。采用微生物法处理由于成本高、反应条件苛刻,难以得到推广应用。湿地法占用面积大,处理周期长,废水中有用金属得不到回收。吸附法能有效处理重金属废水,但再生时,又产生新污染物。铁氧体沉淀法因采用氢氧化钠,其成本高及金属得不到分离而未推广使用。中和沉淀法因效果稳定、运行成本低在工业上得到广泛应用。但是,上述方法均不能使废水中金属离子得到分离及回收。国内外的研究已表明,天然铁的硫化物对重金属具有良好的吸附性能和沉淀作用[9-10],矿物经机械活化后能使反应活性显著提高[11-12],改善矿物吸附性能。本文作者采用机械活化硫精矿吸附除锌、氧化沉淀法去除铁及氢氧化钠沉淀锰[13],使酸性矿山废水中锌、铁、锰得到分离与回收,从而有利于实现酸性矿山废水资源化。
1 实验
1.1 实验步骤及工艺流程
1.1.1 硫精矿的机械活化
在滚动球磨罐中加入250 g硫精矿,自来水500 mL,9个直径为2 cm,65个直径为1.5 cm和230个直径为1 cm的钢球2 kg,将硫精矿机械球磨4 h后过滤,滤渣保存在干燥器中备用。硫精矿主要成分(质量分数)如表1所示。硫精矿活化前后粒度和比表面积变化如表2所示。
表1 硫精矿主要成分
Table 1 Main composition of pyrite %

表2 硫精矿活化前后粒度和比表面积
Table 2 Size and surface area of pyrite and activated pyrite

1.1.2 机械活化硫精矿对废水中锌的去除
取500 mL某酸性矿山废水于烧杯中,启动搅拌,加入质量分数为20%的氢氧化钠溶液,调节pH至一定值后加入硫精矿或活化硫精矿,反应一定时间后过滤。实验所用酸性矿山废水水质如表3所示。
表3 酸性矿山废水水质
Table 3 Quality of acid mine drainage
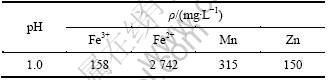
1.1.3 氧化沉淀法去铁
取500 mL经硫精矿吸附除锌后废水于三颈烧瓶中,启动搅拌,通入空气,加入氢氧化钠溶液调节终点pH,反应一定时间并静置1 h后过滤,在60 ℃下烘干滤渣。
1.1.4 氢氧化钠沉淀锰
在除铁废水中加入氢氧化钠溶液调节pH至一定值,反应30 min后过滤得到锰渣。
根据实验步骤,其工艺流程图如图1所示。
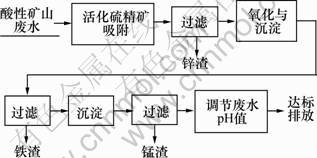
图1 酸性矿山废水中锌铁锰分离及回收工艺流程
Fig.1 Process of separation and recovery of Zn, Fe and Mn in acid mine drainage
1.2 分析与检测
用火焰型原子吸收光谱仪(TAS-990)测定总铁(TFe)、锰和锌质量浓度,用重铬酸钾法测定亚铁质量浓度,用X荧光分析(XRF)仪(菲利浦24)分析沉渣成分,用X衍射(XRD)仪(日本理学,Cu Kα,50 kV,300 mA)分析滤渣物相,采用纳米粒度激光衍射仪(Nano-ZS)对粒度进行分析,采用ASAP2010 V4.02 E比表面积测定仪(Metallurgy公司,N2,77.51 K)对比表面积进行分析。
2 结果与讨论
2.1 机械活化硫精矿对废水中锌的去除
2.1.1 活化硫精矿用量对废水中锌去除率的影响
实验取500 mL废水进行处理,当废水pH为1.0,反应时间为1.5 h时,活化硫精矿用量对废水中锌去除率和废水终点pH的影响如图2所示。
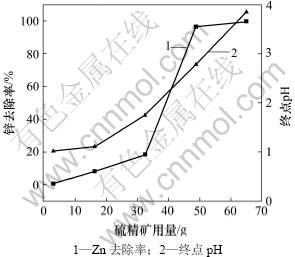
图2 活化硫精矿用量对废水中锌去除率和废水终点pH的影响
Fig.2 Effect of activated pyrite dosage on removal rate of Zn and final pH in wastewater
由图2可知:锌去除率、终点pH随活化硫精矿用量的增加而增加;当活化硫精矿用量从3.25 g增加到65 g时,锌去除率从0.8%增加到99.85%,终点pH从1.02升高到3.85;当活化硫精矿用量为48.75 g时,锌去除率增加显著,其去除率为96.35%。
上述条件下,将未活化硫精矿和活化硫精矿进行对比,用量均为65 g时,处理后废水水质如表4所示。
表4 未活化硫精矿和活化硫精矿处理废水水质
Table 4 Wastewater quality after treating by unactivated pyrite and activated pyrite mg/L
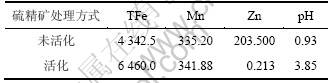
由表4可见:(1) 硫精矿经过活化,能够有效去除废水中Zn2+;(2) 根据废水中铁质量浓度增加量 可知活化硫精矿溶解量大于未活化硫精矿的溶解量;(3) 活化硫精矿溶于废水后pH高于未活化硫精矿的pH,在500 mL废水中加入65 g活化硫精矿,终点pH为3.85,而加入未活化硫精矿时,pH下降为0.93。从而可以判断:废水中Zn2+的去除不仅在于活化硫精矿,pH也是影响Zn2+去除的一个重要因素。
在废水中,硫精矿酸性溶解,发生如下反应[14-15]:
4FeS2(S)+6H++4H2O 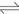 7H2S+SO42-+4Fe2+
7H2S+SO42-+4Fe2+
FeS2(S)+2H+ 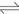 H2S+S+Fe2+
H2S+S+Fe2+
H2S 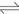 H++HS-
H++HS-
HS- 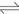 H++S2-
H++S2-
由表2可知:硫精矿经机械活化后,粒度变小,比表面积增大。活化硫精矿溶解量大[16],产生H2S多,且活化硫精矿溶解后pH增加,废水中S2-质量浓度增加,更易于ZnS生成,ZnS生成后被活化硫精矿吸附,使废水中Zn2+得到去除。
机械活化时,硫精矿发生氧化反应,产生Fe2(SO4)3,FeOOH和H2SO4等物质[17],经过过滤,Fe2(SO4)3和H2SO4进入溶液,FeOOH进入活化硫精矿,活化硫精矿加入废水后,FeOOH与废水中H+作用,导致pH增加,有利于废水中S2-的形成,从而增加Zn2+去除效果。活化硫精矿量越大,废水终点pH越高,越有利于Zn2+的去除。
ZnS溶于pH为1的酸性溶液[18],从实验结果判断,在废水中加入未活化硫精矿,硫精矿发生氧化溶解[2],产生H2SO4,pH下降为0.93,铁锰锌离子质量浓度均增加。
2.1.2 pH对废水中锌去除率的影响
上述其他条件不变,当活化硫精矿用量为48.75 g时,废水初始pH对废水中锌去除率和终点pH的影响如图3所示。
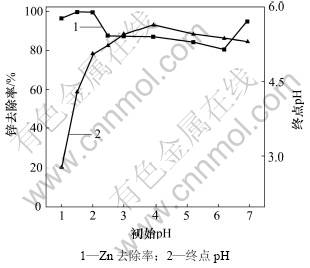
图3 初始pH对废水中锌去除率和废水终点pH的影响
Fig.3 Effect of initial pH on removal rate of Zn and final pH in wastewater
由图3可知:当废水初始pH从1.0增加到2.0时,Zn去除率均在96.44%以上;当废水初始pH从2.0增加到6.19时,Zn去除率有所下降;当废水初始pH从6.19升高到6.94时,锌去除率从80.38%增加到94.84%;当废水初始pH从1.0升高到3.92时,终点pH从2.79升高到5.63;当初始pH从3.92升高到6.94时,终点pH从5.63缓慢下降至5.30。
废水pH对活化硫精矿去除锌影响较大。当pH较低时,活化硫精矿溶解量大,H2S质量浓度增加,有利于去除Zn2+,随着pH的增加,活化硫精矿溶解量减少,废水中H2S质量浓度降低,锌的去除率下 降,当pH达到6.94时,废水中OH-质量浓度增 加,使Zn去除率增加,由于Fe2+氧化生成Fe3+,Fe3+发生水解, Zn,Mn和Fe产生共沉淀作用,同时废水终点pH下降。
2.1.3 反应时间对废水中锌去除率的影响
上述其他条件不变,当废水pH为2时,反应时间对废水中锌去除率和终点pH的影响如图4所示。
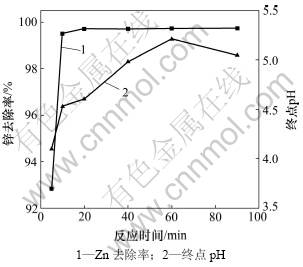
图4 反应时间对废水中锌去除率和终点pH的影响
Fig.4 Effects of reaction time on removal rate of Zn and final pH in wastewater
由图4可知:当反应时间从5 min延长至20 min时,锌去除率从92.83%增加到99.7%,继续延长反应时间,锌去除率基本不变。
反应时间对Zn去除率影响表明活化硫精矿去除锌速度快,说明了Zn2+与S2-反应机理,也说明ZnS易被活化硫精矿(FeS2)吸附。
当反应时间从5 min到60 min时,废水终点pH随着反应时间增加而增加,说明该过程是活化硫精矿中FeOOH与H+作用;当反应时间为90 min时,FeS2发生氧化溶解,导致pH下降。
根据上述适宜条件,取10 L酸性矿山废水进行放大实验,当废水pH为1.83,活化硫精矿为975 g,反应时间为20 min时,处理后废水水质如表5所示。
由表5可知:经活化硫精矿处理后,废水中残留锌质量浓度仅为0.720 mg/L,锌去除率达到99.44%。
表5 活化硫精矿除锌后废水水质
Table 5 Wastewater quality after removing Zn by activated pyrite

2.2 氧化沉淀法去铁
2.2.1 废水pH对铁锰去除率的影响
取经活化硫精矿处理后废水500 mL于三颈烧瓶中,启动搅拌,加入氢氧化钠溶液调节pH,通入空气,其流量为35 mL/min,反应时间为20 min,废水pH对铁锰去除率的影响如图5所示。
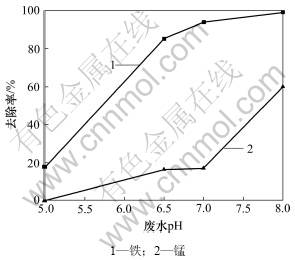
图5 废水pH对铁和锰去除率的影响
Fig.5 Effect of pH on removal rates of TFe and Mn
由图5可知:铁和锰去除率均随pH的升高而增加;当废水pH从5.0增加到8.0时,铁去除率从17.95%增加到98.97%,锰去除率从0.27%增加到60.55%;当反应pH为7.0时,铁的去除率为93.64%,锰的去除率仅为17.28%,为减少锰沉淀,反应pH应控制在6.5~7.0之间。
2.2.2 空气流量对铁锰去除率的影响
上述其他条件不变,当废水pH为7时,空气流量对铁锰去除率的影响如图6所示,所得氧化沉淀干渣XRD谱如图7所示。
由图6可知:当废水为500 mL时,空气流量对铁锰去除率无影响。由图7可知:沉淀产物有α-FeOOH,Fe3O4和γ-FeOOH。
在酸性矿山废水中加入NaOH,通入氧气时,发生如下反应[19-20]:
Fe2++2OH-=Fe(OH)2?
2Fe(OH)2+1/2O2+H2O=2Fe(OH)3↓
Fe(OH)2+2Fe(OH)3=Fe3O4+4H2O
4Fe(OH)2+O2=4α-FeOOH+2H2O
4Fe(OH)2+O2=4γ-FeOOH+2H2O
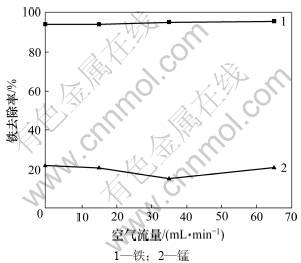
图6 空气流量对铁和锰去除率的影响
Fig.6 Effects of airflow on removal rates of Fe and Mn
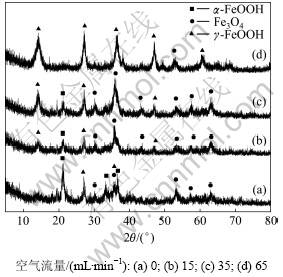
图7 干渣XRD谱
Fig.7 XRD patterns of dried sediments
因此,氧化沉淀产物中有Fe3O4,α-FeOOH和γ-FeOOH,但是主要产物为Fe3O4。
Kiyama[21]研究表明:氧气量增加时,有利于Fe(OH)2快速转化为γ-FeOOH,而不利于Fe3O4的生成。由图7可见:当空气流量为65 mL/min时,γ-FeOOH衍射峰增强。
实验表明:氧化沉淀除铁适宜条件是废水pH为6.5~7.0,1 L废水中空气流量为30~70 mL/min。取 10 L除锌后废水进行放大实验,废水pH为6.92,由于废水量增加,空气流量增加为500 mL/min,延长反应时间至2.5 h,经除铁后废水水质如表6所示。
表6 除锌沉铁后废水水质
Table 6 Wastewater quality after removing Zn and Fe

2.3 氢氧化钠沉淀锰
取沉铁后废水500 mL,pH对废水中锰去除率和终点pH的影响如图8所示。
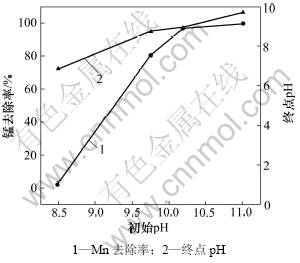
图8 初始pH对废水中锰去除率和终点pH的影响
Fig.8 Effect of initial pH on removal rate of Mn and final pH in wastewater
从图8可以看出:锰去除率随初始pH的升高而升高,终点pH增加幅度不大。当初始pH为11.01时,废水中锰残留质量浓度为1.474 mg/L,总锰质量浓度小于2.000 mg/L,达到国家废水综合排放标准(GB 8978―1996)。
根据上述适宜工艺条件,另取10 L酸性矿山废水进行除锌、除铁及沉锰验证实验,各阶段处理后废水水质如表7所示,除锌渣、铁渣、锰渣化学成分(质量分数)见表8,60 ℃烘干后铁渣和锰渣XRD谱如图9所示。
表7 处理后废水水质
Table 7 Wastewater quality after being treated

表8 锌渣、铁渣和锰渣化学成分
Table 8 Components of Zn, iron and Mn sediments %
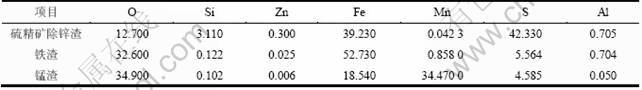
图9 铁渣和锰渣XRD谱
Fig.9 XRD patterns of iron sediment and Mn sediment
由表7结果计算可知:废水经活化硫精矿除锌后,锌去除率达到99.08%,除锌废水经氧化沉淀法回收铁后,铁和锰去除率分别为98.28%和18.45%,除锰废水经氢氧化钠沉淀锰后,锰去除率为99.6%。废水经除锌,除铁及沉锰后,废水中锌、铁和锰质量浓度分别为0,0,1.15 mg/L,锌、铁和锰总的去除率分别为100%,100%和99.63%。处理后废水加硫酸调节pH为7达标排放(GB 8978―1996)。
由表8可知:废水经活化硫精矿除锌后,硫精矿中锌含量由0.115%提高到0.300%,锌被活化硫精矿吸附,吸附锌后硫精矿经过干燥用沸腾炉焙烧制备硫酸。铁渣中铁含量达到52.730%,总铁含量大于50%,达到铁矿石标准(GB/T 13728―92)。锰渣中锰含量为34.470%,锰含量大于25.000%,达到锰矿石B2标准(YB/T 319―1997)。
由图9可知:放大实验铁渣物相为Fe3O4和α-FeOOH。锰渣物相为Mn3O4,Fe2O3和Mn2O3。
3 结论
(1) 未活化硫精矿加入酸性矿山废水中时,废水中锌、铁和锰质量浓度分别由150,2 900和315 mg/L增加到203.5,4 342.5和335.2 mg/L。
(2) 采用活化硫精矿吸附除锌时,锌去除率随着硫精矿用量的增加而增加,随着pH的升高先增加后降低。当废水pH为1.83,10 L废水中硫精矿用量为975 g,反应时间为20 min时,锌残留质量浓度为1.33 mg/L。
(3) 采用氧化沉淀法回收铁时,铁锰去除率随着pH的升高而增加。实验取除锌后废水10 L,当废水pH为6.92,空气流量为500 mL/min,反应时间为 2.5 h时,废水中铁、锰残留质量浓度分别为97.96和290.55 mg/L。
(4) 氢氧化钠沉淀锰时,铁和锰去除率随着初始pH的升高而升高,当初始pH为11.01,反应时间为30 min时,废水中锰质量浓度为1.15 mg/L。
(5) 酸性矿山废水经机械活化硫精矿吸附除锌,氧化沉淀回收铁及氢氧化钠沉淀锰后,锌、铁和锰的去除率分别为100%,100%和99.63%。硫精矿中锌含量由0.115%提高到0.3%,铁渣中铁含量为52.73%,锰渣中锰含量为34.47%。铁渣主要物相为Fe3O4和α-FeOOH,锰渣主要物相为Mn3O4,Fe2O3和Mn2O3。
参考文献:
[1] 罗凯, 张建国. 矿山酸性废水治理研究现状[J]. 资源环境与工程, 2005, 19(1): 45-48.
LUO Kai,ZHANG Jian-guo. Status quo of the disposal of acidic mining wastewater[J]. Resources Environment & Engineering, 2005, 19(1): 45-48.
[2] Akcil A, Koldas S. Acid mine drainage (AMD): Causes, treatment and case studies[J]. Journal of Cleaner Production, 2006, 14(12/13): 1139-1145.
[3] 饶运章, 徐水太, 张见. 含硫矿山酸性废水及其金属离子污染防治方法的探讨[J]. 中国钨业, 2004, 19(4): 33-35.
RAO Yun-zhang, XU Shui-tai, ZHANG Jian. Study on the methods of prevention and cure of acid waste water and metal ion pollution in sulfurous mine[J]. China Tungsten Industry, 2004, 19(4): 33-35.
[4] 李学金, 钱显文, 郑乐平, 等. 某铁矿尾矿库酸性废水处理试验研究[J]. 金属矿山, 2006(9): 73-77.
LI Xue-jin, QIAN Xian-wen, ZHENG Le-ping, et al. Test research on treating acid mine drainage of tailings reservoir in an iron mine[J]. Metal Mine, 2006(9): 73-77.
[5] 赵如金, 王卫星. 常温铁氧体法处理酸性矿山废水的添加剂研究[J]. 金属矿山, 2002(增刊): 280-282.
ZHAO Ru-jin, WANG Wei-xing. Study on the additive used in treating acid mine drainage by ambient temperature ferrite process[J]. Metal Mine, 2002(S): 280-282.
[6] Mohanan D, Chander S. Removal and recovery of metal ions from acid mine drainage using lignite: A low cost sorbent[J]. Journal of Hazardous Materials, 2006, 137(3): 1545-1553.
[7] Whitehead P G, Cosby B J, Prior H. The Wheal Jane wetlands model for bioremediation of acid mine drainage[J]. Science of the Total Environment, 2005, 338(1/2): 125-135.
[8] 万由令, 李龙海. 玉米芯为碳源实现酸性矿山废水生物处理[J]. 工业安全与环保, 2004, 30(5): 11-15.
WAN You-ling, LI Long-hai. Biological treatment for acid mine drainage by using corncob as carbon source[J]. Industrial Safety and Environment Protection, 2004, 30(5): 11-15.
[9] 陈永亨, 张平, 梁敏华, 等. 黄铁矿对重金属的环境净化属性探讨[J]. 广州大学学报: 自然科学版, 2007, 6(4): 23-25.
CHEN Yong-heng, ZHANG Ping, LIANG Min-hua, et al. Research on cleaning characteristic of pyrite[J]. Journal of Guangzhou University: Natural Science Edition, 2007, 6(4): 23-25.
[10] Borah D, Senapati K. Adsorption of Cd(Ⅱ) from aqueous solution onto pyrite[J]. Fuel, 2006, 85: 1929-1934.
[11] 郑雅杰, 龚竹青, 易丹青, 等. 以硫铁矿烧渣为原料制备绿矾新技术[J]. 化学工程, 2005, 33(4): 51-55.
ZHENG Ya-jie, GONG Zhu-qing, YI Dan-qing, et al. New technology of copperas preparation from pyrite cinders[J]. Chemical Engineering, 2005, 33(4): 51-55.
[12] 邹俭鹏, 尹周澜, 陈启元, 等. 机械活化黄铁矿物理性能和表面结构变化的表征[J]. 湖南有色金属, 2001, 17(5): 36-39.
ZOU Jian-peng, YIN Zhou-lan, CHRN Qi-yuan, et al. Characterization of physical properties and surfacial structure of activated pyrite[J]. Hunan Nonferrous Metals, 2001, 17(5): 36-39.
[13] 郑雅杰, 彭映林, 乐红春, 等. 酸性矿山废水中锌铁锰分离及回收的方法: 中国, 200910044501.9[P]. 2009-10-09.
ZHENG Ya-jie, PENG Ying-lin, LE Hong-chun, et al. A method of separation and recovery of Zn, Fe and Mn in acid mine drainage: CN, 200910044501.9[P]. 2009-10-09.
[14] Bower J, Savage K S, Weinman B, et al. Immobilization of mercury by pyrite(FeS2)[J]. Environmental Pollution, 2008, 156(2): 504-514.
[15] Hector M, Lizama, Suzuki I. Rate equations and kinetic parameters of the reactions involved in pyrite oxidation by Thiobacillus ferrooxidans[J]. Applied and Environmental Microbiology, 1989, 55(11): 2918-2923.
[16] 傅崇说. 有色冶金原理[M]. 北京: 冶金工业出版社, 1993: 179-180.
FU Chong-shuo. Principle of non-ferrous metallurgy[M]. Beijing: Metallurgy Industry Press, 1993: 179-180.
[17] 刘书杰, 何发钰. 磨矿环境对黄铁矿矿浆化学性质及浮选行为影响的研究[J]. 矿冶, 2008, 17(4): 6-10.
LIU Shu-jie, HE Fa-yu. Research on effect of grinding environment on pulp property and flotation behavior of pyrite [J]. Mining & Metallurgy, 2008, 17(4): 6-10.
[18] 北京师范大学化学系无机化学教研室. 简明化学手册[M]. 北京: 北京出版社, 1980: 202.
Inorganic Chemistry Staff Room, Department of Chemistry, Beijing Normal University. Concise handbook of chemistry[M]. Beijing: Beijing Press, 1980: 202.
[19] YANG Xi-yun, GONG Zhu-qing, LIU Feng-liang. Kinetics of Fe3O4 formation by air oxidation[J]. Journal of Central South University of Technology, 2004, 11(2): 152-155.
[20] 张首才, 张金晶, 左青卉. 利用废铁屑制备氧化铁黑的研究[J]. 吉林师范大学学报: 自然科学版, 2004(1): 70-71.
ZHANG Shou-cai, ZHANG Jin-jing, ZUO Qing-hui. The preparation of iron black oxid by iron scrat[J]. Journal of Jilin Normal University: Natural Science Edition, 2004(1): 70-71.
[21] Kiyama M. Conditions for the formation of Fe3O4 by the air oxidation of Fe(OH)2 suspensions[J]. Bulletion of the Chemical Society of Japan, 1974, 47(7): 1646-1650.
(编辑 陈爱华)
收稿日期:2010-07-20;修回日期:2010-09-02
基金项目: 广东省教育部产学研重大项目(2008A090300016)
通信作者:郑雅杰(1959-),男,湖南常德人,教授,博士生导师,从事冶金资源综合利用及水污染控制研究;电话:0731-88836285;E-mail: zzyyjj01@yahoo.com.cn