���±�ţ�1004-0609(2007)09-1465-05
�ɽ���þֲ����ϱ���Ϳ����Ʊ���������
�ƾ���1, 2��������1���ű���1���� ��1
(1. �й���ѧԺ �����о��������� 110016;
2. �й���ѧԺ �о���Ժ������ 100864)
ժ Ҫ�����ý�Ϳ���Ʊ�Mgֲ����ϱ��������Ϳ�㣬ͨ��ѡ��ͬ��Է��������ľ����Ტ���ù���ż������Mgֲ����ϱ������Ԥ���������Mgֲ������������Ľ����������ɨ��羵�ó���Ϳʱ�䡢�ۺ���Ũ�ȼ���Ϳ������Ϳ���ȵ�Ӱ�졣����Mgֲ����ϱ���Ϳ����Է�������Ϊ20��ľ�(����?�ǻ�����)�ܹ����㽵�������ͽ������Ҫ����������洦����������Hank��s ��Һ�н���10 d��������������ʧ�����ֱ��洦���������������ʧ���Խ��͡�ʵ�������þ����Ϳ��������Ϳ�㣬������Ч�������ģ����Һ�е���ʴ�ԡ�
�ؼ��ʣ���Ϳ��Mgֲ����ϣ����������ʴ��
��ͼ����ţ�R318.08���� ���ױ�ʶ�룺A
Preparation and property of coating on degradable Mg implant
HUANG Jing-jing1, 2, REN Yi-bin1, ZHANG Bing-chun1, YANG Ke1
(1. Institute of Metal Research, Chinese Academy of Sciences, Shenyang 110016, China;
2. Graduate School of Chinese Academy of Sciences, Beijing 100864, China)
Abstract: To be an implant material, it is necessary to have good corrosion resistance for magnesium and magnesium alloy in the period of tissue healing process. To improve corrosion resistance of pure magnesium, dipping technology was employed in the present work to prepare the poly (lactic acid) coating on Mg implant. Different molecular mass poly (lactic acid) and a surface pretreatment technology applying silane coupling agents on Mg implant was used to improve adhesion strength between Mg implant and poly lactic acid. Scanning electron microscopy (SEM) was used to gain the effect of dipping time, polymer concentration and dipping times for the thickness of coating. The results show that poly (DL-lactide-co-glycolide) (PLGA) with relative molecular mass of 200 thousand can meet the need of degradation condition and strength adhesion of biodegradable implant. The mass loss of PLGA film coated Mg implant is decreased obviously after they are immersed in Hank��s solution. It can be concluded that PLGA coating can effectively protect magnesium from corrosion in simulation biology solution.
Key words: dipping technology; Mg implant; adhesion strength; corrosion resistant
þ��þ�Ͻ���Ϊ����ֲ�������Խ��Խ�ܵ����ǵ����ӣ���Ϊ���������ٴ�ʹ�õ�ֲ�������Ⱦ�������ͻ�����ŵ�[1?2]�����Ҵ������о����֣�þ�����յ�������������[3?5]��
�������������Cl?�ĸ�ʴ�����У�þ��þ�Ͻ���ܻ���Ϊ�������ʽϿ����ǰʧЧ��ͨ����ʱֲ������Ҫ��3���µ�1 a�ķ���ʱ�䣬�������þ��þ�Ͻ���Ϊֲ����Ͻ�������Ӧ������0.1 mm/a�ڣ�����ʵ����ǰ���о����ִ�þ��ģ����Һ�ڵĽ�������Ϊ0.2~1.0 mm/a[6]�������ڶ���ʵ����Ҳ���ִ�þ��δ�������½���Ͽ죬��˿��ܻ��ڷ���ʱ����ʧЧ�����Ա������ƻ�ͨ������Ϳ��ķ�������Сþֲ�����ں�Ľ������ʡ��й�þ��þ�Ͻ����Ϳ����Ʊ������ܶ࣬����þ��Ϊ�ɽ���ֲ����ϣ���Ϳ����뱣֤���ԡ����õ����������ԣ��Լ��ɽ����ԣ�������������б��洦��������þ�Ͻ���Ϊֲ������ϵ�Ӧ�á���������ͨ�����ȴ�������Ч�����˴�þ����ʴ�ԣ���֤�����Ժ��þû�ж�С�����ϸ������ֳ�������ԵĶ�������[7]��������þ��Ϊ�������������һ���²��ϣ���������ѧ���ܣ�������þ����������֯�ij������������Ի�δ������������ѡ��һ�����������ԺõIJ�����Ϊ������Ϳ������о�ǰ������������ѡ�þ�������Ϊþֲ����ϵı���Ϳ�㣬���ý�Ϳ������þֲ����ϵķ����㡣
1��ʵ��
ʵ�����Ϊ����̬��þ������Ϊ99.95%������Fe��0.003%��Ni��0.0002%��Cu��0.0010%��Si��0.029%��Ϳ���еľۺ���ֱ�����Է�������Ϊ8��20���50��ľ�����PLLA�Լ���Է�������Ϊ20��ľ�(����-�ǻ�����)������PLGA�����Ǿ������õ�ѪҺ�����ԣ��ѱ�����ҩ��������塢�����������ߡ��ǿ��ڹ̶����ҽ����е��Ϳ����ʹ��KH?550����ż�������ܼ�Ϊ���ȼ��顣
ʵ����Ͼ�ɰֽ��ĥ��1200#�������ñ�ͪ������ϴ���г��ȥ�ۣ�Ȼ��ʵ�����������ˮ�г���һ��ʱ�䣬���ý�Ϳ���Ʊ�����Ϳ�㣬����ż�������Ʊ���״̬��
�ۺ�������������ճ��ǿ�ȸ���GB7124�� 1986���в��ԣ���������ʵ���ΪZwick/Roell Z050�����������������������Ϊ0.5 mm/min����S?3400Nɨ��羵�¹۲�ʵ������ڲ�ͬ�����µ�Ϳ���ȡ�����δ���κδ����Ĵ�þ��������Ʒ��PLGAͿ������Ʒ�ֱ���Hank��s��Һ�н���10 d��������Һ������(37��0.5) �档Hank��s�˹�ģ����Һ[8]�����Ϊ��NaCl 8.0 g+KCl 0.4 g+CaCl2 0.14 g+NaHCO3 0.35 g+C6H12O6 (������)1.0 g+MgCl2?6H2O 0.1 g+MgSO4?7HO 0.06 g +KH2PO4 0.06 g+Na2HPO4?12H2O 0.06 g+1 L H2O����HCl��NaOH��Һ����pHΪ7.5�����û�ѧ�Լ�ȫ��Ϊ������������ʵ�������ȡ����Ʒ��������������������ʧ��
2�����������
����ֲ�������IJ��ϱ��뱣ֲ֤���������ֲ��λ����Χ��֯�����õ�������[9?10]�������Ʋ�������������Ч�İ취�����ڱ���Ϳ��һ����֪�������������õIJ���[11]�������������ٴ��㷺Ӧ�ã������õ����������ԣ�����þ�Ͻ���Ϊ�����ɽ���֧�ܵIJ���ʱ[12]�����������Ϊþ�Ͻ�֧�ܵĴ�ҩ���壬�Ӷ�����ҩ���ͷ��ٶȡ�
2.1��Ϳ��ͻ���Ľ����
ͼ1��ʾΪ����Ϳ����ͬ��Է���������������ɨ��羵�ɿ�����Է�������Ϊ50���PLLA����Է�������Ϊ20���PLGAͿ����þ����dz�ƽ�����ܡ�����������˷���������ã�ͬʱ��С��þ�ı���ֲڶȣ�������þ����ѪҺ�Ӵ�ʱ������Ѫ�Ŀ����ԣ�Ϊ����Ϊ�ɽ���֧�ܲ��ϵ��о��ṩ�����ݡ�

ͼ1 ��ͬ��Է���������PLLA��PLGAͿ��þ�����ɨ��羵��
Fig.1 SEM images of 80 thousand(a), 200 thousand(b), 500 thousand(c) relative molecular mass of PLLA and 200 thousand relative molecular mass of PLGA surface treated Mg(d)
þ����Ϳ����ͬ��Է����������������������ͼ2��ʾ�����ھ�����PLLA����Է�������ԽС����������þ������Խ�á�Ϳ��Խ��������(����-�ǻ�����)PLGA��Ȼ��Է��������ϴ���þ���Ҳ�Ϻá�
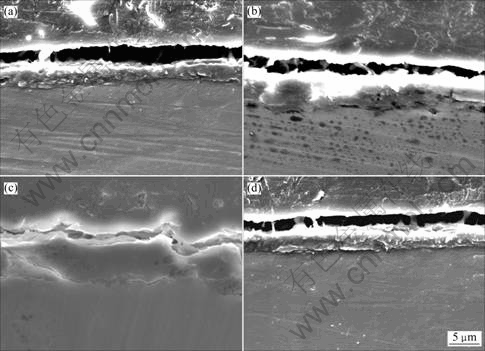
ͼ2 ��ͬ��Է���������PLLA��PLGAͿ��þ�����ɨ��羵��
Fig.2 SEM images on interface of 80 thousand(a), 200 thousand(b), 500 thousand(c) relative molecular mass of PLLA and 200 thousand relative molecular mass PLGA surface treated Mg(d)
ͼ3��ʾΪ��ͬ��Է��������ľ�������þ�Ľ������1#~4#�ֱ�Ϊ��Է�������Ϊ8��20��50���PLLA���Լ���Է�������Ϊ20���PLGA��Ϳ����������Ϳ�������Ľ�����Լ�Ϳ�㱾�������е��ھ�����ʵ����������Ի�����б���Ԥ������ʹ����ֻ��������ճ�������ͬʱ�Ի���������˻���ã����������������Ϳ��֮��Ľ������ͼ3��һ��֤������ѡ�õļ��־������У���Է�������ԽС�����ǿ��Խ����Ϊ��ͬ��Է��������ľۺ�����Ũ����ͬ������£����Ȳ��ܴ�������Է�������Ϊ50���PLLAŨ��Ϊ1%ʱ��Ϊ20 mPa��s���ң�ʵ�ʲ����з��ָ�PLLA���������ܼ�������ͬ��Է��������ľ�����;�(����-�ǻ�����)����ͬ��Ũ���º��ߵ��ȸ�С�����Եõ�������ܽ�ȣ�������ͨ������Ũ�����ı�Ϳ���ȡ���Ȼͼ3��ʾ��Է�������ԽС�������Խ�ã�����Է�������С�ľۺ��������ڽ���ʱ��Ҳ����٣�������Ϳ����þ������ò��ʾ��8����Է�������������Ϳ��������3��Ϳ����ȣ����Ա���þ��������ýϲ��������ѡ��20����Է���������PLGA���н�һ���о���
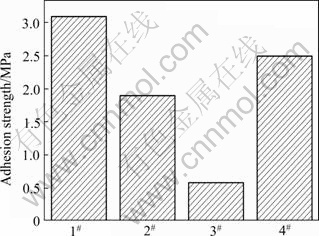
ͼ3 ��������Է��������Խ��ǿ�ȵ�Ӱ��
Fig.3 Effect of different relative molecular mass poly-lactic acid on adhesion strength between Mg implant and poly-lactic acid
ͼ4��ʾΪż�������洦���Խ��ǿ�ȵ�Ӱ�졣�ɼ���þ���澭��ż�����������������Ľ����������ߡ�����ֱ���ڻ������Ϳ���ۺ�������������������ߣ����Ա�����ѡ�����ż������þ���б�����ԡ�����ż����Ҳ����һ���ķ���Ч�����������ڴ�ͳ�������ۻ����ա������о�����[13]����������Ľṹ����������������������γ�Si��O��Me��ѧ��ϼ����Ӷ����Ϳ�����������Ļ�ѧ�����������ͨ����һ���Ż�����ż�����������գ�����ʵ��ʹþ��������������õĽ�ϡ�
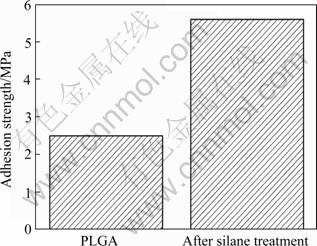
ͼ4 ż�������洦���Խ��ǿ�ȵ�Ӱ��
Fig.4 Effect of silane coupling agents pretreatment on adhesion strength between Mg implant and poly-lactic acid
2.2 Ϳ����
������Ϳ�������þֲ����ڶ�þ�������á����⣬Ϊ�˱�֤�����ڽ���������������ɽ��ܵİ�ȫ��Χ�ھ�����ȫ���⣬������Ϳ��ĺ�ȴ���һ������ֵ��
���о���ѡ��20 mm?10 mm?3 mm�Ĵ�þ����ΪͿ�����壬�о��˽�Ϳʱ�䡢��Ϳ�������ۺ���Ũ�ȶԲ��ϱ���Ϳ���ȵ�Ӱ�죬�õ��˱�1���е��о������
��1 ��Ϳʱ�䡢��Ϳ�����;ۺ���Ũ�ȶ�Ϳ���ȵ�Ӱ��
Table 1 Effect of dipping time, dipping times and effect of polymer concentration on coating thickness
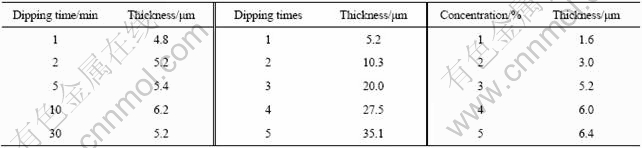
�ɱ�1��֪����Ϳʱ���Ϳ��ĺ��Ӱ���С����Ϳ����Ӱ�����������ǽ�Ϳ����������PLGA�����ı仯���ڱ�֤�������ܽ����Һ�������Ժܺõķ�Χ�ڽ��еģ����Կ����ڽ�Сճ�ȷ�Χ�ڣ�PLGA�����ı仯��Ϳ���ȸı䲻���ԡ����ֻҪȷ���ۺ���Ũ�ȣ��Ϳ���ͨ���ı��Ϳ����������Ϳ��ĺ�ȡ�
��Ȼ���о��ó��˽�Ϳʱ�䡢�ۺ���Ũ�ȼ���Ϳ������Ϳ���ȵ�Ӱ����ɣ������ھ�����Ҳ��һ�ֿɽ�����ϣ�Ϳ���������þֲ�����ں�������ϵľ�����Ľ����ʹ����Ϳ���Ϊ���״�����ܻ�ʹþ���巢����ǰ���⣬���Ի���Ҫ�����о�Ϳ�����뽵������֮��Ĺ�ϵ��
2.3 ��ģ����Һ�е�ʵ��
��ͼ5���Կ�����PLGAͿ����Ĵ�þ��ʴ����������ߣ���δ���κδ����Ĵ�þ��߽���1�����ۺ���Ϳ����Ա�֤��þ��3 d�ڻ������������⡣����Ϊ�ɽ���þֲ����ϵı���Ϳ�㣬Ҫ������þֲ��1���ڴﵽ���õı������á���Ϊ�������̻�����������������λ��Χ����֯����������֯��Χ��ۼ���������ϸ�����ɻ�����֯��������ɵ���֯�ƻ���ҪԼ1��ʱ��ָ�[14]������þ�ı���Ϳ�������ֲ���1���ڴﵽ���õĿ���ʴ����������þֲ����ϵĸ�ʴ�ٶȻ�ӿ죬ʹ����ǰʧЧ���������廷����ʮ�ָ��ӵģ�Witte��[15]�о�����þ�Ͻ�������ĸ�ʴ�붯�����ڸ�ʴ������4�������������ԣ���Ȼ�ڱ����д�þ����ľ�����Ϳ�����֤��þ��3 d�ڻ������������⣬�����ǵ����ڻ����ĸ����ԣ�������ΪͿ���Ѵﵽ����Ҫ���ҿ���ͨ�����ӽ�Ϳ����������Ϳ���ȣ��Ӷ�ʹþֲ�������ʴ�Խ�һ����ߡ�
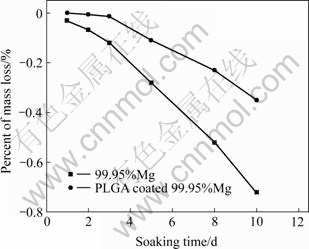
ͼ5 ��Ʒ������ʧ�����ʱ��ı仯
Fig.5 Variations of mass loss of sample with soaking time during immersed in Hank��s solution
3 ����
1) ���ý�Ϳ��������þ�ı����Ʊ�������Ϳ�㡣��ȷ����Ϳʱ�估�ۺ���Ũ���������Ҫͨ���ı��Ϳ����������þ����Ŀɽ���Ϳ���ȡ�
2) þ������Ϳ��������ǰͨ��ż������������������þ�������Ľ������
3) ���������ᴦ�����þ����ʴ��������ߡ�
REFERENCES
[1] Staiger M P, Pietak A M, Huadmai J, Dias G. Magnesium and its alloys as orthopedic biomaterials: A review[J]. Biomaterial, 2006, 27: 1728?1734.
[2] ������. þ�Ļ������ٴ�[M]. �ɶ�: �Ĵ���ѧ����������, 1996.
SHAO Mei-zhen. The fundamental and clinical of magnesium[M]. Chengdu: Sichuan Science and Technology Press, 1996.
[3] Cerre C M, Papillard M, Chavassieux P, Voegel J C, Boivin G. Influence of magnesium substitution on a collagen-apatite biomaterial on the production of a calcifying matrix by human osteoblasts[J]. J Biomed Mater Res, 1998, 42(4): 626?633.
[4] Rude R K, Gruber H E, Wei L Y, Frausto A, Mills B G. Magnesium deficiency: Effect on bone and mineral metabolism in the mouse[J]. Calcif Tissue Int, 2003, 72: 32?41.
[5] Zreiqat H, Howlett C R, Zannettino A, Evans P, Schulze-Tanzil G, Knabe C. Mechanisms of magnesium-stimulated adhesion of osteoblastic cells to commonly used orthopaedic implants[J]. J Biomed Mater Res, 2002, 62: 175?184.
[6] ������, �ƾ���, �� ��, ������, �ű���, Ҧ����. ��þ�����︯ʴ�о�[J]. ����ѧ��, 2005, 41: 1228?1232.
REN Yi-bin, HUANG Jing-jing, YANG Ke, WANG Hao, ZHANG Bing-chun, YAO Zhi-ming. Study of bio-corrosion of pure magnesium[J]. Acta Metallurgica Sinica, 2005, 41: 1228
[7] �ҳ�, ������, �� ��, ����Ӣ. ������Դ�þ��ϸ�����Ժ���Ѫ��[J]. ϡ�н��������빤��, 2005, 34: 903?906.
GAO Jia-cheng, LI Long-chuan, WANG Yong, QIAO Li-ying. Biocompatibility of magnesium after surface modification by heat-organic films-treatment[J]. Rare Metal Materials and Engineering, 2005, 34: 903?906.
[8] IJս��. ��ͬģ����Һ��pHֵ�仯�������ý������������ʴ���ܵ�Ӱ��[J]. �й���ʴ�����ѧ��, 1998, 18(2): 126?130.
MOU Zhan-qi. Effect of different artificial body fluids and their pH on corrosion of biomedical metallic materialsl[J]. Journal of Chinese Society for Corrosion and Protection, 1998, 18(2): 126?130.
[9] Gristina A G. Biomaterial-centered infection��Microbial adhesion versus tissue integration[J]. Science, 1987, 237: 1588?1595.
[10] Hench L L, Polak J M. Third-generation biomedical materials[J]. Science, 2002, 295: 1014?1017.
[11] Gollwitzer H, Thomas P, Diehl P,Steinhauser E, Summer B, Barnstorf S, Gerdesmeyer L, Mittelmeier W S. Biomechanical and allergological characteristics of a biodegradable poly(D,L-lactic acid) coating for orthopaedic implants[J]. Journal of Orthopaedic Research, 2005, 23: 802?809.
[12] Heublein B, Rohde R, Kaese V, Niemeyer M, Hartung W H. Biocorrosion of magnesium alloys: A new principle in cardiovascular implant technology[J]. Heart, 2003, 89: 651?656.
[13] ��ѩ��, ���, �����, �ܴ�ʤ. ����ż�����ڷ���Ϳ�����Ԥ�����е�Ӧ���о�[J]. ���Ͽ�ѧ�빤��ѧ��, 2005, 23: 146?150.
WANG Xue-ming, LI Ai-ju, LI Guo-li, GUAN Chong-sheng. Studies on the application for SCA in the metal pretreatment of anti-corrosion coatings[J]. Journal of Materials Science & Engineering, 2005, 23: 146?150.
[14] Deeb M, Holmes R E. Tissue response to facial contour augmentation with dense and porous hydroxylapatite in Rhesus monkeys[J]. Oral Maxillofac Surg, 1989, 47: 1282?1289.
[15] Witte F, Fischer J, Nellesen J, Crostack H A, Kaese V, Pisch A, Beckmann F, Windhagen H. In vitro and in vivo corrosion measurements of magnesium alloys[J]. Biomaterials, 2006, 27(7): 1013?1018.
�ո����ڣ�2007-03-30�������ڣ�2007-07-13
ͨѶ���ߣ��ƾ�������ʿ�о������绰��024-23971676��E-mail: jjhuang@imr.ac.cn
(�༭������Ⱥ)