DOI:10.19476/j.ysxb.1004.0609.2019.10.23
电解回收铁钨锡合金粉中的铁
范科彪1,郑雅杰1,王 钫1, 李海波2
(中南大学 冶金与环境学院,长沙 41008 3;2. 资兴市鸿锦冶金有限公司,郴州 423400)
摘 要:以钨渣高温还原熔炼所得的铁钨锡合金粉为原料,通过电解的方法回收其中的铁,研究了Fe2+浓度、pH值、温度和电流密度对电流效率及电解铁纯度的影响。结果表明:在电流密度300 A/m2、温度45 ℃、pH=4.5、Fe2+浓度100 g/L的优化工艺条件下,电流效率为92.1%,电解铁纯度为99.1%;在优化工艺条件下进行了连续4天的电解实验,平均电流效率为87.8%,电解铁纯度在97%以上,阳极泥里钨、锡含量(质量分数)分别为19.7%和20.0%,相对于原料中的钨、锡含量(6.98%,6.91%)分别富集了2.82倍和2.89倍;铁的回收率为92.2%,阳极泥产率为33.0%,吨铁电能消耗为4757 kW・h。SEM像表明电解铁呈不规则棒状。
关键词:铁钨锡合金粉;电解;电解铁;电流效率
文章编号:1004-0609(2019)-10-2421-12 中图分类号:TF591.1 文献标志码:A
钨渣是以黑钨矿或白钨矿为主要原料生产WO3或仲钨酸铵(APT)过程中排出的固体废物[1]。目前,我国钨渣总量已经达到100万t左右,且以每年产出钨渣7万t的速度增长[2-3]。钨渣中含有1%~4%W、10%~25%Fe、3%~20%Mn、1%~20%Ca、3%~8%Si[4]、0.2%~0.4%Sc[5]以及少量的Ta、Nb、Sn等多种有价元素。目前,对钨渣的综合回收利用主要在四个方面:1) 回收其中的有价金属[6];2) 将钨渣作为矿物原料生产耐磨材料等新型材料[7];3) 生产钨渣微晶玻璃[8];4) 作吸附材料[9-10]。
对于钨渣中有价元素的回收主要集中在对W、Ta、Nb、Sc、Mn等的回收研究[6, 11-16],而对其中含量较高的Fe的回收方面研究较少[6]。MACΠOB[17]研究钨中间产物与硫酸钠在1150~1200℃的电炉中熔炼时,进行了扩大的实验室和实验室工业矿石还原熔炼试验,以铁合金的形式回收W、Fe,其回收率分别为93%、98.8%。该方法直接从贫钨原料提取铁合金,在一定程度上解决了贫钨中间产物的处理问题。但该工艺存在熔炼温度高,所得铁合金价值低,稀有金属未得到充分利用等缺点。湖南冶金研究所开发了钨渣电炉还原熔炼的工艺流程,控制炉温1500~1600 ℃,W、Ta、Nb、Fe进入铁合金,铁合金中含0.45% (Nb+Ta),含6.22%W。但由于当时中间铁合金售价低,产出的氧化钪无市场,钍饼需深埋,故未能投入工业应用[6]。戴艳阳等[18]研究了以钨渣为原料,经浸出、净化、共沉淀、干燥、预烧等过程制得到了基本满足要求的优质锌锰铁氧体粉末,实现了铁锰的同时回收,但该工艺流程冗长,所得锌锰铁氧体杂质含量高,应用市场小。КAPIIIYHOB等[19]提出了处理高锡钨渣的流程,该流程将W-Sn中间产物中的Sn还原为金属锡和含锡的金属间化合物,然后采用低温氯化的办法将锡以氯化锡的形式回收,氯化残渣经酸处理浸出Mn、Fe、Sc后,浸出液送去进行Mn、Fe、Sc的提取,浸出渣或以湿法冶金的方法回收其中的Nb、Ta、W,或在电弧炉中冶炼铁合金,该工艺可以实现多金属综合回收,但流程复杂,氯化残渣酸浸出液和浸出渣铁含量低,后续回收效率不高。
由此,本文作者选择钨渣高温还原熔炼所得的铁钨锡合金粉为原料,分析其中各主要元素含量、物相、元素分布状态及主要元素的M-H2O系φ-pH图;采用电解的方法以单质铁的形式回收铁钨锡合金粉里的铁和富集钨、锡;研究Fe2+浓度、pH、温度和电流密度对电流效率及电解铁纯度的影响,以期研究成果可为铁钨锡合金粉的资源最大化利用提供新的途径。
1 实验
1.1 实验原料
实验所用铁钨锡合金粉来自湖南某钨冶炼厂,外观呈球状,粒径小于3 mm,密度为5.6 g/cm3,经振磨机磨至粒径小于65 mm后溶解分析其主要化学成分,结果如表1所示,XRD谱如图1所示,SEM-EDS扫描分析结果如图2所示。
由表1可知,实验所用的铁钨锡合金粉的主要成分为Fe、W、Sn、C、Si,其含量分别为72%、6.98%、6.91%、2.92%和2%。此外,还含有少量Mn、Ta和Nb,其含量分别为0.35%、0.18%和0.74%。图1所示为铁钨锡合金粉的XRD谱。由图1可知,铁钨锡合金粉中的Fe以单质Fe、Fe3C和Fe3SnC形式存在,其他元素可能由于含量低,或者结晶性不好,未检测到对应的特征峰。图2所示为铁钨锡合金粉的SEM像和EDS面扫描元素分布图。由图2(a)可见,铁钨锡合金粉大多数颗粒较大,呈不规则块状;由图2(b)、(c)和(d)可见,铁钨锡合金粉中Fe、W、Sn主要以弥散状态分布在整个物料中,Fe的分布最为均匀密集。
表1 铁钨锡合金粉的主要化学成分
Table 1 Main chemical compositions of Fe-W-Sn alloy powder(mass fraction,%)
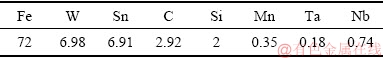
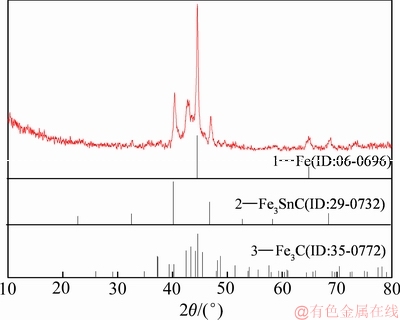
图1 铁钨锡合金粉XRD谱
Fig. 1 XRD pattern of Fe-W-Sn alloy powders
1.2 实验步骤
由于铁钨锡合金粉中W、P含量高,导致其密度高、脆性大,生产实践表明,其浇铸成阳极板容易发生断裂,因此实验过程中直接将铁钨锡合金粉盛装在容器里,再选择适当的导电棒作为阳极,具体步骤如下所述:

图2 铁钨锡合金粉的SEM像及EDS面扫描元素分布图
Fig. 2 SEM image and EDS spectra of Fe-W-Sn alloy powders
1.2.1 阳极制备
用钛篮盛装铁钨锡合金粉,用孔径为5 mm(3000目)的涤纶滤布作为阳极套,以承接阳极不溶物;以铅钙合金为阳极导电棒,事先将铅钙合金插入钛篮正中间,再在铅钙合金周围均匀填充铁钨锡合金粉即制备得阳极。
1.2.2 阴极制备
以316L不锈钢(65 mm×91 mm×3 mm)作为阴极,背面涂AB胶以绝缘,正面分别用粗细砂纸打磨光亮后,再用10%稀盐酸清洗,接着用蒸馏水冲洗2~3遍,吹干称重,待用。
1.2.3 电解液配制
量取适量蒸馏水倒入2 L烧杯内,根据电解质浓度和电解液体积(1.5 L)称取所需固体电解质硫酸亚铁(AR,国药集团化学试剂有限公司)、硫酸铵(AR,衡阳凯信化工股份有限公司)和抗氧化剂抗坏血酸(AR,广州化学试剂厂)加入烧杯内,搅拌至完全溶解再加蒸馏水稀释至1.5 L,用pH计(PHS-25,赛多利斯科学仪器有限公司)测量电解液pH并加稀氨水(西陇化工股份有限公司)或稀硫酸(AR,湖南汇虹试剂有限公司)调整至所需pH。
1.2.4 电解
将配制好的电解液转移至自制聚四氟乙烯电解槽(15 cm×9 cm×13 cm),再将电解槽置于数显恒温水浴锅(HH-S2,上海光正仪器有限公司)中加热至适当温度,将阴阳极平行置于电解槽内调整至适当极距,接通电解液循环系统并调整至适当流量,再接通直流电源(PS305D,郑州长城科工有限公司)进行电解。电解结束后,取出阴极板用蒸馏水冲洗3遍以去除夹带的电解液,于真空干燥箱中烘干,称重,送检测。
1.3 分析与检测
1.3.1 检测方法
采用X射线衍射仪 (XRD,Rigaku D/max-TTR III)分析样品物相 (发光源为Cu Kα靶,管压为40 kV,管流为250 mA,λ=0.154056×10-10 m,2θ为10.0°~ 80.0°);采用电感耦合等离子体光谱仪(ICP-OES,IRIS Intrepid Ⅱ,Thermo Eleetron Corporation)分析溶液中的元素含量;采用扫描电镜-能谱(SEM,FEIQuanta 200)观察样品表面形貌和元素分布;采用重铬酸钾滴定法(GB/T1863-2008)测定电解液中的Fe2+和Fe3+浓度以及分析电解铁纯度。
1.3.2 电流效率计算
1) 电流效率的计算公式如式(1)所示。
 (1)
(1)
式中:η为电流效率,%;m2为电解后阴极板及产品的总质量,g;m1为电解前阴极板的质量,g;q为Fe2+还原为金属铁的电化当量,1.042 g/(A・h);I为电流强度,A;t为电解时间,h。
2 热力学分析
2.1 铁钨锡合金粉的阳极溶解过程
铁钨锡合金粉电解分离Fe和富集含W、Sn的阳极泥类似于粗金属的电解精炼。以铁钨锡合金粉作为阳极,不锈钢板作阴极,硫酸亚铁水溶液作电解液,当通以直流电时,Fe从阳极溶解成离子状态进入电解液,在阴极析出纯电解铁。铁钨锡合金粉中的杂质则不溶解而进入阳极泥,或溶解进入电解液但不再阴极析出,或溶解进入电解液并在阴极与Fe共沉积,从而实现Fe与大部分杂质的分离。铁钨锡合金粉阳极溶解过程可能发生的电极反应如表2所示。
由表2可知,W、Sn的标准电极电位比Fe的正,所以理论上W、Sn不会在阳极溶解,Ta、Nb、Si、Mn的标准电极电位比Fe的负,故会在阳极溶解,但Ta、Nb的电负性较强,在水溶液中容易发生不可逆转的水解反应[20];Si被氧化为SiO2。另外,电极反应2,若令溶液中的Fe2+的活度为1,并假设铁钨锡合金粉阳极中Fe在反应1的平衡电位下发生溶解,则根据能斯特公式,生成的Fe3+的平衡浓度可以按下式求出[21]:
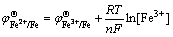
将相应数字代入得:
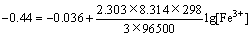
求得[Fe3+]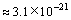 mol/L。故铁钨锡合金粉电解过程中,阳极主要发生铁溶解为Fe2+的反应1,生产Fe3+的反应2进行得极少,将Fe2+氧化为Fe3+的反应3 认为不可能发生,同理,析出氧气的反应14就更不可能发生[22]。即铁钨锡合金粉电解过程中阳极发生的主要反应为反应1、8、9、10、11、12,阴极发生的主要反应为反应1和14,溶解进入电解液的只有Fe和Mn。
mol/L。故铁钨锡合金粉电解过程中,阳极主要发生铁溶解为Fe2+的反应1,生产Fe3+的反应2进行得极少,将Fe2+氧化为Fe3+的反应3 认为不可能发生,同理,析出氧气的反应14就更不可能发生[22]。即铁钨锡合金粉电解过程中阳极发生的主要反应为反应1、8、9、10、11、12,阴极发生的主要反应为反应1和14,溶解进入电解液的只有Fe和Mn。
表2 钨锡合金粉电解过程可能发生的电极反应[23]
Table 2 Electrode reaction which may occur in electrolysis process of Fe-W-Sn alloy powders[23]

2.2 Fe与W、Sn分离可行性研究
Fe、W、Sn都能溶解于酸,但其发生溶解所需的酸度有所差异。298 K 时,W-H2O系、Sn-H2O与Fe-H2O系可能发生的平衡反应式和通过基础热力学数据计算出各φ-pH关系式如表3~5所列,绘制对应的φ-pH图分别如图3~5所示。
由图3~5可知,当pH在1.53~6.57范围以及电位介于-0.44~0.77V范围内(如图3、4、5阴影区域),Fe将处在Fe2+的稳定区域,W、Sn将分别以H2WO4和Sn(OH)2、Sn(OH)4的固相形式存在。即在这个条件下电解,铁钨锡合金粉里的Fe可以不断地溶解生成Fe2+进入电解液,而W、Sn则分别转变为H2WO4和Sn(OH)2、Sn(OH)4富集于阳极泥里。另外,由图5可知,Fe2+易被氧化为Fe3+并进一步水解为Fe(OH)3,所以实验过程中应该尽量保持电解液与空气隔绝并加入适量的抗氧化剂。以上分析表明,控制适当的pH和电位可以实现Fe与W、Sn的分离。
表3 W-H2O系中的主要反应式和热力学平衡方程式
Table 3 Reactions and thermodynamic equations for W-H2O system
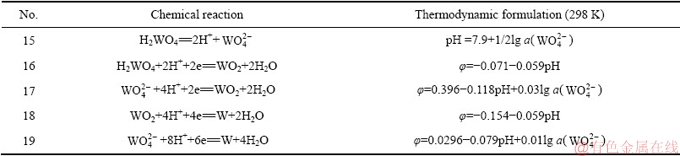
表4 Sn-H2O系中的主要反应式和热力学平衡方程式
Table 4 Reactions and thermodynamic equations for Sn-H2O system
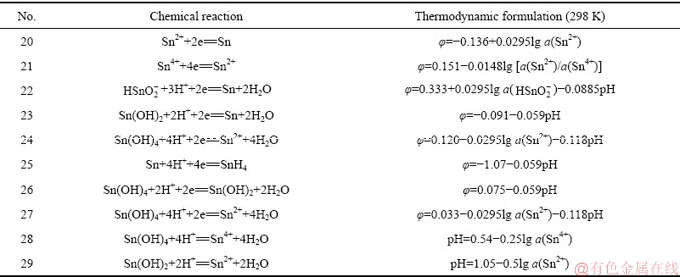
表5 Fe-H2O系中的主要反应式和热力学平衡方程式
Table 5 Reactions and thermodynamic equations for Fe-H2O system
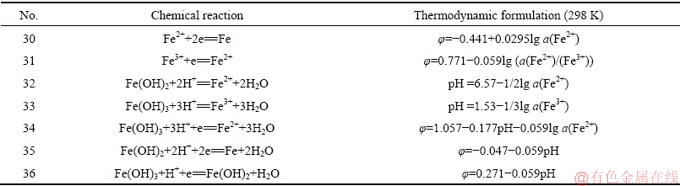
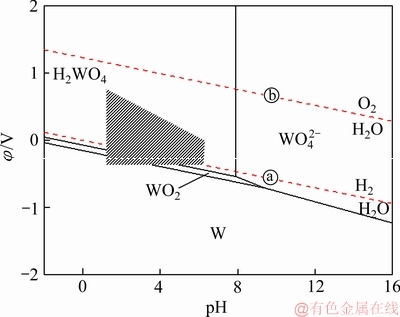
图3 W-H2O系φ-pH图
Fig. 3 φ-pH diagram of W-H2O system (T=298 K; a=10-1; pO2=pH2=101 kPa)

图4 Sn-H2O系φ-pH图
Fig. 4 φ-pH diagram of Sn-H2O system
3 结果与讨论
3.1 Fe2+浓度对电流效率和电解铁纯度的影响
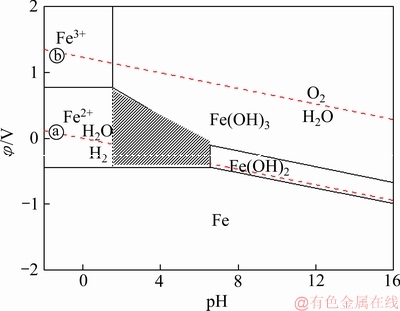
图5 Fe-H2O系φ-pH图
Fig. 5 φ-pH diagram of Fe-H2O system (T=298 K; a=1; pO2=pH2=101kPa)
在电流密度为300 A/m2,温度为45 ℃,pH值为4.5,(NH4)2SO4浓度为100 g/L,抗坏血酸浓度为1 g/L的条件下,考察Fe2+浓度对阴极电流效率和电解铁纯度的影响,结果如图6所示,电解铁的XRD谱如图7所示。
由图6可知,随着Fe2+浓度的增大,电解铁纯度和电流效率均呈现先升高后降低的趋势。当Fe2+浓度为100g/L时,电流效率达到最大为90.9%,电解铁纯度达到最高为98.2%。由图7可知,阴极所得Fe为单质铁,随着Fe2+浓度的增大,Fe特征峰位置几乎未发生偏移,但其峰强呈先增大后减小的趋势。这是因为Fe为负电性金属,在阴极还原析出时往往伴随着不同程度的析氢反应。根据能斯特公式(2)~(3)[23]计算出不同Fe2+浓度下的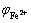 和pH=4.5时的
和pH=4.5时的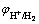 如表6所示,Fe2+浓度当做活度计算,此条件下在铁表面的析氢过电位为0.68V,
如表6所示,Fe2+浓度当做活度计算,此条件下在铁表面的析氢过电位为0.68V,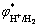 表示减去过电位后H2的实际析出电位,铁的过电位相对较小,可忽略不计。
表示减去过电位后H2的实际析出电位,铁的过电位相对较小,可忽略不计。
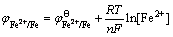 (2)
(2)
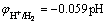 (3)
(3)
由表6可知,增大Fe2+浓度对 的影响甚小,当Fe2+浓度由70 g/L增大至110 g/L,
的影响甚小,当Fe2+浓度由70 g/L增大至110 g/L, 仅正移0.006V,且始终大于
仅正移0.006V,且始终大于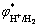 。实验过程中之所以会有H2析出的主要原因是浓差极化和电化学极化造成的,Fe2+浓度较低时,浓差极化严重,加之铁的交换电流密度较小,在阴极放电缓慢而极易发生电化学极化,阴极析氢剧烈,导致电解铁出现大量裂纹夹杂电解液,而且随着H+的消耗,阴极附近pH升高,部分Fe2+发生水解生成Fe(OH)2沉淀附着在阴极表面妨碍铁的析出。故在低Fe2+浓度条件下电流效率和电解铁纯度都较低。随着Fe2+浓度的增大,阴极附近的浓差极化减小,不仅有利于Fe2+的还原,而且减少了阳极中杂质的溶解和在阴极析出的数量,电解铁表面变得光滑平整,所以电流效率和电解铁纯度提高。但随着Fe2+浓度的进一步增大,电解液黏度增大,Fe2+迁移速率减慢,电流效率降低[24]。且随着电解时间的延长,部分Fe2+会以绿矾的形式在阴极和阳极表面结晶,从而阻止阳极的溶解和Fe2+的还原。为了保证电流效率高的同时提高电解铁的纯度,选择Fe2+浓度100 g/L为较优工艺。
。实验过程中之所以会有H2析出的主要原因是浓差极化和电化学极化造成的,Fe2+浓度较低时,浓差极化严重,加之铁的交换电流密度较小,在阴极放电缓慢而极易发生电化学极化,阴极析氢剧烈,导致电解铁出现大量裂纹夹杂电解液,而且随着H+的消耗,阴极附近pH升高,部分Fe2+发生水解生成Fe(OH)2沉淀附着在阴极表面妨碍铁的析出。故在低Fe2+浓度条件下电流效率和电解铁纯度都较低。随着Fe2+浓度的增大,阴极附近的浓差极化减小,不仅有利于Fe2+的还原,而且减少了阳极中杂质的溶解和在阴极析出的数量,电解铁表面变得光滑平整,所以电流效率和电解铁纯度提高。但随着Fe2+浓度的进一步增大,电解液黏度增大,Fe2+迁移速率减慢,电流效率降低[24]。且随着电解时间的延长,部分Fe2+会以绿矾的形式在阴极和阳极表面结晶,从而阻止阳极的溶解和Fe2+的还原。为了保证电流效率高的同时提高电解铁的纯度,选择Fe2+浓度100 g/L为较优工艺。
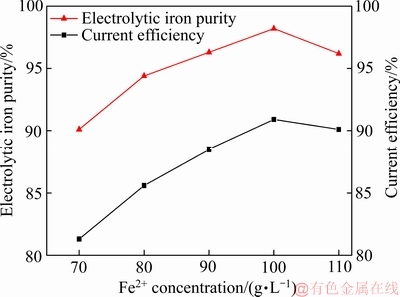
图6 Fe2+浓度对电流效率和电解铁纯度的影响
Fig. 6 Effect of Fe2+ concentration on current efficiency and electrolytic iron purity
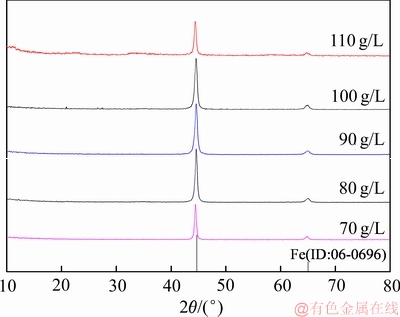
图7 不同Fe2+浓度下电解铁的XRD谱
Fig. 7 XRD patterns of electrolytic iron at different Fe2+ concentration
3.2 pH值对电流效率和电解铁纯度的影响
其他条件不变,当Fe2+浓度为100 g/L时,考察pH对阴极电流效率和电解铁纯度的影响,结果如图8所示,电解铁的XRD谱如图9所示。
表6 不同Fe2+浓度和pH为4.5时的电极电位
Table 6 Electrode potential of different Fe2+ concentrations and pH 4.5
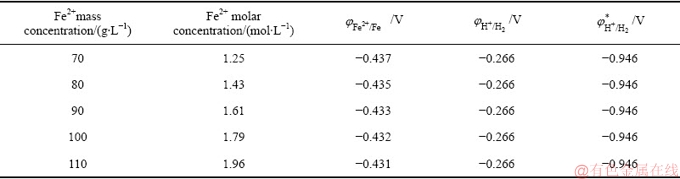
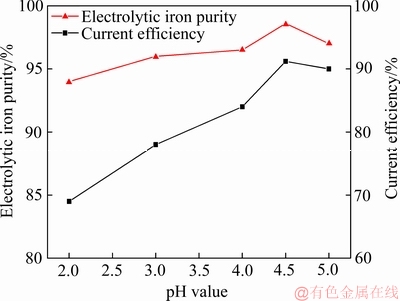
图8 pH对电流效率和电解铁纯度的影响
Fig. 8 Effect of pH value on current efficiency and electrolytic iron purity
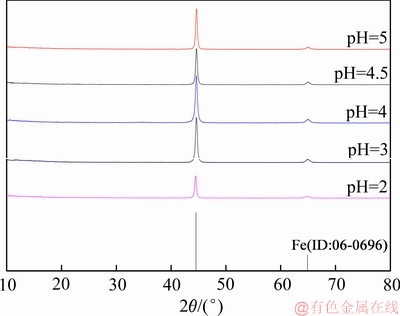
图9 不同pH值下电解铁的XRD谱
Fig. 9 XRD patterns of electrolytic iron at different pH value
由图8可知,随着pH的升高,电流电流效率和电解铁纯度呈先升高后降低的趋势。在pH为4.5时,电流效率达到最高为91.2%,电解铁纯度达到最高为98.6%。图9所示XRD谱表明电解铁为单质铁,无明显杂质峰。这是因为:1) pH较低时,阴极析氢严重,造成电量的浪费;且酸度高时阳极杂质发生的化学溶解较多并在阴极析出;2) 氢气的析出会导致电解铁出现微细裂纹,夹杂电解液,甚至会导致电解铁从阴极板脱落。随着pH升高,析氢减弱,电流效率和电解铁纯度升高。但是,根据反应(4)~(6)可知,随着pH
进一步提高,Fe2+的氧化速率加快,水解生成Fe(OH)3甚至是Fe(OH)2附着在阴极表面,影响Fe2+的还原而使得电流效率和电解铁的纯度降低。为了获得较高的电流效率和纯度较高的电解铁,选择pH=4.5左右为较优条件进行后续实验。
4Fe2++4H++O2=4Fe3++2H2O (4)
Fe3++3OH-=Fe(OH)3 (5)
Fe2++2OH-=Fe(OH)2 (6)
3.3 温度对电流效率和电解铁纯度的影响
其他条件不变,在pH值为4.5时,考察温度对阴极电流效率和电解铁纯度的影响,结果如图10所示,电解铁的XRD谱如图11所示。
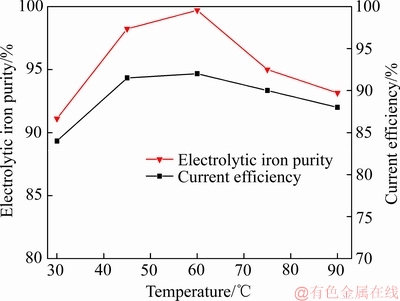
图10 温度对电流效率和电解铁纯度的影响
Fig.10 Effect of temperature on current efficiency and electrolytic iron purity
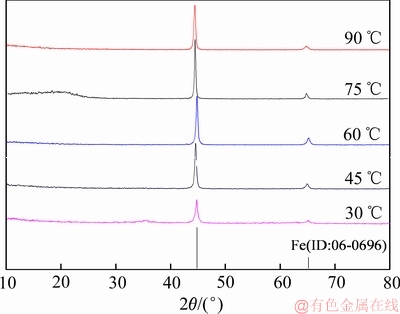
图11 不同温度下电解铁的XRD谱
Fig. 11 XRD patterns of electrolytic iron at different temperatures
由图10可知,随着温度的升高,电流效率和电解铁的纯度呈先增大后减小的趋势。当温度为45 ℃时,电流效率达到最高为91.5%,电解铁的纯度达到最高为98.2%;当温度升高至60 ℃时,电流效率达到92%,电解铁的纯度最高为98.8%,相对于45℃时的情况无明显优势。图11所示XRD谱表明电解铁为单质Fe,随着温度的升高,Fe的特征峰强先增强后减弱。当温度为30℃时,溶液黏度大,Fe2+溶剂化倾向大,迁移速率不及H+的十分之一[22],导致大量H+优先于Fe2+被还原,低温下H2不易逸出镀层而使铁片裂开不能形成完整的铁板。另外,低温下有部分电解质在阴极结晶析出夹杂在电解铁内。因此,低温下电流效率和电解铁纯度都较低。当温度升高至60 ℃时,电流效率和电解铁纯度最高。但随着温度的进一步升高,电流效率和电解铁纯度逐渐下降。这主要因为:1) 温度升高,虽然有利于Fe2+的迁移,但是H+的迁移速率同样增大且随着温度的升高氢的过电位减小。所以氢气析出加快,阴极附近pH升高速率加快,部分Fe2+水解生成Fe(OH)2附着在阴极表面或者悬浮在电解液里,影响Fe2+的析出。2) 温度升高,加快了添加剂抗坏血酸的分解,Fe2+氧化为Fe3+的速率加快[25],Fe3+除了发生水解以外,部分Fe3+在阴极得被还原为Fe2+,Fe2+又迁移到阳极氧化为Fe3+而后又迁移到阴极被还原为Fe2+,如此周而复始,造成了电流的空耗。3) 提高温度加快了阳极化学溶解,杂质进入电解液并随着电解时间的延长而在阴极析出。维持电解液的较高温度增大了升温和维温难度,而且较高温度下电解液蒸发加快,需要经常调整电解液成分。故温度控制为45 ℃较为适宜。
3.4 电流密度浓度对电流效率和电解铁纯度的影响
其他条件不变,当温度为45 ℃时,考察电流密度对阴极电流效率和电解铁纯度的影响,结果如图12所示,电解铁的XRD谱如图13所示。
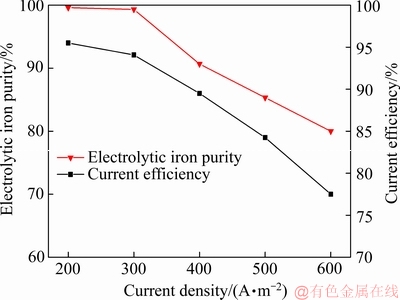
图12 电流密度对电流效率和电解铁纯度的影响
Fig. 12 Effect of current density on current efficiency and electrolytic iron purity
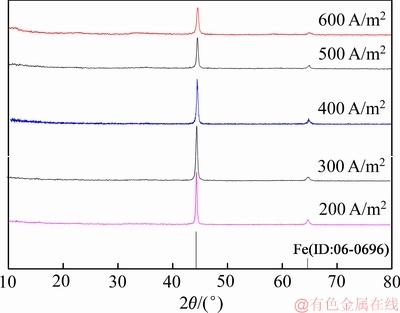
图13 不同电流密度下电解铁的XRD谱
Fig. 13 XRD patterns of electrolytic iron at different current densities
由图12可知,随着电流密度的增大,电流效率和电解铁的纯度逐渐降低。当电流密度为200 A/m2时,电流效率达到最大为94.8%,电解铁纯度达到最高为99.5%;当电流密度增大至300 A/m2时,电流效率达到最大为92.1%,电解铁纯度达到最高为99.1%,相对于200 A/m2无明显缺点。由图13可知,随着电流密度的增大,Fe的特征峰强度逐渐降低,可能由于杂质混入电解铁所致。这主要是因为:1) 电流密度的提高,阳极极化增大,导致一些在低电流密度下不能溶解的金属杂质在高电流密度下发生溶解。加之提高电流密度,阴极附近电解液中Fe2+浓度贫化加剧而无法及时补充Fe2+,浓差极化增大[26],导致杂质金属离子和氢气在阴极析出,从而造成电解铁的纯度和电流效率降低;2) 随着电流密度的增大,达到铁溶解的极限电流密度,阳极发生析氧反应,导致Fe2+氧化为Fe3+并进一步水解为一种黄色固体渣,经XRD鉴定为黄铵铁矾,其XRD谱如图14所示,且电流密度越大,生成的黄铵铁矾渣越多,其形成机理如下所示:
2H2O-4e=O2+4H+ (7)
4Fe2++4H++O2=4Fe3++2H2O (8)
3Fe2(SO4)3+2NH3・H2O+10H2O=2NH4Fe3(SO4)2(OH)6+5H2SO4 (9)
由反应(9)可知,黄铵铁矾的生成消耗了电解质硫酸铵,大部分黄铵铁矾附着在阳极套上导致阳极套发生堵塞,少部分黄铵铁矾随电解液流动分散到电解液并有部分沉积在阴极表面。另外,反应(7)和(9)为放酸反应,随着电解的进行电解液的pH逐渐降低,增大了Fe2+在阴极还原的难度。若加碱调整pH则会导致电解液局部迅速水解产生Fe(OH)2沉淀,实验发现,当电流密度控制在300 A/m2以下时不会产生黄铵铁矾,考虑到生产效率,故选择电流密度为300 A/m2为较优工艺。
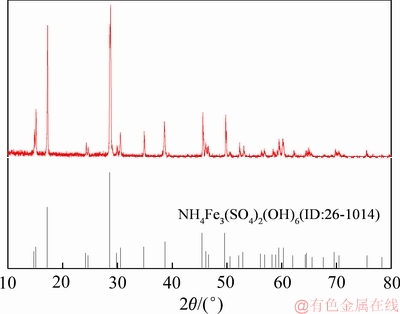
图14 电解液水解渣XRD谱
Fig. 14 XRD pattern of electrolyte hydrolysis residue
3.5 连续电解实验
通过单因素实验的探究,确定铁钨锡合金粉电解法回收铁的优化工艺条件为:Fe2+浓度为100 g/L,pH为4.5,温度为45 ℃,电流密度为300 A/m2,(NH4)2SO4浓度为100 g/L,抗坏血酸浓度为1 g/L。为了排除实验误差和验证该工艺的可行性,在上述优化工艺条件下进行了连续电解实验,设定阳极周期为4天,阴极周期为1天,即每天定期从阴极剥离电解铁,称取230 g铁钨锡合金粉装入钛篮。电解4天共得电解铁片152.7 g,阳极泥76 g,铁的回收率为92.2%,阳极泥产率为33.0%,电解铁纯度和电流效率列于表7,阳极泥化学成分列于表8,电解铁和阳极泥的XRD谱分别如图15和16所示,各阶段电解铁的SEM像如图17所示。
表7 连续电解实验结果
Table 7 Experimental results of continuous electrolysis
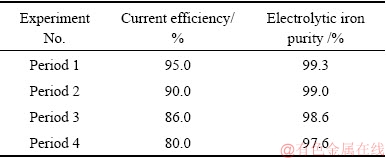
表8 阳极泥的化学成分
Table 8 Chemical composition of anode slime (mass fraction,%)
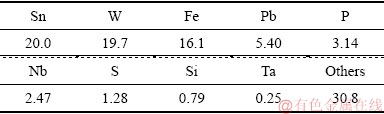
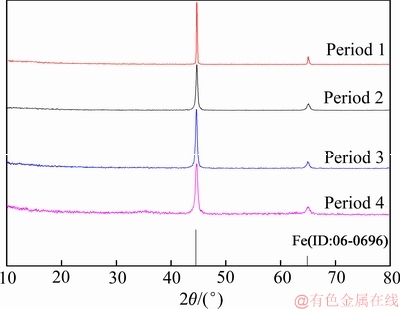
图15 连续电解实验电解铁的XRD谱
Fig. 15 XRD patterns of electrolyticiron in continuous electrolysis experiment
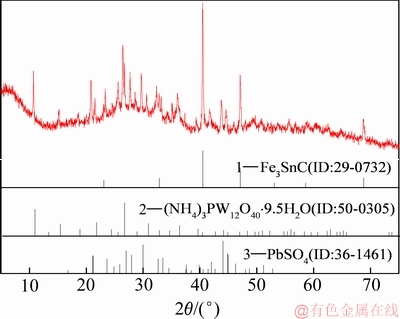
图16 阳极泥XRD谱
Fig. 16 XRD pattern of anode slime
由表7和8可知,在优化工艺条件下进行的连续电解实验,平均电流效率为87.8%,电解铁的纯度在97%以上,可以进一步精炼为高纯铁或者用于粉末冶金工业(基本满足)。阳极泥里W、Sn的含量分别为19.7%和20.0%,相对于原料中W、Sn的含量(6.98%和6.91%)分别富集了2.82倍和2.89倍。由图15可知,阴极铁为单质铁,晶相较纯,无其他杂峰,但是随着电解时间的延长,峰宽略有增大,这可能是由于氢气的夹杂量增大而使微观应力增大所致。如图16所示,阳极泥的主要物相为(NH4)3PW12O40・9.5H2O、Fe3SnC和PbSO4。其中,Fe3SnC在铁钨锡合金粉的XRD谱中也被检测到,该物质应该是在钨渣高温还原熔炼过程中形成的合金相。由于该合金相的形成使Sn的溶出电位正移而不易溶解,这应该是Sn的富集比大于W的富集比的原因。
图17所示为连续电解实验的电解铁的SEM像。由图17可知,电解铁粉呈不规则棒状,这是由于金属镀层的形成过程实际上是外加电场作用下的结晶过程,镀层组织形貌主要取决于电结晶过程中的生长方式。由于实验所采用的电流密度低,外加电场的影响较弱,离子迁移速率也较小,形核驱动力不足以独立成核,镀层结晶时主要依附于基体表面晶粒,沿着电场的方向生长,发生所谓的“垂直长大”,从而形成柱状晶粒组织[27]。同时,第四天的电解铁粉表面裂纹和空洞增多,这主要是因为随着电解时间的延长,阳极铁含量降低导致阳极极化增大,电解过程伴随有水的分解反应而导致电解液酸度升高,故而导致氢气的析出量增大。
这些氢气大部分从铁表面逸出进入电解液,少部分氢则以过饱和方式渗入镀层,除了一部分氢溶于铁原子晶格位置外,相当一部分氢则处于微观结构缺陷处,从而导致内应力增大而出现裂纹。

图17 电解铁的SEM像
Fig. 17 SEM images of electrolytic iron
4 结论
1) 热力学分析表明,当pH在1.53~6.57之间和电位介于-0.44~0.77 V范围内,Fe将不断的溶解为Fe2+,W、Sn则分别以H2WO4和Sn(OH)2、Sn(OH)4的固相形式存在,通过电解可以实现Fe与W、Sn的分离。
2) 阴极电流效率和电解铁纯度随Fe2+浓度的增大、pH和温度的升高呈先增大后减小的趋势,随电流密度的增大而逐渐减小。其中,电流密度对电流效率和电解铁纯度的影响最大,当电流密度超过300A/m2时,阳极析氧严重导致大量的Fe2+氧化为Fe3+并进一步水解为黄铵铁矾而使电解液变质。
3) 铁钨锡合金粉电解法回收Fe的较优工艺条件为:电流密度300 A/m2,温度45 ℃,pH4.5,Fe2+浓度100 g/L。在该条件下,连续电解4天所得电解铁的纯度在97%以上,平均电流效率为87.8%,阳极泥里W、Sn的含量分别为19.7%和20.0%,相对于原料中W、Sn的含量(6.98%和6.91%)分别富集了2.82倍和2.89倍,铁的回收率为92.2%,阳极泥产率为33.0%。
REFERENCES
[1] 朱海玲, 邓海波, 吴承桧, 何小民. 钨渣的综合利用回收技术研究现状[J]. 中国钨业, 2010, 25(4): 15-18.
ZHU Hai-ling, DENG Hai-bo, WU Cheng-hui, HE Xiao-min. The current comprehensive recovery technology of tungsten slag[J]. China Tungsten Industry, 2010, 25(4): 15-18.
[2] 戴艳阳, 钟 晖, 钟海云. 钨渣回收制备四氧化三锰新工艺[J]. 中国有色金属学报, 2012, 22(4): 1242-1247.
DAI Yan-yang, ZHONG Hui, ZHONG Hai-yun. Novel process for preparation of mangano-manganic oxide from tungsten residue[J]. The Chinese Journal of Nonferrous Metals, 2012, 22(4): 1242-1247.
[3] 杨金忠, 高何凤, 王 宁, 陈林, 王健媛, 杨玉飞. 仲钨酸铵(APT)生产中钨渣的污染特性分析[J]. 环境工程技术学报, 2015, 5(6): 525-530.
YANG Jin-zhong, GAO He-feng, WANG Ning, CHEN Lin, WANG Jian-yuan, YANG Yu-fei. Research on polluting characteristic of tungsten residue from ammonium paratungstate (APT)[J]. Journal of Environmental Engineering Technology, 2015, 5(6): 525-530.
[4] 苏正夫, 刘宇晖. 钨渣中钨回收利用新工艺研究[J]. 稀有金属与硬质合金, 2014, 42(4): 11-13.
SU Zheng-fu, LIU Yu-hui. Study on a new process of tungsten recovery from tungsten slag[J]. Rare Metals and Cemented Carbides, 2014, 42(4): 11-13.
[5] 刘彩云, 符剑刚. 钨渣中钪的萃取回收实验研究[J]. 稀有金属与硬质合金, 2015, 43(5): 4-8, 11.
LIU Cai-yun, FU Jian-gang. Experimental study on extraction and recovery of scandium from tungsten residue[J]. Rare Metals and Cemented Carbides, 2015, 43(5): 4-8, 11.
[6] 戴艳阳. 钨渣中有价金属综合回收新清洁工艺研究[D]. 长沙: 中南大学, 2013.
DAI Yan-yang. Study on the new cleaner process of comprehensive recovery of valuble metals from tungsten residues[D]. Changsha: Central South University, 2013.
[7] 史志铭. 钨渣在铸铁生产中的应用[J]. 内蒙古工学院学报(自然科学版), 1993, 12(1): 34-38.
SHI Zhi-ming. Proper application of tungsten slag in iron casting[J]. Journal of Inner Mongolia Institute of Technology (Natural Science Edition), 1993, 12(1): 34-38.
[8] 谢晓霞, 张辛辛. 我国钨渣回收利用研究现状和发展趋势[J]. 上海化工, 2014, 139(5): 26-29.
XIE Xiao-xia, ZHANG Xin-xin. The research status and development trend of tungsten residue recycling in China[J]. Shanghai Chemical Industry, 2014, 139(5): 26-29.
[9] 靖青秀, 王云燕, 柴立元, 唐崇俭, 黄晓东, 郭 欢, 王 魏, 游 威. 硅藻土一钨渣基多孔陶粒对离子型稀土矿区土壤氨氮淋滤液的吸附[J]. 中国有色金属学报, 2018, 28(5): 1033-1042.
JING Qing-xiu, WANG Yun-yan, CHAI Li-yuan, TANG Chong-jian, HUANG Xiao-dong, GUO Huan, WANG Wei, YOU Wei. Adsorption behavior of ammonium in leachate from ionic rare earth mining area soil by diatomite and tungsten residue based porous ceramsite[J].The Chinese Journal of Nonferrous Metals, 2018, 28(5): 1033-1042.
[10] JING Qing-xiu, WANG Yun-yan, CHAI Li-yuan, TAN Chong-jian, HUANG Xiao-dong, Guo Huan, WANG Wei, YOU Wei. Adsorption of copper ions on porous ceramsite prepared by diatomite and tungsten residue[J]. Transactions of Nonferrous Metals Society of China, 2018, 28(5): 1053-1060.
[11] 梁焕龙, 罗东明, 刘 晨, 谢营邦, 黄泰元. 从钨渣中浸出氧化钪的试验研究[J]. 湿法冶金, 2015, 34(2): 114-116.
LIANG Huan-long, LUO Dong-ming, LIU Chen, XIE Ying-bang, HUANG Tai-yuan. Leaching of scandium oxide from tungsten slag[J]. Hydrometallurgy of China, 2015, 34(2): 114-116.
[12] NIE H P, WANG Y B, WANG Y L, ZHAO Z Y, DONG Y M, SUN X Q. Recovery of scandium from leaching solutions oftungstenresidueusing solvent extraction with Cyanex 572[J]. Hydrometallurgy, 2018, 175: 117-123.
[13] 汪加军, 王晓辉, 黄 波, 郑诗礼. 废钨渣中钽、铌、钨高效共提新工艺研究[J]. 有色金属科学与工程, 2013, 4(5): 91-96.
WANG Jia-jun, WANG Xiao-hui, HUANG Bo, ZHENG Shi-li. New process of high efficient co-extraction of tantalum, niobium and tungsten from tungsten residue[J]. Nonferrous Metals Science and Engineering, 2013, 4(5): 91-96.
[14] 杨利群. 苏打烧结法处理低品位钨矿及废钨渣的研究[J]. 中国钼业, 2008, 32(4): 25-27.
YANG LI-qun. Study of processing low-grade tungsten mineral and waste residue of tungsten by soda sintering[J]. China Molybdenum Industry, 2008, 32(4): 25-27.
[15] 杨秀丽, 王晓辉, 向仕彪, 孙 青, 魏 昶, 郑诗礼.盐酸法富集钨渣中的钽和铌[J]. 中国有色金属学报, 2013, 23(3): 873-881.
YANG Xiu-li, WANG Xiao-hui, XIANG Shi-biao, SUN Qing, WEI Chang, ZHENG Shi-li. Enrichment of tantalum and niobium from tungsten residue by hydrochloric acid method[J]. The Chinese Journal of Nonferrous Metals, 2013, 23(3): 873-881.
[16] 张 立, 钟 晖, 戴艳阳. 钨渣酸浸与钠碱熔融回收钽铌的研究[J]. 稀有金属与硬质合金, 2008, 36(2): 6-14.
ZHANG Li, ZHONG Hui, DAI Yan-yang. Study on tantalum and niobium recovery by acid leaching and sodium alkali fusing from tungsten residue[J]. Rare Metals and Cemented Carbides, 2008, 36(2): 6-14.
[17] MACΠOB B H. Processing low grade material bearing tungsten by extraction of tungsten-iron alloy[J]. Non-ferrous Metallurgy, 1992(10): 42-46.
[18] 戴艳阳, 钟 晖, 钟海云.废钨渣中同时回收铁锰的试验研究[J]. 应用化工, 2009, 38(6): 924-927.
DAI Yan-yang, ZHONG Hui, ZHONG Hai-yun. Study on preparation of Zn-Mn ferrite powders from tungsten residue[J]. Applied Chemical Industry, 2009, 38(6): 924-927.
[19] КAPIIIYHOB B Г, 杨家驹. 低品位钨-锡原料综合处理方案[J].国外锡工业, 1994, 22(7): 1-5.
КAPIIIYHOB B Г, YANG Jia-ju. Low-grade tungsten-tin raw material comprehensive treatment scheme[J]. Foreign Tin Industry, 1994, 22(7): 1-5.
[20] 郭青蔚, 王肇信. 现代钽铌冶金[M]. 北京: 冶金工业出版社, 2009: 58-60.
GUO Qing-wei, WANG Zhao-xin. Modern tantalum niobium metallurgy[M]. Beijing: Metallurgical Industry Press, 2009: 58-60.
[21] 刘 琼, 陈 松. 电解法制备高纯铁的工艺研究[J]. 湿法冶金, 2013, 32: 105-108.
LlU Qiong, CHEN Song. Study on the preparation of high purity iron by electrolysis[J]. Hydrometallurgy, 2013, 32(2): 105-108.
[22] 赵秦生, 张 皑. 铁的电解和电镀[M]. 人民交通出版社, 1986: 80-101.
ZHAO Qin-sheng, ZHANG Ai. Electrolysis and electroplating of iron[M]. China Communications Press, 1986: 80-101.
[23] MILAZZO G, CAROLI S. 标准电极电位数据手册[M]. 吴维昌, 冯洪清, 吴开治. 北京: 科学出版社, 1991: 1-264.
MILAZZO G, CAROLI S. Tables of standard electrode potentials(1978)[M]. WU Wei-chang, FENG Hong-qing, WU Kai-zhi. Beijing: Science Press, 1991: 1-264.
[24] 侯 静. 含镓生铁电解分离实验研究[D]. 成都: 西华大学, 2011.
HOU Jing. The experimental study of contain gallium pig iron electrolysis separation[D]. Chengdu: Xihua University, 2011.
[25] 罗北平, 龚竹青, 郑雅杰, 杨余芳, 陈梦君. 因瓦合金箔电沉积的制备及其微观结构和耐蚀性[J]. 中南大学学报(自然科学版), 2006, 37(2): 263-268.
LUO Bei-ping, GONG Zhu-qing, ZHENG Ya-jie, YANG Yu-fang, CHEN Meng-jun. Surface microstructure and corrosion resistance of electrodeposited invar alloy foil[J]. Journal of Central South University (Science and Technology), 2006, 37(2): 263-268.
[26] 郑雅杰, 赵攀峰, 王 勇, 吕重安. 高电流密度电解对阴极铜质量的影响[J]. 中南大学学报(自然科学版), 2009, 40(2): 311-316.
ZHENG Ya-jie, ZHAO Pan-feng, WANG Yong, Lü Chong-an. Effect of electrorefining with high current density on cathode copper[J]. Journal of Central South University (Science and Technology), 2009, 40(2): 311-316.
[27] 杨 森, 孙 凯, 邓汉忠. 低温镀铁层显微组织的分析[J]. 电镀与环保, 2015, 35(6): 1-4.
YANG Sen, SUN Kai, DENG Han-zhong. Analysis on micro-structure of low-temperature iron plating coatings[J]. Electroplating & Pollution Control, 2015, 35(6): 1-4.
Recovery iron from Fe-W-Sn alloy powders by electrolysis
FAN Ke-biao1, ZHENG Ya-jie1, WANG Fang1, LI Hai-bo2
(1. School of Metallurgy and Environment, Central South University, Changsha 410083, China;
2. Zixing Hongjin Metallurgy Co., Ltd., Chenzhou 423400,China)
Abstract: The Fe-W-Sn alloy powders obtained by high-temperature reduction and smelting process of tungsten residue, as raw material, were electrolyzed to recover iron. And the effects of Fe2+ concentration, pH values, temperature and current density on current efficiency and purity of electrolytic iron were investigated. The results show that, under the optimal conditions of current density 300 A/m2, temperature 45 ℃, pH 4.5, and Fe2+ concentration 100 g/L, the current efficiency and purity of the electrolytic iron are 92.1% and 99.1%, respectively. The average current efficiency is 87.8% and the purity of electrolytic iron is above 97% after continuous electrolysis for 4 days under the optimal conditions. The contents of tungsten and tin in the anode slime are 19.7% and 20.0%, which are enriched 2.82 times and 2.89 times compared with the tungsten and tin contents of the raw materials(6.98% and 6.91%), respectively. Meanwhile, the recovery rate of iron is 92.2%, the anode slime yield is 33.0% and the power consumption for producing 1 t of electrolytic iron is 4757 kW・h. The SEM image shows that the morphology of electrolytic iron is irregular-shaped stick.
Key words: Fe-W-Sn alloy powder; electrolysis; electrolytic iron; current efficiency
Foundation item: Project(2017SK2254) supported by the Key Research and Development Program of Hunan Province, China
Received date: 2018-09-03; Accepted date: 2018-11-26
Corresponding author: ZHENG Ya-jie; Tel: +86-731-88836285; E-mail: zyj@csu.edu.cn
(编辑 何学锋)
基金项目:湖南省重点研发计划项目(2017SK2254)
收稿日期:2018-09-03;修订日期:2018-11-26
通信作者:郑雅杰,教授,博士;电话:0731-88836285;E-mail:zyj@csu.edu.cn