苏丹黑B染色法原位检测2株淡水小球藻胞内油脂累积
金雪洁1,巩三强1,夏金兰1, 2,聂珍媛1, 2
(1. 中南大学 资源加工与生物工程学院,湖南 长沙,410083;
2. 中南大学 生物冶金教育部重点实验室,湖南 长沙,410083)
摘要:以2株淡水小球藻Chlorella pyrenoidosa XJ01 和 Chlorella sorokiniana XJ02为研究对象,对苏丹黑B染色法测定微藻胞内油脂质量分数的条件进行优化,建立苏丹黑B染色法原位测定微藻油脂的方法;并在通气条件下,检测微藻脂质质量分数及脂质累积过程。研究结果表明:当辅助染色破壁的盐酸浓度为1.0 mol/L,染色时间和温度分别为10 min和100 ℃时,苏丹黑B染色效果最好;在不同生长阶段,C. sorokiniana XJ02胞内油脂质量分数均比 C. pyrenoidosa XJ01 的高;此外,2株藻胞内油脂质量分数在对数生长期中期开始快速增加,到生长稳定期油脂质量分数达到最高,C. pyrenoidosa XJ01和C. sorokiniana XJ02油脂质量分数最高分别为25%和38.2%,随后油脂质量分数开始缓慢降低;利用苏丹黑B将微藻细胞染色后在显微镜下观察到的胞内油滴结果与其胞内油脂测定结果基本相符。
关键词:苏丹黑B染色;小球藻;油脂累积;原位检测
中图分类号:Q939.97 文献标志码:A 文章编号:1672-7207(2014)08-2547-06
In-situ detection of lipid accumulation in two strains of Chlorella by Sudan black B staining
JIN Xuejie1, GONG Sanqiang1, XIA Jinlan1, 2, NIE Zhenyuan1, 2
(1. School of Minerals Processing and Bioengineering, Central South University, Changsha 410083, China;
2. Key Laboratory of Biometallurgy of Ministry of Education of China, Central South University, Changsha 410083, China)
Abstract: Sudan black B staining method was optimized and applied to measure lipid content and monitor the lipid accumulation in two oil-rich freshwater microalgae C. pyrenoidosa XJ01 and C. sorokiniana XJ02, respectively. The optimal HCl concentration for disrupting cell wall of microalgal strains is 1.0 mol/L, Sudan black B staining has the highest effectiveness when staining time and temperature are 10 min and 100 ℃, respectively. The conducted comparative test with traditional gravimetric method and stability test indicates that Sudan black B staining method can be regarded as a feasible method for quantification of lipids in microalgae in situ. Lipid in microalgal cells starts to accumulate from interim of logarithmic phase and reaches highest value at interim of stationary phase and then begin to decrease, which is consistent with the results of oil-droplet images obtained by microscope.
Key words: Sudan black B staining; Chlorella; lipid accumulation; in-situ detection
微藻作为地球上最古老的光合生物,与传统油料作物相比较,具备光合效率高、生长迅速、环境适应能力强、油脂质量分数高(某些藻种脂质质量超过细胞干质量的50%以上)的特点,因此,被认为是制备生物柴油的理想原料[1-6]。目前,有关微藻生物柴油的研究多数处于实验室研究阶段,微藻生物柴油的生产从实验室走向工业化还有许多问题需要解决。而获得生长快速的富油微藻及研究微藻在不同培养环境条件下脂质的累积过程是微藻生物柴油制备工艺的关键环节之一:因此,建立相应的原位检测胞内油脂质量分数的技术是解决富油微藻的快速筛选问题及深入研究不同条件下微藻细胞内的油脂累积规律的基础。微藻细胞个体小,细胞壁通常较厚,提取油脂时通常需要特殊破壁处理(加温加压、微波破碎、超声破碎等)才能达到较完全的萃取效果。传统的油脂提取方法主要有索氏提取法、有机溶剂法、酸热法等。虽然这些方法简便易行,但分析测定时间长、成本高,在萃取过程中需用大量有毒害作用的有机溶剂,不仅损害人体健康而且易造成环境污染等后果。超临界CO2萃取法也用于微藻油脂提取,但该方法需要昂贵的仪器设备才能完成[7-8]。另外,尼罗红荧光染料法作为一种新型的总脂含量测定方法逐渐受到学者们的关注。与传统脂质测定方法相比,尼罗红荧光染色法不需要破坏细胞、所需样品量少、快速灵敏[9]。然而,尼罗红染色法测定时需要荧光分光光度计和荧光显微镜,价格昂贵,且尼罗红染色后的荧光强度易受各种因子(染色时间、染色温度、尼罗红浓度、藻细胞密度、二甲亚砜浓度)的影响[10],特别是荧光强度极易在短时间内猝灭[11],加大了操作难度。苏丹黑B是一种脂溶性的染色剂,价格低廉,它能够与脂质结合形成黑色物质并在某一波长下有吸收峰,其吸收值的大小与微藻细胞总脂质量分数呈显著线性相关,广泛地用于检测真菌、酵母、动物细胞内油脂质量分数[12-14]。林汝榕等[15]以7种微藻为研究对象探讨了利用此染色方法处理微藻细胞以估测微藻油脂含量的可行性,结果证实苏丹黑B法适宜用来检测微藻油脂质量分数。但是,他们并未对该染色方法进行优化,也没有对微藻细胞内油脂质量分数及油脂累积进行检测。本文作者以2株淡水小球藻为研究对象,对影响苏丹黑B染色的因素进行摸索,并对主要影响因素进行实验优化,提高了染色效果;并利用经典有机试剂提取法对苏丹黑B定量结果进行验证。在此基础上,以2株淡水小球藻为研究对象,利用苏丹黑B染色法研究通气条件下小球藻细胞内油脂积累的规律。该研究建立了原位快速检测微藻油脂的方法,可用于产油微藻的快速筛选,对微藻细胞内油脂累积规律的深入研究也具有指导意义。
1 材料与方法
1.1 藻种和培养条件
所用微藻为本实验室筛选得到的2株淡水小球藻Chlorella sorokiniana XJ02 和Chlorella pyrenoidosa XJ01(18S rRNA Genbank 登录号分别为KC416208 和KC416209)。
实验在管状鼓泡式反应器(装液量为800 mL)中进行,利用BG-11培养基对微藻进行培养[16],pH=8.0~8.3,培养光照强度为6000 lx,培养温度为26 ℃,光与暗周期均为12 h,空气通气量为0.28 vvm。定期取适量藻液在光学显微镜下利用血球计数法测定微藻细胞数,以时间对藻细胞数绘制微藻生长曲线。
1.2 仪器设备
Avanti JE 台式高速冷冻离心机(美国贝克曼仪器公司生产);UV9200分光光度计(北京锐利分析仪器公司生产);50i正置荧光显微镜(日本尼康公司生产)。
1.3 苏丹黑B染色液的配制
利用无水酒精配制0.6%苏丹黑B 工作液。具体配制过程为: 准确称取0.6 g苏丹黑B溶解于100 mL无水乙醇中,混合均匀,置沸水浴煮沸10 min,促进苏丹黑的溶解;然后于10 000 r/min转速下高速离心20 min, 取上清,上清液利用孔径为0.22 μm滤膜过滤,滤液收集置温度为4 ℃的冰箱冷藏备用。
1.4 染色后微藻细胞光吸收特性的测定
取2支试管,各加入5 mL微藻培养液和5 mL HCl溶液(1 mol/L)充分混匀后,一管中加入0.4 mL苏丹黑B工作液;在另一管(对照管)中加入0.4 mL无水乙醇,充分混匀,在沸水浴中加热10 min(不时摇动,使受热均匀),冷却后以6 000 r/min转速离心10 min。取出微藻细胞沉淀物,用50%乙醇洗涤3次后,加入70%乙醇溶液,混匀,利用UV-9200分光光度计测定其特征吸收峰。
1.5 染色后微藻油脂含量标准曲线绘制及其可行性验证
采用传统有机溶剂法提取并测定微藻生长稳定期前期一定体积微藻培养液的胞内油脂质量分数[17],即将一定体积微藻培养液,离心干燥后的干藻粉称质量,加入氯仿与甲醇(体积比为1:2)混合液,再加入一定体积水,使氯仿、甲醇、水的体积比为1:1:0.9,振荡摇匀,在6 000 r/min下离心10 min,取下层氯仿油脂相并用5% NaCl溶液漂洗。通风挥发干燥后,测得微藻总脂质量。然后,将原微藻细胞培养液稀释成5个藻浓度梯度,分别为原液浓度以及5/6,2/3,1/2,1/3和1/6原液浓度,按上述苏丹黑B染色方法对各个梯度的微藻细胞进行染色,在最大吸收波长(610 nm)下测定其吸光值。利用上述传统方法已测得的微藻总脂质量分数,换算出各个梯度下微藻细胞所含的油脂质量分数,从而绘制出吸光值OD610与对应油脂质量分数之间的相关性曲线。
取一定量的待测微藻细胞培养液稀释成2个梯度,分别为原溶液浓度的1/4和1/8,按上述苏丹黑B染色法对2个梯度的微藻细胞进行染色,在610 nm波长光下测定其吸光值,将吸光值OD610代入相应的标准曲线回归方程计算,求得微藻细胞油脂质量分数。将该值与上述采用传统有机溶剂法获得的油脂质量分数进行比较,检验由测定吸光值计算出的微藻细胞油脂质量分数的准确性。
1.6 微藻细胞内油脂累积的检测
取不同培养阶段的一定量待测微藻培养液,用上述苏丹黑B染色法对其进行染色,在610 nm波长光下测定其吸光值,将此吸光值OD610代入相应的标准曲线回归方程,求出微藻细胞油脂质量分数,从而绘制出不同培养阶段微藻胞内油脂质量分数与对应培养时间的关系图。同时,对染色后微藻细胞在正置荧光显微镜下进行胞内油脂脂滴的观察并拍照。
2 结果与讨论
2.1 苏丹黑B染色方法的优化
2.1.1 苏丹黑B染色后微藻细胞的光吸收特性测定
图1所示为2株微藻细胞被苏丹黑B染色后的细胞吸光值曲线,没有染色的细胞吸光值曲线为对照。结果表明:染色后,叶绿素吸收峰(680 nm)明显向短波方向移动,并在610 nm 处出现苏丹黑B与脂质结合的特征性吸收峰。
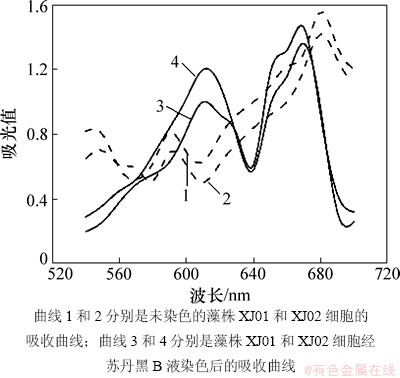
图1 小球藻C. pyrenoidosa XJ01 和 C. sorokiniana XJ02细胞受到苏丹黑B染色前后的光吸收曲线
Fig. 1 Absorption curves of C. pyrenoidosa XJ01 and C. sorokiniana XJ02 cells before and after stained by Sudan black B
2.1.2 典型影响因素对染色效果的影响
微藻细胞胞壁通常较厚,染液进入细胞与胞内油脂结合较困难,因此,有必要考察染色时典型因素对苏丹黑B染色效果的影响。图2所示为盐酸浓度、染色时间、温度及染色后放置时间对苏丹黑B染色效果的影响。由图2(a)可见:当盐酸浓度为1.0 mol/L时染色效果最佳,过低或过高浓度盐酸染色效果都较差。这可能是低浓度的盐酸溶液不能完全溶解微藻细胞壁,在一定程度上阻碍了苏丹黑B进入微藻细胞并与细胞内脂质结合,使吸光度较低。而过高浓度的盐酸在高温条件下可能导致细胞膜的裂解,细胞内脂质释放到胞外,导致吸光值下降。由图2(b)可见:染色时间对染色效果影响不显著,但染色时间为10 min时效果相对较好。由图2(c)可见:染色温度为100 ℃时染色效果最好。由图2(d)可见:苏丹黑B染色法相当稳定,在染色后2 d内所测得的吸光值基本保持不变。因此,在实验操作中,苏丹黑B染色对操作时间要求较低,与尼罗红染色后荧光强度极易在短时间内猝灭的特性相比[11],这是苏丹黑B染色法的突出优势。
2.2 微藻胞内油脂质量分数标准曲线的建立及其可行性验证
2.2.1 微藻胞内油脂质量分数标准曲线的建立
按1.4节所述方法建立油脂质量分数标准曲线,结果如图3所示。藻株XJ01和XJ02的线性关系式分别为y=2.145 4x+0.345 4(相关系数R=0.994 2)和y= 3.331 8x+0.292 8(相关系数R=0.996 2)。结果表明:不同梯度的微藻细胞样品经苏丹黑B染色处理后,微藻细胞的油脂质量分数和吸光值存在良好的线性关系。因此,通过测定染色后微藻细胞的吸光值,然后采用标准曲线线性回归方程式,可计算出微藻细胞内油脂质量分数。
2.2.2 苏丹黑B染色法测定微藻油脂质量分数方法的可行性验证
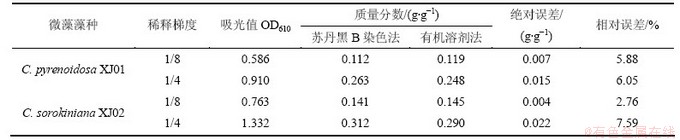
为验证上述所得回归方程的准确性以及应用苏丹黑B染色法测定微藻胞内油脂质量分数的可行性,比较由回归方程式计算的微藻油脂质量分数和采用传统有机溶剂法得到的微藻油脂质量分数,考察2种结果的差异性,分析结果如表1所示。验证结果证明:采用苏丹黑B染色法测得的油脂质量分数与传统方法测得的微藻油脂质量分数很接近,相对误差在常规可允许的10%范围内,因此,采用苏丹黑B染色处理技术,可达到方便、准确检测微藻细胞油脂质量分数的效果,是检测微藻细胞油脂质量分数的好方法。

图2 盐酸浓度(a),水浴加热时间(b),水浴温度(c)和放置时间(d)对染色效果的影响
Fig. 2 Influences of HCl concentration (a), water bathing time (b), water bathing temperature (c) and staying time (d) on staining effect
表1 基于染色后吸光值测得微藻样品油脂质量分数与传统方法的对比
Table 1 Comparison of lipid content in C. pyrenoidosa XJ01 and C. sorokiniana XJ02 determined by Sudan black B staining method and traditional gravimetric method
2.3 利用苏丹黑B法检测2株淡水小球藻胞内油脂质量分数及油脂积累
图4所示为小球藻C. pyrenoidosa XJ01 和 C. sorokiniana XJ02培养14 d内的生长曲线和胞内油脂质量分数的变化情况。由图4可见:在14 d的培养期间,2株小球藻从最初接种浓度3.8×107 个/mL增大到9.0×107 个/mL。2藻株的油脂质量分数在前4 d明显降低,可能原因是培养前4 d藻细胞对新的培养环境(pH、光照)还不太适应,生长处于适应期,胞内油脂被作为碳源用于满足细胞的生长需要。但随着细胞生长进入对数期,油脂质量分数便开始快速增大,且在培养第10天时达到最高,C. pyrenoidosa XJ01 和 C. sorokiniana XJ02油脂质量分数最高分别为25 %和38.2 %,此后又开始有所下降。下降的原因可能是进入稳定期O2等代谢物累积以及部分细胞受到光照减少,细胞的光合作用降低,而光呼吸作用增强。
图5所示为将2株小球藻培养第6,10和14天后对它们的细胞进行苏丹黑B染色后在光学显微镜下观察拍照结果。由图5可见:微藻细胞中的油脂脂滴被染成了黑色,随着细胞的生长,胞内油脂脂滴质量分数逐渐增加,第10天质量分数达最高,第14天都有所下降,且小球藻C. sorokiniana XJ02中油脂含量在各阶段均比C. pyrenoidosa XJ01中要高,此结果与图4中测到的油脂质量分数结果相一致。这进一步表明,苏丹黑B染色法可用于微藻胞内油脂脂粒的观察和油脂质量分数的检测,具有简便快、速的特点。

图3 苏丹黑B法测定微藻C. pyrenoidosa XJ01 和C. sorokiniana XJ02油脂质量分数的标准曲线
Fig. 3 Linear correlation between lipid mass fraction of microalgal strains and optical density of C. pyrenoidosa XJ01 and C. sorokiniana XJ02

图4 小球藻C. pyrenoidosa XJ01 和C. sorokiniana XJ02生长曲线及油脂质量分数变化
Fig. 4 Growth and lipid mass fraction curves of C. pyrenoidosa XJ01 and C.sorokiniana XJ02 over a 14-day cultivation

图5 小球藻C. pyrenoidosa XJ01和C. sorokiniana XJ02不同生长阶段胞内油脂脂滴累积
Fig. 5 Images of lipid mass fraction of C. pyrenoidosa XJ01 and C. sorokiniana XJ02 in different periods of growth
3 结论
(1) 建立了苏丹黑B染色法测定2株淡水小球藻胞内油脂含量及油脂累积的方法。该方法能够用于微藻胞内油脂的原位快速检测。
(2) 2株淡水小球藻在生长的不同阶段胞内油脂质量分数不同,C. sorokiniana XJ02细胞内油脂质量分数均高于 C. pyrenoidosa XJ01 胞内油脂质量分数。且2株藻胞内油脂质量分数均在生长对数期中期开始快速增加,到生长稳定期时油脂质量分数达到最高,C. sorokiniana XJ02和C. pyrenoidosa XJ01油脂含量最高分别为38.2%和25%,随后油脂质量分数开始缓慢降低。
(3) 利用苏丹黑B将2株小球藻细胞染色后,在显微镜下观察到的胞内油滴累积与其胞内油脂测定结果基本相符。
参考文献:
[1] Huang Y Y, Beal C M, Cai W W, et al. Micro-Raman spectroscopy of algae: Composition analysis and fluorescence background behavior[J]. Biotechnology and Bioengineering, 2010, 105(5): 889-898.
[2] Christenson L, Sims R. Production and harvesting of microalgae for wastewater treatment, biofuels, and bioproducts[J]. Biotechnology Advances, 2011, 29(6): 686-702.
[3] Singh R N, Sharma S. Development of suitable photobioreactor for algae Production-a review[J]. Renewable and Sustainable Energy Reviews, 2012, 16(4): 2347-2353.
[4] Chisti Y. Biodiesel from microalgae[J]. Biotechnology Advances, 2007, 25(3): 294-306.
[5] Reda A I, Abou-Shana I A, Matter S K, et al. Characterization and identification of lipid-producing microalgae species isolated from a freshwater lake[J]. Biomass and Bioenergy, 2011, 35(7): 3079-3085.
[6] 缪晓玲, 吴庆余. 微藻油脂制备生物柴油的研究[J]. 太阳能学报, 2007, 28(2): 220-222.
MIAO Xiaoling, WU Qingyu. Study on preparation of biodiesel from microalgal oil[J]. Acta Energy Solaris Sinica, 2007, 28(2): 220-222.
[7] Mendiola J A, Jaime L, Santoyo S, et al. Screening of functional compounds in supercritical fluid extracts from Spirulina platensis[J]. Food Chemistry, 2007, 102(4): 1357-1367.
[8] Canela A P R F, Rosa P T V, Marques M O M, et al. Supercritical fluid extraction of fatty acids and carotenoids from the microalgae Spirulina maxima[J]. Industrial and Engineering Chemistry Research, 2002, 41(12): 3012-8.
[9] Chen W, Zhang C, Song L, et al. A high throughput Nile red method for quantitative measurement of neutral lipids in microalgae[J]. Journal of Microbiological Methods, 2009, 77(1): 41-47.
[10] Uri P, Tatyana R Z. Kinetic anomalies in the interactions of Nile red with microalgae[J]. Journal of Microbiological Methods, 2012, 88(2): 189-196.
[11] Govender T, Ramanna L, Rawat I, et al. BODIPY staining, an alternative to the Nile Red fluorescence method for the evaluation of intracellular lipids in microalgae[J]. Bioresource Technology, 2012, 114: 507-511.
[12] Subramaniam H N, Chaubal K A. Evaluation of intracellular lipids by standardized staining with a Sudan black B fraction[J]. Journal of Biochemical and Biophysical Methods, 1990, 21(1): 9-16.
[13] Thakur M S, Prapulla S G, Karanth N G. Estimation of intracellular lipids by the measurement of absorbance of yeast cells stained with Sudan black B[J]. Enzyme and Microbial Technology, 1989, 11(4): 252-254.
[14] Feng W J, Huang W M, Xu X P, et al. Using different dyes to label storage fat in C. Elegans[J]. Life Science Research, 2012, 16(1): 10-14.
[15] 林汝榕, 邢炳鹏, 蔡文旋, 等. 苏丹黑B染色处理细胞技术在快速检测微藻油脂含量中的应用[J]. 台湾海峡, 2011, 30(2): 293-298.
LIN Rurong, XING Bingpeneg, CAI Wenxuan, et al. Rapid detection of microalgal lipid content through Sudan black B staining[J]. Journal of Oceanography in Taiwan Strait, 2011, 30(2): 293-298.
[16] Phukan M M, Chutia R S, Konwar B K, et al. Microalgae Chlorella as a potential bio-energy feedstock[J]. Applied Energy, 2011, 88(10): 3307-3312.
[17] Yoo C, Jun S Y, Lee J Y, et al. Selection of microalgae for lipid production under high levels carbon dioxide[J]. Bioresource Technology, 2010, 101(1): S71-S74.
(编辑 邓履翔)
收稿日期:2013-08-19;修回日期:2013-10-12
基金项目:湖南省研究生创新学位论文资助课题(2010ssxt246), 中南大学创新教育资助课题 (2010bsxt05, CL11029, CL11038)
通信作者:夏金兰(1964-),男,湖南攸县人,博士,教授,从事生物能源与材料及矿物生物提取的研究;电话:0731-88836944;E-mail:jlxia@csu.edu.cn