þ�Ͻ𣺳ɷ֡���֯����ȼ
��Դ�ڿ����й���ɫ����ѧ��2021���3��
�������ߣ����� ������ ���ٲ�
����ҳ�룺598 - 623
�ؼ��ʣ�þ�Ͻ𣻳ɷ֣���֯��������������ȼ
Key words��magnesium alloy; composition; microstructure; high temperature oxidation; ignition resistance
ժ Ҫ��þ�Ͻ���е��ܶȡ��߱�ǿ�Ⱥͱȸնȣ��ǽ�ͨ��������DZ�ڵ����ʽṹ���ϡ�Ȼ����þ�Ͻ�Ŀ����������Բ����ȼ����������Ӧ�á�������ϸ������þ�Ͻ��ڿ����и���������ȼ�յĻ���ԭ���Լ�þ�Ͻ����������Ӱ�����أ��ܽ���þ�Ͻ������������ȼ�о���չ������Ŀǰ�������þ�Ͻ�����ģ�����ۣ���Ca��Be��Sr��ϡ����Ԫ�غϽ�þ�Ͻ���ȼ�������������ȼþ�Ͻ��ڷ�չ������������һЩ���⣬��ָ������ܵķ�չ����
Abstract: Magnesium alloys as potential lightweight structural material in the transportation field have low density, high specific strength and specific stiffness. However, the poor high-temperature oxidation resistance and flammability of magnesium alloys limit their application. This article described the basic principles of high-temperature oxidation and combustion of magnesium alloys in the air, and the influencing factors of high-temperature oxidation in detail. The research progresses of high temperature oxidation and ignition resistance of magnesium alloys were summarized, including the oxidation resistance model theory and the flame retardant mechanism alloying with elements such as Ca, be, Sr, rare earth elements, etc. Some problems encountered in the development of flame retardant magnesium alloys were put forward and the possible development directions were pointed out.
DOI: 10.11817/j.ysxb.1004.0609.2021-40013
�� ��1��������1�����ٲ�1, 2
(1. ɽ���Ƽ���ѧ ���Ͽ�ѧ�빤��ѧԺ���ൺ 266590��
2. ֣�ݴ�ѧ ���Ͽ�ѧ�빤��ѧԺ��֣�� 450002)
ժ Ҫ��þ�Ͻ���е��ܶȡ��߱�ǿ�Ⱥͱȸնȣ��ǽ�ͨ��������DZ�ڵ����ʽṹ���ϡ�Ȼ����þ�Ͻ�Ŀ����������Բ����ȼ����������Ӧ�á�������ϸ������þ�Ͻ��ڿ����и���������ȼ�յĻ���ԭ���Լ�þ�Ͻ����������Ӱ�����أ��ܽ���þ�Ͻ������������ȼ�о���չ������Ŀǰ�������þ�Ͻ�����ģ�����ۣ���Ca��Be��Sr��ϡ����Ԫ�غϽ�þ�Ͻ���ȼ�������������ȼþ�Ͻ��ڷ�չ������������һЩ���⣬��ָ������ܵķ�չ����
�ؼ��ʣ�þ�Ͻ𣻳ɷ֣���֯��������������ȼ
���±�ţ�1004-0609(2021)-03-0598-25���� ��ͼ����ţ�TG146.22���� ���ױ�־�룺A
���ĸ�ʽ���� ��, ������, ���ٲ�. þ�Ͻ𣺳ɷ֡���֯����ȼ[J]. �й���ɫ����ѧ��, 2021, 31(3): 598-622. DOI: 10.11817/j.ysxb.1004.0609.2021-40013
SONG Xiang, WANG Zhong-wei, ZENG Rong-chang. Magnesium alloys: Composition, microstructure and ignition resistance[J]. The Chinese Journal of Nonferrous Metals, 2021, 31(3): 598-622. DOI: 10.11817/j.ysxb.1004.0609.2021-40013
þ�Ͻ���Ϊ����Ľ����ṹ����[1-2]�����иߵı�ǿ�Ⱥͱȸնȡ����õĿ�����Ժ������ԡ�����ĵ�������Ժ͵����Ե��ŵ㣬��Ӧ���ڽ�ͨ��ͨѶ�����ӵ�����[3-5]����������������Դ��ȱ��CO2�����������ŷŵ�һϵ�л������⣬Ϊ�����ȼ��Ч�ʺͼ������������ŷţ���������·�ͺ��պ��칤ҵ�����ʲ��ϵ������������С���ˣ�þ�Ͻ�Ӧ��Խ��Խ�ܵ����ӡ�Ȼ����þ�Ͻ���и�ѧ���ԣ���400 �����ϵĸ��������������ص������������ȼ�գ��������صİ�ȫ����������������㷺Ӧ�ã��ر����ڸ����ͺ��պ�������[6]������þ�Ͻ���нϸߵ�ȼ�շ����Ҳ�������Ϩ��һֱ������ֹ�����÷ɻ���ʹ��þ�Ͻ�[7]��Ȼ����2012�꣬���պ���淶ίԱ�������չ�����(FAA)�����˼���þ�Ͻ���ģ������¹��еİ�ȫ�ԣ�����Elektronϵ��þ�Ͻ����ο��ͨ���˰�ȫ�Բ��ԣ����ϰ�ȫ������ǰ�ڷɻ�������ʹ��þ�Ľ������ȡ��[8]�����������������Ƕ�����ȼþ�Ͻ���о���Ȥ����ˣ�ȫ���˽�þ����Ͻ��ڸ�����������ȼ����Ϊ��������������������ȼþ�Ͻ𣬶����ؿ�þ�Ͻ��Ӧ�������Ե���Ϊ��Ҫ��
þ�Ͻ��ڸ��»����У����Ȼᷢ����������ʱ�䱩¶�ڸ��¿�����ʱ������Ӧ�Ӿ磬�������ʻ���ֳ�����������֮��þ�Ͻ���ܻᷢ�����ȼ�գ�ֱ�����Ĵ�����þ�Ͻ�ĸ���������ȼ���������[9]��ȼ���Ǹ���������������̣��Ǿ��ҵ�������Ϊ[10]��Ϊ�����þ�Ͻ�����������������Ԫ�غϽ�Ϊ���ǵ��о��ص㡣�о��������Ͻ������þ�Ͻ�ȼ��Ϳ��������ر����ڸ����¿������Ե�һ����Ч����[11-14]��Ŀǰ������þ�Ͻ���ȼ��Ԫ����Ca��Be��Sr��ϡ��Ԫ��[14-16]��������ϸ������þ�Ͻ�ĸ����������̣��ص��ܽ����й�þ�Ͻ���ȼ���о���չ������þ�Ͻ����е���ȼģ�ͺ���ȼԪ�ص���ȼ������
1 þ�Ͻ�ĸ���������ȼ��
���ڶ�����(O2)�ĸ߶����ԣ�þ�Ͻ��ڸ����±�¶�ڿ�����ʱ�������ױ��������ڿ����У�þ�Ͻ�ĸ�������ͨ���漰���������߶���ѧ�ij�ʼ�����κͺ����������Զ���ѧ�ļ���������[17-18]����һ���¶ȷ�Χ�ڣ�þ�Ͻ����һ���Ŀ������ԣ�����������ѧ�����������͡���������һ�¶����䣬����ִ������߶���ѧ�����Զ���ѧ��ת�䣬�յ�ij��ֱ�־�ż��������Ŀ�ʼ����ˣ�þ�Ͻ����������ѧ�����ٽ��¶ȣ�ֻ�г����ٽ��¶ȲŻ���ּ��������Ρ��ٽ��¶��ӺϽ�ɷֶ�����һ��Ϊ400 ����450 ��[19]���������͵������α���Ϊ����������(Oxidation incubation period)���ڴ��ڼ䣬���ܵı������������γɣ���������������е���������[20]������������������DZ����������������������γɵı��������������[10, 20-21]������ͨ���������߹���þ�Ͻ�������������ںͼ���������Ӧ��ʼ��ʱ�䡣��ͼ1��ʾ����470 K��AZ91�Ͻ��������ʺ�С���������ڲ��䡣��֤�����ڵ����ٽ��¶������¼��������β�����֣����ᷢ�������Ե���������710 K��������ԼΪ25 min����760 K�������ڽ���Լ13 min�����������������Խ��͡��о������������¶ȵ����ߣ�þ�Ͻ�ĸ������������ڻ�����[22-24]����þ�Ͻ�����Ľ�����������Ρ���ˣ����þ�Ͻ���������������ȼ����ʵ���Ͼ����ӳ�þ�Ͻ�ĸ������������ڡ�
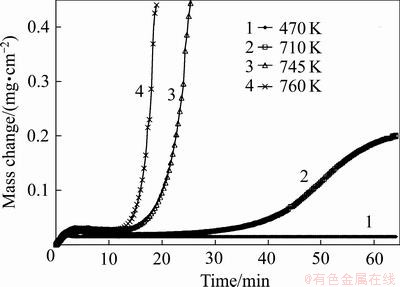
ͼ1 AZ91��̬þ�Ͻ��ڲ�ͬ�¶���������ʱ��仯����������[17]
Fig. 1 Thermogravimetric curves of mass change versus time for as-cast AZ91 in air at different temperatures[17]
þ�Ͻ�ĸ��������漰Mg��������Mg2+�ľ�����ɢ�ȶ�����̣������ս������������Ӧ���Ļ��۵�������������ѣ�������Mg��������ͼ2��ʾΪþ�Ͻ��ڸ���������ֱ��ȼ�ս�����ʾ��ͼ���������ڣ�þ�Ͻ��������������������ı����������㣬��ͼ2(a)��ʾ���ò�ͨ������������������Ϊ�Ͻ��ṩ��һ���̶ȵı���[17, 25]����ʱ�������߶���ѧ�ij�ʼ�����Σ�Ҳ���Ǹ������������ڽΡ����ŷ�Ӧ�Ľ��У����������ͬʱMg2+������ɢ�������ڲ��γɿ�λ���ڽ���/������������γɿ�϶����Щ��϶������ֲ�Ӧ������������������[21]�����⣬Mg�ڸ������������ʺܿ�[26-27]��þ�������������¾ۼ�ʹ�þֲ���ѹ�����ߣ�������ȱ�ݲ����ľֲ�Ӧ����ͬ���ã��ٽ��˱�Ĥ�����ѣ���ͼ2(b)��ʾ��Mg��������Mg���������ĵ���������һ����Ϊ���������Ƶij��������������ڵĽ���[17, 28]��֮����þ�Ͻ���������Ŀ�ʼ����Щ���Ƴ䵱��þ�����Ĵ���ͨ��[20]��ʹ��Mg�����ഫ�䲻���ܱ��������������ơ��˺�þ������O2���Ժ����ش������Ʋ��ںϽ�/���������洦���Ӧ���������ں�����洦�γɶ������þ[28]����ˣ���ͼ2(c)��ʾ�������������У����������������⣬�Ͻ����Ҳ��������̬�仯������γɵ�MgO����ƽ����������̬��Ϊ��ļ�״��̬���������������������������ӣ��������ʼӿ죬��ѭ���Զ���ѧ���ɣ���ͼ1������3��4��ʾ�����������ļ�����þ���������״������������ƽ���������/�������棬��O2���ٷ�����Ӧ���Ӷ��γ�������µ�����ͼ2(d)��ʾ������Mg��O����ɢ�����ܵ����ƣ���֮þ����������������Mg��O2֮��ĽӴ�������ٽ���������Ӧ��������µ����ڱ��������չ���γ������ɶ�������㣬��ͼ2(e) ��ʾ�����������Ե�������
����¶��㹻�ߣ�ʹ���������������þ�Ͻ�����Լ��ȴ������ĵ���������������Ӧ��������У����յ���þ�Ͻ���ȼ�ա�PRASAD��[29-30]�о���һϵ��Mg�Ͻ��ȼ�գ����������е������У�þ�Ͻ�����ֱ�������Ӵ��ļ���ۻ���ſ�ʼȼ�ա���ˣ����̬��Һ̬��þ�Ͻ������ȼ�ա�
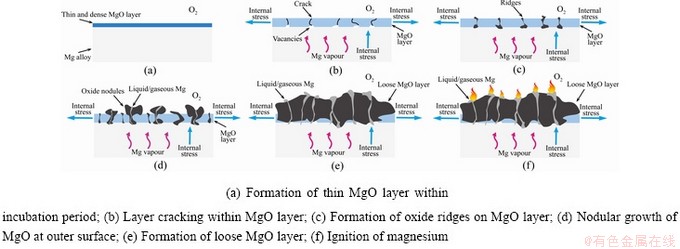
ͼ2 þ�Ͻ����������ȼ��ʾ��ͼ[14, 31]
Fig. 2 Schematic of high temperature oxidation and burning of Mg alloy[14, 31]
��Ҫָ�����ǣ�þ������ά��þ�Ͻ�ȼ�յ����ʣ����ۻ�������þ�Ͻ�����Ⱦ�������þ�Ͻ��ȼ����ܵ����۵�[7]����ͼ2(f)��ʾ������������Ӧ�Ľ��У�þ�Ͻ���¶Ȼ�������ߣ�Һ̬����̬��Mgͨ�������������ԴԴ���ϵ�������ɢ���������Mg��O2�ķ�Ӧ��������������ȼ�ա�Mgȼ�յ�ͬʱ������Mg��������ͬʱ�ų��������ȣ������þ�Ͻ��ܹ�����ȼ�ն�����Ϩ��[19]�����˻�״����̬��þ�Ͻ�ȼ�պ�ĵ�����ò������
2 Ӱ������
һ��������Ӱ��þ�Ͻ��Ż����Ե���Ҫ���ؿɷ�Ϊ�ⲿ���غ��ڲ�����[7]���ⲿ���ذ����Ͻ�ļ�����״��������Ũ�Ⱥͷ�ѹ�����Ե����͡����ȵ����ʵ�[8]��Ŀǰ������һ�������ȼ�������������ȼþ�Ͻ�Ŀ������Ժ���ȼ�ԣ������о��������úϽ�ļ�����״�����Է���������ͬ���ó������ݿ��ܻ��кܴ������磬���ڴ�Mg���ԣ�þ����ȼ��ԼΪ640 ��[27]��þ����ȼ��ԼΪ504 ��[11]��þ�۵�ȼ��ԼΪ437 ��[32]���ɴ˿ɼ���������״����þ�Ͻ��ȼ��Ӱ��ܴ��ڽ��в���ʱ������ȷָ����Ʒ�ļ�����״��LIU��[33]�о��˲�ͬ�������ʶ�þ�Ͻ�ȼ���Ӱ�죬�������ż������ʵ����ӣ�þ�Ͻ��ȼ����Ӧ��ߡ���ԭ���ǵ͵ļ�������ʹ�ø����þ�����ۼ������þ�Ͻ�����ױ���ȼ������ѹ�����߿������ӺϽ������ų���������������ĺ�ȣ�����Ӱ��Ͻ�ĸ���������ȼ����Ϊ[7, 34]��
���þ�Ͻ����ȼ���ܵIJ����о�����������˺ܶ���Է�����������µ���¯���ȡ��������Dz��ԡ���ֱȼ�������[7-8]����Ŀǰ����þ�Ͻ��ȼ������û�й̶�ͳһ�IJ��Ա�����ǰ������ÿ�ֲ��Է�����ʹ�õĺϽ���״�Ͳ�������������ͬ���������ݺͽ��֮�䲻�ܽ��бȽϡ����Ǹ��о��߶��ڿ���������ȼ������̽�ֵó��Ľ��۴���һ���Ĺ��ԡ���ˣ������ص���ܷ����ڲ����أ���þ�Ͻ��в�ͬ�Ͻ�Ԫ�ع��е����ʺ����û�����������������Ľṹ�����ܡ������仯�����ڶ��ࡣ
2.1 �Ͻ�Ԫ��
ͨ��������ͨ��Pilling-Bedworth��(PBR, RPB)����ʾ�ڽ������γɵ�������ı���������PBR���Ա�ʾΪ��
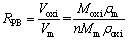 (1)
(1)
ʽ�У�Voxi�ǽ���������Ļ�����Ԫ�������Vm����Ӧ�����Ļ�����Ԫ�������Moxi����������ӵ�Ħ��������MmΪ����ԭ�ӵ�Ħ��������n��һ��������������������ԭ��������m��ʾ�����ܶȣ���oxi��ʾ�������ܶȡ�
PBR�ǽ�����������ڽ����������ɵ��������������������Ľ���ԭ�����֮�ȡ���ӳ������Ĥ�е�Ӧ��״����þ�Ͻ����ȼ������������������������ʺ�����ȼ����Ϊ֮�����������ϵ[35]��PBR��1~2֮��Ľ����������������Ĥ�в���һ���̶ȵ�ѹӦ����Ĥ���������ܣ�������������ǿ����Ӧ����ȼ��ߣ�PBRС��1�����2ʱ��������Ĥ�в�����Ӧ��������ѹӦ�����������Ĥ���ѣ������������Բ�[36]��MgO/Mg��PBRֵΪ0.81������MgO����нϴ���ڲ���Ӧ����Ĥ��ṹ��ɢ��������������������ڲ�Ӧ�������ӣ����������㿪�ѣ�����Ϊ�Ͻ��ṩ��������˴�Mg�Ŀ����������ϲ�[37]�����ֳ��������������PBRֵ����1��
��1 ���ֽ���Ԫ�ؼ�����Ӧ�������PBR[19, 38-39]
Table 1 PBR of some metal elements and their corresponding oxides[19, 38-39]
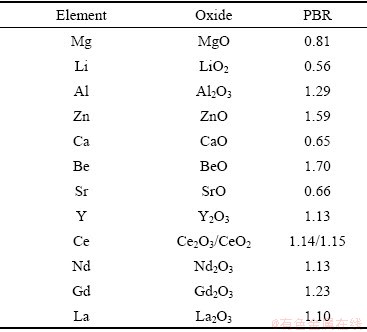
��ǰ������þ�Ͻ����ȼ�����ȼǰ��������������������ʺ�����ȼ����Ϊ֮��ͨ�����ڹ�����ĿǰPBRģ������õĻ���ģ�ͣ�þ�Ͻ�ֵĿ�������������ȼ�����������ø�ģ�������͡�����ģ�Ͷ��ڲ��ֺϽ����ã�����Mg-Sr��Mg-Beϵ�Ͻ𡣾�KIM��[11]������Sr��Mg�еĹ��ܶ�(Ħ������)��������0.03%���������Ԫ�صı�����۲��㡣���⣬SrO��RPB=0.66��1�������γ����ܵ�����������ֹ������þ�����ķ�Ӧ��Ȼ��Sr�������ܴ�����þ�Ͻ��ȼ�㣬�������Ե���ȼЧ��[35]������Mg-Be�Ͻ𣬾���Be��þ�еĹ��ܶȼ���Ϊ�㣬����������Ϊ10-6��������þ�Ͻ���BeO���γ�������ѧ���Dz����еģ����������������������Be�����Ͻ���ɴ����ǿþ�Ͻ�Ŀ�������[40-41]����ˣ���������Ҫ��һ���������ƣ�����AYDIN��[42]��Ϊ�ڿ��������������Ե�ͬʱ����Ҫ�����������O2��ͨ�ԣ��������O2��ͨ�Ժã���������ֹ�Ͻ��ڲ�����Ľ�һ��������
2.1.1 ��Ӧ��Ԫ��(Reactive element)
����Ӧ��Ԫ��ЧӦ��(REE)�漰�Ͻ���������и������ķ�Ӧ��Ԫ��(RE)�Ͻ��������ǿ����������ı����Ե�Ӱ�졣�ݱ�����ϡ����Ca��Be��Ԫ�ش��ڷ�Ӧ��Ԫ��ЧӦ[7, 38, 43]��REEģ��ʾ��ͼ��ͼ3��ʾ��һ����RE������MgO��Ŀ�϶���ѷ��У�����������Ӧ�γ�REO�����������ȱ��[7]����һ���棬����CZERWINSKI[31]��TAN��[38]�����ۣ�REO�ᷢ�����·�Ӧ��
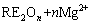 =
=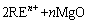 (n=2, 3) (2)
(n=2, 3) (2)
�ڸ������������У�����MgO���������REO�ֽ⣬ͨ��ʽ(2)��Ӧ����REn+�������þ���硣��ͼ3��ʾ��REn+������þ�����ƫ����Ч���谭��Mg2+����ľ�����ɢ��O2��������ɢ��ʹ���������ʼ�����
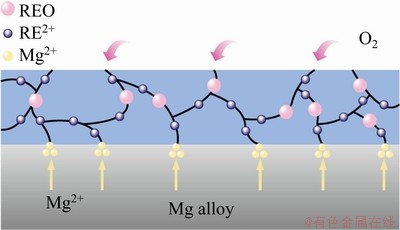
ͼ3 þ�Ͻ����������Ӧ��Ԫ��ЧӦ����ͼ[38]
Fig. 3 Effect mechanism diagram of high temperature oxidation reactive elements of magnesium alloy[38]
2.1.2 �������Ԫ��(Surface-active elemental)
�������Ԫ��(��Sr��Ca��ϡ��Ԫ��)�Ǿ��н���Һ̬�����ı����ܺͱ������������ֳ�ƫ�������ڽ�����������Ƶ�����[38]�����ֱ���ƫ����ı�Һ̬�����ı�����ɡ�������Ϊ���������ʣ��Ӷ����¡��������Ԫ��ЧӦ��(SAEE)[35]���ڶ�Ԫ�û��������У�Wigner-Seitz�뾶�ϴ��Ԫ��(ƽ�������ܶȽϵ�)������ƫ����Һ̬�������沢���ͱ�����[38]���������Ԫ�������ۼ������������������Ѹ����Һ̬�����������е�����[35]���Ӷ���ֹ��O2���ڲ��Ͻ�ĽӴ�������˺Ͻ�Ŀ��������������⣬���ɷֵķ�����ѹ���¶ȺͺϽ�ɷֵı仯���仯���������Ԫ�������ۼ������Խ���Һ̬�Ͻ�Mg�ķ�����ѹ���������Ԫ�صĻ�������[35]����Mg�Ļ��Լ�С�����Һ̬�Ͻ����Mg�������ʵ��ڴ�Mg������ȼ�����ߡ����Ƕ��ڹ�̬�Ͻ𣬱������Ԫ��ЧӦ����������ԭ�����ڹ�̬�Ͻ��б������Ԫ����ɢ����������ʹ���ڱ����־ۼ�[38, 44]��
2.2 ���ʵĹ��ܶ�
�����������PBR֮�⣬Mg�����ںϽ�Ԫ�ص�����Ũ��ҲӦ����Ϊ��Ҫ���ء���ͬԪ����Mg�еĹ��ܶȼ�����2��һ�����������ʵĹ��ܶ�Խ�ߣ��Ͻ����ȼ��Խ��[11]����������Ԫ�غ������͵�þ�Ͻ�������봿Mg�ܽӽ�����ˣ��������γ�����Ĥ�ijɷ���ҪΪMgO������һ���̶����ܹ��ӻ�ͼ2��ʾ�ķ�Ӧ�����俹��������ȼЧ�����ޣ�ȼ����������������ʮ�ȣ�����La��Ce��Ԫ��[45-46]����ͼ4(a)��ʾ������Ͻ�����ȶ���������������й��ܶȵ͵�Ԫ��X��������Ҫ�ӱ�¶�ڿ����еĻ����ʼ����ͼ4(b)��ʾ��������ȹ����й������ܽ⣬����ԭ�Ӵ��ܽ�Ĺ���������ɢ����ʹ�����е�����Ũ�����ӣ��������γ����ܵ�XaOb/MgO�������������Ŀ������ԣ��Ӷ���ֹMg����������Ca��Sm��Ԫ�ء�þ�Ͻ��еĸ߹��ܶ�����ԭ���ڸ����»���������Ӧ�γɾ��������ܵ������㣬��ͼ4(c)��ʾ��ʹ�Ͻ�����������ȼ�ԣ���Y��Gd��Ԫ��[11]���������������ܶȸߵĺϽ�Ԫ�رȹ��ܶȵ͵ĺϽ�Ԫ����ȼЧ�������ԣ���ԭ���Ǹ���ʱ�������γɾ��������ܵ������㡣
��2 ��ͬ�Ͻ�Ԫ����Mg�еĹ��ܶȼ���[11, 31, 47]
Table 2 Solubility limits of different alloying elements in Mg[11, 31, 47]
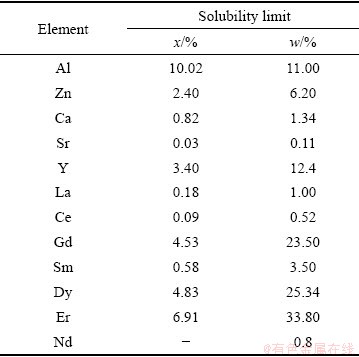
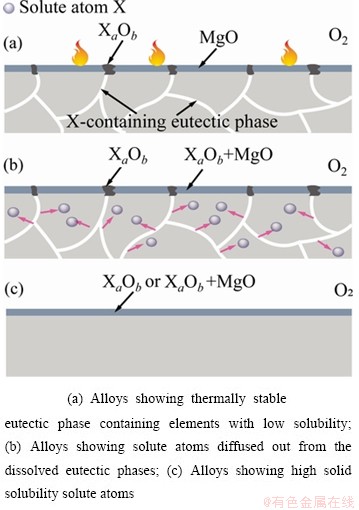
ͼ4 �������þ�Ͻ�������ΪӰ��[11]
Fig. 4 Effect of eutectic phase on oxidation behavior of magnesium alloy[11]
2.3 �����仯����(�ڶ���)
�����仯������Ӱ��Ͻ���ȼ�Ե���Ҫ���ء��ɱ�1��֪��Al��Zn��Ӧ�������PBR����1~2֮�䣬����ʵ��Mg��Al��Zn�ȳ���Ԫ�غϽ�������ߺϽ��ȼ�㣬ԭ����Mg�������γɵ��۵�ڶ���[48-49]��þ�Ͻ�ĸ�������ͨ����������֯�ı仯�͵ڶ�����ۻ�[19]�����۵���ή�ͺϽ��ȼ�㡣þ�Ͻ�ĵ��۵����ڸ���ʱ�������ۻ����ڶ����ںϽ����γ�Һ̬��������Mg���������������ڵ����������⣬���Ե��۵���Ľϸߵ�����ѹ��ٽ������������γɺ����Ƶ�������ʹ�������ɵı���������������[30]�����߹�ͬ���ü����˺Ͻ����������-Mg17Al12 (�����۵�Ϊ437 ��)Ϊþ�Ͻ��г����ĵ��۵���[14]���京����Ӱ��þ�Ͻ���Ƚ�/�������̣��Ͻ��Ц�-Mg17Al12�ĺ���Խ�࣬���ۻ��¶Ⱥ��Ƚ��¶Ⱦ�Խ�ͣ��Ӷ����ºϽ�����������͵����CHENG��[50]���о��У�Mg-0Al��Mg-3Al��Mg-6Al��Mg-8Al�ij�ʼ�ۻ��¶����ͣ��ֱ�Ϊ646��616��555��519 �档��ȼ��Ҳ������ͬ�����ƣ��ֱ�Ϊ627��602��573��567 �档ͬʱ����Mg-0Al��Mg-3Al�Ͻ��Թ�̬ȼ�գ���Mg-6Al��Mg-8Al�Ͻ���Һ̬ȼ�ա���ˣ�����Mg17Al12���������ӣ��Ͻ�Խ�����ۻ���ȼ�շ�����״̬�ӹ�̬��ΪҺ̬����Znþ�Ͻ��Mg2Zn3��Ҳ�ǵ��۵�(341 ��)�࣬�ɵ��ºϽ��ڸ����µľ���������ѡ��������[51]������þ�Ͻ�����仯������۵����3��ʾ�����⣬�����¿��ܷ����Ͻ�Ԫ�ص�������������������ƻ������磬��AZ91D�Ͻ��У��������ۻ������л��������Zn������������������������γ����ƺͿ��������������ʹ��Mg������ֱ�ӷ�����Ӧ���Ӷ������γ��������ޱ����Ե���������[52]��
���۵�����仯����(��Mg17Al12��Mg2Zn3)���ɶ�þ�Ͻ������Ծ��и���Ӱ�죬�����ȶ��Ľ����仯����Ĵ��ڶ��ںϽ�Ŀ������Բ���һ������������Ӱ�졣LIN��[53]��YU��[54]֤���˸����ȶ���Al2Y�ĸ������ã�ָ��Al2Y���γ������˹������е���ȼԪ��Y�����û���㹻��Y���γɾ��������ܵı�����Y2O3(RPB=1.13)�㣬�Ӷ������˺Ͻ�Ŀ������ԡ�ͬ������Mg-Al�Ͻ�ϵ��CeԪ��Ҳ����Al����γ����ȶ���Al11Ce3�������γɺ����������Ļ����еĴ���Ce��ʹ�úϽ���Ce�Ĺ�����Ҳ����Ӧ����[55]������Ceƶ������ʹ�Ͻ�Ŀ����������Լ�����
ͨ���������̺��ȴ�������ʹ��֯���ȣ���ߺϽ�Ԫ�صĹ��ܶȣ������ڶ����Ӱ�죬�������ȼ��[7]����ͬ���ȴ������̻������ͬ���۽ṹ���Ӷ�Ӱ�������ȼ�������ڵĸ������ܡ�һ����˵���������̿ɵ��¹��ܶȵ���ߣ�ϸ���۽ṹ[56]����ͼ5��ʾ��������ȴ���ʵ���ߣ��Ͻ���۽ṹ��ø��Ӿ�ϸ���ڶ����������������������������Ӧ�ļ�С��þ�Ͻ��ȼ��Ҳ��Ӧ�ĵõ���ߡ�LI��[55]�Բ�ͬ��ȴ���ʵ�AZ91D-0.98% Ce�Ͻ�(��������)������ȼ����ԣ�����������ȴ�ٶ����ӣ�ȼ��Ҳ��֮���ӡ���1.5��105 ��/s��ȴ��AZ91D-0.98% Ce�Ͻ��ȼ��ߴ�551 �棬����4.3��10-2 ��/s��2 ��/s��ȴ��AZ91D-0.98.% Ce�Ͻ��ȼ��ֱ�Ϊ470 ���500 �档�������̴���������Mg17Al12��Al11Ce3����γɣ��������ڶ����þ�Ͻ���ȼ�Բ����IJ���Ӱ���ͬʱ��ʹ�������ȼԪ��Ce���ڻ����У��γɹ��������塣֮��LIN��[53]�������ƵĹ�����̽�����������ʶ�AM50-Y�Ͻ�����ɺ���ȼ�Ե�Ӱ�죬��һ�������˿������̴�������ͨ���ı�ڶ���ķֲ����������ߺϽ����ȼ�ԡ�Al2Y����ٵ�ͬʱ��Mg17Al12��ķֲ����Ӿ��ȣ�ʹ�úϽ��ڸ������ؾ���ľֲ���Ӧ�����ȷֲ����Ӷ����������Ĥ���ȶ��ԡ�
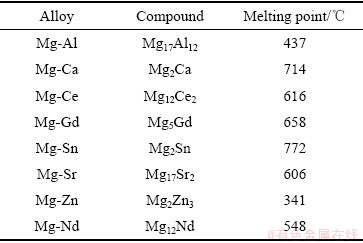
��3 þ�Ͻ�����仯������۵�[51, 57]
Table 3 Melting point of intermetallic compounds of magnesium alloy[51, 57]
�����������۵ĵڶ����۵�ĸߵ�֮�⣬��Ҫ���ǺϽ������˳���еĺϽ����������ȷ����ڵڶ��ദ[58]����ʱ�ڶ�������ཫ����������俹������������ȼ���������м���������þ�Ͻ�Ŀ�����������������ȼ��������ȷ���������Ȼ��Ҫ��������ȫ���̽������������Ҫ��һ�����ơ�
þ�Ͻ�ĸ���������ȼ�չ���ʮ�ָ��ӣ�������Ҫ�ۺϿ����������ز�����Ӱ�죬������Ŀǰ���о�������������ֻ��������һ��ԭ������л�������ʱ������ȫ���ԡ����⣬Ŀǰ���о��������ڶ�Ӱ�������Щ���صĶ��Է�������δ��������֮�������ԡ������TAN��[59]����������������ǿ����þ�Ͻ�������֮��Ķ�����ϵ��Ϊ��ȼþ�Ͻ�ķ�չ�������µĵ�·����һ��̽��þ�Ͻ������������ȼ��Ӱ�����أ����ҽ������������������ȼ����֮��Ķ�����ϵ��������ȼþ�Ͻ�ķ�չ������Ҫ��

ͼ5 ��ͬ��ȴ���ʵ�AZ91D-0.98% Ce��SEM��ò[55]
Fig. 5 SEM morphologies of AZ91D-0.98% Ce with different cooling rates
3 ��ȼþ�Ͻ���о���չ
3.1 ��Ca��ȼþ�Ͻ�
�ձ�ѧ��SAKAMOTO��[60]���翪ʼ�о�Ca�����Ӷ�����þ�Ͻ����������Ϊ��Ӱ�죬���ָƵļ���������þ�Ͻ��ȼ�㣬����þ�Ͻ��ۻ������еĿ����������ڴ�þ�м���5%(��������)��Ca����ʹ��ȼ�����250 ��[15]����AZ91�Ͻ��зֱ����0.5% ��1.0% Ca����ȼ��ɴ�549 ��ֱ������598 ���661 ��[61]����CaO������Ĥ����ֹO2�����ڽ�����ɢ��Mg����ӷ�����Ч���ϣ�ʹ��̬�����̬������̬��þ�Ͻ������Ծ��õ����[60, 62-63]��LEE[64]��AZ31þ�Ͻ����������0.3% Ca���о�������450~600 ��֮��ĸ���������Ϊ�������˺�Caþ�Ͻ����������γɹ��̡�����PBR�ϵͣ�AZ31�ڸ������γɵ�����Ĥ���ѣ������������ʼ�����߲���500 ��ʱ����ɥʧ����������������ȼ�ա�Ȼ��AZ31+0.3% Ca�Ͻ���625 ��ʱ��ʱ���ӳ��Ծ��н�С���������ʣ���������нϺõĿ�����������������Ca2+�������Ǩ�ƣ��������¶�����Ca2+������Ǩ��������Խǿ��ʹ�ñ����Ca�������ߡ����Ÿ�������ʱ����ӳ�������Ĥ����CaO�������ӣ�ȡ��MgO��Ϊ��Ҫ�ɷ֣������γ��˾��нϵ�����ѹ�ĸ�CaO�㣬�ò������Ҿ��ȣ���ֹ��O2������ɢ��Mg��������������һ���̶��ϱ�����Mg��O2ֱ�ӽӴ�����������Ӧ����˺�Ca��ȼþ�Ͻ����ͨ���γɸ�CaO����MgO/CaO�ڲ�������俹�����Ժ���ȼ�ԡ�
�ɱ�2֪��Ca��PBRֵΪ0.65��һֱ����������ΪCa����ȼ����������PBR����ģ�͡�����INOUE��[65]�����������µĽ��ͣ���PBR����ģ�ͽ��������ƣ�CaO/Ca��PBRֵΪ0.65����CaO/þ�Ͻ��PBRֵ������ȣ���˸�ֵ����������������������Ӧþ�Ͻ��ϵ������ԡ���INOUE��[65]�ļ��㣬CaO/Mg-10Al-5Ca��PBRֵΪ1.17������þ�Ͻ���Ca�����ӻ��γ�����CaO�㡣���Ca����ȼ��������PBR����ģ��[7, 65]��
�������ɱ������������⣬Ca�����������Ͻ�Ԫ�ز����ڶ�����Ӱ��þ�Ͻ�Ŀ�������[14, 64, 66-67]��INOUE��[65]�о��˸�Ca�����ĸ�ǿ����ȼMg-10Al-5Ca�Ͻ�(Ħ��������%)������״̬�µ�������Ϊ����AZX912(725 ��)��AZ31 (609 ��)��ȣ�Mg-10Al-5Ca�Ͻ��ȼ��ߴ�1163 �档������ǿ����������������õ�ͬʱ��ָ���˽����仯����(Mg,Al)2Ca����߿������Է������Ҫ���á��ں�Alþ�Ͻ��У�Ca�����ӻ�ʹ�����Ŧ�-Mg�ľ����������ȶ���Al2Ca��(�۵�Ϊ1079 ��)[12, 64]����Ҳ��ʹ�Ͻ���������ߵ�һ����Ҫԭ��Ca�����ܽMg17Al12��[61, 68]�������˦����о������ȶ��Եļ���ǿ��[68]��ʹ��������ȶ������⣬Ca�벿��Al��Ӧ�������˵��۵��-Mg17Al12����γ�[69-70]��ͬʱ���������ȶ���Al2Ca��[14, 67]������˺Ͻ�Ŀ�����������
ֵ��һ����ǣ�Ca�����ӻ����Mg-Mg2Ca����[71]����Mg17Al12�����ƣ����ֹ����ṹ�ڽϸ��¶��»������ۻ����γ�Һ̬��������Mg���������Ӷ��ٽ��˺Ͻ������������Ĥ���γ�[19]��������ֻ�������¶ȵ���Mg-Mg2Ca������֯���ۻ��¶ȣ�������Ч����ֹMg2+�ؾ������ɢ���Ӷ�����������Ȼ�����ݷ������[63]�ı�������Ca����(��������)����1%����Ca���������ӣ��Ͻ�ȼ�������������Ca��������1.7%ʱ���Ͻ����900 �汣�¶���ȼ�գ�˵���ڴ��¶���Mg-Ca�Ͻ���Ȼ���нϺõĿ�������������ԭ�����KIM��[11]�����۽��ͣ����ȹ����й������ܽ⣬����ԭ��Ca���ܽ�Ĺ���������ɢ������������Ca�������ӣ��������γ����ܵ�CaO/MgO�����㣬�������ȼ�ԡ����⣬�����ױ���[7, 70, 72]��Caͬʱ����REE��SAEE������MgO��ķ�϶��Ѹ�ٷ�Ӧ���γ��µ��������������������ơ�
��ȻCa�����������þ�Ͻ�Ŀ���������������������Ӧ����Ȼ����һ���ľ����ԡ����ȣ�Ca�ijɱ��ܸߣ�������������ĸ߷�Ӧ�ԣ��ڰ�װ������Ͱ��˹�������Ҫ�ر�ע�⡣��Σ�Ca�����Ӳ�����ԺϽ����ʴ���ܺ���ѧ������ɲ���Ӱ�졣ZENG��[73]ָ����Ca��þ�Ͻ�ĸ�ʴ����˫�����á�һ���棬��Mg������Ca����ϸ���������Ӷ������ʴ�ԣ���һ���棬Ca����Mg���γɵ�Mg2Ca��ʹ�úϽ���Mg2Ca�ͦ�-Mg֮�䷢����ż��ʴ���Ӷ������˺Ͻ����ʴ�ԡ�����Mg-Al�Ͻ�Ca������������ʹ�Ͻ��ࡣ��LI��[69]��������AZ91D��Ca������0������1%ʱ���伫����ǿ�Ⱥ�����쳤�ʷֱ���14%��40%��ԭ�������ȶ���Al2Ca�����˺Ͻ�ĸߴ��ԣ�����Mg-Ca��Ԫ�Ͻ�Ϊ�˱�֤���������ܣ�Ca����Ӧ������1%����[74]�����Ca����Ҳ���и������������ڱ�¶�ڸ��¿���ʱ����������Ӧ���Ӷ�ɢ�������������������Ͻ��е�Ca���࣬��Ca�ij���������ܽ����������þ�Ͻ�Ŀ�������[64]����Ŀǰ��û�����ʵ��������֤������Ӱ�졣
����������Ca�����þ�Ͻ�Ŀ������Ե�ԭ�����£�1) �γ������ܵĸ�CaO��㣬��Ϊ�谭O2��ɢ��Mg���������ϣ���һ���̶��ϱ�����Mg��O2��ֱ�ӽӴ���2) Ca���������Ƶ��۵�Mg17Al12����γɣ������ܽMg17Al12�У���ߦ�������ȶ��ԣ�3) ���������ȶ��Ľ����仯����Al2Ca��������������Ca��ȱ�㣬һ����������CaO������Ca���Դﵽ���Ƶ���ȼЧ��[75]����һ������Ͻ�����������Ԫ��(��Be��ϡ��Ԫ�ص�)��ʹ���Dz���ЭͬԪ��ЧӦ�����Ǻ�Ca��ȼþ�Ͻ������Ҫ��չ����
3.2 ��Be��ȼþ�Ͻ�
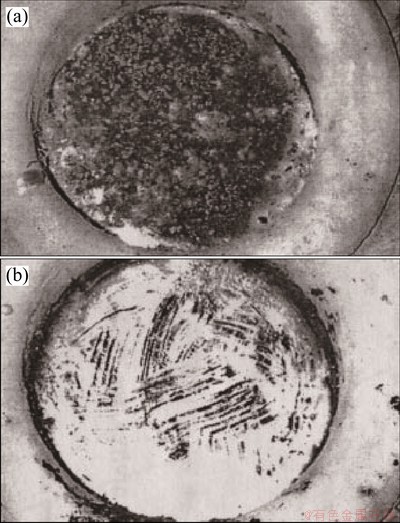
ͼ6 650 ��ʱ����AZ91��AZB910�Ͻ�ĸ���ͼ[78]
Fig. 6 Top view of (a)molten AZ91 alloy and (b)AZB910 alloy held at 650 ��[78]
��Be��ȼþ�Ͻ�ķ�չ���Է�Ϊ�����Ρ�����20���ͳ��ڣ���(Be)�ͱ�֤�������þ�Ͻ������Ե���ЧԪ�ء�Be��O2����������Mg[21]��BeO��PBRֵΪ1.70[61]����ˣ�������ܳ�һ��ʱ�������ǽ�Be������þ�Ͻ������Թ����ڱ�����BeOĤ���γɡ�HUANG��[76]��Mg-2Ca�кϽ�����300��10-6 Be�������������ʴ�ͣ�ȼ�������200 �����ϡ��úϽ��ڸ��±�¶�ڿ����������Ĥ��Ҫ��CaO��MgO��BeO��ɡ�ZENG��[15, 77-78]��AZ91D�м�����0.3%��Be�����ּ�ʹû�ж������屣����Ҳ���Խ���AZB910�Ͻ��ۻ���������ȼ�ա�ͼ6��ʾΪ650 ��������AZ91��AZB910�ĺ��ͼ��AZ91���屻���������︲��(��ͼ6(a))����AZB910�ı�����Թ⻬����(��ͼ6(b))���������нϸߵĿ������ԡ�����⣬����������Ҫ��MgO����BeO/MgO�ڲ���ɡ������ͻ���Ͻ�֮���γɵľ��������ܵ�BeO/MgO�ڲ�䵱���赲�㣬������������Mg2+������ɢ����֤���˱�����BeO����γ�����˺�Beþ�Ͻ�Ŀ��������ܡ����ZENG��[78]ͨ������ѧ�����BeO���γ����������˷������������������£�
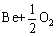 =
=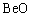 (3)
(3)
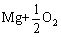 =
=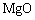 (4)
(4)
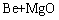 =
=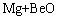 (5)
(5)
ʽ(3)��(4)��(5)������AZB910�Ͻ������ܷ����ķ�Ӧ��ʽ(5)�ı�����˹������Ϊ��
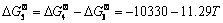 (6)
(6)
��ʽ(6)�ƹ㵽һ�������£���ʽ(7)��
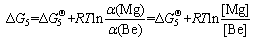 (7)
(7)
Ϊ�˼���Mg��Be�Ļ�ȷֱ�����Ħ������[Mg]��[Be]���ƴ��档����ʽ(7)�ļ��㣬650 ��ʱBe��ƽ��Ũ��(Ħ������)Ϊ2.3%(��������Ϊ0.88%)��ZENG��[78]ָ���������֮�£���Ũ�Ⱥܵͣ�BeO����ͨ��ʽ(3)�з�Ӧ�γɶ���ͨ��ʽ(5)�еĻ�ԭ��Ӧ�γɡ���ˣ���Be��Ũ�ȴ���ƽ��Ũ��ʱ��������BeO���γɡ�����ƫ��ЧӦ��0.3%��Be��AZ91�п���������һ����ѧҪ��������ѧ��֪���ںϽ������BeO����������Ũ�Ⱥ��¶�����[15]��
��Be��þ�Ͻ�ĸ߿������Թ�����BeO���γɣ��������Ƕ��ں�Be��ȼþ�Ͻ���ʶ�ĵ�һ�Ρ�
���������о���Be������Ҫ�ﵽһ����ֵʱ��Beþ�Ͻ�Ż���нϺõĿ����������ԡ�Ȼ����Ҳ���о���������ʹ������(10-6��)Be��Ҳ��ʹþ�Ͻ�������õĿ����������ԡ�CZERWINSKI[21]�о���Be����Ϊ5��10-6��10��10-6��AZ91Dþ�Ͻ���200��500 ��֮���������������Ϊ�����ط�������������ڶ�����������·�Ӧ�ڼ䣬Be������Mg�������������������з�Ӧ�ڼ䣬Be�����ӱ����������ε�ʱ�䡣TAN��[40]��AZ91þ�Ͻ��벻ͬ����(10��10-6~60��10-6) ��Be�Ͻ�������400 ��ʱ��AZ91Be�����������Խ��͡�ͼ7(a)��ʾ��TGA�����������AZ91�Ͻ���ȣ�Be���Ͻ����������˸ò����¶��µ����������ʡ���ͼ7(b)��֪����400 �����������144 h��AZ91�Ͻ��ƻ����أ����֮�£�AZ91Be�����Ͻ����������������ڣ������ò����û�з����仯�����AZ91Be60��ȼ��Ϊ659 �棬��AZ91��549 ��������˺ܴ�����[61]������Be�ĺ������ͣ�δ�ܼ�����ڣ�AZ91Be60��������ΪMgO������ò��ʾ�ò����������ơ�����Be�Ͻ�þ�Ͻ𣬼�ʹͨ��ƫ�����ã�Be�ľֲ�Ũ��Ҳ���ܴﵽ0.88%����ˣ��ۺ�����ѧ�����һϵ�в��Ծ�������þ�Ͻ���治�����γ�������BeO�㡣���ں�����Be��þ�Ͻ��俹������������������ǰ�����������͡���Ȼδ��Be����TAN��[40]��Ϊ����MgO����γ�������Be��ǿ�����á�TAN��[40]��CZERWINSKI[21, 31]����Be��������REE����ȣ��Ի��������˼Ľ��ͣ���Be�ںϽ�����Ӧ��Ԫ�ص����ã�Be2+��MgO�����ƫ��������Mg2+�ؾ����������ɢ���Ӷ������������ʽ��͡����ں�����Be��þ�Ͻ���һ��ȼ����������δ�õ�ֱ�ӵ�ʵ����֤��
���ں���Be����ȼþ�Ͻ���REE�������俹���������ԣ��������Ƕ��ں�Be��ȼþ�Ͻ���ʶ�ĵڶ��Ρ�
�ڵڶ��Σ�һ����Ϊ����MgO����γ�������Be��ǿ�����ã�Be��MgO���ʵ��ǿ���������������������һ����˵���Ʋ���ܵ�ԭ��TAN��[41]֤����Be��AZ91Be60����Ĥ���о���ϸ�������ܻ������ã���(Mg��Be)O���Ӳ�Ⱥ�ǿ�ȶ���MgO��ߡ������Be�ԺϽ�������������Ե���ǿ���á���һ���۲췢�֣�AZ91�����������е������ᄃ����СΪ15~20 nm��AZ91Be60������ľ����ߴ�ԼΪ5 nm�������AZ91��Be���Ͻ�ʹ�������������е������ᄃ��ϸ��������ϸ����ԭ����Be���Դٽ�������ijɺ�[41]��������Be2+��MgO����������ɢ�γ��˸�Be��MgO�㣬ͬʱMgO�����еIJ���Mg2+��Be2+ȡ���γ���(Mg��Be)O�û�������[41, 59]������Ļ���������λ���˶����������ݣ�����λ���˶������¹���ǿ��[79-80]��
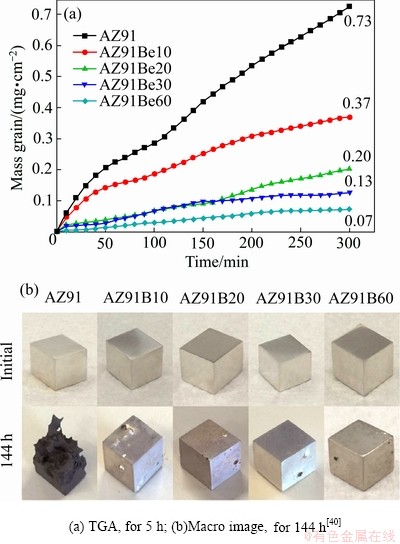
ͼ7 AZ91Be�Ͻ���400 ��������������TGAͼ��ͺ��ͼ��[40]
Fig. 7 TGA image and macro image of AZ91Be alloy oxidized in air at 400 ��
����������(Mg��Be)O���ǿ���ǹ���ǿ����ϸ��ǿ����ͬ���õĽ�����ڸ������������У�ϸ��(Mg��Be)O������㹻��ǿ�����ֿ���������Ӧ����Mg�����ۼ���ɵĸ�����ѹ���ӻ��������㿪�ѺͰ��䣬������Mg������������ɢ��ʵ���˸߿������ԡ�
�����TAN��[59]��Be��ǿ�����۽����ƹ��һ�㻯����Mg-2Zn��Mg-2Y��Mg-2Sn��AS21��AM60��ZK20 ��ZC63�ֱ���60��10-6 ��Be�Ͻ������������ѧ������þ�Ͻ����ȼ������ϵ�����������ʾ��Mg-2Zn-Be��Mg-2Y-Be��Mg-2Y��Mg-2Sn-Be��AS21-Be��ZC63-Be�����нϵ͵��������ʣ���͵������������������ǿ�Ⱥ�Ӳ�����Ӧ����AM60��ZK20 ��ȣ�AM60-Be�� ZK20-Be�������������������ǿ�Ⱥ�Ӳ�ȱ仯�����ԣ�ԭ����Zr��Mn������Ͻ�Be������ѧ��Ӧ���γ����ȶ��ĺ�Be�����仯�����ֹ��Be������ɢ��ǿ���������Լ����������Be��Zr��Mn�����þ�Ͻ������Է�����ڲ������ԡ��ɴ˿�֪��þ�Ͻ�Ŀ������������ʼ�������ǿ�ȡ�Ӳ��������أ����γɾ��и���еǿ�Ⱥ�Ӳ�ȵ�������ʱ�������Ÿ��ߵĿ����ԣ�����ӳ���þ�Ͻ�����������ڣ�������俹�����ԡ�
Be���Ͻ�þ�Ͻ��������ǿ�����ã������Ƕ��ں�Be��ȼþ�Ͻ���ʶ�ĵ����Σ������Ƕ��ں�Beþ�Ͻ���������������ʶ���봫ͳ���ԵĿ���������������ͬ����һ���۵����������������ǿ���뿹������֮��Ķ�����ϵ��������ȼþ�Ͻ�ķ�չ������Ҫ���塣������Ҫ���и�������о���1) Be���з�Ӧ��Ԫ��ЧӦ��ֱ���оݣ�2) ��ԭ��ˮƽ�Ͻ�һ���о�(Mg��Be)O�ṹ����Be���������еķֲ����������˽⺬Be����þ���ǿ������[38]��3) Be������Ԫ��Эͬ���õ�����ȡ�
Ȼ����Be�ļ۸�߶����ж���[61, 81]��Be������ɵ��·ΰ�[82]������ڹ�����Ӧ��������Be��ʹ�á����⣬�����о�����[15, 77, 83]��ʾ��������Be���������ֻ����������ȼ�Ե�ͬʱ��������ѧ���ܡ�һ��þ�Ͻ�������Be����Ҫ������0.02%����[84]����ˣ�Be���Ͻ��Ǻ�Be��ȼþ�Ͻ������Ч���ȫ���ֶΡ�һ������º��ٵ���ʹ��Be��������Ca��ϡ����Ԫ��Эͬ���ã����ܱ�֤þ�Ͻ����õ���ȼ�����ܱ������Be��ɵľ����ֻ���
3.3 ��Sr��ȼþ�Ͻ�
SrԪ����ͨ���������Ԫ��ЧӦ(SAEE)���þ�Ͻ������Եľ��д����Ե�Ԫ�ء�AYDIN��[35]��ʵ����������������6% Sr������£���̬þ�Ͻ��ȼ���640 ����ߵ�854 �棬�����Ƶ�ʵ�������£���������ȼþ�Ͻ�WE43��ȼ��(750 ��)���ߡ�SrԪ�ص����ӣ�ʹ�Ͻ��ڸ������γ���MgO/SrO����㡢��SrO���м���MgO���ڲ㣬���������������ͼ8��ʾ�����������ӵ���ɢϵ�������Ӱ뾶�����Ӷ�����[85]��Mg2+����뾶��Sr2+С���Ӷ�ʹ��Mg2+��ɢ���죬�����������MgO�㣬SrO������ɡ���ˣ���������������������ͼ8(a)��ʾ��������ṹ�����Ͻ��ۻ���SrԪ�ؼ��������ۼ����γɸ�SrO��MgO/SrO���������㣬��ͼ8(b)��ʾ����2.2��������Sr��Mg�еĹ��ܶȼ������ͣ�Mg-6%Sr�Ͻ��д��ڴ����ĵڶ���Mg17Sr2�ࡣ���¶ȳ����乲���¶�(Լ600 ��)ʱ���������(Mg17Sr2+��-Mg)���ۻ�������ԭ��Sr���ܽ�Ĺ���������ɢ�������γɸ�SrҺ��ʹ������SrŨ�����ӣ�Srԭ�Ӽ��������ۼ�����ͼ8(c)��ʾ�����ڽ���/����������ø�Sr���������γ�SrO�Ļ������ӣ���˸���MgO/SrO����·��γɸ���SrO���ڲ㡣����������ļ���������������������Ӧ�����Ӷ��������ƣ������·�Һ���Sr�ı�����Ժ�Sr��O2������ʹ��SrO�γɣ��Ӷ��������ƣ����˱����ڲ���������ã���Ҳ�DZ������Ԫ��ЧӦ�ĵ������û���������һ�Σ�����MgO�ķ�Ӧ���٣�Mg�������ﵽ��С�����������þ�Ͻ���ȼ�ԵĹؼ���һ����SrO���γɽ���ɱ���Sr�ĺľ���������/������������������Χ�����ಿ�ֽ��γɸ�MgO�㣬�����γ�����ͼ8(d)��ʾ�ĸ���������ṹ��֮������������Ӧ�ļ������У������㿪�ѣ��Ͻ����������������ȼ�ա��ɱ�1֪��SrO��RPB=0.66����ˣ�Sr����ȼ����������PBR���������ͣ���Ӧ����Sr�ı������Ԫ��ЧӦ�����͡����⣬���ڱ�����ԣ�SrԪ���ڱ���ۼ�ռ���˱����Mgԭ�ӵ����������������˺Ͻ�����Mg�ķ�����ѹ����������Һ̬�Ͻ�ı���������������������Ŀ����Ծ�����Ҫ����[35]��
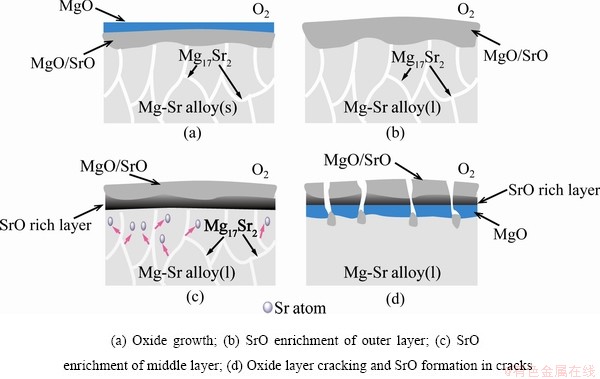
ͼ8 Mg-Sr�Ͻ��������ʾ��ͼ[35]
Fig. 8 Schematic showing oxidation on Mg-Sr alloys[35]
AYDIN��[44]�Թ�̬˫��Mg-Sr�Ͻ�(Mg17Sr2/��-Mg)�ĸ���������Ϊ�������о������о������ڴӺϽ��۽ṹ������SrԪ�صĿ������������á��о����֣���̬Mg-Sr�Ͻ��ڸ����³�ʱ�����Ҳ�����Sr�ı���ƫ����ɢ�������γ�MgO/SrO���������㡣����Srͨ����̬ƫ���ڱ����Ͼۻ��������俹����Ч������Һ̬�Ͻ����������ͬʱ������Sr���������ӣ��κ��������ӣ������ᄃ���ߴ��С�������ᄃ����Mg-Sr�Ͻ���Sr�Ŀ�����ɢ·�������������ʹ��Sr�Ŀ�����ɢ·�����࣬�Ӷ����¸����SrO�����ھ��紦���Ӷ�����˺Ͻ�Ŀ������ԡ�
����������������Mg�еı�����ԺͶ�O2��������Sr����Ч�������Mg�Ͻ�Ŀ������Ժ�ȼ�㣬������Sr���������ӣ�ȼ�����ߡ�������Һ̬ʱSr�ı���ƫ���Ϲ�̬ʱ��Ϊ����������ȼ�Զ��ԣ���Srþ�Ͻ�ȼ���ѳ���������ȼþ�Ͻ�WE43����ˣ���Sr��ȼþ�Ͻ��кܴ�ķ�չǰ����
3.4 ϡ��Ԫ����ȼþ�Ͻ�
��Ca��Be����ȼþ�Ͻ�������ϲ����ѧ���ܡ���ʴ���ܺ�Be�Ķ��ԣ���δ�ڹ�ҵ�еõ��㷺Ӧ�á�ϡ��þ�Ͻ��ǽ���������������о��ȵ�֮һ��ϡ��Ԫ�ؿ��Խ���þ��Һ̬��̬�����������г������������ã�ʹϡ��þ�Ͻ�������õ������Ժ���ʴ�ԡ���ϡ��Ԫ����þ�Ͻ��еĹ��ܶȱȽϸߣ����к�ǿ�Ĺ���ǿ��������ǿ�����ã����Ը���þ�Ͻ�ĸ�����ѧ���ܺͿ�������ܣ�ͬʱ�������������ʴ��[86-87]��ϡ��Ԫ�ز������Ը�����֯����ѧ���ܣ��������γɱ���������Ĥ����ߺϽ����ʴ�ԡ������������Ժ���ȼ�ԡ��ݱ��������ڴ��ԭ�Ӱ뾶��ϡ��Ԫ����������Զ����������γɵ�Mg��������Ŀ�϶[30]������ֹ�˽���ԭ�ӵ���ɢ��ϡ��Ԫ�ؾ�������ĵ������з�ʽ���ڲ���������������Ҫ����[88]��������ߺϽ����ѧ����ʴ�����⣬�����ڽ��洦�γ�ϡ�����������ǿ����Ĥ����������[89]����������[90]���о������������ZM5þ�Ͻ��м���һ�����Ļ��ϡ��(Ce��La��Nd)��ȼ����654 ����ߵ�823 �档RAO��[91]���֣�ϡ��Ԫ�����Ծۼ������ڵ�þ�Ͻ���棬Ϊ�γ����ܵ�����Ĥ�ṩ�����õ�����ѧ��������ָ����ȼ�Եõ���ߵ�ԭ���Ǹ���ʱϡ��Ԫ�ؿ��ڱ���ۼ��γ�һ�����ܵ������㡣ͬʱ���ʵ�������ϡ��Ԫ�أ���ʹ����ϸ�������紦���������࣬����֦������̣��Ͻ�Ŀ���ǿ�Ⱥ������ʶ�������ߡ�
ϡ��Ԫ�ص���ȼ���ÿ��������ᵽ�����л���ģ�ͽ��н��ͣ�����PBRģ�͡�REE��SAEE�ȡ����ڽ��������ϡ��Ԫ�ض�þ�Ͻ��������ܵ�Ӱ����ơ�
3.4.1 ��(Y)
Y�����þ�Ͻ���ȼ�Ե���Ч�Ͻ�Ԫ��֮һ����ʹþ�Ͻ�ȼ���������ߡ���״WE43 (4% Y)�ڸߴ�750 �����Բ�����ȼ�ա�Y2O3��PBRֵΪ1.13����һ������ȶ������������Yþ�Ͻ�¶�ڸ��»���ʱ������Ʒ�����ϻ��γ����ܵ�MgO/Y2O3���������㡣�ø�����������Ϊ�������Ͽ��谭������Ӧ�Ľ��У��Ӷ�������þ�Ͻ�Ŀ�������[92]�����⣬Y��Ϊ��Ӧ��Ԫ�أ����Ͻ������������ʱ��Y�Ἧ�����ѷ촦������O2��Ӧ����Y2O3�������������[93]��YU��[94]�о�����̬Mg-Y-Sn��Mg-Y��Mg-Sn�Ͻ���500 ��ʱ�ĸ���������Ϊ����ָ��Y�ڸ�������Ĥ�ı������ܷ������������á�Mg-Y��Mg-Y-Sn�Ͻ�����ڸ������γ��˱����⻬���ܵ�����Ĥ��û�й۲쵽���Ե����ƻ����䣬��Ĥ���������O2��������ɢ��Mg2+��������ɢ���Ӷ������������ʡ�YU��[95]�о���Mg-xY (x=0.5, 1.0, 1.7, 3.7, 5.5������������%)�Ͻ����۵㸽����������Ϊ���������ò��ͼ9��ʾ��Y�����͵ĺϽ������Խϲ����������кܶ�MgO���������ƣ�����Y���������ӣ�Mg-xY�Ͻ������������ƽ�������ܣ��ҵ�Y�����ﵽ5.5%ʱ������������ƺ�MgO������ȫ��ʧ��Mg-0.5Y�Ͻ��Mg-1.0Y��Mg-1.7Y��Mg-3.7Y�Ͻ�����ؽ�����������Ρ�������Mg-5.5Y�Ͻ�����������������δ�۲쵽���Ե������仯����ˣ����Եó����ۣ�����Y���������ӣ�Mg-Y�Ͻ�Ŀ�����������ߡ�
Mg-Y�Ͻ��������ṹ�ɷ�Ϊ���㣺��Y2O3������MgO���ڲ�[46, 54, 94-95]��������������ͼ10��ʾ��Y��������Ӧ�ļ���˹�����ܱ�Mg������Ӧ�ļ���˹�����ܸ���[96]�������Y��O2���и��ߵ��������ڸ����£�YԪ�������������л���Ͻ�����ƶ����Ҹ���[94, 97]��Ԫ��Y�ĸ߱�����ԺͶ�O2�������ٽ��˱������Y2O3���γ�[98]��ͨ������ѧ���㣬����ʱY2O3Ҫ����MgO�γɣ�������Y3+��ȣ�Mg2+���и����������ɢ���ʣ�MgO����������/���������γɲ���������γɵ�Y2O3��Ȼ����Ĥ�ⲿ������MgO�㲻������ֹO2��������ɢ�������������/�������洦�γ�Y2O3[95]���Ӷ����˱���MgO������ơ�
Y��Mg�й��ܶ�(��������)���ϴ�ԼΪ12.4%[31, 99]��������[95]��������Y����Ϊ0~12.4%��Χ�ڣ�Ԫ��Y����Խ�ߣ�Mg-Y�Ͻ�Ŀ�������Խ�á�FAN��[46]���ֵ�Y����С��8%ʱ���Ͻ��ȼ��û�����Եı仯��ԭ���ǵ͵�Y���������γ�������Y2O3��[100]�������ڴ�֮������Y�����IJ������ӣ��Ͻ�ȼ�����ӣ����ҵ�Y��������10%ʱ���Ͻ�ﵽ900 ��ʱ�Բ���ȼ�ա����ǣ���Y��������8%ʱ��þ�Ͻ�Ĵ��Ի���[101]������ʧ��ѧ����Ϊ��������俹�������Dz���ȡ�ģ��������ϡ��Ԫ�غϽ����ӳɱ�������Mg-Al�Ͻ𣬽��2.3�������Ľ����仯�����Ӱ�죬Y�����ӻ��γɴ�����Al2Y��(�۵�Ϊ1485 ��)���Ӷ�������Al2Y�����������е�Y�����������˱���������Ĥ�������ԡ���������Y���ᵼ��Mg-Al�Ͻ����ѧ���ܽ��͡��ݱ�������AZ91�Ͻ��У���Y��������0.9%ʱ��������ʼ�ֻ�������������AZ61��Y�ٽ缫��Ϊ1.4%[102]���ɴ˿ɼ�������Mg-Al�Ͻ�ϵͳ��ͨ����Y�Ͻ������ƿ��������Dz���ʵ�ʵġ�������ˣ�Y�����ӻ����Mg24Y5�࣬����Լӿ�������Ӧ���ʴӶ����þ�Ͻ�ʴ����[103]����ˣ����ں�Y��ȼþ�Ͻ�ɷֵ���ƣ�������и��������̽�����������ܹ�����������ȼ�Ե�ǰ���£�Ce��Ca�����ӣ��ܴ��Y����[46, 104]��ʹ�Ͻ�������õ��ۺ����ܡ�

ͼ9 Mg-Y�Ͻ���550 ���������з���6 h������ı�����ò[95]
Fig. 9 Surface morphologies of Mg-Y alloys oxidized at 550 �� for 6 h in dry air[95]
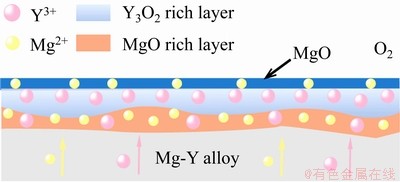
ͼ10 Mg-Y�Ͻ��������ʾ��ͼ
Fig. 10 Schematic diagram showing oxidation on Mg-Y alloys
3.4.2 ��(Nd)
ͨ����Nd�Ͻ������Mg�Ͻ�Ŀ������������˵��չ�������ǽ�ʮ�������Ƚϻ�Ծ��һ���о�����[19]��ZHAO��[105]������Nd�ķ�Ӧ��Ԫ��ЧӦ��Nd2O3���γɾ��������������Ƶ����á�WANG��[106]����Mg-Nd�Ͻ���ڸߴ�550 ����¶��±���90 min�Բ�����ȼ�գ���600 ������Լ80 min��ͻȻ�������ָ������������ߵ�ԭ�����ڸ������������в�����Nd2O3/MgO���Ͻṹ������Nd�Ĺ������ӻ������ã���Mg-Nd�Ͻ�Ŀ������ԡ���Y��ͬ��Nd��Mg�еĹ��ܶȺܵͣ����ܶȵ͵ĺϽ�Ԫ����Mg�Ͻ�ʱ�����γɵڶ��࣬���Ӱ��ı�Ͻ���Ԫ�ص�����˳�����������۽ṹ������Ӱ��Ͻ�Ŀ�������[107]����WANG��[106]���о��У�û�н��������Nd�����ή�ͺϽ��������Ե�ԭ����Ȼ�����˽����仯����Mg12Nd������δ���۸����Mg-Nd�Ͻ�������Ϊ��Ӱ�졣
AYDIN��[27, 42, 58]��Mg-Nd��Ԫ�Ͻ�ϵͳ(w(Nd)=0.3%, 0.5%, 2.5%, 6%)��500 ���µĸ���������Ϊ�����˸�Ϊ������о������ֵ�Nd������0.3%���ӵ�0.5%ʱ���Ͻ�ȼ���Լ660 ��������Լ770 �棻���ǣ���Nd������һ��������6%ʱ���Ͻ�ȼ����ά����770 �渽���������������м���Mg12Nd�Ĵ���������أ�Mg12Nd�Ǵ�Һ̬������ȴ�ĺϽ��з��ֵ�������[108]���о����֣����ڵ���Mg-Nd�Ͻ�(w(Nd)=0.3%, 0.5%)���Ͻ��н����仯������ܽ������ӽ�ƽ��ĵ����-Mg�����塣���ڽ�������Ĵ��������٣���Щ����Mg-Nd�Ͻ������������Ҫ�ǹ�����������������¡�����Mg-Nd�Ͻ������������ʾ��ͼ��ͼ11(a)��ʾ��Nd3+���б�Mg2+����ijߴ磬�������ͬ�����£�Mg2+��Nd3+������������ɢ[106]��Mg2+����������ɢ��������/���������O2��Ӧ����������γ�MgO�����Mg2+�ᴩ��������ɵ�MgO����������ɢ����������/��������ϼ�������MgO�����������������������������MgO�㡣��������ʼ�Σ�MgO���γɻή�ͦ�-Mg����������ϵ�Mg����������Nd�Ļ��ԣ��Ӷ����±�����Nd2O3���γɡ�ֵ��ע����ǣ�Nd2O3����Nd�����ʱ�Nd��ɢ������/��������������Ҫ�����Ӷ��������������´���Nd����������֤�˳����Nd��Ӧ[27]�����ܵ�Nd2O3/MgO������ʹ���ʵ������ܵ������ƣ�����MgO���γɣ��Ӷ����±����¶ȵ��������ʱ������ӳ���Mg�������͵��
��������Mg-Nd�Ͻ�(w(Nd)=2.5%, 6%)�����ڴ��ڴ����ij���״�ֲ��Ľ����仯����Mg12Nd�������������Ϊ��������ṹ�뵥��ϡMg-Nd�Ͻ����ͬ[58]�����������������ͼ11(b)��ʾ���ڵ���ϡMg-Nd�Ͻ���������ڣ���������MgO����Nd2O3����[27]������������Mg-Nd�Ͻ���������Ӧ���ȷ�����Mg12Nd�ϣ���Nd2O3Ӧ����MgO���ɣ�������������Ϊ��1) �����仯�����е�Nd��O2��Ӧ����Nd2O3��2) �ڽ����仯����ͦ�-Mg�ϼ���ͬʱ�γ�MgO��3) �ڦ�-Mg���γ�Nd2O3����������γ���Ҫ������ѧ�ʹ��ʵĿ���[85]���ڸ�ʵ�������£�O��MgO�е���ɢϵ��(4.3��10-24 cm2/s)��Mg��MgO�е���ɢϵ��(1��10-17~1��10-13 cm2/s)С�ö࣬����MgO�����ɷ�Ӧ��������������/������档��ˣ�����Mg-Nd�Ͻ��γ����뵥��Mg-Nd�Ͻ���ȫ��ͬ��������ṹ������Nd2O3/MgO������Nd2O3���ڲ�[42, 58]���������ܵĸ��Ͻṹ�谭�����ʴ��ݣ�����˺Ͻ�Ŀ������ԡ����У���Nd2O3���ڲ�ij�����Ҫ������Mg12Nd������[58]����ȻNd2O3��PBRֵΪ1.13��Ԥ�����ڸ����������д���Խ�ཫ��������ǿ�����ı�������������Nd2O3��һ�־�������λ��������ȱ�ݰ뵼�壬Nd2O3��ΪO2�ṩ������ɢ������ɢ·�����Ӷ������˽���/����������������������ˣ������仯����Mg12Nd����������������Χ������Nd���������ͼ11(b)��ʾ��Ndƶ������ʹ�ø����Mg������ɢ�����棬������MgO���γɺͱ����¶ȵľֲ����ߣ��Ӷ����ºϽ���������Ż�[42]�����⣬����Ndƶ�����Ĵ���ʹ��������ֲ��������������ܵ��谭����Ҳ�ͽ�������ϡMg-Nd�Ͻ���Ƚϣ���Nd������þ�Ͻ���ȼ�Ե�Ӱ�첢�����ԡ�
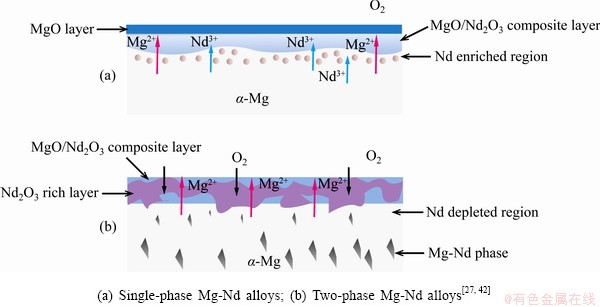
ͼ11 Mg-Nd�Ͻ��������ʾ��ͼ[27, 42]
Fig. 11 Schematic diagram showing oxidation on Mg-Nd alloys
����þ�Ͻ���ȼ�Ե�������Ҫ�Ӷ���Ƕȡ����������ۺϿ��ǡ����絥����PBRģ�ͻ��������ܽ���Nd�����ߵ�Mg-Nd�Ͻ���ֳ����������ء�ȼ��仯�����Ե��������ۺϿ��ǵڶ����Nd2O3���е����ʲ��ܽ��к������͡����⣬Ϊ���ƹ���ȼMg-Nd�Ͻ��ʵ��Ӧ�ã�����Ҫ����Nd����(��������)�ԺϽ���ѧ���ܵ�Ӱ�졣ARRABAL��[52]���֣�AZ91D�е�Nd����Ϊ0.7%~1.4%ʱ����Ȼ����˺Ͻ�Ŀ������Ե��ǻ�ʹ�侧���ֻ���ZHANG��[109]���о�����AZ31-xNd�Ͻ�(x=0.38%~1.46%)�ľ����ߴ���Nd������������������С��Nd����Ϊ1.05%ʱ�����������ܴﵽ���ֵ����ˣ���Ҫ��һ���о�Nd��þ�Ͻ���������ܵ�Ӱ�죬����������������ȼ�������õ���ѧ����֮���ҵ�ƽ��㣬����һϵ�������������ȼþ�Ͻ�
3.4.3 ��(Ce)
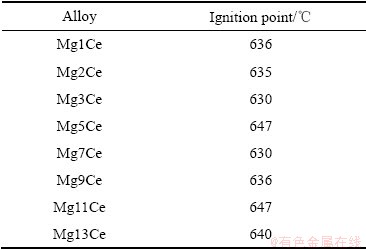
ϡ��Ce����þ�Ͻ��У��ɴٽ��Ͻ��������Ĥ�����ɱ�Ϊ���ܣ����ͺϽ���Һ̬��̬�µ��������Ӷ����þ�Ͻ�Ŀ�������������[110-111]��DING��[9]��AZ31��Ʒ����ע��Ce���о�������500 ������б���96 h��ѭ��������Ϊ����ָ��ע��Ce��AZ31�Ŀ������Եõ���ߣ���Ҫԭ���DZ����γ������ܵ�Ce��������㡣������Nd���ƣ�Ce��Mg�еĹ��ܶȼ��ͣ���Ce����(��������)��������ܶ�ʱ������ԺϽ��ȼ��������Ե�Ӱ�졣��FAN��[46]���о��У���ô�Mg��ȼ��Ϊ615 �棬Ce�����ӿ������Mg�Ͻ��ȼ�㣬��Ce����(1%~13%)��Mg-Ce��Ԫ�Ͻ��ȼ��Ӱ�첢������(����4)��PRASAD��[112]���֣���Ce����Ϊ0.5%~3%ʱ��Ce��Mg-Ce�Ͻ����ȼ�Լ�����Ӱ�졣������Щ�����ԭ����Ce�����ѳ�����Ce��Mg�еĹ��ܶȡ�
�� 4 Mg-Ce(1%~13 %)��Ԫ�Ͻ�ȼ��[46]
Table 4 Ignition point of Mg-Ce(1%-13%) binary alloys[46]
����Mg-Alϵ�Ͻ�Ce�Ĺ��ܶ�Լ��0.25%~0.3%֮��[74, 113]��Ce���������γɽ����仯����Ӷ�Ӱ��Ͻ�Ŀ������ԡ�LIN��[74]��AM50��AZ91D�Ͻ������Ӳ�ͬ������Ce (0~1%)���о���Ce������AM50��AZ91D�Ͻ��ĩ��ȼ�㼰��ؿ������Ե�Ӱ�졣��ʵ����AM50��AZ91D��ȼ��ֱ�Ϊ484 ���482 �档����Ce���������ӣ����ֺϽ��ȼ�㶼���ֳ������ߺ͵����ƣ�����Ce����Ϊ0.25%ʱ�ﵽ��ֵ(535 ���525 ��)����Ce�����ϵ�ʱ(0~0.15%)��Mg-Al�Ͻ����Ҫ�ɷ�Ϊ��-Mg�ͦ�-Mg17Al12����Ce����Ϊ0.25%ʱ�������п�ʼ��������������״�ṹ��Al11Ce3�����仯�����ʱ����Ĥ����������ߣ�����û�п�϶��ȱ�ݡ�Ce2O3��PBRֵΪ1.16�������¹����У��������е�Ԫ��Ce�����γ�����������Ce2O3���Ӷ�����˺Ͻ�Ŀ�������[114]������Mg-Al�Ͻ���Ce���������ӣ������Ce�������γ����ȶ���������Al11Ce3[115]������ȷ��Al11Ce3����Χ�������е�ƽ��Ce����Ҫ���ڦ�-Mg�е�ƽ��Ce�������ڸ�����Χ�γ���Ce��ƶ����(��NdԪ�ػ�������)�����ڸ�������Mg������Խϸߣ���Ce�����ϵ�[74]����ˣ�����������Ĥ�Ľṹ�ȱ����ϵ���������Ľṹ�������ɣ����ջ���Al11Ce3����Χ������Ĥ���γɸ���Ŀ���ȱ�ݣ������俹�����Ի���Ӧ������ZHOU��[55]��ZHAO��[116]Ҳ֤ʵ��Al11Ce3�����þ�Ͻ������Եĸ���Ӱ�죬����Al11Ce3��ĺ���Խ�٣�AZ91D�Ͻ��ȼ��Խ�ߡ���2.3�����������Al11Ce3����ɵ�Ӱ�죬��ͨ���������̼��������⡣�ü�����ʹ�����ӵ�Ce���ܽ�Ͻ��У��γɹ����������������Al11Ce3��[117]��ʹ���������㹻��Ce���γ�Ce2O3����Եģ�Al11Ce3����γɻ���������AlԪ�أ�ʹ�æ�-Mg17Al12�ľ����ߴ������������ͣ�����һ���̶�������߹�̬�Ͻ�Ŀ�����������
ͬʱ��Ce��Ϊ��Ӧ��Ԫ�أ�������þ�Ͻ�����γ�Ce2O3����Ĥ�⣬������CeO2��ʽ��MgO�����ƫ������Mg2+�ڹ���Ͻ��е�������ɢ���Ӷ��ӻ�����[20]�����б�����[38, 118-119]��Ce������Ϊ�������Ԫ�أ���������þ�Ͻ��������ۼ�����������Ĥ�ı������ȣ������Ce�����ڱ���������Ĥ�Ľ���֮�䣬�����ڱ�����ڸ����Ce2O3��ͬʱ���ͺϽ�����ı����������Ӷ����þ�Ͻ�Ŀ������ԡ�
��Y��Nd��ͬ��Mg�Ͻ���Ce�Ĵ��ڶ�����ѧ����û�в���Ӱ�죬�ر��Ƕ���Mg-Al���Ͻ�[19]������Ce���������ӣ���Mg-Al�Ͻ���Mg17Al12���������γ���������״�ṹ�������������ʴ����[117]����ˣ��Ӽ�����ʵ���ԽǶ���������Ce��Mg�Ͻ�ֵ�ý�һ���о���
3.4.4 ��(La)
��ȻLEONTIS������1946�귢������La��La����������Խ���þ�Ͻ����������[19]����֮����La�Ͻ�þ�Ͻ�����о����б���������La�����ȼ�Ե�����ȱ��ϵͳ���о�����������û����д���һ��̽����֤��
ZHANG��[120]�õ�һ��ԭ��ͨ�����ۼ���Ԥ����LaԪ���ܹ����þ�Ͻ���ȼ�Ե�3�����û�����������������Laԭ��������Mg(0001)������룬ȡ��Mg(0001)�����Mgԭ�ӣ����Laԭ�Ӹ�������ƫ��Mg�ı���㡣������ӦO����������Ϊ���ȹ��̣���La�Ͻ��Mg(0001)����ķ�����С�ڴ�Mg���棬�Դ������þ�Ͻ��ȼ�㡣�Ͻ�ȼ���ȼ��������Mg��LaԪ�ض���O�к�ǿ��ԭ����������ˣ���Laþ�Ͻ������Ĥ��MgO��La2O3��ɡ�La2O3��PBRֵΪ1.10������ϡ����������γ���ֹ������þ�Ͻ��һ��������La-O���ۼ�����La2O3���ܻ���ԭ��[120]��La�Ͻ�����Mg��La��O�ĵ��ת�ƣ�������MgO�����ɴӶ������þ�Ͻ����ȼ����[120]��
PRASAD��[112]���֣�Mg-0.2La��Mg-3La�Ͻ�ʱ�䱩¶�ڻ����о��ᷢ���������ۻ��͵���������Ʒ���δ������ۻ����ֻᷢ�������Ż����ڻ����Ƴ�ʱϨ�𡣶�������IJ�֮ͬ����Mg-0.2La�Ͻ��������IJ��ּ���ȼ�գ���Mg-3La�Ͻ��������IJ��ֻ���Ϩ�𡣿ɼ���Mg-0.2La�Ͻ��Mg-3La�Ͻ���ȼ�Խϲ��Mg-3La���������������ſ���м�̵������ﲢ�Ҳ���ȼ�գ���ȼ�ԽϺá�������γ����������ﱣ��Ĥ��Ҫ�������LaŨ�ȣ�ֻ�г�����һŨ�ȲŻ��нϺõ���ȼЧ����
�����ڶ�Ԫ�Ͻ�La�����ý�Ϊ���ӣ�La�ĺ������߶����ȼ��������á�ZHAO��[45]�о���LaԪ���ڸ���AZ31�Ͻ�Ŀ��������е����á�����La������0.35%���ӵ�1.15%ʱ��AZ31�Ͻ��ȼ����ֳ������Ӻ͵����ơ���La����ԼΪ0.7%ʱ��AZ31�Ͻ���ֳ����ȼ��(Լ575 ��)����ʱ�γɵ������������ܣ��������ܵ��������������ߵ���ȼ���ܣ���La������������ʱ��������ṹ�����ɢ�������������ߡ���Ce��Nd���ƣ�La��Mg�еĹ��ܶ�Ҳ�ܵͣ��ݱ���La������������ܶ�ʱ����ʹ�Ͻ�Ŀ������Խ�һ����ߣ������ή������ȼ��[45, 120-121]����Mg-Al�Ͻ��У���La����δ����ܶ�֮ǰ�����������������ӣ�La������Ͻ��У���ʱ�Ͻ����ߴ��С���۽ṹ����ϸ������La����������Mg�еĹ��ܶ�ʱ�����ؾ����γɽ����仯����Al11La3[45]����ʱ�Ͻ������֯��֡�Al11La3�����˹������е�La���ƻ�������������ľ����ԣ��Ӷ����ºϽ�Ŀ����������½���ֵ��ָ�����ǣ�����ZHAO��[45]��ʵ������������������La���ܽ����������ʣ����Dz�������þ�Ͻ�����������ڡ���ԭ�������������ͽ�����ɢ���ʵIJ��쵼����������IJ�������[122]����ʹ������ͻ���Ľ��������ܱ����ڲ��������Ӷ�ʹ�������ʼӿ졣��MEENASHISUNDARAM��[121]���о��У�Mg-0.5Zr�Ͻ�ȼ��Ϊ615 �棬����1%��La�ܹ�ʹ�úϽ��ȼ��������645 �档��������La�����ԺϽ��ȼ��û��������Ӱ�졣�����о�����˵���������������û�ж���ԭ�����н��͡�
������������֪��La���Ǹ��ƹ�̬����̬��Mg�Ͻ������Ե�ʵ�����ʣ�����������Mg�еĹ��ܶȼ��ϵͣ���ȼЧ�����ޡ���Щ���������Ƕ��о���La��þ�Ͻ��������Ϊȱ����Ȥ����Ҫԭ��[19]������LaԪ�������þ�Ͻ�Ŀ������Է���ȷʵ���ŷdz����������ã�ֵ�ý�һ������̽�������⣬La�������Mg�Ͻ�ijߴ��ȶ��ԡ�����ǿ�Ⱥ�ѹ��ǿ�ȶ����л���Ӱ��[121]����ˣ���Laþ�Ͻ���нϴ�ķ�չDZ����
3.4.5 ��(Gd)
GdҲ�Ƕ����Mg�Ͻ����ȼ�Ծ��л������õ�ϡ��Ԫ��֮һ����PRASAD��[112]��ȼ���Բ����У���״Mg-5Gd�Ͻ����¶ȴﵽ600 ��ʱ�ۻ�������ۻ��������ĵ�𣬻�������۵ε��䣬�����������˻�����۵λ����Ϩ�𡣸úϽ�ĵ�����ⲿ������ڵ�������Ϩ��������GdԪ�ص���ȼ���á���ԭ�����γ�����ѧ���ܺõ����������������ܵ��������谭�˽�һ��������ȼ�շ�Ӧ[112]��ARRABAL��[52]������AZ91D������GdԪ�أ����Դ��̬�Ͻ�ĸ����������ʣ���410 ����7���ƽ���������ʱ�δ����GdԪ�ص�AZ91D�Ͻ���81%��ԭ����GdԪ�صļ��룬�ٳ����м���Al2Gd���γɣ��ɼ�С���۵��-Mg17Al12��ijߴ���������������Gd���������ӣ���-Mg17Al12���������١���2.2������������GdԪ����Mg�еĹ��ܶ�(Ħ������)�ܸ�(Լ4.53%)�����ܶȽϸߵ������ڻ������������л���ȫ���Ȼ����ٽ�����������������γɣ��Ӷ������þ�Ͻ����ȼ�ԡ���KIM��[11]��ʵ���У�Mg��ȼ��Ϊ504 �棬��Mg-0.48%Gd(Ħ������)��ȼ��ߴ�707 �档����Ԥ���ڴﵽ���ܶ�ǰ���Ͻ���Gd����Խ�ߣ���ȼ���������ߡ�WU��[123]�Ʊ���һ�ָ�ǿ����ȼþ�Ͻ�Mg-15.3Gd-1.8Ag-0.3Zr (GQ152K)����Gd�����ߴ�15.3%���úϽ����930 ��Ļ����·���6 min���ϣ�ȼ��ߴ�935 �档��G11��WE43��Mg-Alϵ�����úϽ���ȣ�GQ152K�Ͻ��ȼ����ߣ���ȼ���ܸ������죬������Ϊ���ڸ���ʱ�γ�Gd2O3��Ag2O��ɵ���������Ĥ��
3.4.6 ��(Er)
ErԪ�ض�þ�Ͻ�����������������б�����Er����Mg�У�����O2������Ӧ����MgO�е�O�����û���Ӧ����Er2O3����ϡ���������PBRֵ����1�����������ܹ���Ч��ֹO2���ڲ�Mg������Ӧ���Ӷ���Һ̬þ�Ͻ������ȼ����[124]�����⣬����Er��Mg�еĹ��ܶȺܸߣ���ȫ���ܵĺϽ��ڸ����¿����γɾ��������ܵ������㣬��ˣ���Erþ�Ͻ���нϸߵ�ȼ��[11]�����⣬��Mg-Al�Ͻ���ErԪ�ص����ӣ�������Чϸ������ִ��Mg17Al12�࣬����ǿ����Mg17Al12��������ʹMg17Al12���ȷ�ɢ����ߺϽ����ѧ����[125]�����γɵ�Al3Er���λ���������ã�ʹ�Ͻ����ѧ���ܺ��쳤�ʵõ��������[126]������Al3Er����γɣ����۵����-Mg17Al12����������С����ˣ��ڽ����о��пɴӽ����仯����Ƕ���̽��ErԪ�ض�þ�Ͻ�ȼ���Ӱ�졣
3.5 ��Ԫ��ȼþ�Ͻ�
�о���������һԪ�ص����û��������Ƿ�����Mg���������ֻ����Ԫ���ܹ��������õ���ȼЧ����ͬʱ���ܱ������ӵ�һԪ����ɵIJ���Ӱ�졣
ϡ��Ԫ��֮�䳣����ЭͬԪ��ЧӦ��������[100]ָ������ԪMg-Y��ȼ�Ͻ���Y���������10%����Y��������8%ʱ�Ͻ���ࡣ��Mg-Y��Ԫ�Ͻ�������������Ce������Ϊ����Ԫ�ز���������Ԫ��ЧӦ�����ɴ��Y����ֵ������Mg3Y0.7Ce (����������%)�ɴﵽ��ȼ��Ч����LI��[127]�о���Nd��Dy��AZ91D�Ͻ����ȼ���ܵ�Эͬ���á�һ���棬Dy2O3��䵽MgOĤ�Ŀ��У���һ���棬Nd��Dy�����ӿ��Դ����ٵ��۵����-Mg17Al12���γɡ����⣬Nd��Dy������ʹ��-Mg17Al12������AZ91D�Ͻ�ľ�������������Ϊ��AZ91D-Nd-Dy�Ͻ��еķ�ɢ�ֲ�����������ɢͨ���ļ��٣��Ӷ���������ߺϽ�Ŀ������ԡ�����ϡ��Ԫ��֮���Эͬ���ã���Y��Nd[92]��Y��Gd[128]��Ҳ��ͨ���γ��������ܵĸ���������ı�ڶ�����ɼ��ֲ�����ߺϽ�Ŀ����������ԡ�
þ�Ͻ��е�������CaԪ��ʱ��Ҫ�����õ���ȼЧ�����������������ܸ�(>1.7%)[63]���γɵ�Al2Ca����������߿������Ե���ʹ�Ͻ��࣬��ˣ�ͨ�����Ӵ�����Ca��ʵ�����õ���ȼЧ����ʵ��Ӧ�����Dz���ȡ�ġ�Ca����ϡ��Ԫ�����ʹ�ã����������ȼ�Ե�ͬʱ����Al2Ca��Բ��ϻ�е���ܴ����ĸ���Ӱ�졣��Caþ�Ͻ�������ϡ��Ԫ�ػ�ʹ����ϸ�����Ӷ������������ܣ��������쳤��[129]��CHENG��[81]��AZ91������Ca�������ڸ������γɵ�����Ĥ���Ҵ࣬�ڱ��ι������������ѡ���������Y��������������Y2O3���γɴ���������Ĥ���ܶȺ����ԡ�����Ca��Y������Эͬ���ã���������Mg-4Zn-4Al-0.7Ca-0.6Y��ȼþ�Ͻ�[130]������ʱ�γ�CaO��Y2O3��ɵ�����������ṹ[36, 129-130]����ȼ����ߵ�ԭ���⣬Ca��Gd��Эͬ���ÿ������ٽ����ȶ���Al2Ca�������Ҿ��ȷֲ���һ���̶��������˵��۵��-Mg17Al12�࣬�Ӷ�����˹�̬�Ͻ�Ŀ�������[131]������Ca��Nd��Эͬ���ã�Nd���ʵ����ӿ���ͨ���γ�Ca-Mg-Nd-O�����������ֹMg������ɢ�������������Ͻ�������ͬʱ�γɹ������AlxNdy��������ǿ���������ǿ�Ⱥ���չ��[132]��
Be����Ca��ϡ��Ԫ�ز���ЭͬԪ��ЧӦ�����Be�ĸ߳ɱ������Լ���Be������ɵľ����ֻ���������Be��������ȼMg�Ͻ���м�����ʵ�����塣Be��Ca��Эͬ�����ڱ�֤������ȼ�Ե�ͬʱ�ɴ��Be������
TAN��[61]���о��з��֣�AZ91+20��10-6 Be+0.5%Ca��������Ϊ��AZ91+60��10-6 Be��������Ϊ�൱����Be����������ǿ�ȵ�ͬʱ��Ca�����ӻ���Beǿ����������������·��γ�CaO/MgO���������㣬�ṩ����Ŀ�����������Be��ϡ��Ԫ��������Ҳ����ǿ�����á�INOUE��[43]�ں�Yþ�Ͻ��м���Be���о��������������Ϊ��������δ����Beʱ�������ºϽ�����γ��˴ֲ��Һ��Y2O3�㣬��ʱ�Ͻ�ȼ��ԼΪ1150 K�������뼫������Beʱ���Ͻ��ڸ������γ��˱����������ܵ�Y2O3�㣬��ȼ��ߴ�1320 K��ͬʱ����ָ����Be��Y2O3�㾧���ƫ���谭�������Ӻ������ӵľ�����ɢ�������������û�����Ч��ֹ�˺Ͻ����������Ϊ������˺Ͻ�Ŀ������ԡ�
ЭͬԪ��ЧӦΪ������������þ�Ͻ��ṩ���µ�˼·��Ŀǰ��ͨ��ЭͬԪ��ЧӦ���ѿ�������WE43(Y+Nd)��Elektron21(Nd+Gd)�ȸ�ǿ����ȼþ�Ͻ�[8, 92]�����ѴﵽFAA��ģ��ʵ����Ա������������ú��պ������������˽����Ԫ��Эͬ���û����Ը�������ȼþ�Ͻ�Ŀ����ռ�������Ҫ���塣
4 ����
����������Ŀǰ�ձ������ȼԪ�ص�PBRģ�ͺͽ����仯���������ͺϽ������Ժ���ȼ�Եı仯�������������о��ɹ����Եó����ۣ������仯������ڹ�̬þ�Ͻ���������Ӱ��ϴ�������ṹ�����ʶ��ڹ�̬�����̬��Һ̬þ�Ͻ������Ծ�Ӱ��ϴ��ر��Ƕ��ڰ��̬��Һ̬þ�Ͻ�ZHAO��[133]ָ�����ڶ���Ĵ�С���������������Źؼ����ã�Mg17Al12��ֻҪΪ������״��ʽ�����Ϳ��Գ䵱�谭������Ӧ�����ϡ������۵���Mg17Al12������ڻ����ۻ������ٺϽ��ɹ�̬��Һ̬��ת�䣬�Ӷ�������������ȼ�ա�Ca��ϡ����Ԫ�ص������ܼ�СMg17Al12�������������γ����ȶ��м��࣬�Ӷ�ʹ��̬�Ͻ�ĸ����������ʼ��������¶ȼ������ߣ���Ȼ���ȶ��м���ᷢ���仯�������忪ʼ�ɹ�̬����̬��Һ̬ת�䣬��ʱ���ȶ��м������ô����������������������ʶ��俹�����Ժ���ȼ������������á������������ȶ��м��������˻����е���ȼԪ�أ���˲����γ������Ҿ��ȵı���������Ĥ����ʱ���ȶ��м���������á����ں�Caþ�Ͻ𣬸���LEE��[64]��INOUE��[65]���о���֤���������ۡ�ϡ��Ԫ��þ�Ͻ��Ժ�Ndþ�Ͻ�Ϊ����ARRABAL��[52]�о��˺�Nd��AZ91D�Ͻ��̬�εĸ���������Ϊ��ָ��Nd��Al������Nd-Al�����仯��������˺Ͻ��Ц�-Mg17Al12�ĺ�����ʹ�Ͻ��������ʴ�����͡�ZHAO��[105]�о���Nd�����Ӷ�AZ91D�Ͻ�ȼ���Ӱ�죬ȼ�յ�þ�Ͻ��ڰ��̬��Һ̬������ָ������Nd���ںϽ�����������Nd�γ�Al3Nd�࣬ʹ��û���㹻��Nd���ɱ����Ե�Nd2O3�����㣬����ȼ�㽵�͡���������Nd������5%ʱ���Ͻ�ȼ��Ϊ590 �棬��AZ91D��40 �档������Ϊ��ʱ������Nd�������㣬���������ܵ�MgO/Nd2O3/ Al2O3���������㣬�����þ�Ͻ����ȼ�ԡ���˽����仯����ֻ������ߺϽ���ǰ�ĸ������������ã���Ҫ���þ�Ͻ��ȼ�㣬������ṹ�����ʲ��Ǿ��������ء�
��Ȼ���Ƕ���Mg�ĸ���������ȼ�ջ������������˽⣬���ڸ�Ԫ�ص���ȼ���û�������һ������֪��������ȼþ�Ͻ�ķ�չ��Ȼ����һЩ�����벻�㣺
1) Ŀǰ���ںϽ���ȼ�Ļ��������ǿ��ǵ������в�ȫ�棬���ֻ����Ľ��ʹ�������Ԥ�⣬ȱ�����ݵ�֧�֡����⣬�Ի����Ľ���ֻ�Ƕ��Է�����û�н����Ͻ���ȼ������������(����ѧ���ܡ���ʴ����)֮��Ķ�����ϵ�����ֶ�����ϵ���ڿ������ͺϽ�������Ҫ������Ҫ������ʵ��̽����
2) þ�Ͻ����ȼ�����伸����״�ͼ�������Ӱ��ܴ�Ŀǰ����þ�Ͻ���ȼ���ܵIJ���û�й̶��ı���ʹ�����ǶԺϽ�Ŀ����������Լ���ȼ�Ե���������û�б��綨����ˣ����ڲ�ͬ���������µ�þ�Ͻ��б�Ҫ������������������þ�Ͻ�������������µķ��ա�
3) �Ͻ����Ǹ��Ƹ��������Ե���Ч�ֶΣ�����Ҫ���ǵ����ؽ϶࣬����Ϊʵ�ֹ���Ӧ��Ҫ�ۺϿ��ǺϽ�Ԫ�ض���ѧ���ܡ���ʴ�Եȵ�Ӱ�죬���Dz�ͬԪ��֮���Ƿ�����Ӱ�졣���õ���ȼ��������������֮���ì����δ�����������Լ������������һì�ܡ�þ�Ͻ�ı�����Լ����ѱ����ڸ��������Ӳ�ȡ���ʴ�Ժ���ĥ�Եȹ������ԣ����й�þ�Ͻ���ȼͿ����о����б�����ԭ����þ�Ͻ����������ϵ�����ߵ�ȱ�㣬������ϵ���Ľϴ����ʹ��Ϳ���ڸ����»ᷢ�����䡣��ˣ��б�Ҫ������þ�Ͻ�������ϵ����ƥ���Ϳ�㣬��������ȼ���ܽ��������������ۺ��������������þ�Ͻ�Ϳ�㡣
REFERENCES
[1] BUHA J. Mechanical properties of naturally aged Mg-Zn-Cu-Mn alloy[J]. Materials Science and Engineering A, 2008, 489(1): 127-137.
[2] NEZAMDOUST S, SEIFZADEH D. Application of Ce-V/sol-gel composite coating for corrosion protection of AM60B magnesium alloy[J]. Transactions of Nonferrous Metals Society of China, 2017, 27(2): 352-362.
[3] ���ٲ�, �� ΰ, ������, ��. Mg�Ͻ�����·�չ��Ӧ��ǰ��[J]. ����ѧ��, 2001, 37(7): 673-685.
ZENG Rong-chang, KE Wei, XU Yong-bo, et al. Recent development and application of magnesium alloys[J]. Acta Metallurgica Sinica, 2001, 37(7): 673-685.
[4] LI C Y, FENG X L, FAN X L, et al. Corrosion and wear resistance of micro-arc oxidation composite coatings on magnesium alloy AZ31-the influence of inclusions of carbon spheres[J]. Advanced Engineering Materials, 2019, 21(9): 1900446.
[5] ������, �� ��, �����, ��. �����������AZ31þ�Ͻ���֯�����ܵ�Ӱ��[J]. �й���ɫ����ѧ��, 2020, 30(1): 60-68.
LI Yan-sheng, QU Cheng, WANG Jin-hui, et al. Effect of multi-pass warm rolling process on microstructure and properties of AZ31 magnesium alloy[J]. The Chinese Journal of Nonferrous Metals, 2020, 30(1): 60-68.
[6] CZERWINSKI F. Controlling the ignition and flammability of magnesium for aerospace applications[J]. Corrosion Science, 2014, 86: 1-16.
[7] HAN D, ZHANG J, HUANG J, et al. A review on ignition mechanisms and characteristics of magnesium alloys[J]. Journal of Magnesium and Alloys, 2020, 8(2): 329-344.
[8] TEKUMALLA S, GUPTA M. An insight into ignition factors and mechanisms of magnesium based materials: A review[J]. Materials & Design, 2017, 113: 84-98.
[9] DING W, WANG X, ZENG X, et al. Cyclic oxidation behaviour of cerium implanted AZ31 magnesium alloys[J]. Materials Letters, 2007, 61(6): 1429-1432.
[10] CZERWINSKI F. Overcoming barriers of magnesium ignition and flammability[J]. Advanced Materials and Processes, 2014, 172(5): 28-31.
[11] KIM Y M, YIM C D, KIM H S, et al. Key factor influencing the ignition resistance of magnesium alloys at elevated temperatures[J]. Scripta Materialia, 2011, 65(11): 958-961
[12] KAWABATA H, YAGI Y, AOKI Y, et al. Effect of calcium on the combustion behavior of molten AZ91 magnesium alloy[J]. Journal of the Japan Institute of Metals and Materials, 2019, 83(2): 46-53.
[13] WANG W, WANG W, WANG Q, et al. Flame resistance and oxidation behavior of Mg-Y-Ce-Zr alloys[J]. Materials Research Express, 2018, 6(1): 016536.
[14] CHENG C, LAN Q, WANG A, et al. Effect of Ca additions on ignition temperature and multi-stage oxidation behavior of AZ80[J]. Metals, 2018, 8(10): 766.
[15] ZENG X Q, WANG Q D, L�� Y Z, et al. Study on ignition proof magnesium alloy with beryllium and rare earth additions[J]. Scripta Materialia, 2000, 43(5): 403-409.
[16] VILLEGAS-ARMENTA L A, PEKGULERYUZ M O. The ignition behavior of a ternary Mg-Sr-Ca alloy[J]. Advanced Engineering Materials, 2020, 22: 1901318.
[17] CZERWINSKI F. The oxidation behaviour of an AZ91D magnesium alloy at high temperatures[J]. Acta Materialia, 2002, 50(10): 2639-2654.
[18] LOPEZ M D, MUNEZ C J, CARBONERAS M, et al. Influence of temperature on oxidation behaviour of ZE41 magnesium alloy[J]. Journal of Alloys and Compounds, 2010, 491(1/2): 131-136.
[19] TAN Q, ATRENS A, MO N, ZHANG M X. Oxidation of magnesium alloys at elevated temperatures in air: A review[J]. Corrosion Science, 2016, 112: 734-759.
[20] CZERWINSKI F. Oxidation characteristics of magnesium alloys[J]. JOM, 2012, 64(12): 1477-1483.
[21] CZERWINSKI F. The early stage oxidation and evaporation of Mg-9%Al-1%Zn alloy[J]. Corrosion Science, 2004, 46(2): 377-386.
[22] MEDVED J, MRVAR P, VONCINA M. Oxidation resistance of cast magnesium alloys[J]. Oxidation of Metals, 2009, 71(5/6): 257-270.
[23] DONG B L, NGUYEN T D, KIM Y J. Oxidation of ZC63 Mg alloys reinforced with SiC particles between 390 �� and 500 �� in air[J]. Metals & Materials International, 2010, 16(5): 761-766.
[24] LOPEZ M D, MUNEZ C J, CARBONERAS M, et al. Influence of temperature on oxidation behaviour of ZE41 magnesium alloy[J]. Journal of Alloys and Compounds, 2010, 491(1/2): 131-136.
[25] TODA-CARABALLO I, GALINDO-NAVA E I, RIVERA-DIAZ-DEL-CASTILLO P E J. Understanding the factors influencing yield strength on Mg alloys[J]. Acta Materialia, 2014, 75: 287-296.
[26] SMELTZER W W. Oxidation of an aluminum-3 per cent magnesium alloy in the temperature range 200 ��C550 ��[J]. Journal of The Electrochemical Society, 1958, 105(2): 67-71.
[27] AYDIN D S, BAYINDIR Z, HOSEINI M, et al. The high temperature oxidation and ignition behavior of Mg-Nd alloys part I: The oxidation of dilute alloys[J]. Journal of Alloys and Compounds, 2013, 569: 35-44.
[28] CZERWINSKI F. Factors affecting the oxidation nature of magnesium alloys[J]. JOM, 2004, 56(5): 29-31.
[29] PRASAD A, SHI Z, ATRENS A. Flammability of Mg-X binary alloys[J]. Advanced Engineering Materials, 2012, 14(9): 772-784.
[30] PRASAD A, SHI Z, ATRENS A. Influence of Al and Y on the ignition and flammability of Mg alloys[J]. Corrosion Science, 2012, 55: 153-163.
[31] CZERWINSKI F. The reactive element effect on high- temperature oxidation of magnesium[J]. International Materials Reviews, 2015, 60(5): 264-296.
[32] YUAN C, HUANG D, CHANG L, et al. Ignition behavior of magnesium powder layers on a plate heated at constant temperature[J]. Journal of Hazardous Materials, 2013, 246-247: 283-290.
[33] LIU C, LU S, FU Y, et al. Flammability and the oxidation kinetics of the magnesium alloys AZ31, WE43, and ZE10[J]. Corrosion Science, 2015, 100: 177-185.
[34] JEURGENS L P H, VINODH M S, MITTEMEIJER E J. Initial oxide-film growth on Mg-based MgAl alloys at room temperature[J]. Acta Materialia, 2008, 56(17): 4621-4634.
[35] AYDIN D S, BAYINDIR Z, PEKGULERYUZ M O. The effect of strontium(Sr) on the ignition temperature of magnesium(Mg): A look at the pre-ignition stage of Mg-6wt% Sr[J]. Journal of Materials Science, 2013, 48(23): 8117-8132.
[36] ZHOU N, ZHANG Z, DONG J, et al. Selective oxidation behavior of an ignition-proof Mg-Y-Ca-Ce alloy[J]. Journal of Rare Earths, 2013, 31(10): 1003-1008.
[37] ZENG R, HAN E, KE W. A critical discussion on influence of loading frequency on fatigue crack propagation behavior for extruded Mg-Al-Zn alloys[J]. International Journal of Fatigue, 2012, 36(1): 40-46.
[38] TAN Q, YIN Y, MO N, et al. Recent understanding of the oxidation and burning of magnesium alloys[J]. Surface Innovations, 2019, 7(2): 71-92.
[39] ���ٲ�. ���ϵĸ�ʴ�����[M]. ����: ��ѧ��ҵ������, 2006.
ZENG Rong-chang. Corrosion and protection of materials[M]. Beijing: Chemical Industry Press, 2006.
[40] TAN Q, MO N, JIANG B, et al. Oxidation resistance of Mg-9Al-1Zn alloys micro-alloyed with Be[J]. Scripta Materialia, 2016, 115: 38-41.
[41] TAN Q, MO N, LIN C L, et al. Improved oxidation resistance of Mg-9Al-1Zn alloy microalloyed with 60 wt ppm Be attributed to the formation of a more protective (Mg,Be)O surface oxide[J]. Corrosion Science, 2018, 132: 272-283.
[42] AYDIN D S, HOSEINI M, PEKGULERYUZ M O. Understanding the high temperature oxidation and ignition behaviour of two-phase Mg-Nd alloys and a comparison to single phase Mg-Nd[J]. Philosophical Magazine, 2015, 95(3): 259-274.
[43] INOUE S I, YAMASAKI M, KAWAMURA Y. Oxidation behavior and incombustibility of molten Mg-Zn-Y alloys with Ca and Be addition[J]. Corrosion Science, 2019, 149: 133-143.
[44] AYDIN D S, BAYINDIR Z, PEKGULERYUZ M O. High temperature oxidation behavior of hypoeutectic Mg�CSr binary alloys: The role of the two-phase microstructure and the surface activity of Sr[J]. Advanced Engineering Materials, 2015, 17(5): 697-708.
[45] ZHAO S, ZHOU H, ZHOU T, et al. The oxidation resistance and ignition temperature of AZ31 magnesium alloy with additions of La2O3 and La[J]. Corrosion Science, 2013, 67: 75-81.
[46] FAN J F, YANG G C, CHEN S L, et al. Effect of rare earths (Y, Ce) additions on the ignition points of magnesium alloys[J]. Journal of Materials Science, 2004, 39(20): 6375-6377.
[47] ��־��, �����, �� ��, ��. Mg-Ndϵ�Ͻ�Nd��þ�Ͻ��е�Ӧ����չ��[J]. ���켼��, 2012, 33(2): 151-154.
LIU Zhi-jie, WU Guo-hua, PANG Song, et al. Mg-Nd alloy and application of Nd in magnesium alloys[J]. Foundry Technology, 2012, 33(2): 151-154.
[48] �� ��, ������, ������, ��. ��ͭAZ31þ�Ͻ�ĸ�ʴ��Ϊ[J]. �й���ɫ����ѧ��, 2019, 29(1): 18-26.
ZHOU Miao, LIU Chu-ming, GAO Yong-hao, et al. Corrosion behavior of Cu-containing AZ31 magnesium alloy[J]. The Chinese Journal of Nonferrous Metals, 2019, 29(1): 18-26.
[49] BAHMANI A, ARTHANARI S, SHIN K S. Corrosion behavior of Mg-Mn-Ca alloy: Influences of Al, Sn and Zn[J]. Journal of Magnesium and Alloys, 2019, 7(1): 38-46.
[50] CHENG C, LE Q, LI X, et al. Understanding on ignition mechanism of Mg-xAl (x=0, 3, 6 and 8wt.%) alloys in atmospheric environment[J]. Corrosion Science, 2020, 168: 108565.
[51] HUANG H, YUAN G, CHU Z, et al. Microstructure and mechanical properties of double continuously extruded Mg-Zn-Gd-based magnesium alloys[J]. Materials Science and Engineering A, 2013, 560: 241-248.
[52] ARRABAL R, PARDO A, MERINO M C, et al. Oxidation behavior of AZ91D magnesium alloy containing Nd or Gd[J]. Oxidation of Metals, 2011, 76(5/6): 433-450.
[53] LIN P Y, ZHOU H, LI W P, et al. Effect of cooling rate on oxidation resistance and powder ignition temperature of AM50 alloy with addition of yttrium[J]. Corrosion Science, 2009, 51(2): 301-308.
[54] YU X, SHEN S, JIANG B, et al. The effect of the existing state of Y on high temperature oxidation properties of magnesium alloys[J]. Applied Surface Science, 2016, 370: 357-363.
[55] LI W, ZHOU H, ZHOU W, et al. Effect of cooling rate on ignition point of AZ91D�C0.98wt.% Ce magnesium alloy[J]. Materials Letters, 2007, 61(13): 2772-2774.
[56] GOVIND, NAIR K S, MITTAL M C, et al. Development of rapidly solidified (RS) magnesium-aluminium-zinc alloy[J]. Materials Science and Engineering A, 2001, 304-306: 520-523.
[57] �˸���, ������. �����ܱ���þ�Ͻӹ�����[M]. ����: ��ѧ������, 2007.
PAN Fu-sheng, HAN En-hou. High performance wrought magnesium alloy and its processing technology[M]. Beijing: Science Press, 2007.
[58] AYDIN D S, BAYINDIR Z, PEKGULERYUZ M O. The high temperature oxidation behavior of Mg-Nd alloys. Part II: The effect of the two-phase microstructure on the on-set of oxidation and on oxide morphology[J]. Journal of Alloys and Compounds, 2014, 584: 558-565.
[59] TAN Q, MO N, LIN C L, et al. Generalisation of the oxide reinforcement model for the high oxidation resistance of some Mg alloys micro-alloyed with Be[J]. Corrosion Science, 2019, 147: 357-371.
[60] SAKAMOTO M, AKIYAMA S, OGI K. Suppression of ignition and burning of molten Mg alloys by Ca bearing stable oxide film[J]. Journal of Materials Science Letters, 1997, 16(12): 1048-1050.
[61] TAN Q, MO N, JIANG B, et al. Combined influence of Be and Ca on improving the high-temperature oxidation resistance of the magnesium alloy Mg-9Al-1Zn[J]. Corrosion Science, 2017, 122: 1-11.
[62] YOU B S, PARK W W, CHUNG I S. The effect of calcium additions on the oxidation behavior in magnesium alloys[J]. Scripta Materialia, 2000, 42(11): 1089-1094.
[63] ������, �����, ������, ��. ��Ca��ȼþ�Ͻ�ĸ���������Ϊ[J]. �й���ɫ����ѧ��, 2004, 14(10): 1666-1670.
FAN Jian-feng, YANG Gen-cang, CHENG Su-ling, et al. Oxidation behavior of ignition-proof magnesium-calcium alloys[J]. The Chinese Journal of Nonferrous Metals, 2004, 14(10): 1666-1670.
[64] LEE D B. High temperature oxidation of AZ31+0.3wt.%Ca and AZ31+0.3wt.%CaO magnesium alloys[J]. Corrosion Science, 2013, 70: 243-251.
[65] INOUE S I, YAMASAKI M, KAWAMURA Y. Formation of an incombustible oxide film on a molten Mg-Al-Ca alloy[J]. Corrosion Science, 2017, 122: 118-122.
[66] KIM Y H, KIM W J. Flame-resistant Ca-containing AZ31 magnesium alloy sheets with good mechanical properties fabricated by a combination of strip casting and high-ratio differential speed rolling methods[J]. Metals and Materials International, 2015, 21(2): 374-381.
[67] KWAK T Y, LIM H K, KIM W J. The effect of 0.5 wt.% Ca addition on the hot compressive characteristics and processing maps of the cast and extruded Mg-3Al-1Zn alloys[J]. Journal of Alloys and Compounds, 2016, 658: 157-169.
[68] MIN X, DU W, FENG X, et al. Analysis of EET on Ca increasing the melting point of Mg17Al12 phase[J]. Chinese Science Bulletin, 2002, 47(13): 1082-1086.
[69] LI P, TANG B, KANDALOVA E G. Microstructure and properties of AZ91D alloy with Ca additions[J]. Materials Letters, 2005, 59(6): 671-675.
[70] HAN G, CHEN D, CHEN G, et al. Development of non-flammable high strength extruded Mg-Al-Ca-Mn alloys with high Ca/Al ratio[J]. Journal of Materials Science & Technology, 2018, 34(11): 2063-2068.
[71] �� ��, ���Ӵ�, ������, ��. ��Caþ�Ͻ�����۸�ʴ��һ��ԭ���о�[J]. �й���ɫ����ѧ��, 2019, 29(2): 361-369.
ZHANG Yong, BAI Pu-cun, CUI Xiao-ming, et al. First principle study on micro-corrosion of magnesium alloy with Ca contents[J]. The Chinese Journal of Nonferrous Metals, 2019, 29(2): 361-369.
[72] GRADINGER R, GNEIGER S, BETZ A. Investigations on fire-resistant magnesium alloys for aerospace applications[J]. Materials Science Forum, 2015, 828/829: 492-498.
[73] ZENG R C, QI W C, CUI H Z, et al. In vitro corrosion of as-extruded Mg-Ca alloys��The influence of Ca concentration[J]. Corrosion Science, 2015, 96: 23-31.
[74] LIN P Y, ZHOU H, LI W, et al. Interactive effect of cerium and aluminum on the ignition point and the oxidation resistance of magnesium alloy[J]. Corrosion Science, 2008, 50(9): 2669-2675.
[75] LEE J K, KIM S K. Effect of CaO addition on the ignition resistance of Mg-Al alloys[J]. Materials Transactions, 2011, 52(7): 1483-1488.
[76] HUANG Y B, CHUNG I S, YOU B S, et al. Effect of be addition on the oxidation behavior of Mg-Ca alloys at elevated temperature[J]. Metals and Materials International, 2004, 10(1): 7-11.
[77] ZENG X, WANG Q, L�� Y, et al. Influence of beryllium and rare earth additions on ignition-proof magnesium alloys[J]. Journal of Materials Processing Technology, 2001, 112(1): 17-23.
[78] ZENG X, WANG Q, L�� Y, et al. Behavior of surface oxidation on molten Mg-9Al-0.5Zn-0.3Be alloy[J]. Materials Science and Engineering A, 2001, 301(2): 154-161.
[79] MISRA A, SHARIF A A, PETROVIC J J, et al. Rapid solution hardening at elevated temperatures by substitutional Re alloying in MoSi2[J]. Acta Materialia, 2000, 48(4): 925-932.
[80] ZHOU Y C, CHEN J X, WANG J Y. Strengthening of Ti3AlC2 by incorporation of Si to form Ti3Al1-xSixC2 solid solutions[J]. Acta Materialia, 2006, 54(5): 1317-1322.
[81] CHENG S L, YANG G C, FAN J F, et al. Effect of Ca and Y additions on oxidation behavior of AZ91 alloy at elevated temperatures[J]. Transactions of Nonferrous Metals Society of China, 2009, 19(2): 299-304.
[82] WARD E, OKUN A, RUDER A, et al. A mortality study of workers at seven beryllium processing plants[J]. American Journal of Industrial Medicine, 1992, 22(6): 885-904.
[83] CAO P, QIAN M, STJOHN D H. Grain coarsening of magnesium alloys by beryllium[J]. Scripta Materialia, 2004, 51(7): 647-651.
[84] ������, �� ��, Ѧ����, ��. ��ȼþ�Ͻ��о���״[J]. ���Ͽ�ѧ, 2011, 1(2): 56-59.
LI Yong-yan, DING Jian, XUE Hai-tao, et al. Current research on ignition-proof magnesium alloys[J]. Material Sciences, 2011, 1(2): 56-59.
[85] VAN ORMAN J A, CRISPIN K L. Diffusion in oxides[J]. Reviews in Mineralogy and Geochemistry, 2010, 72(1): 757-825.
[86] ������. ������ϡ��þ�Ͻ��о���Ӧ�ý�չ[J]. ������ɫ����, 2018, 511(19): 167-168.
DONG Tian-yu. Progress in research and application of high performance rare earth magnesium alloys[J]. World Nonferrous Metal, 2018, 511(19): 167-168.
[87] �� ǫ, �ܹ���. ϡ��þ�Ͻ��йؼ��༰����������ܵ������[J]. �й���ɫ����ѧ��, 2019, 29(9): 1934-1952.
LI Qian, CHOU Kuo-chih. Relationships between key phases and their interfaces with properties in rare earth-magnesium alloys[J]. The Chinese Journal of Nonferrous Metals, 2019, 29(9): 1934-1952.
[88] CHEN Zhi-hong, REN Xue-ping, ZHANG Ya. Effect of RE on the ignition-proof, microstructure and properties of AZ91D magnesium alloy[J]. International Journal of Minerals Metallurgy and Materials, 2005, 12(6): 540-544.
[89] ISSA A, SAAL J E, WOLVERTON C. Physical factors controlling the observed high-strength precipitate morphology in Mg-rare earth alloys[J]. Acta Materialia, 2014, 65: 240-250.
[90] ������, ���, Ѧ����, ��. ���ϡ����ZM5þ�Ͻ�������ȼ�¶ȵ�Ӱ��[J]. �����ѧѧ��, 2003, 26(5): 33-36.
ZOU Yong-liang, LI Hua-ji, XUE Han-song, et al. Effect of mischmetal additions on the ignition temperature of molten ZM5 magnesium alloy[J]. Journal of Chongqing University, 2003, 26(5): 33-36.
[91] RAO Jin-song, LI Hua-ji, XUE Han-song. Ignition-proof mechanism of ZM5 magnesium alloy added with rare earth[J]. Journal of Central South University of Technology, 2010, 17(1): 28-33.
[92] ZHAO X, NING Z, LI Z, et al. In-mold oxidation behavior of Mg-4.32Y-2.83Nd-0.41Zr alloy[J]. Journal of Materials Science, 2018, 53(15): 11091-11103.
[93] RAVI KUMAR N V, BLANDIN J J, SUERY M, et al. Effect of alloying elements on the ignition resistance of magnesium alloys[J]. Scripta Materialia, 2003, 49(3): 225-230.
[94] YU X, JIANG B, YANG H, et al. High temperature oxidation behavior of Mg-Y-Sn, Mg-Y, Mg-Sn alloys and its effect on corrosion property[J]. Applied Surface Science, 2015, 353: 1013-1022.
[95] YU X, JIANG B, HE J, et al. Oxidation resistance of Mg-Y alloys at elevated temperatures and the protection performance of the oxide films[J]. Journal of Alloys and Compounds, 2018, 749: 1054-1062.
[96] WANG X M, ZENG X Q, ZHOU Y, et al. Early oxidation behaviors of Mg-Y alloys at high temperatures[J]. Journal of Alloys and Compounds, 2008, 460(1): 368-374.
[97] FAN J F, YANG C L, HAN G, et al. Oxidation behavior of ignition-proof magnesium alloys with rare earth addition[J]. Journal of Alloys and Compounds, 2011, 509(5): 2137-2142.
[98] WANG H, YU B, WANG W, et al. Improved corrosion resistance of AZ91D magnesium alloy by a zinc-yttrium coating[J]. Journal of Alloys and Compounds, 2014, 582: 457-460.
[99] OKAMOTO H. Mg-Y (magnesium-yttrium)[J]. Journal of Phase Equilibria, 1992, 13(1): 105-106.
[100] ������. Mg-Y-Ce��ȼþ�Ͻ����Ĥ����ȼ����[J]. �й���ɫ����ѧ��, 2011, 21(11): 2799-2804.
FAN Jian-feng. Ignition-proof mechanics of surface film of Mg-Y-Ce alloy system[J]. The Chinese Journal of Nonferrous Metals, 2011, 21(11): 2799-2804.
[101] LUO A, PEKGULERYUZ M O. Cast magnesium alloys for elevated temperature applications[J]. Journal of Materials Science, 1994, 29: 5259�C5271.
[102] SINGH L K, SRINIVASAN A, PILLAI U T S, et al. The effect of yttrium addition on the microstructure and mechanical properties of Mg alloys[J]. Transactions of the Indian Institute of Metals, 2015, 68(3): 331-339.
[103] SUDHOLZ A D, GUSIEVA K, CHEN X B, et al. Electrochemical behaviour and corrosion of Mg-Y alloys[J]. Corrosion Science, 2011, 53(6): 2277-2282.
[104] ������, �����, ��Ң��, ��. Mg-3.5Y-0.8Ca��ȼþ�Ͻ�ĸ�����������[J]. �й���ɫ����ѧ��, 2006, 16(10): 1716-1723.
FAN Jian-feng, YANG Gen-cang, ZHOU Yao-he, et al. Oxidation characteristic of ignition-proof Mg-3.5Y-0.8Ca alloys at high temperatures[J]. The Chinese Journal of Nonferrous Metals, 2006, 16(10): 1716-1723.
[105] ZHAO W M, ZHAO Y, WANG Z F, et al. Effect of Mg-Nd master alloys on ignition-proof performance of AZ91D magnesium alloy[J]. Advanced Materials Research, 2011, 214: 118-121.
[106] WANG X M, ZENG X Q, WU G S, et al. Surface oxidation behavior of MgNd alloys[J]. Applied Surface Science, 2007, 253(22): 9017-9023.
[107] BOBRYSHEV B L, ALEKSANDROVA Y P. Ignition of magnesium and its alloys[J]. Metal Science and Heat Treatment, 1988, 30(3): 219-222.
[108] ROKHLIN L L. Magnesium alloys containing rare earth metals: Structure and properties[M]. London: CRC Press, 2003.
[109] ZHANG A, HAO H, LIU X, et al. Effects of precipitates on grain size and mechanical properties of AZ31-x%Nd magnesium alloy[J]. Journal of Rare Earths, 2014, 32(5): 451-457.
[110] �Ž���, ����ƽ, �� ��. þ�Ͻ�Ce�Ͻ��о���չ[J]. ���켼��, 2011, 32(1): 111-113.
ZHANG Jin-tao, CHEN Le-ping, YIN Jian. Application of Ce alloying in magnesium alloy[J]. Foundry Technology, 2011, 32(1): 111-113.
[111] CHEN H K, GONG Z F. Oxidation behaviour of molten ZK60 and ME20 magnesium alloys with magnesium in 1,1,1,2-tetrafluoroethane/air atmospheres[J]. Transactions of Nonferrous Metals Society of China, 2012, 22(12): 2898-2905.
[112] PRASAD A, SHI Z, ATRENS A. Flammability of Mg-X binary alloys[J]. Advanced Engineering Materials, 2012, 14(9): 772-784.
[113] HONG Z, WANG M, WEI L. Effect of Ce addition on ignition point of AM50 alloy powders[J]. Materials Letters, 2006, 60(27): 3238-3240.
[114] �� ��, ��˳��, ������. ϡ����þ�Ͻ��е����ú�Ӱ��[J]. �Ϻ���ɫ����, 2003, 24(1): 27-31.
LIU Bin, LIU Shun-hua, JIN Wen-zhong. Functions and influences of rare earths in magnesium alloys[J]. Shanghai Nonferrous Metals, 2003, 24(1): 27-31.
[115] ZHOU H, ZENG X, LIU L, et al. Effect of cerium on microstructures and mechanical properties of AZ61 wrought magnesium alloy[J]. Journal of Materials Science, 2004, 39(23): 7061-7066.
[116] ZHAO H, ZHANG Y, KANG Y. Effect of cerium on ignition point of AZ91D magnesium alloy[J]. China Foundry, 2008, 5(1): 32-35.
[117] LIN P Y, ZHOU H, SUN N, et al. Influence of cerium addition on the resistance to oxidation of AM50 alloy prepared by rapid solidification[J]. Corrosion Science, 2010, 52(2): 416-421.
[118] DING J, ZHAO W M, QIN L, et al. Study of Ca and Ce additions on different ignition resistance behavior of magnesium alloy[J]. Materials Science Forum, 2014, 788: 7-11.
[119] QIN L, DING J, ZHAO W M, et al. Oxidation behavior and surface tension of Mg-1.2Ca alloy with Ce addition[J]. Rare Metal Materials and Engineering, 2016, 45(1): 23-27.
[120] ZHANG G, LUO Z, ZHANG H, et al. Ignition-proof mechanism of magnesium alloy added with rare earth La from first-principle study[J]. Journal of Rare Earths, 2012, 30(6): 573-578.
[121] MEENASHISUNDARAM G K, ONG T H D, PARANDE G, et al. Using lanthanum to enhance the overall ignition, hardness, tensile and compressive strengths of Mg-0.5Zr alloy[J]. Journal of Rare Earths, 2017, 35(7): 723-732.
[122] GHENO T, MONCEAU D, YOUNG D J. Mechanism of breakaway oxidation of Fe-Cr and Fe-Cr-Ni alloys in dry and wet carbon dioxide[J]. Corrosion Science, 2012, 64: 222-233.
[123] WU Yu-juan, PENG Li-ming, ZHAO Su, et al. Ignition-proof properties of a high-strength Mg-Gd-Ag-Zr alloy[J]. Journal of Shanghai Jiaotong University(Science), 2012, 17(6): 643-647.
[124] ����ƽ, ����ƽ, �� ��, ��. Er�Ͻ���þ�Ͻ��е������о���չ[J]. ���켼��, 2012, 33(8): 904-906.
GUO Lian-ping, CHEN Le-ping, YIN Jian, et al. Research progress on effect of Er alloying in magnesium alloy[J]. Foundry Technology, 2012, 33(8): 904-906.
[125] Ф����, �� �G, �¿���, ��. Er����̬Mg-Al-Zn-Mn�Ͻ���֯����ѧ���ܵ�Ӱ��[J]. �������켰��ɫ�Ͻ�, 2007, 27(11): 824-826.
XIAO Dai-hong, SONG Min, CHEN Kang-hua, et al. Effects of erbium addition on microstructure andmechanical properties of as-cast Mg-AI-Zn-Mn magnesium alloys[J]. Special Casting & Nonferrous Alloys, 2007, 27(11): 824-826.
[126] ZHANG J, QU-BO H E, PAN F S, et al. Effects of erbium on microstructure and mechanical properties of as-cast Mg-7Zn-3Al alloy[J]. Transactions of Nonferrous Metals Society of China, 2008, 18(S1): s22-s26.
[127] LI Yong-yan, ZHAO Wei-min, DING Jian, et al. Ignition- proof performance and mechanism of AZ91D-3Nd-xDy agnesium alloys at high temperatures[J]. China Foundry, 2018, 15(2): 97-102.
[128] XUEMIN W, WEIDONG W, YONGJIAN T, et al. Early high temperature oxidation behaviors of Mg-10Gd-3Y alloys[J]. Journal of Alloys and Compounds, 2009, 474(1/2): 499-504.
[129] LEE D B, ABRO M A, YOU B S. High-temperature oxidation of AZ91-0.3%Ca-0.1%Y alloy in air[J]. Metals and Materials International, 2017, 23(4): 720-725.
[130] YOU B S, KIM Y M, YIM C D, et al. Oxidation and corrosion behavior of non-flammable magnesium alloys containing Ca and Y[M]. New York: John-wiley: Magnesium Technology, 2014, 325-329.
[131] CHENG C, LAN Q, LIAO Q, et al. Effect of Ca and Gd combined addition on ignition temperature and oxidation resistance of AZ80[J]. Corrosion Science, 2019, 160: 108176.
[132] YUE C F, HUANG S J, CHEN J K, et al. Effects of neodymium and calcium on the thermal stability of AZ71 magnesium alloys[J]. Metals and Materials International, 2018, 24(2): 307-313.
[133] ZHAO M C, LIU M, SONG G, et al. Influence of the ��-phase morphology on the corrosion of the Mg alloy AZ91[J]. Corrosion Science, 2008, 50(7): 1939-1953.
SONG Xiang1, WANG Zhong-wei1, ZENG Rong-chang1, 2
(1. College of Materials Science and Engineering, Shandong University of Science and Technology, Qingdao 266590, China
2. College of Materials Science and Engineering, Zhengzhou University, Zhengzhou 450002, China)
Abstract��Magnesium alloys as potential lightweight structural material in the transportation field have low density, high specific strength and specific stiffness. However, the poor high-temperature oxidation resistance and flammability of magnesium alloys limit their application. This article described the basic principles of high-temperature oxidation and combustion of magnesium alloys in the air, and the influencing factors of high-temperature oxidation in detail. The research progresses of high temperature oxidation and ignition resistance of magnesium alloys were summarized, including the oxidation resistance model theory and the flame retardant mechanism alloying with elements such as Ca, be, Sr, rare earth elements, etc. Some problems encountered in the development of flame retardant magnesium alloys were put forward and the possible development directions were pointed out.
Key words: magnesium alloy; composition; microstructure; high temperature oxidation; ignition resistance
Foundation item: Project(51571134) supported by the National Natural Science Foundation of China
Received date: 2020-08-08; Accepted date: 2020-12-08
Corresponding author: ZENG Rong-chang; Tel: +86-532-80681226; E-mail: rczeng@foxmail.com
(�༭ ��ѧ��)
������Ŀ��������Ȼ��ѧ����������Ŀ(51571134)
�ո����ڣ�2020-08-08�������ڣ�2020-12-08
ͨ�����ߣ����ٲ������ڣ���ʿ���绰��0532-80681226��E-mail��rczeng@foxmail.com

