ҽ��þ��HA����Ϳ����о�����չ��״
��Դ�ڿ����й���ɫ����ѧ��2020���7��
�������ߣ��ž� �Ŵ��� ������ ������
����ҳ�룺1559 - 1574
�ؼ��ʣ�þ�Ͻ��ǻ���ʯ������Ϳ�㣻�������
Key words��magnesium alloy; hydroxyapatite; composite coating; biomaterials
ժ Ҫ��þ��þ�Ͻ����������õ����������ԺͿɽ������ܣ�������ҽ�ò���������о��Ӧ��DZ����Ȼ��������Ľ����������������ٴ�Ӧ�á��ǻ���ʯ(HA)Ϳ��������õĹ��յ��ԺǴ����ԣ�������Ч���ӻ�þ��þ�Ͻ�ĸ�ʴ���ʡ����ǣ���һ���ǻ���ʯͿ�㲻������þ��ֲ�����ʹ������Ҫ�����������һ���ĸ��ԡ����Ĵ����������ԡ��ɽ������Լ���ѧ���ܵȷ�������þ�Ͻ�������ǻ���ʯΪ�������Ը߷��Ӳ��ϡ��������Լ����Ӳ��Ӷ��ɵĿɽ���þ��HA����Ϳ��ķ�չ���о���״��
Abstract: Magnesium and magnesium alloys have great potential as biomedical materials due to their good biocompatibility and biodegradability. However, the rapid degradation rate limits their clinical application. Hydroxyapatite (HA) coating has good osteoinductivity and osteoconductivity, which can delay the corrosion of magnesium alloy to some extent. But a single hydroxyapatite coating cannot meet the requirements for the clinical service life of magnesium implants, so the HA coating needs to be further modification. In this paper, the research and development about biocompatibility, biodegradability and mechanical properties of HA composite coating modified by polymer, ceramic and doped-ions on magnesium and its alloys were reviewed.
DOI: 10.11817/j.ysxb.1004.0609.2020-37414
�� ��1���Ŵ���1, 2��������1��������1, 2
(1. ����������ѧ ���Ͽ�ѧ�빤��ѧԺ������ 400054��
2. ���������ֺ��Ӳ����뼼����У�����о����ģ����� 400054)
ժ Ҫ��þ��þ�Ͻ����������õ����������ԺͿɽ������ܣ�������ҽ�ò���������о��Ӧ��DZ����Ȼ��������Ľ����������������ٴ�Ӧ�á��ǻ���ʯ(HA)Ϳ��������õĹ��յ��ԺǴ����ԣ�������Ч���ӻ�þ��þ�Ͻ�ĸ�ʴ���ʡ����ǣ���һ���ǻ���ʯͿ�㲻������þ��ֲ�����ʹ������Ҫ�����������һ���ĸ��ԡ����Ĵ����������ԡ��ɽ������Լ���ѧ���ܵȷ�������þ�Ͻ�������ǻ���ʯΪ�������Ը߷��Ӳ��ϡ��������Լ����Ӳ��Ӷ��ɵĿɽ���þ��HA����Ϳ��ķ�չ���о���״��
�ؼ��ʣ�þ�Ͻ��ǻ���ʯ������Ϳ�㣻�������
���±�ţ�1004-0609(2020)-07-1559-15���� ��ͼ����ţ�TG174.4���� ���ױ�־�룺A
þ��þ�Ͻ���ܶȺ͵���ģ����������������������ѧ�����ݶ����µ�Ӧ������ЧӦ���Ҿ������õ����������Ժ�����ɽ����ԣ��������ѳ�Ϊ��ע���ȵ�[1]�����ǣ�þ�����ڽ����ٶȹ��죬������ֲ��λ�ֲ�������������ͷ��ٶȹ��죬�γ����ң�Ӱ����֯����[2]����ˣ��ӻ��Ϳ���þ�Ͻ�Ľ����Ϊ���ٴ�Ӧ�õĹؼ���
�����������þ�Ͻ����ͨ����ͬ�����γɱ����㣬ͨ����ֹþ�Ͻ��������ֱ�ӽӴ��������併�����ʣ���һ�����þ�Ͻ���ʴ�Ե���Ч����[3-4]���ǻ���ʯ(HA)���˹ǵ����������[5]�����й��յ��Ǵ�������[6]��ͨ����ͬ������þ�Ͻ�����γ��ǻ���ʯͿ������ǿþ��ֲ����ϵĹǽ���������ӻ�þ�Ͻ�Ľ���[7-13]��Ȼ����HAͿ����Ӧ�����������ѣ�������Һ�������þ�Ͻ�ľֲ���ʴ���Ӷ�ʧȥ������ԡ���ˣ���һ��HAͿ�㲢���ܶ�þ�Ͻ��ṩ�㹻��ʱ�����Ч���������������о����������л��������϶��ǻ���ʯ���и����Ʊ�HA����Ϳ�㣬�Խ�һ������HAͿ�������ѧ���ܺ�������þ�Ͻ�ķ���Ч���������˽϶���о�������
����������þ�Ͻ�������ǻ���ʯΪ�������ø߷��Ӳ��ϡ������ϻ����Ӳ��Ӹ��϶��ɵ�����ɽ���þ��HA����Ϳ��ķ�չ���о���״�������������ԡ��ɽ������Լ���ѧ���ܵȷ��������������
1 HA/�л��︴��Ϳ���о�
����ҽ�ø߷��Ӳ��ϴ��������õ������������Լ�����ɽ����ԣ�����ҩ�Ի���ʵ��ҩ��ľֲ��ɿ��ͷ�[14]��Ŀǰ���Ʊ��߾���Ϳ��ķ�����Ҫ�ǽ�Ϳ������Ϳ�����֡���þ�Ͻ�����Ʊ��߷���Ϳ������һ���̶����ӻ�þ�Ͻ����Ľ���[15-17]�����ǣ���һ�ĸ߷���Ϳ����þ�Ͻ�Ľ�����ܽϲ�װ��䣬�����ܶ�þ�����ṩ��Ч�ı���[18]����������ģ����Ȼ�ǵĽṹ��ɣ���ϸ߷��Ӳ��Ϻ�HA�����������Ʊ����ϲ����ѳ�Ϊ�������������������о��ȵ�[19]��
1.1 HA/PLA����Ϳ��
������(PLA)�����オ�⣬����ѭ�����ã��ѹ㷺������������ߣ�ע�佺�ҵ�ҽ�Ʋ�Ʒ���������������(PLLA)�����Ժ�HA�ĸ��ԣ���PLLA��HA���ϣ�����ǿͿ��ͽ��������ճ������[20]��ABDAL-HAY��[21]ʹ�õ������������ɴ��(AJS)�����������ǻ���ʯ(nHAp)��PLA������ά�Ļ����Ϳ����AM50þ�Ͻ���档�����������Ϳ��������ǿ��AM50�Ŀ����︯ʴ���Լ���Ч������AM50��ʼ�������ʣ�����ϸ���������Ҳ��ʾAJSͿ����и��ߵ�������ԡ�Ȼ����ͨ��HA��PLLA�������ǿ�Ƚϵͣ�Ϊ�˿˷���һȱ�ݣ��о�����ʹ�ÿ�ʴ[22]��������������Ϊ�м���ɲ�[24]����ǿHA/PLLA��ճ��ǿ�ȡ�KIM��[22]ʹ�ù�̷���þ�Ͻ�����γ�ͼ����Ȼ��ͨ��ˮ�ȷ��ڴ�þ�������Ʊ���HAͿ�㣬���PLLA��Ϳ������棬�ȴ�����õ�HA��PLLA������е�������Ϳ��(��ͼ1)�����������ȣ�HA/PLLAͿ����þ������10 d�Ľ���������H2���ͷ�������Ϊ�㡣��ʹ��MC3T3-E1ϸ������5 d��ֻ������������ϸ����������¶��þ�Ͻ���Ʒ���棬������Ϳ�����ϸ���Ի���ϸ���Ǽ��������չ��˵����Ϳ����������������ã�������ϸ������ֳ�ֻ���������5%���쳤�ʵ�����¸�HA/PLLAͿ�����ɱ�����ã�˵����Ϳ����þ�����Ľ�����ܽϺá�LI��[23]���õ�����������ȴ����Ʊ�HA�ڲ㣬��ͨ����Ϳ���Ʊ��м�TiO2�������PLA�㡣ʵ��������HA����TiO2��ͨ���˻��γ�CaTiO3����������TiO2��������ˮ����������֦��OH���ţ���PLA��ͨ��������ӣ�������ǿ�˽������ԡ�������PLA���и���������Լ����ߵIJ�����ת���¶�(Tg)���������ΪͿ����и������Ӧ������ʴҺҲ����������Ϳ�������ֱ�ӽӴ�����H2��ʹͿ������װ����������ơ�JIN��[24]ͨ����AZ91D��������ʹ�õ绯ѧ�������ͽ�Ϳ���Ʊ�FHA/PLA����Ϳ�㣬���ڼ��˻�������֣�����������PLA����������������ͷ���ʯ�ĸ���Ϳ��(MAO/FHA)�����ܼ���ȫ������ʱ��������γɻ�еҧ�ϡ�����FHA���и��ֲڵı��棬��еҧ�ϸ���Ч��ճ��ǿ��Ҳ�õ����ơ����⣬���ڴ���ʹPLA��������ȫ���������У�ʹ������ϸ���֣���һ���棬�˻�������������������ϵ����ͬ������PLAͿ����MAO/FHA֮�����Ӧ����ճ��ǿ�Ƚ�һ����ߡ�
���������о�����ͨ���Ż���ƻ��Ʊ�PLA��Ϊþ���ǻ���ʯ������㣬ǿ����HA��PLA֮��Ľ�����ǿ�ȡ�Ȼ������HA���ɽ��⣬��PLLA�ɽ��⣬PLLA�ڽ�������У�Ϳ��֮�䡢Ϳ��ͻ���֮��Ľ��״����α仯���Լ�PLLA����������������ʶ�þ�Ͻ���к��ڽ������ѧ���ܻ����������Ӱ�죬��������һ���Ľ������ѧ����ʵ�顣
1.2 HA/PCL����Ϳ��
PCL�ɽ��⣬�����ڽ�������CO2�Լ�H2O���������õ����������ԡ�Ŀǰ���㷺������֯���ܺ�ҩ�����塣

ͼ1 HA/PLLA����Ϳ��Ĵ�����FE-SEM��[22]
Fig.1 Representative FE-SEM images of HA/PLLA microtexture coatings[22]

ͼ2 ��ͬ��Ʒ������ò��SEM��[25]
Fig. 2 SEM images of surface morphologies of different samples [25]
ABDAL-HAY��[25]��HA��������PCL��ֻ���Ƴɽ��壬Ȼ�����õ�AM50þ�Ͻ���뽺���Ʊ���PCL/HA���϶��Ĥ�����϶��Ĥ������PCL���������ӱ���ֲڶ�Ҳ��֮����(��ͼ2)�����δͿ��þ�Ͻ��PCL��һͿ�㣬MTTϸ������ʵ��������PCL/HA����Ϳ����и��õ����������ԣ�Ȼ�����в�û�о�Ϳ��ֲڶȺ�ϸ��ճ������ֳ֮���ϵ����һ�����о���BAKHSHESHI-RAD��[26]��ZOMORODIAN��[27]�ֱ���õ�������ͽ�Ϳ����þ�Ͻ�����Ʊ���FHA/PCL��PCL/HA����Ϳ�㣬ǰ�߽����ʾFHA/PCLͿ��ӵ�и��ߵĽ�����ܣ�����Ϳ���ڽ��ݹ�����ӵ�и������ʯ�ɺ�λ����͵ĸ�ʴ�ʡ�����������ʾPCL/HA����Ϳ�������������������ԡ��о���ΪF-���ӽ���HA�ṹʹHA������С��ӵ�и�С�ı����ܣ��Ӷ�������ѧ��FHA�����ȶ���������ϸ����ճ����Ȼ������ͬʱҲ������Ca2+���ͷ����������ڹ�ϸ������ֳ�����HA/PCL��FHA/PCL���������Ը���[27-28]�����⣬ZOMORODIAN��[28]����PCL����ҩ�ԣ�ʹ�ý�Ϳ����AZ31�������ɺ�14~15 ��m����nanoHA���Բ�����ͷ�߰���(������)��PCLͿ�㡣����40 d��PCL+1.4%ͷ�߰���+2%HA(��������)����Ϳ���迹ģֵ��PCLͿ����һ����˥������������������δͿ����AZ31����ġ�Ȼ������ȻPCL�������õ���ҩ���ܣ����Ǹ���ҩ����Ϳ�㲢û�н�����Ӧ�����ڶ���ʵ�飬��˻����һ��ȷ�����ڶ������ڵı��֡�
1.3 HA/�Ǿ��Ǹ���Ϳ��
�Ǿ���(CS)��һ����Ȼ�߷��ӣ�������������������ڿ��Ƶ��̴���Ԥ����Ѫѹ����������й�ؽ������кܺõĹ�Ч��
WU��[29]����ͬ����nHAp/�Ҵ�����Һ�ͿǾ���/������Һ��ϣ�ʹ�õ�Ӿ����(EPD)��AZ91D�����Ʊ���Ca-P/�Ǿ���Ϳ�㣬������ͬ��ȵ�Ϳ���������������λ���Һ(PBS)�н���ת���γ�HA/�Ǿ��Ǹ���Ϳ�㣬������ֲ�ͬ���������nHAp/�Ǿ���-����ˮ��Һ�ܵõ���ͬ��ۺ���ɵ�Ϳ�㣬����PBSת��������ʹͿ������ȣ�������ճ��ǿ�ȸ��ߡ�ZHANG��[30]Ҳʹ����ͬ��ʽ�ó����ƵĽ�����о���Ϊ���Ǿ��ǵIJ�������Ϳ������Ӱ�첻��������ĵ�ѹ��Ϳ��Ľ������Ӱ���Ϊ������HAHN��[31]�Ƚ��ǻ���ʯ�ͿǾ��ǵĸɷ۽��л�ϣ�Ȼ���������ܽ�������(AD)��AZ31�����Ʊ���HA/�Ǿ���Ϳ�㣬Ϳ������Ӧ�ķ�ĩ�������Ƶ������۽ṹ����ͼ3��ʾ�����ſǾ��ǵ�Ũ�����ӣ�Ϳ��Խ��Խ���ܣ���϶Խ�١�HA����Ǿ���֮�������ĸ�ʴ�����ܶ�����������Ϳ���ճ��ǿ�Ƚϸ�(24.6~27.7 MPa)�����⣬��HAͿ����ȣ�HA/�Ǿ��Ǹ���Ϳ������ϸ����չ����ǿ�������Ǿ��ǵIJ����һ��������HAͿ������������ԡ�ͨ����ͬ�ķ�ʽ�Ʊ���HA/�Ǿ���Ϳ�㣬���ȡ���ѧ���ܡ�ճ��ǿ�Ⱦ��в�ͬ�̶ȵIJ��죬����þ�Ͻ����ʴ�Ժ������������������ơ�ͬʱ���Ǿ������������Ľ��������ͬ��ø���ͿǾ��Ǻ�ˮ����HA�ĸ��ϲ����ɸı䵥������Ľ������ʣ����һ�ı�ֲ����ϵ��������ܡ�Ȼ�������Ǿ�����Ϊ����Ϳ�������þ�Ͻ��ϵĽ�������о������࣬�����ٴ�ʹ�û���Ҫ������̽����
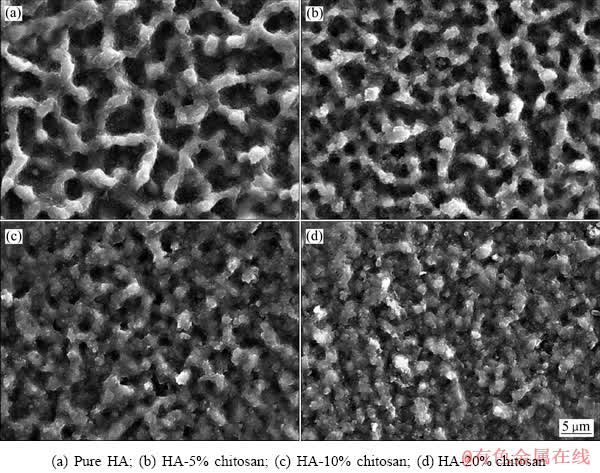
ͼ3 ��ͬ��Ʒ������ò��SEM��[31]
Fig. 3 SEM images of surface morphologies of different samples[31]
1.4 HA/ֲ�Ḵ��Ϳ��
ֲ��(PA)����Ȼ�����ʣ�������ǿ��Ľ���������������������Mg2+��Na+��Ca2+�����ӣ��Ӷ���������������������γɱ���Ĥ[32]��
��һ��ֲ��ת��Ĥ���߱���������������ѣ�����Ϊþ�Ͻ��ṩ��ʱ��ı�������ֲ����HA������ɸ��Ƶ�һֲ��Ϳ���ȱ�ݡ��ŷ����[33]������������(MAT)�� AZ31þ�Ͻ�����Ʊ���ֲ��þ/�ǻ���ʯ(PA/HA)����Ϳ�㡣�����������ֲ����Һ��pH=5.0 ʱ�Ʊ��� PA/HA ����Ϳ��Ͼ��ȣ�������ܽϺá�ZHANG��[34-35]��JIANG��[36]ʹ�û�ѧת��������(CCD)��AZ31�������Ʊ�ֲ��/HA����Ϳ�㡣�绯ѧ���Ժͽ���ʵ�鷢�֣�AZ31�����ֲ��/HA����Ϳ�㲻���ܸ��ƻ������������Ժ���ʴ�ԣ������ܹ��ܺõ��յ�Ca-P�������ڱ���ʴ�Ĺ����в��������ϣ��Ӷ��Ի����ṩ���ౣ��[34-36]�����⣬5 d��ϸ������ʵ���������ø���Ϳ�����ԣ��������õ�ϸ��ճ������ֳ����[37]��Ȼ����ʹ�û�ѧת���������Ʊ���ֲ��/HA����Ϳ�������γ����ƣ��Ӷ����½���SBF��Һ���γɸ�ʴ��ż���ӿ���Mg����ĸ�ʴ��
���������ָ߷��Ӳ����⣬����þ�Ͻ�����Ʊ�HA/�л�����Ϳ��Ļ���Ӳ֬���Լ�PEI�ȡ�ZHANG��[37]ʹ��Ӳ֬��(SA)��þ�Ͻ�����������Ʊ���HAͿ��������Ρ��ø���Ϳ��������þ�Ͻ����ʴ�ԡ�Ȼ������Ӳ֬�����ʹ����Ϳ��ı��������ܽ��ͣ����ֳ���ˮ���ԣ���˲�����ϸ����ճ����CHEON��[38]ʹ�ü���Ϳ̳�þ�Ͻ����ͼ����Ȼ����������Ʊ�PEI/HA����Ϳ�㡣�ñ���ʹ�������HAͿ������ı��������Ӷ�ʹ����������ѧ�����ȶ�����ʴ�����ã������ڱ���ʱҲ�ܱ������õ����������ԡ����⣬JOHNSON��[39]ϵͳ�о���þ�Ͻ����HA/PLLA��HA/PCL�Լ�HA/PLGA����Ϳ���ճ��ǿ�ȡ���ʴ���Լ�ϸ�����ԡ����������HA�����־ۺ��ﶼ����һ���̶������þ�������ʴ�ԡ�Ȼ����������������ָ���Ϳ�㣬HA/PLGA����Ϳ������ĵ�ճ��ǿ�����Բ��㣬�ڽ��ݹ����г����������ͷ���ɵĿ�϶���Ӷ����¸���Ϳ�����װ��������
��������������ͨ����ͬ�ķ�ʽ��þ�Ͻ�����Ʊ�����ʴ�����Լ����������Ծ��õ����Ƶ�HA/�л�����Ϳ�㡣��1�����ͱȽ��˼���þ��þ�Ͻ����HA/�л�����Ϳ�����ʴ���о�����������ԣ���ͬ���Ʊ���ʽ�Լ�ʹ�ò�ͬ�ĵ���ʺͽ���ʱ�䣬��ͬ������ĸ���Ϳ��ӵ�в�ͬ�Ħ�corr��Jcorr��Ȼ�����뵥���Լ�δͿ����þ�Ͻ���ȣ�HA/�л�����Ϳ��ȷʵ��������������ʴ�ԣ���Jcorr�仯��ԼΪ1��5�����������Ҵӱ�1�п�����ȷ�ؿ���Ϳ�����ʴ��������Լ��л���������صġ���ͨ������F-Ҳ���Լ������HA���ȶ��ԣ��Ӷ������ڸ��Ƹ���Ϳ�����ʴ�ԡ�
�߷��Ӳ���Ŀǰ�����������������ٻ�ֲ����ϣ���ΪͿ����ٴ�Ӧ�û����١����߷��Ӳ�����HA����Ϳ����þ��þ�Ͻ���Ϊֲ��������Ϳ�����Ӱ��þ�Ͻ�Ľ�����̡���ѧ���ܺ�����ѧ���ܣ����д���һ���о���
2 HA/�����ϸ���Ϳ��
�л��߷���Ϳ�����ǻ���ʯ�Ľ�����ǿ����Խϵͣ������Ϊ������϶��ǻ�ѧ���ϣ���ʹ����������ֲ��Ӧ��ʱ���ܵ���Ϳ�����ݴӶ��ӻ�����䡣���������Ͽ�����Ч�ظ���Ϳ��Ľ�����ܣ�����Ҳ�ܶԻ�������������Խ��и��ơ�
2.1 HA/MgF2����Ϳ��
MgF2����������ѧ�����Լ����Ʊ����ճ���Ϊþ��þ�Ͻ����ı����㡣��������о��߽�MgF2��Ϊ�м�㣬���������Ϳ����Ϊ��Ϳ��������þ��þ�Ͻ���档
BAKHSHESHI-RAD��[40]��Mg�Ͻ����ʹ��40% HF��Һ�Ʊ�Fת��Ϳ��绯ѧ�����Ʊ�DCPD/MgF2����Ϳ�㣬�ټ��ȴ����õ�HA/MgF2����Ϳ�㡣����ʵ�������HA/MgF2��DCPD/MgF2����Ϳ������������ͷţ����Ҹ�����ʯ���κ�λ�á�Ȼ����������ʾ���͵���ʴ�ԡ��Ŵ���[41]ʹ�����Ʒ����Ʊ�MgF2Ϳ�㣬Ȼ����Ca(OH)2����Ϳ���γ�CaF2�����ͨ���绯ѧ�������Ʊ���MgF2/HA����Ϳ�㣬�о��������⽵�����ܡ������ʾ��Ϳ���ڽ���12 d���Ա���1��104 ����cm2���ϵ��迹ģֵ���������ͬ�Ʊ���ʽ��Ϳ�����ܵ�Ӱ��Ҳ�Dz�һ���ġ�FENG��[42]ʹ�����巴����������(PRC)���Է�ת��Ϳ��Ϊ�ڲ��Mg�Ͻ�����Ʊ��ǻ���ʯͿ�㡣�봫ͳ���������(TED)�Ʊ����ǻ���ʯ���Ϳ����ȣ�PRC-HA/MgF2Ϳ��������ܾ��ȣ��������װ�״�ṹ����TED-HA/MgF2Ϳ������Խ�Ϊ��ɢ(��ͼ4)��PRC-HA/MgF2����Ϳ����и��õ���ʴ�Ժ���H2�ͷ�������������Ϳ������յ�Ca-P�Ŀ��ٳ������������ַ�ʽ�Ʊ���Ϳ����ܸ���þ��þ�Ͻ��������������ԣ�ֻ�Dz�ͬ���Ʊ���ʽ�������ܵĸ��Ƴ̶Ⱦ��в��졣
��MgF2Ϳ�����Ʊ�HAʱ��FͿ���ܽ��ͷŵ�F������Ϊ�κ˼��Ͳ��Ӽ�������HA�Ľᾧ�ͳ���[43-44]���ƾ���ĶԳ��ԣ��õ����׳߶ȵ�HA�������Ӷ���һ��������Ϳ�����ʴ�ԡ�Ȼ��FͿ���ܽ⣬Ҳͬʱ������MgF2��Ϊ�м��ķ���Ч�������⣬�����þ��HA/MgF2����Ϳ������������Ժ�ϸ����������һ���������о�������ֲ���ʵ�顣
��1 þ�Ͻ����HA/�л�����Ϳ��ĵ绯ѧ��ʴ���ܱȽ�
Table 1 Comparison of electrochemical corrosion performance of HA/organic composite coating on magnesium alloy surface
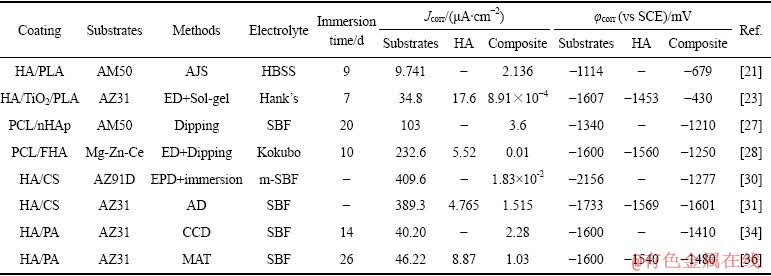

ͼ4 ��ͬ�Ʊ���ʽ�µ�MgF2/HA����Ϳ��SEM��[42]
Fig. 4 SEM images of MgF2/HA composite coating in different preparation modes[42]
2.2 HA/TiO2����Ϳ��
TiO2Ϳ�������������������Լ�����Ľϸߵĸ�����[45]������Ϊ������ǰ;����Ϳ�ϡ��о�����þ�Ͻ����TiO2Ϳ������Ч����������ʴ���ʣ��������������Խϲ����TiO2�������롪OH�������ܽϴ�����յ�HA����������[46-47]����ˣ�TiO2��Ϊҽ��Ϳ���ǿ��еģ����ǵ�һ��TiO2Ϳ�����������Ի����һ�����ơ�AMARAVATHY��[48]ʹ��������ѵ���Һ�Ʊ���TiO2��������HA��ĩ�����AZ31�����Ʊ�HA/TiO2����Ϳ�㣬�ø���Ϳ��ȵ�һ��HAͿ����ֳ����ߵĹ��յ�������������������������HA/TiO2Ϳ�㻹���и��õ�ճ���ԡ�
���˼Ľ�TiO2��HA����֮�⣬�о���ʹ��һЩ���Ӳ���HA���Ʊ�HA/TiO2����Ϳ�㣬��һ�����Ƹ���Ϳ�����ʴ�ԣ�����F����[49]��Zn����[50]��
Mg����[51]��Ag��Sr���ӹ�����[52]�ȵȡ����ӵIJ��ӿ��Ը���HA/TiO2����Ϳ���µ����ܣ����翹�����ܣ�ͬʱҲ����ǿ����Ϳ��ĹǴ������ܡ�BAKHSHESHI-RAD��[50]ʹ��������������TiO2�ķ�����Mg�Ͻ�����Ʊ���TiO2-MAO(TM)Ϳ�㣬�����õ�Ӿ��������MAOͿ�����Ʊ���Zn����HA(ZH)���������Բ��Խ����ʾ��ZHͿ�����������TMͿ������������ࡣʹ��MG63�ɹ�ϸ�����е�ϸ�����Խ����ʾ��ZH��ȡ��������MG63�ɹ�ϸ����ϸ�����Ա��������TMͿ��Ķ�Ҫ�ߡ���Щ�����֤ʵ��TM/ZHͿ����þ�Ͻ���ֳ����ѵĿ������ԡ���������Լ�ϸ�������ԡ�
��Ȼʹ��TiO2��������HA�����Ļ�ѧ�ȶ��ԣ����о��߷��ֵ�HA��ȫ�����ڲ��TiO2ʱ��TiO2/HA����Ϳ�㲢�����кܺõ��������[53]����ˣ�ĿǰһЩ�о���[48]��TiO2��Ϊ���ʣ���HA�������ӽ���TiO2�����У���ʱTiO2/HA�����������ã�Ҳ�����ȶ��ģ����о��Ӧ��DZ����
2.3 HA/̼���ܸ���Ϳ��
����̼����(CNTs)��HA���ϣ�HA�������CNTs�����ܴ�ͣ�����ʹ���ɢ�Եõ����ƣ����������ڱ���HA���������Ե�ͬʱ���ϴ���ȵ����HA����ѧ���ܡ�OSORIO��[54]ͨ����HA�����м���0.5% CNTs(��������)������Ϳ��Ķ������ܵõ����Ը��ơ�MOHAJERNIA��[55]���õ�������Ϳ������AZ31�����Ʊ��˺����̼����(MWCNT)��HAͿ�㡣��ģ����Һ��AZ31þ�Ͻ��Ӧ����ʴ����(SCC)���жȴ�26.8%(HAͿ������Ʒ)���͵�9.8% (HA/MWCNTs����Ϳ��)���о�����MWCNTs������HAp��Ƭ�е��Ž�����(��ͼ5)�ڸ���HApͿ�����ѧ���ܺ͵绯ѧ�Լ�Ӧ����ʴ��������ؼ����á�Ȼ�����ǹ�����̼����(�ر���MWCNTs)����ϸ�����ԣ���˶��̼������Ϊ�������Ӧ�ø�������ʹ�á�����ѧ���ܻ���SWNT���Ѿ��ɹ�����ϸ�������Ļ��ġ��о�������SWNTs/HAͿ���ϵijɹ�ϸ����ϸ��ճ������MWCNTs/HAͿ���Լ��3 ��[56]��������ˣ�PEI��[57]��Ti�Ͻ����ʹ�õ绯ѧ�������Ʊ���HA/SWCNTs����Ϳ�㡣����ϸ������������ʵ��(4 d)����������ø���Ϳ����бȵ�һHAͿ����ߵ����������ԣ��ܸ��õ��յ��ɹ�ϸ������ֳ�����ң�SWCNTs/HAͿ��������ճ��ǿ�ȴﵽ��25.7 MPa����HAͿ��������Լ70%�������о����֤����SWCNTs/HA����Ϳ��������ҽ�������Ƿdz���DZ����Ϳ����ϡ�Ȼ����Ŀǰ����SWCNTs/HAͿ����þ�Ͻ������о���û�й���������������þ�Ͻ�������ʴ���Լ����ڡ���������������ԵȻ���Ҫ��һ�����о�ȷ�ϡ�
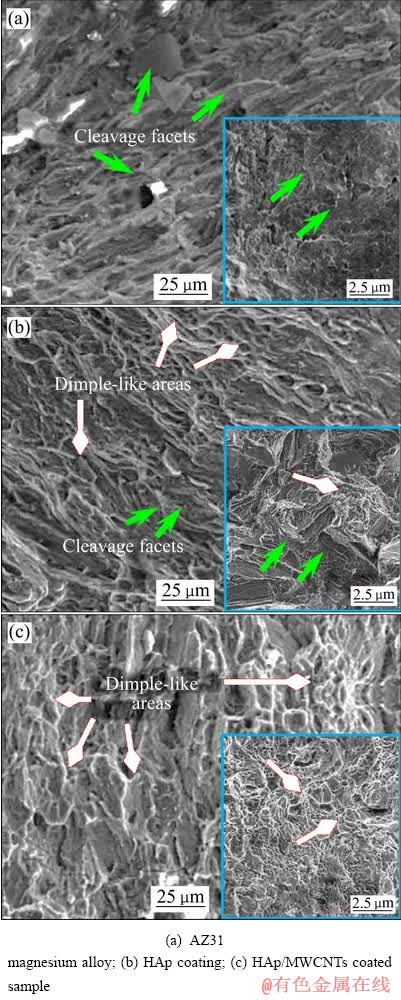
ͼ5 ��ͬ��Ʒ�Ķ��ѱ���[55]
Fig. 5 Fracture surfaces of different samples[55]
�������������������⣬���в������ڸ���HA����ѧ�����Լ�������Ե������ϣ����磬MAO/HA����Ϳ��[58]������˸�(OCP)/HA����Ϳ��[59]�ȵȣ�������һ���̶��ϸ��ƻ������ʴ���Լ�������ԡ������HA/�л�����Ϳ�㣬HA�������ϵĸ��ϸ�������������ĵ���ʴ�ԣ���HA�����������ԡ�ϸ�������Լ��������Ծ��ܸ��ơ������л�����Ϳ�㳣�õ��ǽ�Ϳ������Ϳ���������ַ�������ʹ������Ե����Ӧ�����ߡ���ˣ��ڽ���ʵ����������״�������Ե������������ƣ������ڱ��ֳ��ڻ�е�����ԡ���HA/�����ϸ���Ϳ����Ʊ���ʽ����Խ϶࣬�Ӷ�ͨ��ѡ��ͬ���Ʊ���ʽ�������Ʊ����ղ������ܵõ��Ϻõ�Ԥ����Ʒ�����ǣ�Ŀǰ��HA/�����ϸ���Ϳ�㡢HA/�л�����Ϳ����������ͬ�����⣺Ϳ�������Ľ���Ի�����ƣ���������ֲ��ʵ����еĶ�̫�٣��ٴ�ʹ�û���һ���·Ҫ�ߡ�
3 ���Ӳ���HA����Ϳ��
�˹��ϳɵ��ǻ���ʯ����Ca/PΪ1.67�Ļ�ѧ�����ȣ�Ȼ�������ǻ���ʯ���пɱ�Ļ�ѧ�����Ȳ��ҿ��������ֲ�ͬ������ȡ����������Ȼ��ȱ��HA(CDHA)�����Ӳ��Ӳ����ܸı�HA�ľ������Ⱦ���ѧ���ʡ���ò�����ȶ����Լ���ѧ���ܣ������ܸ���HA���������[60]��
3.1 F���Ӳ���HA����Ϳ��
ǰ������Fת��Ϳ����Ҫ��MgF2ת��Ϳ����Mg�Ͻ���棬Ȼ���Ʊ�HAͿ�㡣��ʵ�ϣ����γ�MgF2/HA����Ϳ������У�����������F�����ͷŲ���ɢ���������У���Ϊ���õijɺ˼���������������F���Ӳ���HA(FHA)�ṹ[42]��������F����HA���и߶ȵ������オ�����ܣ����Ҳ�����ڸ��ֹǿƺ�����ֲ�����ϵı���Ϳ��[61-62]��
LI��[63]ʹ�õ绯ѧ������Mg�Ͻ�����Ʊ��˷������ǻ���ʯ(FHA)Ϳ�㣬��FHAͿ��������Mg�Ͻ�����������ԣ�������ϸ����ֳ�ͷֻ��Լ������オ����Ϊ�Ŀ��ơ�MENG��[64]����������������(PRC)��Mg�Ͻ�����Ʊ���FHAͿ�㡣�봫ͳ���������������(TED)��ȣ� PRC�����Ʊ�������FHAͿ��ṹ���������ܣ�����Խϸߵıȱ�����ܹ����õ��յ�Mg2+��Ca2+�� �����ӵij�����RAZAVI��[65]ͨ������ʹ���������Լ���Ӿ����������þ�Ͻ�����Ʊ�FHAͿ�㡣��FHAͿ��þ�Ͻ�ֲ�����ӵĴ�ת���������������������ԣ������������δͿ����ֲ������ȣ�FHA/MAOͿ����ֲ���������������������ǿ��Ϳ���������ʧ��Ѫ���е�Mg2+�ͷ��������٣�ֲ�����ܱߵ��¹������������첢����֢���١������о��Ա���FHAͿ������ǿþ�Ͻ�ֲ��������������ԡ�������ˣ��봿HAͿ����ȣ�FHAͿ�������ϸ���������ṩ���������ܽ��ԣ����õ���ʯ״���������õĵ��������������õ�ϸ�����ź��Ƽ�������ø����[63]���ɴ˿ɼ���FHAͿ��þ�Ͻ���һ�ֺ���ǰ���Ŀ����オ��Ĺ�ֲ�����Ͷ��ʵ���ٴ�ʹ�û���Ҫ��һ���о������ڽ�����Ϊ��
�����ӵij�����RAZAVI��[65]ͨ������ʹ���������Լ���Ӿ����������þ�Ͻ�����Ʊ�FHAͿ�㡣��FHAͿ��þ�Ͻ�ֲ�����ӵĴ�ת���������������������ԣ������������δͿ����ֲ������ȣ�FHA/MAOͿ����ֲ���������������������ǿ��Ϳ���������ʧ��Ѫ���е�Mg2+�ͷ��������٣�ֲ�����ܱߵ��¹������������첢����֢���١������о��Ա���FHAͿ������ǿþ�Ͻ�ֲ��������������ԡ�������ˣ��봿HAͿ����ȣ�FHAͿ�������ϸ���������ṩ���������ܽ��ԣ����õ���ʯ״���������õĵ��������������õ�ϸ�����ź��Ƽ�������ø����[63]���ɴ˿ɼ���FHAͿ��þ�Ͻ���һ�ֺ���ǰ���Ŀ����オ��Ĺ�ֲ�����Ͷ��ʵ���ٴ�ʹ�û���Ҫ��һ���о������ڽ�����Ϊ��
3.2 Ag���Ӳ���HA����Ϳ��
HAͿ������������������ʡ���������л����ʣ��Ӷ�����ϸ����HA���������븴�ƣ�����ܱ���֯��Ⱦ����[66]��Ag��Ϊ�������ؼ����������ںܵ�Ũ���µĿ������ܺ����õ�����������[67]��Ag���Ӳ���HA�ṹ�У�ͨ���仺���ͷſ��ṩ�������á�
����HA����Ϳ����Ҫ������������ʽ��һ������Ag+ͨ�����ӽ������ӽ���HA�ṹ������ʹ���ܽ���������HA�ṹ�е�Ca2+��Ag+ȡ�����γ�ȱ����ʯ�����ǣ��Ƶ����Ŀ��ܶ�HA�Ľṹ�ȶ��Լ���Ǵ���������ɸ���Ӱ��[68]����һ��������Ag������������������HA���棬Ȼ�������á�HU��[69]ʹ�û�ѧת������Mg�Ͻ�����Ʊ�����Ag����������ʽ���ڵ�Ag/HA����Ϳ�㡣�����־�Ȧ������Ag/HA����Ϳ��Ŀ������ԣ���316L����ֺͲ���Ag��HAͿ����ȣ����ֺ�����û�п������ԣ���Mg�Ͻ�����ϵ�Ag/HA����Ϳ����ֳ����ȵĿ������ԣ�Mg�Ͻ���Ʒ��Χ�������������������������õ��������ù�����Ag������Ag/HA����Ϳ���ͷŵ���Χ�����С����⣬Ag/HA����Ϳ�㲻������HAͿ�����õĿ������ܣ����������Ϳ�������Ľ�����ǿ�ȡ�Ȼ����Ag���Ӻ�������̫�ߣ���Ag�����ͷ����ﵽijһŨ�Ƚ���ʱ�����������ϸ�����ԣ���������֯���ϡ�
Ŀǰ������Ti�Ͻ����ʹ�ò�ͬ�����Ʊ��������������������Լ��������Ե�[70-72]��������þ�Ͻ�����Ʊ�Ag/HA����Ϳ����о����١���ˣ�Ag����HA����Ϳ���þ�Ͻ����ܵ�Ӱ�컹���һ���о���
3.3 Sr����HA����Ϳ��
Sr�����������е�����������Ca������ǿ�ҵ�Ѱ������[73]��Sr���ӿ�ͨ�������ƹ�ϸ�����������ٹ����գ���ͨ���̼��ɹ�ϸ�����������ƹ��γ�[74]��Sr�����ܸ���HAͿ�������ѧ���ܺ�ʹ������[75]��YU��[76]��AZ31��������������������Ʊ�Sr����HA����Ϳ�㣬Ϳ���(Ca+Sr)/P�ı�Ϊ1.61��SBF��Һ�н���ʵ��͵绯ѧ�����о�������Sr����HAͿ��������õĿ�����������ǿ��AZ31�������ʴ�ԡ����ǣ��ÿ����鲢δ��Sr����HA����Ϳ�����ʴ�Ժʹ�HAͿ�����ʴ����Ƚϣ���˵�����Ժ��Ϳ����ʴ���Լ�������Եı仯��SINGH��[77]���ȶ�AZ31���в�ͬ��ʽ��Ԥ������Ȼ����AZ31�Ʊ���Sr����Ca-PͿ�㣬����Ca-PͿ��ɷ���Ҫ�Ǧ�-TCP�Լ�HA��ɡ���MC3T3-E1��hMSCϸ������ϸ�����ԣ������������Sr����Ũ�Ⱥ���ϸ����ֳ���½���Ȼ������Sr����Ũ�ȵ����ӣ��ɹǻ���͵����ʱ�����������ӡ����������δ���ӵ�CaPͿ����ȣ�Sr2+���ӵ�Ϳ���ܹ��ٽ���ϸ����������
Ŀǰ��Sr����HA����Ϳ���Լ�ʹ������������Sr���ӹ�ͬ����HAͿ�㣬����Zn[78]��Ag[79]�Լ���������[80]�����ӵ�HA����Ϳ�㣬���������о��ߵĹ�ע��
3.4 Si����HA����Ϳ��
���ǹ��������������Ԫ�أ��ڹǿ�����֯���������ڽ��DZز����ٵ�[81]������������ǻ���ʯ�Ľṹ�п�����������HA�������Ӧ�����͵�ȱ�ݣ���ǿ��ʯ����Ϳ�������������[82]��Ŀǰ�������HA����Ϳ����Ҫ������������ʽ��һ�����ǻ���ʯ�еIJ�����������ű� ȡ������һ�����Dz�����������ű�
ȡ������һ�����Dz�����������ű�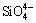 ȡ����DEHGHANIAN��[83]ʹ��Na2SiO3��Ϊ
ȡ����DEHGHANIAN��[83]ʹ��Na2SiO3��Ϊ Դ����Mg�Ͻ������õ绯ѧ�������Ʊ���Si����HA����Ϳ�㡣���������
Դ����Mg�Ͻ������õ绯ѧ�������Ʊ���Si����HA����Ϳ�㡣��������� �Ĵ���ʹͿ��ĺ�ȼ�С���������ܶ����ӣ��봿HAͿ����ȣ�Si����HA����Ϳ����и��õ���ʴ�ԡ�ϸ��ʵ����Խ��(��ͼ6)������Si-HAͿ�����ȡ����HA����ȡ����ȣ����ʺ���ϸ������ֳ��QIU��[84]��AZ31������õ�������ɹ��Ʊ���Si-HA����Ϳ�㣬��Ϳ��Ϊ˫��ṹ�������ǿ�״�㣬�ڲ���Ҫ��Ƭ״�ṹ���绯ѧ���Խ��������Si����Ca-PͿ�����ʴ�Ե����ӱ�AZ31�����Լ60������һ����ϸ�����Ժ�ALP���Բ�����ʾ��Si����Ca-PͿ��ϸ������Ϊ�����ҹ�����5 d��ϸ�����������������Զ����飬������������õ����������ԡ���ʵ��Ŀǰֻ��һ�������о��������ٴ�Ӧ�������ṩ������Ϣ�����ã���Si����HA����Ϳ����þ�Ͻ�����Ʊ����о�ĿǰҲ��Խ��١����ң�SiO2�����ڹ����ᵼ�·β�����ˣ�����Ҫ�о��ߵIJ���̽���о���
�Ĵ���ʹͿ��ĺ�ȼ�С���������ܶ����ӣ��봿HAͿ����ȣ�Si����HA����Ϳ����и��õ���ʴ�ԡ�ϸ��ʵ����Խ��(��ͼ6)������Si-HAͿ�����ȡ����HA����ȡ����ȣ����ʺ���ϸ������ֳ��QIU��[84]��AZ31������õ�������ɹ��Ʊ���Si-HA����Ϳ�㣬��Ϳ��Ϊ˫��ṹ�������ǿ�״�㣬�ڲ���Ҫ��Ƭ״�ṹ���绯ѧ���Խ��������Si����Ca-PͿ�����ʴ�Ե����ӱ�AZ31�����Լ60������һ����ϸ�����Ժ�ALP���Բ�����ʾ��Si����Ca-PͿ��ϸ������Ϊ�����ҹ�����5 d��ϸ�����������������Զ����飬������������õ����������ԡ���ʵ��Ŀǰֻ��һ�������о��������ٴ�Ӧ�������ṩ������Ϣ�����ã���Si����HA����Ϳ����þ�Ͻ�����Ʊ����о�ĿǰҲ��Խ��١����ң�SiO2�����ڹ����ᵼ�·β�����ˣ�����Ҫ�о��ߵIJ���̽���о���
���Ӳ�������һ���̶��ϸ���HA�����������ԣ����ܸ���HA���µĹ��ܡ���2�г�һЩ�������HA���������ӵ�ʵ������Sr2+��F-��Mg2+��Zn2+�� �����Ӳ���HA����ˣ��������ӻ������Ӳ���HA����ṹ�зdz�Ƶ�����������в���ʹ�ö������Ӳ���HA���о�������BAKHSHESHI-RAD��[86]��þ�Ͻ�����Ʊ�nano-SiO2�ڲ�����Ʊ�Ag-FHA��㣬�����ʾͿ����ֳ����õ����������ԡ�HA�������ӵ���Ͽɸ��ݻ�е���ʡ��ܽ���Ϊ����ϸ��������������������������Ҳ���ӽ�����ʵ�Ĺ���֯[68]��Ȼ�������һ���о���ͬ���Ӳ��ӵ�ȡ��ˮƽ����Щ���ӵĿ����������һ����ȷ�������������ʵ��䷴��
�����Ӳ���HA����ˣ��������ӻ������Ӳ���HA����ṹ�зdz�Ƶ�����������в���ʹ�ö������Ӳ���HA���о�������BAKHSHESHI-RAD��[86]��þ�Ͻ�����Ʊ�nano-SiO2�ڲ�����Ʊ�Ag-FHA��㣬�����ʾͿ����ֳ����õ����������ԡ�HA�������ӵ���Ͽɸ��ݻ�е���ʡ��ܽ���Ϊ����ϸ��������������������������Ҳ���ӽ�����ʵ�Ĺ���֯[68]��Ȼ�������һ���о���ͬ���Ӳ��ӵ�ȡ��ˮƽ����Щ���ӵĿ����������һ����ȷ�������������ʵ��䷴��
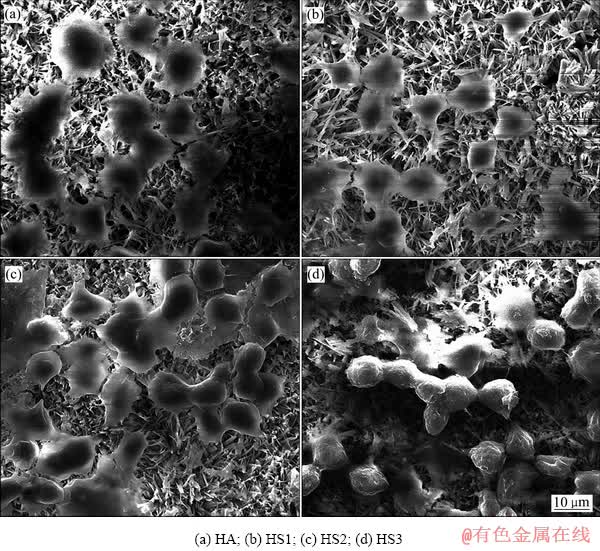
ͼ6 ϸ������7 h��ͬŨ�� ���ӵ�HA����Ϳ�������MG63�ɹ�ϸ������ò[83]
���ӵ�HA����Ϳ�������MG63�ɹ�ϸ������ò[83]
Fig. 6 Morphologies of MG63 osteoblasts on surface of different concentrations of  doped HA composite coating after 7 h of cell culture[83]
doped HA composite coating after 7 h of cell culture[83]
��2 þ�Ͻ����������Ӳ���HAͿ��ʵ��
Table 2 Example of ion-doped HA coating on surface of magnesium alloy

4 ����
þ�Ͻ�����ǻ���ʯ����Ϳ�㣬��HA/�߷��ӡ�HA/������Ϳ���Լ����Ӳ���HA����Ϳ��ȣ���Ȼ����һ���̶��ϸ���þ�Ͻ������ѧ���ܺͽ������ܣ�������Щ����Ϳ��Ҳ����һЩȱ�㣬����HA/�л�����Ϳ���оۺ���Ľ����ٶȺ�����֯���γ��ٶ��Ƿ�ƥ�䣬�л�Ϳ����HA�Ľ�����ǿ���Լ����Ӳ���HAͿ����һЩ���ӵĿ����������⡣������ˣ�Ŀǰ��δ��Ϳ��������ٴ�Ӧ�ã���Ҫ������ͨ��������ԵĽ���ֲ����϶�������ʵ����е�̫�٣����ʵ���о������ࡣ��Ȼ����ʵ����н϶࣬��������ʵ��ֻ�Ƕ����ڵ�һ��ģ�⣬���ڵ�������������Ը��ӵöࡣ��ˣ�δ�����о�Ӧ�ò����ڿ������ж�ܵ�Ϳ�㣬�������ڵ������²��ԡ�ͨ��������Ӳ���HA���л��������ϸ��ϳ�Ϳ�㣬���������Կɿص��ٶȽ��⣬ʹ������֯�����ٶ���ƥ�䣬ͬʱ��һ�����þ��HA����Ϳ������������Ժ���ʴ�ԡ�
REFERENCES
[1] STAIGER M P, PITEAK A M, HUADMAI J, DIAS G. Magnesium and its alloys as orthopedic biomaterials: A review[J]. Biomaterials, 2006, 27(9): 1728-1734.
[2] HORNBERGER H, VIRTANEN S, BOCCACCINI A R. Biomedical coatings on magnesium alloys��A review[J]. Acta Biomaterialia, 2012, 8(7): 2442-2455.
[3] MARTINEZ SANCHEZ A H, LUTHRINGER B J, FEYERABEND F, WILLUMEIT R. Mg and Mg alloys: How comparable are in vitro and in vivo corrosion rates; A review[J]. Acta Biomaterialia, 2015, 13: 16-31.
[4] LI X, LIU X, WU S L, YEUNG K.W.K, ZHENG Y F, CHU P K. Design of magnesium alloys with controllable degradation for biomedical implants: From bulk to surface[J]. Acta Biomaterialia, 2016, 45: 2-30.
[5] WANG F, CAI S, SHEN S B, YU N, ZHANG F Y, LING R, LI Y, XU G H. Preparation of phytic acid/silane hybrid coating on magnesium alloy and its corrosion resistance in simulated body fluid[J]. Journal of Materials Engineering & Performance, 2017, 26(9): 4282-4290.
[6] CHEN X, LI G, LIAN J, JIANG Q. Study of the formation and growth of tannic acid based conversion coating on AZ91D magnesium alloy[J]. Surface & Coatings Technology, 2009, 204(5): 736-747.
[7] SZCZES A, HOLYSZ L, CHIBOWSKI E. Synthesis of hydroxyapatite for biomedical applications[J]. Advances in Colloid & Interface Science, 2017, 249: 321-330.
[8] ROJAEE R, FATHI M, RAEISSI K. Controlling the degradation rate of AZ91 magnesium alloy via sol-gel derived nanostructured hydroxyapatite coating[J]. Mater Sci Eng C Mater Biol Appl, 2013, 33(7): 3817-3825.
[9] PRAKASH C, SINGH S, PABLA B S, UDDIN M S. Synthesis, characterization, corrosion and bioactivity investigation of nano-HA coating deposited on biodegradable Mg-Zn-Mn alloy[J]. Surface & Coatings Technology, 2018, 346: 9-18.
[10] DUNNE C F, LEVY G K, HAKIMI O, AGHION E, TWOMEY B, STANTON K T. Corrosion behaviour of biodegradable magnesium alloys with hydroxyapatite coatings[J]. Surface & Coatings Technology, 2016, 289: 37-44.
[11] MUKHAMETKALIYEV T M, SURMENEVA M A, VLADESCU A, COTRUT C M, BRAIC M, DINU M, VRANCEANU M D, PANA I, MUELLER M, SURMENEV R A. A biodegradable AZ91 magnesium alloy coated with a thin nanostructured hydroxyapatite for improving the corrosion resistance[J]. Materials Science & Engineering C, 2017, 75: 95-103.
[12] MAGESH S, SUWAS S, SUBRAMANIAN B, GEETHA M. Comparison of electrochemical behavior of hydroxyapatite coated onto WE43 Mg alloy by electrophoretic and pulsed laser deposition[J]. Surface & Coatings Technology, 2016, 309: 840-848.
[13] SEYEDRAOUFI Z S, MIRDAMADI S H. Biodegradability and biocompatibility of porous Mg-Zn scaffolds coated with nano-hydroxyapatite by pulse electrodeposition[J]. Chinese Journal of Nonferrous Metals Edition, 2015, 25(12): 4018-4027.
[14] ZHEN Z, XI T F, ZHENG Y F. Surface modification by natural biopolymer coatings on magnesium alloys for biomedical applications[C]// Surface modification of Magnesium and its Alloys for Biomedical Applications. Cambridge: Elsevier, 2015: 301-333.
[15] WONG H M, YEUNG K W K, LAM K O, TAM V, CHU P K, D.K.LUK K, CHEUNG K M C. A biodegradable polymer-based coating to control the performance of magnesium alloy orthopaedic implants[J]. Biomaterials, 2010, 31(8): 2084-2096.
[16] CHEN L, ZHAO J, YU K, CHEN C, DAI Y L, QIAO X Y, YU Z M. Improving of in vitro, biodegradation resistance in a chitosan coated magnesium bio-composite[J]. Rare Metal Materials & Engineering, 2015, 44(8): 1862-1865.
[17] YE C H, ZHENG Y F, WANG S Q, XI T F, LI Y D. In vitro corrosion and biocompatibility study of phytic acid modified WE43 magnesium alloy[J]. Applied Surface Science, 2012, 258(8): 3420-3427.
[18] XU L, YAMAMOTO A. Characteristics and cytocompatibility of biodegradable polymer film on magnesium by spin coating[J]. Colloids & Surfaces B Biointerfaces, 2012, 93(93): 67-74.
[19] KRAMER E, KUNKEMOELLER B, WEI M. Evaluation of alkaline pre-treatment of PLLA fibers for biomimetic hydroxyapatite coating[J]. Surface & Coatings Technology, 2014, 244(5): 23-28.
[20] Ԭ�ﻪ, ����, �ز�ƺ, ��־��, ����ԣ, ������, ������, ������. �ǻ���ʯ-�����Ḵ��Ĥ���Ʊ������[J]. ���ڴ�ѧѧ��(������), 2016, 33(1): 10-17.
YUAN Qiu-hua, WU Jian-bo, QIN Cao-ping, GUO Zhi-wei, LIU Jia-yu, LIN Song-xin, KE Shan-ming, ZHANG Pei-xin. Preparation and characterization of hydroxyapatite-polylactic acid composite membrane[J]. Journal of Shenzhen University (Science and Engineering), 2016, 33(1): 10-17.
[21] ABDAL-HAY A, HASAN A, YU-KYOUNG, LEE M H, HAMDY A S, KHALIL A. Biocorrosion behavior of biodegradable nanocomposite fibers coated layer-by-layer on AM50 magnesium implant[J]. Materials Science & Engineering C, 2016, 58: 1232-1241.
[22] KIM S M, KANG M H, KIM H E, LIM H K, BYUN S H, LEE J H, LEE S M. Innovative micro-textured hydroxyapatite and poly(l-lactic)-acid polymer composite film as a flexible, corrosion resistant, biocompatible, and bioactive coating for Mg implants[J]. Materials Science & Engineering C, 2017, 81: 97-103.
[23] LI B, ZHANG K, YANG W Z, YIN X S, LIU Y. Enhanced corrosion resistance of HA/CaTiO3/TiO2/PLA coated AZ31 alloy[J]. Journal of the Taiwan Institute of Chemical Engineers, 2016, 59(3): 465-473.
[24] JIN J, ZHOU S, DUAN H. Preparation and properties of heat treated FHA@PLA composition coating on micro-oxidized AZ91D magnesium alloy[J]. Surface & Coatings Technology, 2018, 349(15): 50-60.
[25] ABDAL-HAY A, AMNA T, LIM J K. Biocorrosion and osteoconductivity of PCL/nHAp composite porous film-based coating of magnesium alloy[J]. Solid State Sciences, 2013, 18(2): 131-140.
[26] BAKHSHESHI-RAD H R, HAMZAH E, KASIRI- ASGARANI M, JABBARZARE S, LQBAL N, ABDUL KADIR M R. Deposition of nanostructured fluorine-doped hydroxyapatite-polycaprolactone duplex coating to enhance the mechanical properties and corrosion resistance of Mg alloy for biomedical applications[J]. Materials Science & Engineering C, 2016, 60: 526-537.
[27] ZOMORODIAN A, GARCIA M P, MOURA E S T, FERNADES M H, MONTEMOR M F. Biofunctional composite coating architectures based on polycaprolactone and nanohydroxyapatite for controlled corrosion activity and enhanced biocompatibility of magnesium AZ31 alloy.[J]. Materials Science & Engineering C, 2015, 48: 434-443.
[28] ZOMORODIAN A, SANTOS C, CARMEZIM M J, MOURA E S T, FERNADES M H, MONTEMOR M. ��In-vitro�� corrosion behaviour of the magnesium alloy with Al and Zn (AZ31) protected with a biodegradable polycaprolactone coating loaded with hydroxyapatite and cephalexin[J]. Electrochimica Acta, 2015, 179: 431-440.
[29] WU C, WEN Z, DAI C, LU Y X, YANG F X. Fabrication of calcium phosphate/chitosan coatings on AZ91D magnesium alloy with a novel method[J]. Surface & Coatings Technology, 2010, 204(20): 3336-3347.
[30] ZHANG J, DAI C S, WEI J, WEN Z H. Study on the bonding strength between calcium phosphate/chitosan composite coatings and a Mg alloy substrate[J]. Applied Surface Science, 2012, 261(8): 276-286.
[31] HAHN, BYUNG-DONG, PARK D S, CHOI J J, RYU J. Aerosol deposition of hydroxyapatite-chitosan composite coatings on biodegradable magnesium alloy[J]. Surface & Coatings Technology, 2011, 205(8): 3112-3118.
[32] PAK S N, JIANG Z, YAO Z, JU J M, JU K S, PAK U J. Fabrication of environmentally friendly anti-corrosive composite coatings on AZ31B Mg alloy by plasma electrolytic oxidation and phytic acid/3-aminopropyltrimethoxysilane post treatment[J]. Surface and Coatings Technology, 2017, 325: 579-587.
[33] �ŷ���, �� ��, �� ��, ������, �� ��. ���������Ʊ�þ�Ͻ��ֲ��þ/�ǻ���ʯ����Ϳ�㼰����ʴ�� ��[J]. ���ϲ���ѧ��, 2017, 34(12): 2819-2825.
ZHANG Fei-yang, CAI Shu, LING Rui, WANG Feng-wu, YU Nian. Microwave-assisted preparation of magnesium phytate/hydroxyapatite composite coating for magnesium alloy and its corrosion resistance[J]. Journal of Composite Materials, 2017, 34(12): 2819-2825.
[34] ZHANG M, CAI S, ZHANG F Y, XU G H, WANG F W, YU N, WU X D. Preparation and corrosion resistance of magnesium phytic acid/hydroxyapatite composite coatings on biodegradable AZ31 magnesium alloy[J]. Journal of Materials Science: Materials in Medicine, 2017, 28(6): 82-91.
[35] ZHANG M, CAI S, SHEN S B, XU G H, LI Y, LING R, WU X B. In-situ defect repairing in hydroxyapatite/phytic acid hybrid coatings on AZ31 magnesium alloy by hydrothermal treatment[J]. Journal of Alloys & Compounds, 2016, 658: 649-656.
[36] JIANG S, CAI S, ZHANG F Y, XU P, LING R, LI Y, JIANG Y Y, XU G H. Synthesis and characterization of magnesium phytic acid/apatite composite coating on AZ31 Mg alloy by microwave assisted treatment[J]. Materials Science & Engineering C, 2018, 91: 218-227.
[37] ZHANG X, LI Q, LI L Q, ZHANG P, WANG Z W, CHEN F N. Fabrication of hydroxyapatite/stearic acid composite coating and corrosion behavior of coated magnesium alloy[J]. Materials Letters, 2012, 88(12): 76-78.
[38] CHEON K H, GAO C, KANG M H, JUNG H D, JANG T S, KIM H E, LI Y, SONG J H. A crack-free anti-corrosive coating strategy for magnesium implants under deformation[J]. Corrosion Science, 2017, 132: 116-124.
[39] JOHNSON I, WANG S M, SILKEN C, LIU H N. A systemic study on key parameters affecting nanocomposite coatings on magnesium substrates[J]. Acta Biomaterialia, 2016, 36: 332-349.
[40] BAKHSHESHI-RAD H R, IDRIS M H, ABDUL-KADIR M R. Synthesis and in vitro degradation evaluation of the nano-HA/MgF2, and DCPD/MgF2, composite coating on biodegradable Mg-Ca-Zn alloy[J]. Surface & Coatings Technology, 2013, 222(19): 79-89.
[41] �Ŵ���, ������, �����, �� ѧ. þ�Ͻ����MgF2/HA����Ϳ������⽵������[J]. �й���ɫ����ѧ��, 2018, 28(4): 766-773.
ZHANG Chun-yan, ZHANG Shi-yu, LIU Xin-peng, LIU Xue. In vitro degradation of MgF2/HA composite coating on magnesium alloy surface[J]. The Chinese Journal of Nonferrous Metals, 2018, 28(4):766-773.
[42] FENG Y S, ZHU S J, WANG L G, CHANG L, YAN B B, SONG X Z, GUAN S K. Characterization and corrosion property of nano-rod-like HA on fluoride coating supported on Mg-Zn-Ca alloy[J]. Bioactive Materials, 2017, 2(2): 63-70.
[43] WANG J, CHAO Y, WAN Q B, ZHU Z M, YU H Y. Fluoridated hydroxyapatite coatings on titanium obtained by electrochemical deposition[J]. Acta Biomaterialia, 2009, 5(5): 1798-1807.
[44] MENG E C, GUAN S K, WANG H X, WANG L G, ZHU S J, HU J H, REN C X, GAO J H, FENG Y S. Effect of electrodeposition modes on surface characteristics and corrosion properties of fluorine-doped hydroxyapatite coatings on Mg-Zn-Ca alloy[J]. Applied Surface Science, 2011, 257(11): 4811-4816.
[45] HU J, ZHANG C, CUI B, BAI K F, GUAN S K, WANG L G, ZHU S J. In vitro degradation of AZ31 magnesium alloy coated with nano TiO2, film by sol-gel method[J]. Applied Surface Science, 2011, 257(21): 8772-8777.
[46] CHEN S, GUAN S, CHEN B, LI W, WANG J, WANG L G, ZHU S J, HU J H. Corrosion behavior of TiO2 films on Mg�CZn alloy in simulated body fluid[J]. Applied Surface Science, 2011, 257(9): 4464-4467.
[47] TENG H P, YANG C J, LIN J F, HUANG Y H, LU F H. A simple method to functionalize the surface of plasma electrolytic oxidation produced TiO2, coatings for growing hydroxyapatite[J]. Electrochimica Acta, 2016, 193: 216-224.
[48] AMARAVATHY P, SATHYANARAYANAN S, SOWNDARYA S, RAJENDRAN N. Bioactive HA/TiO2, coating on magnesium alloy for biomedical applications[J]. Ceramics International, 2014, 40(5): 6617-6630.
[49] �ƴ���, �ܶ���, �� ��, �� ��. ����������ǻ���ʯ/���������Ѹ���Ϳ��ı����������о�[J]. �����Ϳ��, 2011, 30(12): 73-75.
HUANG Chun-peng, GUAN Dong-hau, ZHANG Li, WANG Jian. Characterization and properties of electrodeposited fluorinated hydroxyapatite/nano-TiO2 composite coatings[J]. Electroplating & Finishing, 2011, 30(12): 73-75.
[50] BAKHSHESHI-RAD H R, HAMZAH E, ISMAIL A F, AZIZ M, DAROONPARVAR M, SAEBNOORI E. In vitro degradation behavior, antibacterial activity and cytotoxicity of TiO2-MAO/ZnHA composite coating on Mg alloy for orthopedic implants[J]. Surface & Coatings Technology, 2018, 334: 450-460.
[51] YAN Y, DING Q, HUANG Y, HAN S G, PANG X F. Magnesium substituted hydroxyapatite coating on titanium with nanotublar TiO2, intermediate layer via electrochemical deposition[J]. Applied Surface Science, 2014, 305(16): 77-85.
[52] HUANG Y, ZHANG X, ZHANG H, QIAO H X, ZHANG X Y, JIA T J,HAN S G, GAO Y, XIAO H Y, YANG H J. Fabrication of silver- and strontium-doped hydroxyapatite/ TiO2 nanotube bilayer coatings for enhancing bactericidal effect and osteoinductivity[J]. Ceramics International, 2017, 43(1): 992-1007.
[53] KURODA K, SHIDU H, ICHINO R, OKIDO M. Osteoinductivity of titania/hydroxyapatite composite films formed using pulse electrolysis[J]. Materials Transactions, 2007, 48(3): 328-331.
[54] OSORIO A G, SANTOS L A D, BERGMANN C P. Evaluation of the mechanical properties and microstructure of hydroxyapatite reinforced with carbon nanotubes[J]. Reviews on Advanced Materialsence, 2011, 27(1): 58-63.
[55] MOHAJERNIA S, POUR-ALI S, HEJAZI S, SAREMI M, KIANI-RASHID A-R. Hydroxyapatite coating containing multi-walled carbon nanotubes on AZ31 magnesium: Mechanical-electrochemical degradation in a physiological environment[J]. Ceramics International, 2018, 44(7): 8297-8305.
[56] ZANELLO L P, ZHAO B, HU H, HADDON R C. Bone cell proliferation on carbon nanotubes[J]. Nano Letters, 2006, 6(3): 562-567.
[57] PEI X, ZENG Y, HE R, LI Z J, TIAN L Y, WANG J, WAN Q B, LI X Y, BAO H. Single-walled carbon nanotubes/ hydroxyapatite coatings on titanium obtained by electrochemical deposition[J]. Applied Surface Science, 2014, 295(3): 71-80.
[58] TANG H, WU T, WANG H, JIAN X, WU Y F. Corrosion behavior of HA containing ceramic coated magnesium alloy in Hank's solution[J]. Journal of Alloys & Compounds, 2016, 698: 643-653.
[59] HIROMOTO S. Self-healing property of hydroxyapatite and octacalcium phosphate coatings on pure magnesium and magnesium alloy[J]. Corrosion Science, 2015, 100: 284-294.
[60] LAURENCIN D, ALMORA-BARRIOS N, de LEEUW N H, GERVAIS C, BOHNOMME C, MAURI F, CHRZANOWSKI W, KNOWS J C, NEWPORT R J, WONG A, GAN Z H, SMITH M E. Magnesium incorporation into hydroxyapatite[J]. Biomaterials, 2011, 32(7): 1826-1837.
[61] CHENG K, ZHANG S, WENG W J, ZENG X T. The interfacial study of sol-gel-derived fluoridated hydroxyapatite coatings[J]. Surface & Coatings Technology, 2005, 198(1): 242-246.
[62] BAKHSHESHI-RAD H R, HAMZAH E, DAROONPARVAR M, YAJID M A M, KASIRI-ASGARANI M, ABDUL-KADIR M R, MEDRAJ M. In-vitro degradation behavior of Mg alloy coated by fluorine doped hydroxyapatite and calcium deficient hydroxyapatite[J]. Transactions of Nonferrous Metals Society of China, 2014, 24(8): 2516-2528.
[63] LI J N, SONG Y, ZHANG S X, ZHAO C L, ZHANG F, ZHANG X N, CAO L, FAN Q MTANG T T. In vitro responses of human bone marrow stromal cells to a fluoridated hydroxyapatite coated biodegradable Mg-Zn alloy[J]. Biomaterials, 2010, 31(22): 5782-5788.
[64] MENG E C, GUAN S K, WANG H X, WANG L G, ZHU S J, HU J H, REN C X, GAO J H, FENG Y S. Effect of electrodeposition modes on surface characteristics and corrosion properties of fluorine-doped hydroxyapatite coatings on Mg-Zn-Ca alloy[J]. Applied Surface Science, 2011, 257(11): 4811-4816.
[65] RAZAVI M, FATHI M, SAVABI O, VASHAEE D, TAYEBI L. In vivo assessments of bioabsorbable AZ91 magnesium implants coated with nanostructured fluoridated hydroxyapatite by MAO/EPD technique for biomedical applications[J]. Materials Science & Engineering C, 2015, 48: 21-27.
[66] RAMESHBABU N, SAMPATH KUMAR T S, PRABHAKAR T G, SASTRY V S, MURTY K V, PRASAD RAO K. Antibacterial nanosized silver substituted hydroxyapatite: Synthesis and characterization[J]. Journal of Biomedical Materials Research Part A, 2010, 80A(3): 581-591.
[67] FIELDING G A, ROY M, BANDYOPADHYAY A, BOSE S. Antibacterial and biological characteristics of silver containing and strontium doped plasma sprayed hydroxyapatite coatings[J]. Acta Biomaterialia, 2012, 8(8): 3144-3152.
[68] BARBA F, MIRANDA M. Synthesis and antimicrobial activity of a silver-hydroxyapatite nanocomposite[J]. Journal of Nanomaterials, 2009, (1687-4110): 14.
[69] HU G, ZENG L, DU H, FU X D, JIN X X, DENG M, ZHAO Y J, LIU X W. The formation mechanism and bio-corrosion properties of Ag/HA composite conversion coating on the extruded Mg-2Zn-1Mn-0.5Ca alloy for bone implant application[J]. Surface and Coatings Technology, 2017, 325: 127-135.
[70] TIAN B, CHEN W, YU D, LEI Y, KE Q F, GUO Y P, ZHU Z N. Fabrication of silver nanoparticle-doped hydroxyapatite coatings with oriented block arrays for enhancing bactericidal effect and osteoinductivity[J]. Journal of the Mechanical Behavior of Biomedical Materials, 2016, 61: 345-359.
[71] MIRZAEE M, VAEZI M, PALIZDAR Y. Synthesis and characterization of silver doped hydroxyapatite nanocomposite coatings and evaluation of their antibacterial and corrosion resistance properties in simulated body fluid[J]. Materials Science & Engineering C, 2016, 69: 675-684.
[72] ��־��, �� ��, �ֲ���. �绯ѧ�������������ǻ���ʯͿ�㼰���������о�[J]. �绯ѧ, 2008(3): 243-247.
GENG Zhi-wang, WANG Hui, LIN Chang-jian. Electrochemical deposition of nano-silver hydroxyapatite coating and its antibacterial properties[J]. Journal of Electrochemistry, 2008(3): 243-247.
[73] MARIE P J. Strontium ranelate: a dual mode of action rebalancing bone turnover in favour of bone formation[J]. Current Opinion in Rheumatology, 2006, 18 (S1): 11-15.
[74] WU C, RAMASWAMY Y, KWIK D, ZREIQAT H. The effect of strontium incorporation into CaSiO3 ceramics on their physical and biological properties[J]. Biomaterials, 2007, 28(21): 3171-3181.
[75] ��ѩ÷, �� ��, ��ѩ��, ������, ������. ���������ǻ���ʯ���Ʊ��������о�[J]. ���ι�ҵ, 2015, 47(1): 30-32.
GU Xue-mei, AN Yan, YANG Xue-yan, YIN Ya-ting, CHANG Ai-xiang. Preparation and properties of cerium- containing nano-hydroxyapatite[J]. Journal of Inorganic Salts, 2015, 47(1): 30-32.
[76] YU N, CAI S, WANG F W, ZHANG F Y, LING R, LI Y, JIANG Y Y, XU G H. Microwave assisted deposition of strontium doped hydroxyapatite coating on AZ31 magnesium alloy with enhanced mineralization ability and corrosion resistance[J]. Ceramics International, 2017, 43(2): 2495-2503.
[77] SINGH S S, ROY A, LEE B E, OHODNICHI J, LOGHMANIAN A, BANERJEE I, KUMTA P N. A study of strontium doped calcium phosphate coatings on AZ31[J]. Materials Science & Engineering C, 2014, 40: 357-365.
[78] LOWRY N, BROLLY M, HAN Y, MCKILLOP S, MEENAN B J, BOYD A R. Synthesis and characterisation of nanophase hydroxyapatite co-substituted with strontium and zinc[J]. Ceramics International, 2018, 44(7): 7761-7770.
[79] GENG Z, CUI Z D, LI Z Y, ZHU S L, LIANG Y Q, LIU Y D, LI X, HE X, YU X X, WANG R F, YANG X J. Strontium incorporation to optimize the antibacterial and biological characteristics of silver-substituted hydroxyapatite coating[J]. Materials Science & Engineering C, 2016, 58(6): 467-477.
[80] COX S C, JAMSHIDI P, GROVER L M, MALLICK K K. Preparation and characterisation of nanophase Sr, Mg, and Zn substituted hydroxyapatite by aqueous precipitation[J]. Materials Science & Engineering C, 2014, 35(35): 106-114.
[81] CARLISLE E M. Silicon: A requirement in bone formation independent of vitamin D1[J]. Calcified Tissue International, 1981, 33(1): 27-34.
[82] Ф���, �� ӱ, ���ٻ�, �߾���. ������ǻ���ʯ��������۶���Ѫ�������������[J]. ���ϲ���ѧ��, 2009, 26(2): 149-154.
XIAO Feng-juan, ZHANG Ying, WANG Shao-hui, GAO Jun-feng. Adsorption of human serum albumin by silicon-doped hydroxyapatite bioactive micropowder[J]. Journal of Composite Materials, 2009, 26(2): 149-154.
[83] DEHGHANIAN C, ABOUDZADEH N, SHOKRGOZAR M A. Characterization of silicon-substituted nano hydroxyapatite coating on magnesium alloy for biomaterial application[J]. Materials Chemistry & Physics, 2017, 203: 27-33.
[84] QIU X, WAN P, TAN L L, FAN X M, YANG K. Preliminary research on a novel bioactive silicon doped calcium phosphate coating on AZ31 magnesium alloy via electrodeposition[J]. Materials Science & Engineering C, 2014, 36(1): 65-76.
[85] SHEPHERD J H, SHEPHERD D V, BEST S M. Substituted hydroxyapatites for bone repair[J]. Journal of Materials Science Materials in Medicine, 2012, 23(10): 2335-2347.
[86] BAKHSHESHI-RAD H R, HAMZAH E, ISMAIL A F, KASIRI-ASGARANI M, DAROONPARVAR M. Novel bi-layered nanostructured SiO2/Ag-FHAp coating on biodegradable magnesium alloy for biomedical applications[J]. Ceramics International, 2016, 42(10): 11941-11950.
ZHANG Jun1, ZHANG Chun-yan1, 2, ZHANG Shi-yu1, LIU Cheng-long1, 2
(1. School of Materials Science & Engineering, Chongqing University of Technology, Chongqing 400054, China;
2. Chongqing Municipal Engineering Research Center of Institutions of Higher Education for Special Welding Materials and Technology, Chongqing 400054, China)
Abstract: Magnesium and magnesium alloys have great potential as biomedical materials due to their good biocompatibility and biodegradability. However, the rapid degradation rate limits their clinical application. Hydroxyapatite (HA) coating has good osteoinductivity and osteoconductivity, which can delay the corrosion of magnesium alloy to some extent. But a single hydroxyapatite coating cannot meet the requirements for the clinical service life of magnesium implants, so the HA coating needs to be further modification. In this paper, the research and development about biocompatibility, biodegradability and mechanical properties of HA composite coating modified by polymer, ceramic and doped-ions on magnesium and its alloys were reviewed.
Key words: magnesium alloy; hydroxyapatite; composite coating; biomaterials
Foundation item: Project(51201192) supported by the National Natural Science Foundation of China; Project (cstc2018jcyJAX0712) supported by the Natural Science Foundation of Chongqing, China
Received date: 2018-07-30 ; Accepted date: 2019-12-02
Corresponding author: ZHANG Chun-yan; Tel: +86-13658321150; E-mail: zhangchunyan@cqut.edu.cn
(�༭ �� ��)
������Ŀ��������Ȼ��ѧ����������Ŀ(51201192)����������Ȼ��ѧ����������Ŀ(cstc2018jcyJAX0712)
�ո����ڣ�2018-07-30�������ڣ�2019-12-02
ͨ�����ߣ��Ŵ��ޣ������ڣ���ʿ���绰��13658321150��E-mail��zhangchunyan@cqut.edu.cn

