���±��: 1004-0609(2006)10-1665-07
һ������ϳ�Nb����LiFePO4/C����绯ѧ����
��ѧ��, ���±�, �ܸ�ۿ, ��ʤ��, л ��, ������
(�㽭��ѧ ����ϵ, ���� 310027)
ժ Ҫ: �����۵����������ӻ�����Ϊ��Դ, �Ծ۱�ϩΪ��ԭ����̼Դ, ��һ�����෨�ϳ�Nb����LiFePO4��ͬʱʵ�ֿ�������̼����Ĥ��ԭλ������ �������: һ������ϳɵ�Nb����LiFePO4/C�������������ʯ��LiFePO4����ṹ�ͽ�����״�Ŀ�����ò, �����ߴ�Ϊ100~500nm; �۱�ϩ�ֽ���ڿ�������Ϳ���֮���γ���ͨ������״̼Ĥ�� �绯ѧ���Խ������, ��Nb�IJ�����Ϊ1.0%(Ħ������)ʱ������õı��ʷŵ����ܺ�ѭ������; ��2C��ŵ�ʱ����130mA��h/g�ķŵ�����, ѭ��100��������˥��, ��4C��ŵ�ʱ�Ծ���105mA��h/g�ķŵ�������
�ؼ���: �������; ����ӵ��; ��������; ����ϳ�; Nb���� ��ͼ�����: TM912.9
���ױ�ʶ��: A
Electrochemical properties of Nb doped LiFePO4/C prepared by one-step solid-state synthesis
CHEN Xue-jun, ZHAO Xin-bing, CAO Gao-shao,
MA Sheng-lin, XIE Jian, ZHU Tie-jun
(Department of Materials, Zhejiang University, Hangzhou 310027, China)
Abstract: Nb-doped lithium iron phosphates were synthesized and in-situ carbon coated by one-step solid-state reaction using ferrous compound as the iron source and polypropylene as the reductive agent and carbon source. The results show that the one-step solid-state synthesized Nb doped LiFePO4/C powders are near-spherical particles of 100-500nm with the olivine type LiFePO4 structure, and wrapped with carbon nets decomposed from polypropylene. Electrochemical analyses show that LiFePO4/C with 1.0% Nb(in mole fraction) doping has the best rate performances and cycling stability with a discharge capacity of 130mA��h/g retained up to 100 cycles at 2C rate and 105mA��h/g at 4C rate.
Key words: lithium iron phosphate; lithium ion batteries; cathode materials; solid-state synthesis; niobium doping
���ʯ���������(LiFePO4)����170mA��h/g������������3.5V���ҵĶ�﮳�ŵ�ƽ̨��ѹ, ��1997���״α����ò��Ͽɱ���������ӵ��������������[1], �����˹㷺�Ĺ�ע�ʹ������о��� �봫ͳ��LiCoO2��LiMn2O4�����������, LiFePO4ԭ����Դ���㷺�� �۸�������� ������Ⱦ�� �ر���LiFePO4�ڵ�����о��кܸߵ����ȶ��Ժͻ�ѧ������[2], �ڳ�ŵ�����о�������Ľṹ�ȶ���[1, 3], ���LiFePO4�������Ͼ���ͻ���İ�ȫ���ܺ��ر������ѭ���ȶ���[4]�� ��Լ��ʵ��Ӧ�õ���Ҫ������LiFePO4�ĵ絼�ʺܵ�(������ԼΪ10-9 S/cm)[5, 6]�� ���LiFePO4�絼�ʵ���Ҫ��������: 1)����ˮ�ȷ�[7, 8]�� ������[9]�Ȼ�ѧ�������е��ĥ[10]�����������ϳɲ���, ͨ����С�����ߴ������̵��Ӻ������ڿ����ڲ���Ǩ�ƾ���; 2)��LiFePO4�����������̼[11, 12]�������ߵ�����[6]���γ����ӻ������ʿ����ĵ�������; 3)ͨ����LiFePO4�в��Ӹ۽�������[5, 13, 14]����߲��ϵı���絼�ʡ� ���ڵ��о���ʾ[15, 16], ͬʱ���õ�����Ӻ͵���������ķ���, �����LiFePO4�絼�ʵ���Ч;����
����������������һ��һ�����෨�ϳ�ԭλ̼����LiFePO4�ļ���[17], ���ص��Dz������۵�������������Ϊ��Դ, ��һ�ι��౺�������Fe3+��Fe2+ ��ԭ�� LiFePO4����ϳɺ�ԭλ̼������ 700�決��10h����ϳɲ�����0.1C��ŵ籶���µ���������ﵽ164mA��h/g, ����1C���������������½��� Ϊ��, �������߲���һ�����෨�ϳ���Nb���ӵ�ԭλ̼����LiFePO4��������, �о���Nb�����Բ��ϵ绯ѧ���ܵ�Ӱ��, �ر��Ǹ߱��ʳ�ŵ������µ�ѭ���������ԡ�
1 ʵ��
�Է������Լ�LiOH��H2O�� FePO4��4H2O��Nb2O5Ϊԭ��, ��Li1-xNbxFePO4 (x=0, 0.005, 0.01, 0.015, 0.02)��ѧ�����ȳ����� ��ÿĦ��Ŀ������ԭ��������35g�۱�ϩ��Ϊ��ԭ����̼Դ�� ���������ƾ���Ϊ��ĥ��, ��ĥ��Ͼ��ȡ� �������60���º�ɺ�, ��N2(����Ϊ1L/min)��������10��/min�����ٶȼ��ȵ�600��, ����10h����Nb���ӵ�̼����������ﮡ�
������X��������(XRD)��Rigaku-D/MAX-2550PC��X���߷�ĩ�������Ͻ��С� ʹ��CuK������Դ, ��=1.5406�@, Ni�˲�Ƭ, ����20mA, ��ѹ40kV, ɨ�跶Χ10��~80��, ɨ���ٶ�4(��)/min, ����0.02�㡣 ����FEI Sirion�ͳ�����ɨ���������(FESEM)������ĩ��ò�� ������������ɢ����(EDS)��ѡ����������(SAED)�������ܵ�Philips-CM�߷ֱ��������(HRTEM)�������ϵ��۽ṹ�����ɷֲַ��� ����EA-1112��Ԫ�ط����Ƿ����ϳɲ����е�̼��������
����ť����ģ���ؽ����������ϵĵ绯ѧ���ԡ� �����缫�е��������ϻ������ʡ� �������Ȳ�ڡ� ճ�Ӽ���ƫ����ϩ��������Ϊ75��15��10, �Ե缫Ϊ�����Ƭ, ��ĤΪ�۱�ϩ��Ĥ(Celgard-2300)�� ���ҺΪ1mol/L��LiPF6�ĵ������̼����ϩ��(EC)�� ����ϩ̼����(EMC)�� ����̼����(DMC)��Һ�� ����ڳ������������������װ�䡣 ����PCBT-138-32D��ͨ����س̿ز����ǽ��к������ŵ����, ��ŵ籶��Ϊ0.5C�� 1C�� 2C��4C�� ����Solartron 1255B��Ƶ���Ǻ�1237�͵�λ�ǽ��н����迹����, ������ѹ���Ϊ5mV, Ƶ�ʷ�ΧΪ106~10-2 Hz��
2 ���������
����Ԫ�ط���, һ������ϳ�Nb����LiFePO4/C���ϲ����е�̼����(��������)Ϊ2.6 %�� ͼ1��ʾΪNb������(ԭ�����ʱ������ɷ�, Ħ��������ͬ)xΪ0�� 0.5�� 1.0�� 1.5��2.0%ʱ�ĺϳɲ���XRD�ס� ��ͼ���Կ���, ����������Ϊ���ʯ��LiFePO4, �ɷֱ�����嶼�ɸ���JCPDS 83-2092�����߱궨, �������������, ˵����һ�����౺���������Fe3+�Ļ�ԭ��Nb����LiFePO4�ĺϳɡ� ����XRD���ݼ���õ��ĺϳɲ��ᄃ���������ڱ�1�� �������, Nb���ӵ�
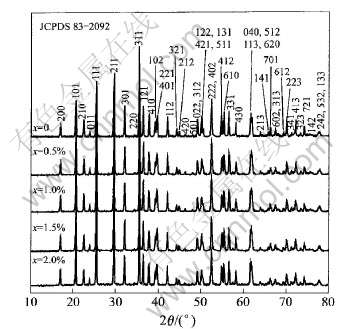
ͼ1 ��ͬNb��������LiFePO4/C��XRD��
Fig.1 XRD patterns of LiFePO4/C with different doping amounts of Nb
��1 ��ͬNb��������LiFePO4/C�ľ�������
Table 1 Unit cell parameters of LiFePO4/C with different doping amounts of Nb
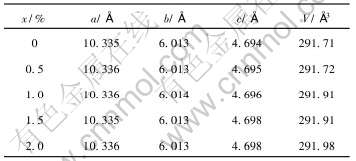
LiFePO4��a�� b�᷽��������û�б仯, ��c�ᾧ������Nb������������������ ����Nb��LiFePO4�еľ���ռλ����в����, ��һ����ΪNb��LiFePO4����+5��������ʽ����[5, 13], ������Shannon���������[18], �ڰ�������λ��Nb5+�����Ӱ뾶С��Fe2+�İ뾶, ����Nb����ռ��LiFePO4�е�Feλ����������ռ��Liλ�á�
ͼ2(a)�� (b)��(c)�ֱ���ʾΪNb������Ϊ0�� 1.0%��2.0%ʱ��LiFePO4/C��SEM��Ƭ�� ����SEM�۲�, Nb����LiFePO4/C�Ŀ����ߴ���100~500nm��Χ�ڡ� ��ͼ2�л����Կ���, һ��������ϳɵ�Nb����LiFePO4/C���н�����״�Ŀ�����ò, ͬʱNb�������Կ�����̬����û��Ӱ�졣 ͼ2(d)��ʾΪ150��ˮ�ȷ��ϳ�LiFePO4��SEM��Ƭ�� ���Կ���, ˮ�Ⱥϳɲ���������侧��ṹ���Ƶ�Ƭ״������������ò, ˵��LiFePO4����������Եı����ܸ������ԡ� ��ͼ������ע�, ���¹���ϳɲ���Ŀ����ߴ���ϳ��¶ȵ͵ö��ˮ�Ⱥϳɲ����൱�� ˵�����IJ��õ�һ������ϳɷ�������Ч������LiFePO4�Ŀ�������
ͼ3��ʾΪNb������Ϊ1.0%��LiFePO4/C��TEM��Ƭ�� ��ͼ3(a)�ɿ���̼Ĥ������LiFePO4�������沢�ڿ���֮���γ���ͨ���硣 ������̬��̼Ĥ����������߿�������Ϳ���֮��ĵ��Ӵ�������, �Ӷ����Ʋ��ϵĵ������ܡ� ͬʱ, ������LiFePO4�ϳɹ�����ԭλ�γɵ�̼����ĤҲ��Ч���谭��LiFePO4�����ij��� ��Ҳ��������ͼ2�п����Ĺ���ϳɲ�������ߴ���ˮ�Ⱥϳɲ����൱��ԭ�� ͼ3(b)��ʾ�ĸ߷ֱ�����ʾ, ��LiFePO4����������һ��Ǿ�̬����, ������5nm���ҡ� Delacourt��[15]Ҳ���۲쵽�����������ṹ, ������Ϊ�ǷǾ�̬Fe2P�� ��Fe2P��ֱ���۵�(1370��)�ȶ��Ľ����仯����, ���෴Ӧ�������γ�Fe2P�Ǿ�������ѧ���ݲ���֡� ��ͼ3(b)�п���, ����Ǿ�����LiFePO4����֮������á� ��������Ʋ�, �������ڲ����Ʊ������б����������γɵ�ij��Fe�� P�� O������Ǿ����㡣
FePO4/C������TEM��ò�Ͷ�Ӧ��Fe�� Nb�� PԪ����ֲ��� ��ͼ�ɼ�, ��ȻNbԪ�صķֲ����ں����ϵͶ����Ƿdz�����, ��Nb�ڿ����еķ�
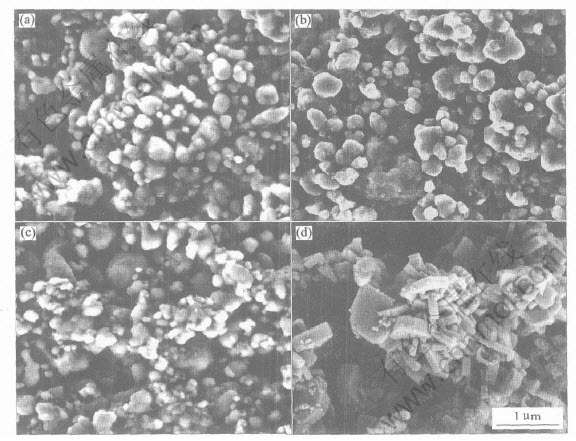
ͼ2 ����ϳ�Nb����LiFePO4/C(������: (a) x=0, (b) x=1.0%,(c) x=2.0%)��ˮ�Ⱥϳɴ�LiFePO4(d)��SEM��Ƭ
Fig.2 SEM images of the solid-state calcined LiFePO4/C composite powders with various Nb doping of x=0 (a), x=1.0% (b), x=2.0% (c) and hydrothermally synthesized LiFePO4 powders (d)

ͼ3 Nb������Ϊ1.0%��LiFePO4/C��TEM��Ƭ(a)��HRTEM����SAED��(b)
Fig.3 TEM photo (a) and HRTEM image withSEAD pattern (b) of LiFePO4/C doped with 1.0% Nb

ͼ4 Nb������Ϊ1.0%��LiFePO4/C��HRTEM��Ԫ�ص���ֲ�
Fig.4 HRTEM image (a) and elemental mapping distributions ((b), (c) and (d)) of LiFePO4/C doped with 1.0% Nb
���������Եġ��м�ࡢ �����١������� ���ֲַ�������P�� Fe����һ��, ���ڵ��͵ġ����ڷֲ��������� ��һ����Delacourt��[15]���о������ͬ�� ���Ƿֱ������Һ����ͻ�е��ĥ�Ʊ�ǰ����, Ȼ��350���700�����α����Ʊ�Nb����LiFePO4�� ���Ƿ������۲������ַ���, �ϳ�ʱ���ӵ�Nb��û�в��ӵ�LiFePO4������, �����γ��˰�����LiFePO4��������Ħ�-NbOPO4��Fe�� P�� Nb�� C�� O�ķǾ�̬���ӻ���� ��ͼ4��ʾ��Nb��Ԫ�طֲ���������, �������߲���һ��������ϳɵ�Nb����LiFePO4/C��, ����Ԫ��Nb(�������е�һ����)�Ѿ����ܵ�LiFePO4�����С� �����ڲ�����(�������)����, �й�Nb��ռλ�����ͷֲ������д���һ���������о���
ͼ5��ʾΪNb����LiFePO4/C�������ϵ��״�1C��ŵ����ߡ� ��ͼ�п��Կ���, δ�����������״�1C�ŵ������ӽ�120mA��h/g, ���ڱ��������ǰ���о����[17]�� ˵����ȷ���ϳɷ�Ӧ��ȫ��ǰ����, �ʵ����ͱ����¶�������ġ� ������0.5��1.0mol% Nb��, LiFePO4/C�������ϵ��״�1C�ŵ������ֱ�������130��140mA��h/g���ҡ� ֤��Nb���ӿ���Ч��߲��ϵĴ������ŵ������� ����, ��Nb��������������ʱ, ���ϵķŵ��������ν��͡� ���ڱ�ʵ��Nb����ߺ���ֻ�൱��LiĦ������2%, Nb����������IJ�����Li���ļ������ֻ�൱��3.4mA��h/g������ ���Թ���Nb����������������½�ֻ�ܱ���Ϊ���γ���ij���谭���ӻ�Li+Ǩ�Ƶ��ṹ����, �����γɷǵ����ࡣ ��һ����Ӱ����������д��о���
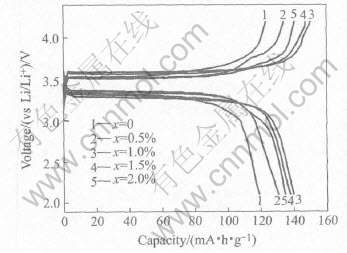
ͼ5 ����ϳ�Nb����LiFePO4/C�������ϵ��״�1C��ŵ�����
Fig.5 Initial charge/discharge voltage profiles of Nb doped LiFePO4/C at 1C
ͼ6��ʾΪNb����LiFePO4/C�ڳ�ŵ�ǰ�Ľ����迹�ס� ��ͼ�ɼ�, �����������迹����һ��ѹ��ĸ�Ƶ��Բ��һ����Ƶֱ�߹���, ˵�����������������Ƶ��迹������ ����Nb��������x=0��x=1.0%, ��Ƶ��Բ��Z��ֵ��600���½���370��; ���������������ߵ�x=1.5%��x=2.0%ʱ, Z��ֵ����֮������ ������Nb�������仯���迹��������ͼ5��ʾ��1C��ŵ������仯������һ�µġ�
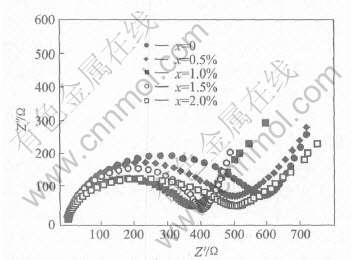
ͼ6 Nb����LiFePO4/C�������ϵĽ����迹��
Fig.6 Electrochemical impedance plots of Nb doped LiFePO4/C
ͼ7��ʾΪLiFePO4/C��Nb������Ϊ1.0%��LiFePO4/C�ڲ�ͬ��ŵ籶��������ѭ��ʱ�ķŵ������� ��ͼ�п��Կ���, ��δ���ӵ�LiFePO4/C���, 1.0% Nb���ӵ�LiFePO4/C��������ͬ�����������ϸ�, ���ұ��ֳ��������ѭ�����ܡ� 2C�ŵ�������130mA��h/g���Ҳ�����100��ѭ����˥��, 4C�ŵ�����Ҳ�ﵽ105mA��h/g�� �ر��Ǿ���100��2Cѭ���ͽ�10��4C��ŵ��, 1Cѭ���ŵ������Խӽ�145mA��h/g, �����Ը�
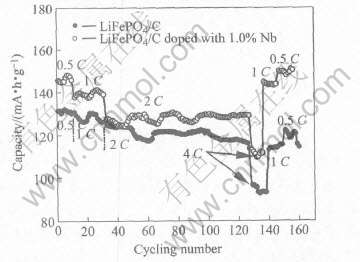
ͼ7 ����ϳ�LiFePO4/C��Nb������Ϊ1.0%��LiFePO4/C�ڲ�ͬ����������ѭ��ʱ�ķŵ�����
Fig.7 Discharge capacities of LiFePO4/C and 1.0 % Nb doped LiFePO4/C in continuous cycling at various rates
�ڳ�ʼ��140mA��h/g������ �����, ��������Nb, ������������߲��ϵĵ绯ѧ����, ���������ڲ���ѭ���ȶ��ԵĽ�һ����ߡ� ��ͼ7��, ���Ƿ��ֶ���δ���ӵ�LiFePO4/C, ����ŵ籶�ʴ�0.5C������ߵ�1C��2Cʱ, �ŵ�����û��ͻȻ�½�, ����������˥������ �й���������IJ������Ը�Դ�͵绯ѧ���ƻ��д��о���
ͼ8��ʾΪNb������Ϊ1.0%��LiFePO4/C��158��ѭ��ǰ��Ľ����迹�Ƚϡ� ��ͼ���Կ���, ��Ƶ����İ�Բ��ѭ����������С�� ��˵��ѭ��������, ���ŵ��Һ�����缫�Ŀ�������, ����ӵ���ɢͨ������, �����˸���ļ��Ӧλ��, ʹ�õ��Һ/��������֮�������ӵĴ����ٶȼӿ�, ����������, ���Һ������֮����迹��֮�½�[19]��
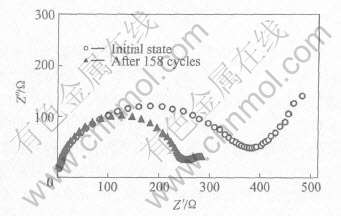
ͼ8 Nb������Ϊ1.0%��LiFePO4/C��158��ѭ��ǰ��Ľ����迹��
Fig.8 Electrochemical impedance plots of 1.0 % Nb doped LiFePO4/C before and after 158 cycles
3 ����
��Nb2O5�� FePO4��4H2O�� LiOH��H2O�;۱�ϩһ�����෨�ϳ���Nb���ӵ�LiFePO4/C�� �ϳɲ���������������ʯ��LiFePO4����ṹ, ��ĩ��״�ӽ�����, �ߴ�Ϊ100~500nm, ̼����(��������)Ϊ2.6%, �����ڿ������沢�ʱ�Ĥ��״��ͨ����֮�䡣 Nb����LiFePO4/C�������ϵĵ绯ѧ������x=0~1.0%(Ħ������)��Χ����Nb���������Ӷ��������, ����������Nb���������½��� �ڱ�ʵ�鷶Χ��, ����ɷ�ΪLi0.99Nb0.01FePO4/C�ĺϳɲ��������õĵ绯ѧ����: 2C�ŵ�������130mA��h/g���Ҳ�����100��ѭ����˥��, 4C�ŵ�����Ҳ�ﵽ105mA��h/g�� �ر��Ǿ���100��2Cѭ���ͽ�10��4C��ŵ��, 1Cѭ���ŵ������Խӽ�145mA��h/g, ���ֳ����õĸ߱��ʳ�ŵ�ѭ�����ԡ�
REFERENCES
[1]Padhi A K, Nanjundaswamy K S, Goodenough J B. Phospho-olivines as positive-electrode materials for rechargeable lithium batteries[J]. J Electrochem Soc, 1997, 144(4): 1188-1194.
[2]MacNeil D D, Lu Z H, Chen Z H, et al. A comparison of the electrode/electrolyte reaction at elevated temperatures for various Li-ion battery cathodes[J]. J Power Sources, 2002, 108(1-2): 8-14.
[3]Padhi A K, Nanjundaswamy K S, Masquelier C, et al. Effect of structure on the Fe3+/Fe2+ redox couple in iron phosphates[J]. J Electrochem Soc, 1997, 144(5): 1609-1613.
[4]Takahashi M, Ohtsuka H, Akuto K, et al. Confirmation of long-term cyclability and high thermal stability of LiFePO4 in prismatic lithium-ion cells[J]. J Electrochem Soc, 2005, A152(5): 899-904.
[5]Chung S Y, Bloking J T, Chiang Y M. Electronically conductive phospho-olivines as lithium storage electrodes[J]. Nat Mater, 2002, 1(2): 123-128.
[6]Herle P S, Ellis B, Coombs N, et al. Nano-network electronic conduction in iron and nickel olivine phosphates[J]. Nat Mater, 2004, 3(3): 147-152.
[7]Yang S F, Zavalij P Y, Whittingham M S. Hydrothermal synthesis of lithium iron phosphate cathodes[J]. Electrochem Commun, 2001, 3(9): 505-508.
[8]ׯ���, ���±�, �ܸ�ۿ, ��. ˮ�ȷ��ϳ�LiFePO4����ò�ͷ�Ӧ����[J]. �й���ɫ����ѧ��, 2005, 15(12): 2034-2039.
ZHUANG Da-gao, ZHAO Xin-bing, CAO Gao-shao, et al. Morphology and reaction mechanism of LiFePO4 prepared by hydrothermal synthesis[J]. The Chinese Journal of Nonferrous Metals, 2005, 15(12): 2034-2039.
[9]Franger S, Le Cras F, Bourbon C, et al. Comparison between different LiFePO4 synthesis routes and their influence on its physico-chemical properties[J]. J Power Sources, 2003, 119: 252-257.
[10]Yamada A, Chung S C, Hinokuma K. Optimized LiFePO4 for lithium battery cathodes[J]. J Electrochem Soc, 2001, A148(3): 224-229.
[11]Huang H, Yin S C, Nazar L F. Approaching theoretical capacity of LiFePO4 at room temperature at high rates[J]. Electrochem Solid State Lett, 2001, A4(10): 170-172.
[12]�ű�, ���ı�, ���º�, ��. LiFePO4/C����ӵ���������ϵĵ绯ѧ����[J]. �й���ɫ����ѧ��, 2005, 15(2): 300-304.
ZHANG Bao, LUO Wen-bin, LI Xin-hai, et al. Electrochemical properties of LiFePO4/C for cathode material of lithium ion batteries[J]. The Chinese Journal of Nonferrous Metals, 2005, 15(2): 300-304.
[13]Chung S Y, Chiang Y M. Microscale measurements of the electrical conductivity of doped LiFePO4[J]. Electrochem Solid State Lett, 2003, A6(12): 278-281.
[14]�߽���, �ܺ��, �¼���, ��. ������������Ӹ���LiFePO4�绯ѧ����[J]. ����ѧѧ��, 2005, 21(4): 472-476.
NI Jiang-feng, ZHOU Heng-hui, CHEN Ji-tao, et al. Improvement of LiFePO4 electrochemical performance by doping metal oxides[J]. Chinese J Inorg Chem, 2005, 21(4): 472-476.
[15]Delacourt C, Wurm C, Laffont L, et al. Electrochemical and electrical properties of Nb-and/or C-containing LiFePO4 composites[J]. Solid State Ion, 2006, 177(3/4): 333-341.
[16]Xie H, Zhou Z T. Physical and electrochemical properties of mix-doped lithium iron phosphate as cathode material for lithium ion battery[J]. Electrochim Acta, 2006, 51(10): 2063-2067.
[17]Mi C H, Zhao X B, Cao G S, et al. In situ synthesis and properties of carbon-coated LiFePO4 as Li-ion battery cathodes[J]. J Electrochem Soc, 2005, A152(3): 483-487.
[18]Shannon R D. Revised effective ionic radii and systematic studies of interatomic distances in halides and chalcogenides[J]. Acta Crystallogr A, 1976, A32(5): 751-767.
[19]Liao X Z, Ma Z F, He Y S, et al. Electrochemical behavior of LiFePO4/C cathode material for rechargeable lithium batteries[J]. J Electrochem Soc, 2005, A152(10): 1969-1973.
(�༭��ѧ��)
�ո�����: 2006-05-24; ������: 2006-08-16
ͨѶ����: ���±�, ����; �绰: 0571-87951451; ����: �绰: 0571-87951451; E-mail: zhaoxb@zju.edu.cn