3 V锂离子电池用层状α-Na0.67MnO2.26的电化学性能
杨顺毅,王先友,伍 文,胡 涛,王 欣,易四勇
(湘潭大学 化学学院,湖南 湘潭,411105)
摘 要:以Mn(CH3COO)2・4H2O和Na2CO3为原料,通过sol-gel技术合成前驱体,在600 ℃焙烧前驱体得到一种新的无水层状α-Na0.67MnO2.26材料。用等离子体光谱、X射线衍射仪、扫描电镜、恒流充放电和循环伏安(CV)等对产物的结构、组成、形貌及电化学性能进行研究。结果表明:得到的样品为稳定的六方层状P2结构,且颗粒细小;该样品在充放电电流密度为25 mA/g和电压为2.0~4.3 V时,首次充电比容量为188 mA?h/g,第2次放电比容量为176 mA?h/g,充放电库仑效率高达94%;在电压为2.0~4.3 V,电流密度为25,50,125和250 mA/g充放电条件下,其第2次放电比容量分别为176,168,139和110 mA?h/g,40次循环后,其放电比容量分别为150,142,121和105 mA?h/g,显示材料有较好的循环稳定性和大电流充放电性能。
关键词:锂离子电池;层状钠锰氧化物;正极材料;电化学性能;结构稳定性
中图分类号:O646 文献标识码:A 文章编号:1672-7207(2009)01-0072-06
Electrochemical performance of layered α-Na0.67MnO2.26 as
cathode material of 3 V lithium ion batterie
YANG Shun-yi, WANG Xian-you, WU Wen, HU Tao, WANG Xin, YI Si-yong
(School of Chemistry, Xiangtan University, Xiangtan 411105, China)
Abstract: The new layered sodium manganese oxides α-Na0.67MnO2.26 was synthesized at 600 ℃ by the method of solid-state reaction combined with sol-gel process, and using both Mn(CH3COO)2・4H2O and Na2CO3 as the start material. The structure, composition, appearance and electrochemical performances of the product were characterized by Inductively coupled plasma (ICP), X-ray diffraction (XRD), scanning electron microscope (SEM), the constant current charge/discharge and cyclic voltammogram. The results indicate that α-Na0.67MnO2.26 has hexagonal layered P2 structure with small particle size. The first specific charge capacity of the material is 188 mA?h/g and the second specific discharge capacity of the material is 176 mA?h/g, and the coulomb efficiency in the first charge-discharge process reaches 94%. Besides, it was found that the sample has the better cycle stability and rapid charge-discharge performance. In the potential window 2.0-4.3 V, the second specific discharge capacities of 176, 168, 139 and 110 mA?h/g are obtained at the rate of 25, 50, 125 and 250 mA/g, respectively. After 40 cycles, attractive specific capacities of 150, 142, 121 and 105 mA?h/g are obtained, respectively.
Key words: lithium-ion battery; layered sodium manganese oxides; cathode material; electrochemical properties; structure stabilit⊙
锰氧化物具有资源丰富、价格低廉(锰价仅为钴价的1/20)、低毒性、安全性能好等优点,被认为是一种很有前景的高比能量锂离子电池正极材料[1]。然而,锰酸锂材料在锂离子电池实际应用中仍然存在很多问题,如:尖晶石LiMn2O4由于存在Jahn-Teller晶格扭变,在高电压[2]和高温下(一般大于50 ℃)[3]易溶解在电解液中,导致循环容量迅速衰减;层状LiMnO2在深度循环时极易向尖晶石相转变,导致容量急剧下降[4]。为了解决这些问题,人们对另一种电化学活性锰氧化物NaxMnO2+δ[5-8]的合成和电化学性能进行了研究。
层状NaxMnO2+δ材料通常用作离子交换法合成层状LiMnO2正极材料的前驱体[9-10],而对其直接作为锂离子电池正极材料的研究却很少。LeGoff等[6]以NaMnO4为锰源,以富马酸为还原剂,通过sol-gel法合成了具有层状结构的Na0.45MnO2.14?0.76H2O材料,在C/6的放电倍率下,循环40次后,容量为110 mA?h/g左右。Hibino等[11]用CH3CH2OH还原NaMnO4,并通过在合成过程中和制作极片时加入乙炔黑,合成了能进行大电流充放电的含水型钠锰氧化物(HSMO)复合材料,在1 A/g电流密度下,其初始容量达250 mA?h/g,但是经10 次循环后,容量衰减过半,这可能与复合材料中含有部分结晶水有关。Masayuki等[12]通过共沉淀法和氧化法合成了掺钴型的Na-birnessite材料,在电流线密度为0.1 mA/cm,电压为2.0~4.0 V时,掺Co为30 %的材料首次容量达184 mA?h/g,但循环容量有待提高。Bach等[7]以NaMnO4为锰源,以CH3OH为还原剂,通过sol-gel法合成了无水的层状α-Na0.66MnO2.13材料,在2.0~4.0 V电压范围内,在C/20倍率下循环容量达150 mA?h/g,50次循环后,材料结构并没有向尖晶石发生转变,这说明无水的层状钠锰氧化物是一种稳定的锂离子电池正极材料。作者以Mn(CH3COO)2?4H2O为锰源,通过sol-gel合成干凝胶前驱体,将前驱体在空气气氛中煅烧得到Na-Mn-O材料,主要讨论了600 ℃制备样品的电化学性能。
1 实 验
1.1 钠锰氧正极材料的制备
按Na与Mn摩尔比为0.7?1称取适量的无水Na2CO3(AR)和Mn(CH3COO)2・4H2O(AR)溶于二次蒸馏水,在80 ℃搅拌蒸发,得到浅黄色的干凝胶,将干凝胶在ND2-2L超级球磨机中球磨2 h,再置于马弗炉中,在250 ℃预烧12 h,然后升温至600 ℃,保温1 h,冷却,球磨1 h得到层状钠锰氧化物正极材料。
1.2 材料的表征
采用Perkin Elemeroptima 5300DV等离子发射光谱仪(ICP)分析产物的组成。采用D/Max-3C型X射线衍射仪(XRD)对正极活性物质进行结构分析,射线源为Cu Ka,管电流为20 mA,管电压为36 kV,扫描速度为8 (°)/min,扫描范围为10?~80?。采用日本JEOL公司制造的型号为JSM-5600LV型扫描电子显微镜来观察样品的颗粒大小和表面形貌。
1.3 电池的制备及电化学性能测试
将制备好的正极材料与乙炔黑、石墨、粘结剂(PVDF)按质量比70?20?5?5混合,滴加少量溶剂N-甲基-2-吡咯烷酮(NMP)后,搅拌为均匀糊状,涂膏于铝箔上,经80 ℃真空干燥12 h后作为正极;以金属锂片(天津中能锂业公司生产)作为对电极和负极,l mol/L LiPF6/EC+DMC(1?1)溶液为电解液,Celgard 2400为隔膜,在充满氩气的手套箱中装配成CR2025型扣式电池。采用BTS-XWJ-6.44S-00052多通道电池程控测试仪在室温下对电池进行恒流充放电测试,采取先放电后充电的原则,充放电电压范围为2.0~4.3 V或2.0~4.8 V,电流密度分别为10,25,50,125和250 mA/g。电池的循环伏安采用上海辰华CHI660A电化学工作站进行测试,扫描电压范围为2.0~4.3 V,扫描速率为0.05 mV/s。
2 结果与讨论
2.1 材料的组分分析
采用ICP元素分析方法对产物中金属离子的含量进行测试,结果为n(Na)?n(Mn)=0.629?0.938,近似为0.67?1。样品中Mn的平均价态分析如下:称取100 mg样品,溶于体积比为1?1的浓硫酸中,再加入过量的(NH4)2Fe(SO4)2?6H2O溶液,直至完全溶解,冷却至室温后,过量的(NH4)2Fe(SO4)2?6H2O用KMnO4进行滴定,结果得锰的平均价态约为z(Mn)=3.85。通过拟合得到钠锰氧化物的近似分子式:α-Na0.67MnO2.26。
2.2 材料的结构分析
图1所示为前驱体经600 ℃热处理后所得样品的XRD图谱。从图1可以看出,经600 ℃热处理的样品在2θ为15.86?,32.13?,36.47?,44.58?和65.44?出现α-Na0.7MnO2+z的(002),(004),(101),(103)和(110)衍射峰,各峰符合六方晶系特征,属于六方层状P2结构,空间群为P63/mmc,通过PowderX软件计算发现其晶胞参数为:a=2.84×10-10 m,c=1.12×10-9 m,这与Parant等[5]报道的在600 ℃以下合成的α-Na0.7MnO2+z(z≥0.05)的衍射峰相一致,只是部分峰有所宽化,这可能是晶体结构中有部分层错堆垛[13](分子中有较高的氧含量,从而产生较多的阳离子空缺)的缘故,Paulsen等[8]则称之为LT-Na2/3MnO2,他们认为该物质的衍射峰应该对应于P2结构。层状六方P2结构材料的结构示意图见图2,据文献[13]报道该材料具有棱柱形碱金属离子位,Na处在三棱柱的顶端位置,2个八面体[MnO6]夹着一个钠离子层,每两层都是镜像对称的,即ABC→CBA,它不同于一般的对称结构,结构不易发生转变,P2结构的这种稳定性有利于Li+的嵌入和脱出,因而,具有这种结构的材料在充放电过程中具有较高的容量,且结构稳定。
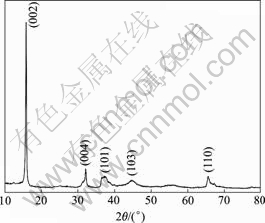
图1 样品的X射线衍射图谱
Fig.1 XRD pattern of sample
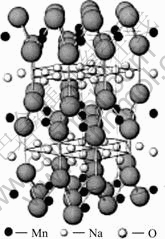
氧堆垛形式为ABBAAB…,锰处于八面体位置,
钠处于三棱柱位置
图2 层状P2结构图
Fig.2 Structures of layered P2
2.3 材料的形貌分析
图3所示为于600 ℃制备的α-Na0.67MnO2.26在不同放大倍率下的SEM像。从图3(a)可以看出,大量一次粒子聚集在一起,构成疏松多孔结构的二次粒子,且粒度分布比较均匀,虽然微粒间有一定的团聚,但颗粒细小,而且从图3(b)中可以看出,这些粒子是由多个薄片聚集在一起形成的。

放大倍率:(a) 5 000;(b) 50 000
图3 样品在不同放大倍率时的SEM像
Fig.3 SEM images of sample at different magnifies
2.4 电化学性能分析
2.4.1 电位窗口对库仑效率的影响
图4所示为样品的首次放电、充电和第2次放电曲线,图4(a)的电位窗口为2.0~4.3 V,图4(b)的电位窗口为2.0~4.8 V。首次放电是一个嵌锂过程,即Li+嵌入到MnO6层间,部分取代Na+成为支撑层状结构的骨架,图4(a)和4(b)的嵌锂量都在x=0.55 (约140 mA?h/g)左右。首次充电是一个脱锂和脱钠过程,由于Na+半径(9.5×10-11 m )比Li+的半径(7.6×10-11 m)大,它在一定程度上会阻碍Li+在MnO6层间的嵌/脱,适量Na+的脱出有利于减小锂离子在MnO6层间发生嵌/脱的阻力[6]。图4(a)中首次充电比容量为188 mA?h/g,第2次放电比容量为176 mA?h/g,对应于0.67个锂离子嵌入层间,库仑效率高达94%;而图4(b)中的首次充电比容量高达207 mA?h/g,第2次放电比容量为174 mA?h/g,对应于0.66个锂离子嵌入层间,库仑效率仅为84%。这可能是由于在充电过程中,电压范围从2.0~4.3 V变到2.0~4.8 V,电压范围拓宽,钠离子脱出量(0.3 mol左右)明显比图4(a)的(0.2 mol左右)大,过量Na+脱出,会引起部分层状结构坍塌,导致可逆容量下降[7]。
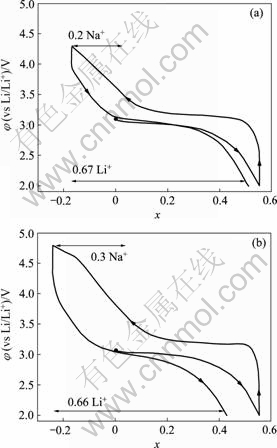
(a) 2.0~4.3 V; (b) 2.0~4.8 V
图4 样品在25 mA/g充放电电流密度下的首次放电、充电曲线和第2次放电曲线
Fig.4 First discharge―charge and second discharge profiles of sample at rate of 25 mA/g
2.4.2 电流密度对充放电过程的影响
在室温下,采用不同的电流密度对电池进行恒流充放电实验,充放电电压控制在2.0~4.3 V;由于过多Na+脱出会导致层状结构坍塌,为了保持材料结构的稳定性,必须先让Li+嵌入层状α-Na0.67MnO2.26中,部分取代Na+成为支撑层状结构的骨架,因此,对该材料采取先放电(嵌入部分锂离子)后充电(脱出部分钠离子和锂离子)的原则。从图5(a)可以看出,随着电流密度的增大,容量依次下降,在10,25,50,125和250 mA/g充放电电流密度下材料的首次放电比容量(即嵌锂量)分别为150,143,134,126和112 mA?h/g。首次充电之后,部分Na+从MnO6层间脱出来,使得锂离子在MnO6层间发生嵌/脱的阻力减小,在第2次放电时将有更多的Li+嵌入。从图5(b)可以看出,样品在电流密度为10,25和50 mA/g时,在3.0 V左右有一个非常明显的放电平台,其放电比容量在分别为180,176和168 mA?h/g;当电流密度增加到125和250 mA/g时,放电平台有所下降,放电比容量明显降低,仅为139和110 mA?h/g,这可能是在大电流密度下,电极内部极化增大引起的。
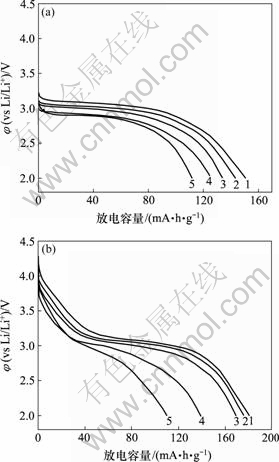
(a) 首次放电;(b) 第2次放电
电流密度/(mA?g-1): 1―10; 2―25; 3―50; 4―125; 5―250
图5 不同电流密度下样品的放电容量曲线
Fig.5 Discharge capacity plots of sample at differentcurrent density
2.4.3 材料的循环稳定性分析
图6所示为样品在不同充放电电流密度下的循环寿命曲线。可以看出,在充放电电流密度为25 mA/g时,样品的放电比容量在10次循环后下降至160 mA?h/g (为第2次放电比容量的92.5 %),之后变得平稳,30次循环后,容量稳定在150 mA?h/g左右;样品在充放电电流密度为50和125 mA/g时的循环曲线与25 mA/g的循环曲线基本一致;在充放电电流密度为250 mA/g时,循环容量稳定在105 mA?h/g左右;40次循环后,在25,50,125和250 mA/g时,其放电比容量分别为151,140,120和107 mA?h/g。比较不同放电倍率的放电性能发现,该材料具有较为优良的大电流放电性能。
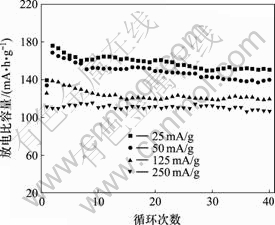
图6 样品的放电比容量―循环曲线
Fig.6 Discharge specific capacity vs. cycle number curves between 2.0-4.3 V
关于层状结构在充放电过程中的结构稳定性问题,Croguennec等[14-15]认为层状结构材料在充放电过程中会逐渐向类尖晶石结构转化。图7所示为样品在25 mA/g下进行充放电时经过2,20,30和40次循环的放电―充电曲线,可以看出,第2次放电―充电曲线仅出现3 V左右充放电平台,随着循环的进行,3 V区域的平台有所下降,并且在4.0 V左右出现一个小平台;30次循环后,充放电曲线趋于稳定。这说明层状P2结构(由于存在部分层错堆垛)在充放电过程中逐渐向类尖晶石结构转化,但是,这种类尖晶石结构相对于传统的尖晶石结构,在电化学性能上有其更好的循环稳定性。
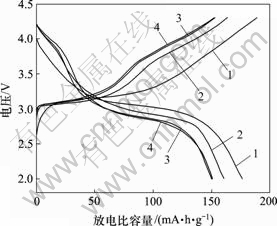
循环次数:1―2;2―20;3―30;4―40
图7 样品在25 mA/g充放电电流密度下的放电―充电循环曲线
Fig.7 Discharge―charge cycles curves of sample at rate of 25 mA/g
2.4.4 循环伏安曲线分析
图8所示为在2.0~4.3 V的电压范围内,以0.05 mV/s的扫描速度进行扫描时的循环伏安曲线。可见,随着循环的进行,在阴极过程中,在3.0 V左右的峰电位向低电位移动,10次循环后,在4.0 V左右出现1个宽峰,20次循环后,4.0 V左右的峰分裂为2个相邻的还原峰(3.9~4.2 V)。在阳极过程中,在3.2 V左右的峰电位向低电位移动;10次循环后,在4.0 V左右出现1个宽峰,20次循环后,4.0 V左右的峰分裂为2个相邻的氧化峰(3.9 V~4.2 V)。循环伏安曲线在4.0 V区域的双峰特征[16]是尖晶石结构中的阳离子相互作用的反映:当少量的Li进入晶体的八面体位置时,相邻的Li―Li之间相互作用很小,但是,随着更多的Li进入其他的八面体位置,嵌入的Li+将受到周围相邻的4个Li+的相互作用,这种相互作用导致的能量分裂使循环伏安曲线出现2个峰。循环伏安测试中所反映的阳极峰电位和阴极峰电位的峰位值与充放电循环实验相应的充放电平台电压基本相同。
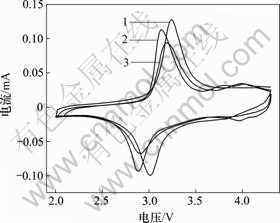
循环次数:1―2;2―20;3―10
图8 样品的循环伏安曲线
Fig.8 Cyclic voltammograms of sample
3 结 论
a. 样品是由大量一次粒子聚集在一起,构成疏松多孔结构的二次粒子,且粒度分布比较均匀,各衍射峰符合六方晶系特征,属于层状P2结构,空间群为P63/mmc。
b. 在2.0~4.3 V之间的首次充电比容量为188 mA?h/g,第2次放电比容量为176 mA?h/g,充放电库仑效率高达94 %;而在2.0~4.8 V之间的首次充电比容量高达207 mA?h/g,第2次放电比容量为174 mA?h/g,充放电库仑效率仅为84 %。
c. 在电压为2.0~4.3 V,充放电电流密度为25,50,125和250 mA/g时,在3.0 V左右都出现一个非常明显的放电平台,其第2次放电比容量分别为176,168,139和110 mA?h/g,40次循环后,其放电比容量分别为150,142,121和105 mA?h/g,显示材料有较好的循环稳定性和大电流充放电性能。
d. α-Na0.67MnO2.26材料在充放电过程中有向类尖晶石结构转变的趋势,深度循环时,结构趋于稳定。
参考文献:
[1] Tarascon J M, Kinnon W R Mc, Coowar F B, et al. Synthesis conditions and oxygen stoichiometry effects on Li insertion into the spinel LiMn2O4[J]. J Electrochem Soc, 1994, 141(6): 1421-1431.
[2] Amatucci G, Pasquier A, Blyr A, et al. The elevated temperature performance of the LiMn2O4/C system: failure and solutions[J]. Electrochim Acta, 1999, 45(1/2): 255-271.
[3] 胡传跃, 李新海, 王志兴, 等. 材料对锂离子电池热稳定性的影响料[J]. 中南大学学报: 自然科学版, 2005, 36(4): 587-593.
HU Chuan-yue, LI Xin-hai, WANG Zhi-xing, et al. Influence of materials on thermal stability of lithium-ion batteries[J]. Journal of Central South University: Science and Technology, 2005, 36(4): 587-593.
[4] Vittins G, West K. Lithium Intercalation into Layered LiMnO2[J]. J Electrochem Soc, 1997, 144(8): 2587-2592.
[5] Parant J P, Olazcuaga R, Devalette M, et al. Sur quelques nouvelles phases de formule NaxMnO2 (x≤1)[J]. J Solid State Chem, 1971, 3(1): 1-11.
[6] LeGoff P, Baffier N, Bach S, et al. Structural and electrochemical characteristics of a lamellar sodium manganese oxide synthesized via a sol-gel process[J]. Solid State Ionics, 1993, 61(4): 309-315.
[7] Bach S, Pereira-Ramos J P, Willmann P. A sodium layered manganese oxides as 3V cathode materials for secondary lithium batteries[J]. Electrochim Acta, 2006, 52(2): 504-510.
[8] Paulsen J M, Dahn J R. Studies of the layered manganese bronzes, Na2/3[Mn1-xMx]O2 with M=Co, Ni, Li, and Li2/3[Mn1-xMx]O2 prepared by ion-exchange[J]. Solid State Ionics, 1999, 126(1/2): 3-24.
[9] Robertson A D, Armstrong A R, Bruce P G. Layered LixMn1-yCoyO2 intercalation Electrodes influence of ion exchange on capacity and structure up on cycling[J]. Chem Mater, 2001, 13(7): 2380-2386.
[10] Armstrong A R, Paterson A, Robertson A J, et al. Nonstoichiometric layered LixMnyO2 with a high capacity for lithium intercalation/deintercalation[J]. Chem Mater, 2002, 14(2): 710-719.
[11] Hibino M, Kawaoka H, Zhou H, et al. Two-step addition of acetylene black to hydrated sodium manganeseoxide: its effect on the performance of rapid discharge cathode[J]. J Power Sources, 2003, 124(1): 143-147.
[12] Masayuki T, Hajime A, Yoji S. Improvedcyclability of Na-birnessite partially substituted by cobalt[J]. J Power Sources, 2002,110(1): 52-56.
[13] Paulsen J M, Thomas C L, Dahn J R. Layered Li-Mn-Oxide with the O2 structure: a cathode material for Li-ion cells which does not convert to spinel[J]. J Electrochem Soc, 1999, 146 (10): 3560-3565.
[14] Croguennec L, Deniard P, Brec R. Electrochemical cyclability of orthorhombic LiMnO2[J]. J Electrochem Soc, 1997, 144(10): 3323-3330.
[15] Jang Y I, Huang B Y, Chiang Y M, et al. Stabilization of LiMnO2 in the α-NaFeO2 structure type by LiAlO2 addition[J]. Electrochem Solid State Lett, 1998, 1(1): 13-16.
[16] 陈立宝, 贺跃辉, 汤义武. 采用固相配位法制备超细LiMn2O4正极材料[J]. 中南大学学报: 自然科学版, 2005, 36(3): 390-395.
CHEN Li-bao, HE Yue-hui, TANG Yi-wu. Preparation of ultrafine LiMn2O4 cathode materials by solid state coordination method[J]. Journal of Central South University: Science and Technology, 2005, 36(3): 390-395.
收稿日期:2008-02-19;修回日期:2008-06-04
基金项目:国家自然科学基金资助项目(20871101)
通信作者:王先友(1962-),男,湖南湘潭人,教授,从事锂离子电池及其电极材料研究;电话:0732-8293043;E-mail: wxianyou@yahoo.com