文章编号:1004-0609(2013)12-3423-07
富氢气基还原钛铁矿及其气相组分的耦合作用
肖 玮,鲁雄刚,邹星礼,李重河,丁伟中
(上海大学 上海市现代冶金与材料制备重点实验室,上海 200072)
摘 要:利用大载荷热重分析仪、质谱仪、碳分析仪、SEM和XRD测定不同还原条件下钛铁矿(FeTiO3)气基还原产物的质量损失率、钛和镁元素分布、微观结构及物相组成,研究富氢气体还原钛铁矿过程中各气体组分间的耦合作用机制。结果表明:在氢气还原过程中金属铁在颗粒外层聚集,并伴随着钛和镁两种元素的聚集形成致密层; 富氢气体还原则不形成相应的致密层,金属铁以细小颗粒状较均匀地分布在颗粒内部,钛和镁也较为均匀地分散在整个颗粒内部。此外,富氢气体中的CO能在金属铁的表面形成一定量的表面碳,并能将H2O分子重新还原为氢气,从而提高了氢气在还原过程中的利用率。
关键词:钛铁矿;镁;富氢气体;直接还原;耦合反应
中图分类号:TF823 文献标志码:A
Hydrogen-rich gas reduction of ilmenite and coupling reaction of gaseous compositions
XIAO Wei, LU Xiong-gang, ZOU Xing-li, LI Chong-he, DING Wei-zhong
(Shanghai Key Laboratory of Modern Metallurgy and Materials Processing, Shanghai University, Shanghai 200072, China)
Abstract: Thermogravimetric analyzer, mass spectrometer, carbon analyzer, SEM and XRD were utilized to study the reduction product of ilmenite (FeTiO3). The mass loss, distribution of titanium and magnesium, micromorphology and phase transitions were investigated. The coupling reaction between different components of hydrogen-rich gas was also discussed. The results show that a dense layer forms inside ilmenite particle with the beneficiation of metal iron, titanium, and magnesium in the hydrogen reduction process. Unlike the hydrogen direct reduction, the dense layer can not form in the hydrogen-rich gaseous reduction. The metal iron in the form of granule type distributes evenly in the body of the particle, and titanium and magnesium also distribute in all particles. In addition, the CO in hydrogen-rich gas can be dissociated on the surface of metal iron which plays the role of catalyst. The surface carbon which is formed by the dissociation of CO can reduce H2O molecule again, so that the utilization of hydrogen can be elevated.
Key words: ilmenite; magnesium; hydrogen-rich gas; direct reduction; coupling reaction
我国攀西地区的钛铁矿属于典型的岩矿型矿物[1-2],风化程度低,结构致密,难于还原。目前,使用的电炉熔炼―浓硫酸浸出流程三废量大[1-4],不符合我国绿色低碳的发展要求,因此,研发符合矿物特点的新型钛铁矿还原技术就成为合理利用攀枝花钛资源的关键[5-9]。从20世纪60年代起,以天然气为还原剂的铁矿石直接还原技术开始工业化生产,越来越多的研究者试图将此类气基还原技术应用于钛铁矿的直接还原过程[10-11]。LEWIS等[12]指出月球月海中蕴藏大量的钛铁矿,而这些钛铁矿被氢气还原,产物水用来电解制备氧气并得到副产物金属铁和金红石。ZHAO等[13-14]研究了800~1 100 ℃下氢气还原钛铁矿的宏观动力学及反应机理,发现氢气还原过程分为3个阶段,即诱发、加速和减速阶段。VIJAY等[15]用流化床反应器研究了钛铁矿的预氧化和氢气直接还原并指出预氧化能够明显加速氢气还原。SUN[16-17]运用Mossbauer谱对氢气还原过程进行了研究,发现经预氧化合成的钛铁矿在还原过程中的反应步骤为Fe3+→Fe2+→Fe0,也会出现一些中间产物,如Fe3O4和Fe2TiO4等。然而,大规模制氢技术的落后制约了氢气直接还原技术的发展,使其难以实现工业化。
中国是钢铁生产大国,而在钢铁的生产过程会产生大量的富氢气体。以焦化过程为例,产生的富氢煤气可达到420 m3/t,将钢铁工业产生的炉气进行重整,提高富氢还原气中氢含量并用于钛铁矿的直接还原,不仅是资源的高端利用,同时也可实现冶金工业的节能和减排[18]。
目前,多元气基直接还原钛铁矿的研究较少,特别是针对各气体组分在还原过程中耦合反应的研究则未见报道。本文作者通过热重分析研究富氢气体的组成对钛铁矿还原过程的影响,并对比氢气直接还原讨论金属铁的形成及钛、镁两种元素的分布。采用质谱仪检测还原过程中尾气成分的变化,对富氢气体中H2和CO的耦合反应进行讨论。
1 实验
1.1 实验原料
原料为攀枝花钢铁公司提供的钛铁矿,其化学组成见表1。经过XRD物相分析,其主要物相为钛铁矿(FeTiO3),其余为含铁绿泥石等脉石(见图1)。
表1 钛铁矿的主要化学成分
Table 1 Main chemical composition of ilmenite concentrate (mass fraction, %)

1.2 TG曲线
将钛铁矿试样置于大载荷热重分析仪(Cahn Ins. Inc., Thermax 700)的样品台上,密封反应器。首先通氩气作为保护性气氛,以10 ℃/min的升温速率将样品加热至设定温度,然后迅速切换至反应气体。钛铁矿样品发生还原反应,联机热重分析仪的计算机,记录样品的质量变化曲线。实验过程中,反应气体的组成及流量由质量流量计进行测量及控制,并经换算得到各气体组分的体积分数。装置如图2所示。

图1 攀枝花钛铁矿的XRD谱
Fig. 1 XRD pattern of Panzhihua ilmenite concentrate

图2 热重分析仪示意图
Fig. 2 Schematic diagram of thermogravimetric analyzer
反应结束后,快速切换至氩气排空反应室内的反应气体,并将试样取出,置于氩气气氛中冷却。采用Rigaku D/Max-2550 X射线衍射仪(XRD)对样品进行物相组成分析,采用JSM-6700F型扫描电子显微镜(SEM及BSE)观察还原产物的微观形貌,并采用X射线荧光能谱(EDS, Oxford INCA EDS system)对样品的元素分布进行分析。
1.3 还原过程中尾气成分的检测
采用质谱仪对还原过程中的尾气成分进行连续在线检测。为更加清晰地说明富氢气体中CO和H2的耦合作用,设计如下实验:首先,将固定床反应器加热到设定温度(900~1 100 ℃),将高纯CO通入固定床反应器,等待CO质谱信号平稳后,吹入高纯氩气以排空CO。然后通入高纯H2,检测H2进入反应器后质谱信号的变化。
2 结果与讨论
2.1 气体组成对还原质量损失率的影响
图3所示为恒温条件下的氢气还原TG曲线图。从图3中可以明显地看出,在反应初始阶段质量损失非常迅速。约4~6 min后,TG曲线的斜率出现明显变化,质量损失速率变慢,最终样品质量基本稳定,还原过程完成。对比不同温度(900~1 200 ℃)下的TG曲线可以发现,温度是影响还原过程的重要因素,在900~1 100 ℃范围内,随着温度的升高,质量损失率明显增加,而1 100 ℃和1 200 ℃的TG曲线差异并不明显。

图3 不同温度下氢气还原过程的TG曲线
Fig. 3 TG plots of hydrogen reduction at different temperatures
富氢气体的主要成分为H2和CO,两者均具有较高的还原活性。待热重反应室预加热至1 100 ℃后,将H2和CO按不同比例混合并通入反应室中,还原过程的TG曲线如图4所示。由图4可以看出,在1 100 ℃恒温条件下,质量损失率会随着氢气比例的增加而迅速加大,最终的质量损失率也随着氢气比例的升高而增大。当氢气体积分数等于或大于60%时,富氧气体的TG曲线和纯氢气的TG曲线非常接近。
ZHAO等[13-14]研究了氢气还原合成钛铁矿的宏观动力学行为,发现氢气还原过程分为3个阶段:诱发、加速和减速阶段。但是,在本文作者的富氢气体直接还原过程中并未观察到明显的初始诱发阶段,当热重反应器中的气体切换为氢气时,钛铁矿样品出现非常明显的瞬时质量损失,而后质量损失速率开始减小,进入扩散控速阶段,最后反应完全样品的质量不再出现明显变化。郭宇峰[4]指出,镁元素的富集会在颗粒外层形成致密的固溶体,从而对传质过程造成较大阻力。结合各温度下TG曲线的变化规律,在初始反应的4~6 min内(见图3中插图),金属铁开始形成并迅速聚集为金属壳层,钛和镁元素开始发生聚集,由于传质阻力增加,质量损失速率变慢,进入扩散控制环节。

图4 不同组成的富氢气体在1 000 ℃恒温还原钛铁矿的热重曲线
Fig. 4 TG plots of ilmenite reduced by hydrogen-rich gas with different compositions at 1 000 ℃
2.2 气体组成对还原过程物相转变的影响
图5所示为不同富氢气体组成还原钛铁矿的XRD谱。从图5的物相分析可以看出,随着氢气含量的升高,还原过程中物相转化也出现差异。当富氢气体组成为20%H2+80%CO(体积分数)时,还原产物的物相组成主要为金红石(TiO2)金属铁(Fe)及未反应的钛铁矿相(FeTiO3),而当氢气含量超过50%时,钛铁矿相的衍射峰几乎消失,同时出现大量的亚铁板钛矿相固溶体((Fe,Mg)Ti2O5),这主要是由于攀枝花钛铁矿中含有的大量杂质镁易与铁和钛形成稳定固溶体,而在此种固溶体中铁的活度较低,此时还原反应较难进行,这一分析结果对应于图3和4还原过程中20~40 min时TG曲线斜率的明显变化。

图5 1 000 ℃恒温条件下不同组成富氢气体还原钛铁矿的物相组成
Fig. 5 XRD patterns of ilmenite of hydrogen-rich gas with different compositions at 1 000 ℃
2.3 气体组成对还原产物微观形貌及钛和镁元素分布的影响
图6所示为钛铁矿于1 000 ℃恒温氢气还原200 min后矿物颗粒的微观形貌。图6(a)所示为横截面的光学照片,从图6(a)可以清楚地观察到金属铁的分布情况,在还原过程的初始阶段,钛铁矿颗粒外层被迅速还原,金属铁在这一区域快速形核并生长,靠近外层的铁向该区域发生迁移,在颗粒外层聚集并生长为金属壳层。通过对颗粒横截面的EDS扫描可以看出,在还原过程中,伴随着金属铁的形成,钛和镁也会随之向钛铁矿颗粒中发生聚集。图6(b)所示为颗粒横截面的SEM像;图6(c)和(d)所示分别为颗粒横截面的钛和镁的元素分布。图7所示为氢气还原钛铁矿过程示意图。由图7可看出,金属铁在矿物颗粒边缘聚集,而另一侧的金属铁则以细小的金属铁晶体形式存在,氢气通过致密层才能扩散至金属颗粒内部。这一现象已经被氢气直接还原球团矿所证实[10-11, 19]。结合还原产物物相分析得出,还原过程中镁元素会聚集在反应界面附近,与铁和钛等元素共同形成致密层,并对气体扩散造成阻力。
图8(a)所示为富氢气体还原后钛铁矿横截面上金属铁的分布情况。由图8(a)可见,富氢气体还原过程中铁并未在颗粒外层发生明显的聚集,金属铁呈现细小颗粒状弥散在矿物颗粒内部。通过EDS对颗粒横截面进行面扫描,图8(b)所示为钛铁矿颗粒横截面的SEM像,图8(c)和(d)分别为钛和镁元素在颗粒横截面上的分布情况, 可以看出,钛和镁并没有随着还原的进行出现明显的聚集,而是较为均匀地分散在整个颗粒内部。
2.4 气相组分的耦合作用
为了精确考察H2和CO气体组分间的耦合作用,采用质谱仪连续监测固定床反应器中尾气组分的变化。图9所示为实验过程中通入H2后CO的质谱曲线。由图9可以看出,随着H2进入反应器,CO的质谱信号重新出现,而后缓慢消失,并且CO的生成量随着反应温度的升高而减少。
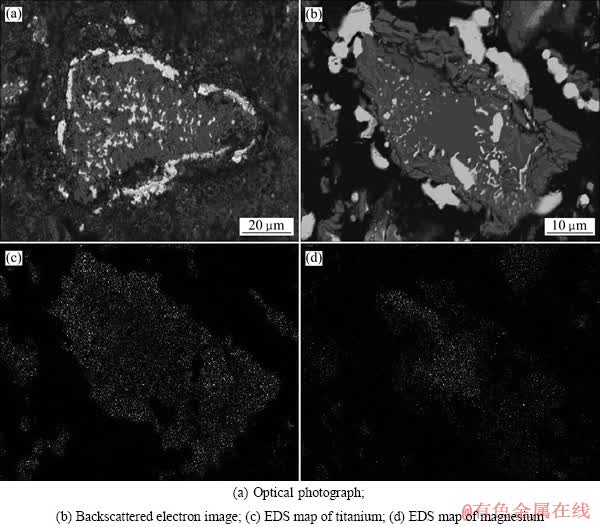
图6 氢气直接还原后矿物颗粒横断面的显微形貌及EDS元素分布
Fig. 6 Morphologies and EDS maps of cross section of ilmenite particle after hydrogen direct reduction

图7 氢气直接还原钛铁矿示意图
Fig. 7 Schematic diagram for hydrogen reduction of ilmenite
表2所列为纯氢气还原产物和富氢气体还原产物中的碳含量。由表2可知,氢气还原产物碳含量变化不明显,并且维持在非常低的水平(<0.01%,质量分数)。而富氢气体还原产物中碳元素的含量随着温度的升高而迅速降低,可见在富氢气体还原过程会出现较微量的碳沉积现象,碳沉积量随着温度的降低而增加。当温度低于800 ℃时,就会出现非常明显的积碳现象。因此,碳元素的差异可能是导致还原过程中元素分布差异的关键,CO参与反应时,可在还原产物(主要为金属铁)表面形成一定量的碳,阻止铁的聚集,使其较为弥散地分布于矿物颗粒中。

图8 富氢气体还原后颗粒横断面的形貌及元素分布
Fig. 8 Morphologies and EDS maps of cross section of ilmenite particle after hydrogen-rich gaseous reduction

图9 不同温度下尾气中CO组分变化的质谱曲线
Fig. 9 CO change curves of tail gas detected by mass spectrometer at different temperatures
表2 不同温度下还原120 min后还原产物的碳含量
Table 2 Carbon contents of reduced products at different temperatures for 12 min

在钛铁矿的还原过程中会生成具有较高催化活性的金属铁。因此,富氢气体的两种组分(H2和CO)会在金属铁表面发生耦合反应。质谱仪检测结果表明,在富氢气体还原过程中,一部分CO会发生解离,生成表面碳(C*),附着在金属铁表面。文献[20-21]中基于DFT-GGA-PBE的分子模拟也证实了在金属铁的(110)晶面上会发生CO的吸附→解离→扩散的过程。而在反吹氩气排空一氧化碳的过程中并不能将这部分表面碳除去,因此,当氢气进入反应器时,氢气的反应产物H2O与这部分能量较高的表面碳重新作用,发生水煤气反应,生成CO和氢气,反应(4)和(5)可以使产物H2O重新被还原为氢气,从而提高了整个还原过程中氢气的利用率。根据质谱检测结果,可以推断反应过程大致如下:
CO+*→CO* (1)
H2+2* 2H* (2)
2H* (2)
FeTiO3+2H*→Fe+TiO2+H2O* (3)
CO*+*→C*+O* (4)
C*+H2O*→H2+CO+2* (5)
CO*+O*→CO2+2* (6)
式中:*表示固相表面的吸附活性位置;C*、H*、CO*和H2*分别表示吸附在固相表面的C、H、CO和H2。
3 结论
1) 纯氢气能在900~1 200 ℃内快速还原钛铁矿,但在氢气还原过程中金属铁会在颗粒边缘区域聚集。与此同时,元素钛和镁也在颗粒内部聚集,形成阻碍气体传质且较为致密的壳层。
2) 富氢气体的还原速率会随着气体中氢气含量的增加而加快,当氢气体积分数达到或超过60%时,其还原速率接近纯氢气的还原速率,因此,富氢气体完全可以取代纯氢气成为一种廉价易得的气基还原剂。在富氢气体还原过程中并未观察到明显的元素聚集现象,金属铁呈细小颗粒状均匀分布在整个颗粒内部。
3) 还原生成的金属铁具有一定的催化活性,富氢气体中的氢气和CO能在金属铁的表面发生耦合反应。CO发生解离生成高活性的表面碳,这种表面碳能与还原产物H2O进一步发生水煤气反应,重新产生氢气和CO,从而提高了氢气利用率。
REFERENCES
[1] 杨绍利, 盛继孚. 钛铁矿熔炼钛渣与生铁技术[M]. 北京: 冶金工业出版社, 2006.
YANG Shao-li, SHENG Ji-fu. Slag and pig iron technology of ilmenite smelting[M]. Beijing: Metallurgical Industry Press, 2006.
[2] 王立平, 王 镐, 高 颀, 李献军, 陈战乾, 窦永庆. 我国钛资源分布和生产现状[J]. 稀有金属, 2004, 28(1): 265.
WANG Li-ping, WANG Gao, GAO Qin, LI Xian-jun, CHEN Zan-qian, DOU Yong-qing. Distribution and production status of titanium resources in China[J]. Rare Metals, 2004, 28(1): 265.
[3] 莫 畏, 邓国珠, 罗方承. 钛冶金[M]. 北京: 冶金工业出版社, 1998: 118.
MO Wei, DENG Guo-zhu, LUO Fang-cheng. Titanium metallurgy[M]. Beijing: Metallurgical Industry Press, 1988: 118.
[4] 郭宇峰. 钒钛磁铁矿固态还原强化及综合利用研究[D]. 长沙: 中南大学, 2007.
GUO Yu-feng. Study on strenthening of solid-state reduction and comprehensive utilization of vanadiferous titanomagnetite[D]. Changsha: Central South University, 2007.
[5] BECHER R, CANNINA R G, GOODHEART B A, UUSNA S. A new process for upgrading ilmenite mineral sands[C]// Proceedings of Australian IMM. Canberra, 1965: 21-44.
[6] GUO S H, LI W, PENG J H, NIU H, HUANG M Y, ZHANG L B, ZHANG S M, HUANG M. Microwave-absorbing characteristics of mixtures of different carbonaceous reducing agents and oxidized ilmenite[J]. International Journal of Mineral Process, 2009, 93(3/4): 289-293.
[7] GUO Sheng-hui, CHEN Guo, PENG Jin-hui, CHEN Jin, LI Dong-bo, LIU Li-jun. Microwave assisted grinding of ilmenite ore[J]. Transaction of Nonferrous Metals of China, 2011, 21(9): 2122-2126.
[8] CHEN G, XIONG K, PENG J H, CHEN J. Optimization of combined mechanical activation-roasting parameters of titania slag using response surface methodology[J]. Advanced Powder Technology, 2010, 21(3): 331-335.
[9] LU Xiong-gang, ZOU Xing-li, LI Chong-he, ZHONG Qing-dong, DING Wei-zhong, ZHOU Zhong-fu. Green electrochemical process solid-oxide oxygen-ion-conducting membrane (SOM): Direct extraction of Ti-Fe alloys from natural ilmenite[J]. Metallurgical and Materials Transactions B, 2012, 43(3): 503-512.
[10] PINEAU A, KANARI N, GABALLAH I. Kinetics of reduction of iron oxides by H2. Part Ⅰ: Low temperature reduction of hematite[J]. Thermochimica Acta, 2006, 447: 89-100.
[11] JOZWIAK W K, KACZMAREK E, MANIECKI T P, IGNACZAK W, MANIUKIEWICZ W. Reduction behavior of iron oxides in hydrogen and carbon monoxide atmospheres[J]. Applied Catalysis A, 2007, 326: 17-27.
[12] LEWIS J S, LEWIS R A. Space resources, breaking the bonds of earth[M]. New York: Columbia University Press, 1987: 26-37.
[13] ZHAO Y, SHADMAN F. Kinetics and mechanism of ilmenite reduction with carbon monoxide[J]. AICHE Journal, 1990, 36(9): 1433-1438.
[14] ZHAO Y, SHADMAN F. Reduction of ilmenite with hydrogen[J]. Industrial & Engineering Chemistry Research, 1991, 30(9): 2080-2087.
[15] VIJAY P L, VENUGOPALAN R, SATHIYAMOORTHY D. Preoxidation and hydrogen reduction of ilmenite in a fluidized bed reactor[J]. Metallurgical and Materials Transactions B, 1996, 27: 731-738.
[16] SUN K. Mathematical simulation on oxidation of ilmenite of ilmenite in fluidized bed[J]. Rare Metals, 1996, 15(1): 51-58.
[17] SUN K. Mossbauer spectrum study on hydrogen reduction of preoxidized ilmenite[J]. Rare Metals, 1997, 16(1): 59-62.
[18] CHENG H W, LU X G, ZHANG Y W, DING W Z. Hydrogen production by reforming of simulated hot coke oven gas over nickel catalysts promoted with lanthanum and cerium in a membrane reactor[J]. Energy Fuels, 2009, 23: 3119-3125.
[19] EL-GEASSY A A. Gaseous reduction of Fe2O3 compacts at 600 to 1 050 ℃[J]. Journal of Materials Science, 1986, 21: 3889-3900.
[20] BROMFIELD T C, FERRE D C, NIEMANTSVERDRIET J W. A DFT study of the adsorption and dissociation of CO on Fe(110): Influence of surface coverage on the nature of accessible adsorption states[J]. Chem Phys Chem, 2005, 6(2): 254-260.
[21] JIANG D E, CARTER E A. Adsorption and dissociation of CO on Fe(110) from first principles[J]. Surface Science, 2004, 570: 167-177.
(编辑 陈卫萍)
基金项目:国家自然科学基金资助项目(51074105);国家杰出青年科学基金资助项目(51225401)
收稿日期:2012-09-13;修订日期:2013-05-30
通信作者:鲁雄刚,研究员,博士;电话:021-56335768;E-mail: luxg@shu.edu.cn