文章编号:1004-0609(2012)06-1705-06
Y2Cu2O5光催化剂的制备及模拟太阳光催化产氢
孟 燕
(长安大学 环境科学与工程学院,西安 710054)
摘 要:分别用固相法和液相法制备Y2Cu2O5光催化剂,利用热重-差热分析(TG-DTA)、X射线衍射(XRD)、扫描电子显微镜(SEM)、紫外-可见光漫反射光谱(UV-Vis DRS)等技术对光催化剂进行表征。在模拟太阳光照射条件下,以草酸(H2C2O4)为牺牲剂对所制得的光催化剂制氢性能进行评价,考察制备方法和牺牲剂类型等因素对其产氢性能的影响以及光催化剂的稳定性能。结果表明:溶胶-凝胶法所得样品中含有Y2O3杂质,为Y2Cu2O5与Y2O3的混合物;固相法所得样品为纯净的Y2Cu2O5,具备较高的光催化产氢活性。用固相法制备的光催化剂Y2Cu2O5,当其用量为0.8 g/L、草酸为牺牲剂且初始浓度为0.05 mol/L时,表现出最佳光催化产氢活性,其产氢量为3.78 mmol/(h・g)。但Y2Cu2O5在草酸溶液中不稳定,会与草酸反应生成Y2(C2O4)3・2H2O,导致产氢活性降低。
关键词:Y2Cu2O5;光催化;产氢;模拟太阳光
中图分类号:O614.32 文献标志码:A
Preparation of Y2Cu2O5 photocatalyst for
H2 production under simulated sunlight irradiation
MENG Yan
(School of Environmental Engineering, Changan University, Xi’an 710054, China)
Abstract: Y2Cu2O5 photocatalyst was successfully synthesized via solid state reaction and sol-gel method, respectively. The thermogravimetry and differential thermal analysis (TG-DTA), X-ray diffraction (XRD), scanning electron microscopy (SEM) and ultraviolet visible diffuse reflectance absorption spectra (UV-Vis DRS) were employed to characterize the as-synthesized Y2Cu2O5 products. The photocatalytic H2 evolution activity of the as-obtained samples was evaluated from oxalic acid solution used as sacrificial reagent under simulated sunlight irradiation. The influences of synthesis methods and sacrificial reagent types on the photocatalytic H2 evolution activity and durability of the as-obtained photocatalyst were investigated in detail. The results show that the sample synthesized by sol-gel method is mixture of Y2Cu2O5 and Y2O3, while that synthesized by solid state reaction is pure Y2Cu2O5 photocatalyst that exhibits better photocatalytic H2 evolution activity. When the concentration of the photocatalyst synthesized by solid state reaction is 0.8 g/L, the oxalic acid is used as the sacrificial reagent, and the initial concentration is 0.05 mol/L, the highest photocatalytic H2 evolution activity (3.78 mmol/(h・g)) is obtained over the as-synthesized Y2Cu2O5 photocatalyst. But Y2Cu2O5 photocatalyst is also unstable in the oxalic acid solution, and can change into Y2(C2O4)3・2H2O, which will decrease the photocatalytic H2 evolution activity.
Key words: Y2Cu2O5; photocatalysis; H2 production; simulated sunlight irradiation
Y2Cu2O5作为高温超导材料YBa2Cu3O7-x的第二相存在,具备较好的电磁性能,是一种优良的p型半导体材料[1]。目前,对Y2Cu2O5的研究主要集中在磁性结构[2-3]、平面缺陷[1, 4]等物理性质方面。研究表明[5-6],Y2Cu2O5属正交体系,具有Cu2O5二聚链结构和YO6八面体结构,其中两个铜原子通过两个键角近90o的Cu―O―Cu键结合,Y原子位于YO6八面体的中心,两个结构相互交叉结合,形成特殊的层状结构。已有的研究表明,具有层状结构的光催化剂具有较高的光催化产氢活性,如K4Nb6O17[7]、InMO4 (M=Nb5+, Ta5+)[8]和Sr2(Ta1-xNbx)2O7[9]等。因此,具有层状结构的Y2Cu2O5,也可作为一种新的光催化剂应用于光催化制氢领域。目前,利用Y2Cu2O5作为光催化剂,在模拟太阳光条件下分解水制氢还未见报道。
本文作者以固相法高温煅烧制备Y2Cu2O5光催化剂,并用溶胶-凝胶法进行对照实验。采用TGA-DTA、XRD、SEM和UV-Vis DRS等技术对其进行表征,考察制备方法和牺牲剂的种类等因素对Y2Cu2O5光催化剂在模拟太阳光照射下光催化产氢活性的影响。
1 实验
实验所用试剂均为分析纯,在使用前并未做任何处理,实验用水为膜过滤去离子水。
1.1 光催化剂的制备
Y2Cu2O5光催化剂采用如下两种方法制备。
1) 固相法:按化学计量比准确称取一定量的 CuO和Y2O3,将两者充分混合并于玛瑙研钵中研磨30 min,然后在950 ℃下煅烧12 h(升温速率为10 ℃/min),待冷却后反复研磨。如此方法处理3次,即得Y2Cu2O5样品。
2) 溶胶-凝胶法:按化学计量比分别将Cu(NO3)2・3H2O和Y(NO3)3・6H2O溶于50 mL无水乙醇中,再在磁力搅拌下将两者混合。随后在磁力搅拌下缓慢加入一定量0.3 mol/L柠檬酸溶液,使其与金属离子络合。于80 ℃水浴下加热搅拌得到凝胶,再在120 ℃下干燥。最后于950 ℃下煅烧12 h(升温速率为10 ℃/min),冷却研磨后再次于950 ℃下煅烧12 h,待冷却后研磨即得Y2Cu2O5样品。
1.2 光催化剂的表征
样品的热分析采用热重分析仪(TGA/DTA, Perkin Elmer, TAC 7/DX)进行分析。以空气为载气,加热温度范围为25~1 000 ℃,加热速度为10 ℃ /min。
利用X射线衍射研究样品晶体结构,所用仪器为日本理学Rigaku D/max 2550 VB+ 18 kW转靶X射线衍射测定仪,工作条件为:Cu靶,石墨片滤波,管压40 kV,管流300 mA,扫描范围2θ为10°~80°。
SEM用来观察催化剂的表面形貌,采用日本JEOL JSM-5600LV扫描电镜对样品进行检测。
UV-Vis DRS直接用来测定样品对光的吸收性质。本实验采用日本100-60型紫外可见光谱仪进行测定,扫描范围200~700 nm,催化剂样品在5 MPa压力下成型,采用标准BaSO4白板为参比。
用氮吸附比表面分析仪(BET)测试样品的比表面积,采用贝士德仪器科技(北京)有限公司生产的3H-2000BET-A型全自动氮吸附比表面积测定仪对样品进行测试。
1.3 光催化剂的活性测定
光催化制氢实验在自制的三圆筒状石英光反应器中进行,并连接着气体收集装置,使用外循环水和内风双重冷却。内激发光源为150 W氙灯(常州玉宇电 光器件有限公司生产,波长范围200~1 100 nm,主波长400~700 nm,紫外光<5%,未使用滤波片滤光)。称取一定量催化剂经过超声处理后加到600 mL去离子水中,并加入一定量的牺牲剂,一起转移到反应器中,然后通氮气30 min排尽反应液中的溶解氧,反应过程中用电磁搅拌以保持悬浮状态。产生气体的量通过测量排出液体的体积来确定,用气相色谱仪(TCD, N2作载气,使用沸石NaX柱子)检测生成的气体。在排水法收集H2之前,让产生的气体通过饱和NaOH溶液以除去产生的少量杂质气体。
2 结果与讨论
2.1 光催化剂的表征结果
2.1.1 TG-DTA分析
图1所示为柠檬酸辅助溶胶-凝胶法制备的Y2Cu2O5样品前驱体的TG-DTA分析曲线。TG曲线表明,在100 ℃以内就开始有明显的质量损失,并有吸热反应发生,主要是样品前驱体中水分的挥发;在260 ℃左右的吸热峰,温度继续增加后有出现放热峰是由于合成中所用的有机物络合剂柠檬酸、硝酸盐的分解过程,这个过程从260~500 ℃,热量变化情况较为复杂,说明有多种物质在本温度段分解,质量损失约25%。从800~950 ℃热量变化情况复杂,但质量损失不大,该阶段是由于CuO与Y2O3复合为Y2Cu2O5的晶型转换过程[10]。
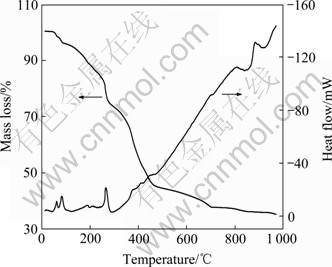
图1 样品的TG-DTA曲线
Fig. 1 TG-DTA curves of as-synthesized metal-citrate precursors
2.1.2 XRD分析
图2所示为固相法和溶胶-凝胶法制备样品经950 ℃焙烧后的XRD谱。由图2可以看出,固相法制备所得样品为较纯净的Y2Cu2O5结构,没有其它杂质相存在,属正交晶系(No.81-0703)。而溶胶-凝胶法制备所得样品中除了Y2Cu2O5外,还含有Y2O3和CuO杂质。这可能是由于在溶胶-凝胶法的制备过程中,有机物的引入影响了两种氧化物的有效接触,当焙烧温度和时间没达到最佳值时,氧化钇与氧化铜转化为铜酸钇受到影响。另外,固相法制备的Y2Cu2O5样品的衍射峰强度明显大于溶胶-凝胶法的,表明固相法制备的Y2Cu2O5样品具备更好的结晶性。通过X射线衍射数据估算,两种方法制备的样品平均单晶粒径约为40 nm。
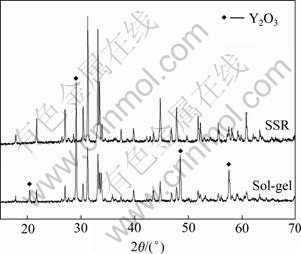
图2 Y2Cu2O5光催化剂的XRD谱
Fig. 2 XRD patterns of Y2Cu2O5 photocatalyst
2.1.3 SEM分析
图3所示为用固相和液相法制备的样品经950 ℃焙烧后的SEM像,其中图3(a)为固相法制备样品。从图3中可以看出,该法制备所得样品为不规则球状结构,颗粒大小不均匀,由于原始CuO和Y2O3粉体颗粒不均匀,经过高温煅烧后,研磨不充分而使得样品粒径不均匀,且部分团聚较严重。图3(b)所示为液相法制备样品的SEM像。可见,表观颗粒明显比固相法的大,但其结晶结构状态相对均匀,也呈现一定的团聚现象。

图3 不同方法制备样品的SEM像
Fig. 3 SEM images of samples prepared by different methods: (a) Solid state method; (b) Sol-gel method
2.1.4 UV-Vis DRS分析
图4所示为样品的UV-Vis漫反射光谱分析图。 从图4中可以看出,样品Y2Cu2O5从240 nm处到整个可见光区都有较好吸收,其反射率较小。但在500 nm处具有一个较大的反射峰,反射率近20%,显示其吸收边的存在,根据公式(1)[11]计算得其带隙能(Eg)约为 2.48 eV。
Eg=1 240/λ (1)
UV-Vis漫反射光谱是一种常用的跟踪金属及其化合物纳米粒子的电荷转移及d-d跃迁的方法,从而可以获得固体能带结构的信息。样品的光谱信息表 明,该光催化价带隙能适中,可见光响应强,只要光催化剂价、导带电位与分解水产氢电位相匹配,Y2Cu2O5
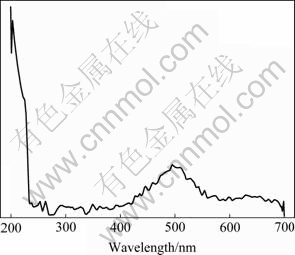
图4 样品Y2Cu2O5的UV-Vis DRS谱
Fig. 4 UV-Vis diffuse reflectance spectrum of Y2Cu2O5
就不失为一种具有研究价值的产氢光催化剂。
2.1.5 BET分析
表1所列为固相和液相法制备的样品经950℃焙烧后的比表面积、孔径和孔容量对比结果。由表1可知,固相法所获得的光催化剂的比表面积显著地大于液相法的,分别为2.150 9 m2/g和0.043 7 m2/g。但液相法获得样品孔径大于固相法样品孔径,分别为63.26和13.46 nm,说明在柠檬酸辅助溶胶-凝胶法中,由于有机物的引入,在焙烧过程中有机物的分解后会留下较大的孔径。固相法样品孔容量是液相法的10倍,说明液相法制备的样品微孔最小。数据结果表明,制备方法和焙烧温度会对样品的比表面积、孔径和孔容量均产生较大影响。
表1 样品经950 ℃焙烧后的参数
Table 1 Parameters of samples after calcined at 950 ℃

2.2 影响光催化产氢活性的因素
2.2.1 制备方法对产氢活性的影响
不同制备方法获得的光催化剂在模拟太阳光条件下的产氢活性影响如图5所示。在反应中光催化剂用量为0.8 g/L,草酸为牺牲剂,浓度为0.05 mol/L。可以看出,两种方法制备所得Y2Cu2O5样品均在反应5 h时达到最佳产氢量,固相法(SSR)制备所得样品的最佳产氢量为3.78 mmol/(h・g),高于溶胶-凝胶法(Sol-gel)制备所得样品的产氢活性(3.33 mmol/(h・g))。XRD检测结果(图2)表明,固相法制备所得为纯净的Y2Cu2O5样品,而溶胶-凝胶法制备所得样品中含有CuO和Y2O3杂质。通过UV-Vis检测结果算出,Y2Cu2O5的带隙能为2.48 eV,具有很高的可见光响应活性,而Y2O3的禁带宽度为5.6 eV[12],不具备可见光响应活性。因此,在催化剂浓度相同的情况下,由于溶胶-凝胶法所得样品中含有Y2O3,降低了活性反应物Y2Cu2O5的浓度,导致其对光的吸收减弱,从而产生的光生电子-空穴对数量减少,光催化产氢活性降低。所以本研究后面的实验所使用的Y2Cu2O5光催化剂均为固相法。
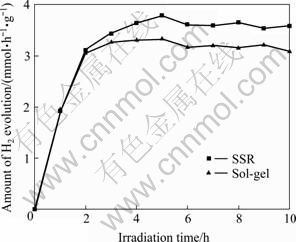
图5 制备方法对产氢活性的影响
Fig. 5 Effect of photocatalyst preparation routes on photocatalytic H2 evolution activity (Reaction condition: photocatalyst mass concentration, 0.8 g/L; initial oxalic acid concentration, 0.05 mol/L; distilled water amount, 600 mL; irradiation time, 5 h)
2.2.2 牺牲剂对产氢活性的影响
不同牺牲剂对相同光催化剂的产氢活性具有不同的影响。这里分别以KI、Na2SO3、Na2S、CH3COOH以及H2C2O4为牺牲剂,考察它们对固相法制得样品在模拟太阳光条件下产氢活性的影响,如图6所示,其中各牺牲剂浓度均为0.05 mol/L。由图6可以看出,在该光催化制氢体系里,KI作为电子供体牺牲剂不具备产氢性能;当以Na2SO3为牺牲剂时,其最佳产氢活性仅为0.06 mmol/(h・g);以Na2S、CH3COOH和H2C2O4为牺牲剂时,其最佳产氢活性分别为0.61、1.65和3.78 mmol/(h・g),即以H2C2O4为牺牲剂时,Y2Cu2O5的光催化产氢活性最高。与牺牲剂对CuO光催化剂产氢活性的影响相似[13],酸性牺牲剂更有利于Y2Cu2O5光催化产氢活性的提高。但是不论选择哪种牺牲剂,Y2Cu2O5光催化产氢活性均要高于CuO光催化剂的产氢活性[13]。因此,两种氧化物复合后能有效提高光催化产氢活性。
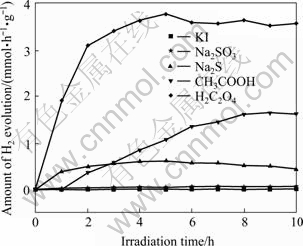
图6 不同牺牲剂对Y2Cu2O5可见光产氢活性的影响
Fig. 6 Effect of sacrificial reagent type on H2 evolution activity of as-obtained Y2Cu2O5 photocatalyst
2.2.3 Y2Cu2O5的稳定性
为了测试光催化剂产氢后循环使用情况,进行连续光催化产氢实验,每12 h为一个循环。在光照12 h后,将反应体系在黑暗处放置10 h,随后将反应产物进行超声处理,以避免反应产物在反应器壁上的粘附和自身的积聚,然后向反应体系中加入与第一次循环等量的草酸,并在黑暗中搅拌30 min,然后通入氮气30 min,再重新光照,开始下一轮产氢实验,连续进行4个循环实验。在第一个12 h的反应阶段,随着光照时间的增加,产氢速率首先不断增加,并在第6 h达到最高值,然后随着光照时间进一步延长,产氢速率有所下降。这是因为反应中存在一个活化过程,在反应开始的前几个小时,草酸的吸附达到平衡,光生电子-空穴的产生、分离及消耗也逐渐达到动态平衡,故产氢活性增加并达到最佳值及稳定状态;同时由于草酸的不断消耗,引起产氢活性有所下降。在随后的两个循环里,Y2Cu2O5的光催化产氢活性相对于第一次循环稍有降低,但基本维持在一个稳定的水平上,只是由于牺牲剂草酸的消耗导致在循环的后几个小时里产氢量有所减少。然而,当进行到第四个循环的时候,产氢活性有较为明显的下降,这是因为长时间反应后,光催化剂活降低了。为了证明这个结论,对反应前后光催化剂的XRD谱进行比较(见图7)。从图7中可以看出,反应48 h后,光催化剂为Y2Cu2O5与Y2(C2O4)3・2H2O的混合物,且Y2(C2O4)3・2H2O已成为主要物质。因此可以得出,在以H2C2O4为牺牲剂的光催化反应体系中,Y2Cu2O5光催化剂不能够稳定地存在。随着反应的进行,Y2(C2O4)3・2H2O的量将不断增加,对光催化剂的产氢活性的影响增大,导致其光催化产氢活性的降低。
虽然Y2Cu2O5光催化剂在以H2C2O4为牺牲剂的光催化反应体系中不稳定,但是其在模拟太阳光条件下的光催化产氢活性仍然远高于文献[14-15]报道的CuO或Cu掺杂复合光催化剂的光催化产氢活性,通过改变牺牲剂或对Y2Cu2O5进行修饰以增加其稳定性是本光催化剂后续研究的重点内容。
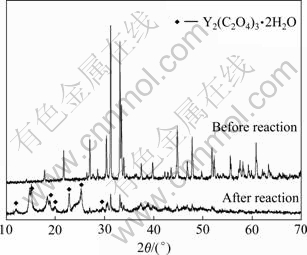
图7 反应前后Y2Cu2O5光催化剂的XRD谱
Fig. 7 XRD patterns of Y2Cu2O5 photocatalyst before and after reaction
3 结论
1) 固相法所得样品经过XRD检测证明为较纯净的Y2Cu2O5光催化剂,具备较高的光催化产氢活性;而溶胶-凝胶法所得样品中含有少量CuO和Y2O3杂质。
2) 不同牺牲剂对产氢活性有很大影响,以H2C2O4为牺牲剂时,Y2Cu2O5的光催化产氢活性最高。
3) 固相法制备的Y2Cu2O5在最佳催化剂用量和H2C2O4为0.05 mol/L时,其模拟太阳光下产氢活性为3.78 mmol/(h・g)。但长时间反应后,光催化剂会与H2C2O4反应生成Y2(C2O4)3・2H2O,导致其产氢活性降低。
REFERENCES
[1] FENG C N, LOVETT D R. The characteristics and nature of planar defects in Y2Cu2O5 and Y2-xCaxCu2O5 with x=0.05, 0.1, 0.2 and 0.4[J]. J Phys: Condens Matter, 1998, 10: 3497-3507.
[2] MATSUOKA Y, NISHIMURA Y, MITSUDO S, NOJIRI H, KOMATSU H, MOTOKAWA M, KAKURAI K, NAKAJIMA K, KARASAWA Y, NIIMURA N. Metamagnetic transition in Y2Cu2O5[J]. Journal of Magnetism and Magnetic Materials, 1998, 177/181: 729-730.
[3] BABA-KISHI K Z, CAMPS R A, THOMAS P A. Tranmission electron microscope studies of the crystal structure of Y2Cu2O5 and the nature of non-periodic planar defects in Y2Cu2O5[J]. J Phys: Condens Matter, 1990, 2: 5085-509.
[4] FAMERY R, QUEYROUX F. Crystal structure refinement of Y2Cu2O5 from single crystal X-ray diffraction data[J]. Mat Res Bull, 1989, 24(3): 275-281.
[5] GARCIA-MUNOZ J L, RODRIGUEZ-CARVAJAL J, OBRADORS X, VALLET-REG? M, GONZALEZ CALBET J, GARC?A E. Ferromagnetic layers in Y2Cu2O5: A neutron diffraction study[J]. Physics Letters A, 1990, 149(5/6): 319-327.
[6] ZOU Zhi-gang, YE Jin-hua, ARAKAWA H. Photocatalytic water splitting into H2 and/or O2 under UV and visible light irradiation with a semiconductor photocatalyst[J]. International Journal of Hydrogen Energy, 2003, 28: 663-669.
[7] SARAHAN M C, CARROLL E C, ALLENA M, LARSEN D S, BROWNING N D,OSTERLOH F E. K4Nb6O17-derived photocatalysts for hydrogen evolution from water: Nanoscrolls versus nanosheets[J]. Journal of Solid State Chemistry, 2008, 181: 1678-1683.
[8] KATO H, KUDO A. Energy structure and photocatalytic activity for water splitting of Sr2(Ta1- xNbx)2O7 solid solution[J]. Journal of Photochemistry and Photobiology A: Chemistry, 2001, 145: 129-133.
[9] HENGLEIN A. Physicochemical properties of small metal particles in solution: “Microelectrode” reactions, chemisorption, composite metal particles, and the atom-to-metal transition[J]. J Phys Chem, 1993, 97(21): 5457-5471.
[10] LOUIS W, SHEN R, EMIEL A S, DAVE H A B. Analysis of reactions during sintering of CuO-doped 3Y-TZP nano-powder composites[J]. Journal of the European Ceramic Society, 2009, 29: 2549-2557.
[11] KUDO A, MISEKI Y. Heterogeneous photocatalyst materials for water splitting[J]. Chemical Society Reviews, 2009, 38: 253-278.
[12] LI Ling. Synthesis of Y2O3 nano-powder from yttrium oxalate under ambient temperature[J]. Journal of Rare Earths, 2005, 23: 358-361.
[13] YAN Jian-hui, YAO Mao-hai, ZHANG Li, TANG You-gen, YANG Hai-hua. Photocatalytic H2 evolution activity of CuO/ZrO2 composite catalyst under simulated sunlight irradiation[J]. J Cent South Univ Technol, 2011, 18(1): 56-62.
[14] MIWA T, KANECO S, KATSUMATA H. Photocatalytic hydrogen production from aqueous methanol solution with CuO/Al2O3/TiO2 nanocomposite[J]. International Journal of Hydrogen Energy, 2010, 35: 6554-6560.
[15] ZHANG Hong-jie, CHEN Gang, LI Ying-xuan, TENG Yu-jie. Electronic structure and photocatalytic properties of copper-doped CaTiO3[J]. International Journal of Hydrogen Energy, 2010, 35: 2713-2716.
(编辑 李艳红)
收稿日期:2011-05-16;修订日期:2011-11-10
通信作者:孟 燕,讲师,硕士;电话:13991119856;E-mail: mengyan@chd.edu.cn