文章编号:1004-0609(2008)10-1920-06
12CaO?7Al2O3溶出动力学
孙会兰1,于海燕1,王 波1,苗 瑜2,涂赣峰1,毕诗文1
(1. 东北大学 材料与冶金学院,沈阳 110004;
2. 中国铝业河南分公司,郑州 450041)
摘 要:采用粒径不变的收缩未反应核模型法研究12CaO?7Al2O3溶出动力学,考察搅拌强度、溶出温度和碳碱浓度对12CaO?7Al2O3溶出性能的影响。结果表明:当搅拌速度达到600 r/min之后,不再影响Al2O3溶出率,从而消除液膜扩散对溶出过程的影响;其它条件相同的情况下溶出温度和碳碱浓度越高,溶出性能越好;在实验范围内,溶出过程符合一级反应,受表面化学反应控制,频率因子为1.089×10-5,表观活化能为27.74 kJ/mol。
关键词:12CaO?7Al2O3;动力学;溶出;活化能;未反应核模型
中图分类号:TF 111.31 文献标识码: A
Leaching dynamics of 12CaO?7Al2O3
SUN Hui-lan1, YU Hai-yan1, WANG Bo1, MIAO Yu2, TU Gan-feng1, BI Shi-wen1
(1. School of Materials and Metallurgy, Northeastern University, Shenyang 110004, China;
2. Henan Branch of China Aluminum, Zhengzhou 450041, China)
Abstract: Leaching dynamics of 12CaO?7Al2O3 was studied using shrinking unreacted core model. The effects of stirring intensity, leaching temperature and concentration of reagents were investigated. The results show that the stirring intensity doesn’t influence alumina leaching ratio when it is higher than 600 r/min; the leaching property of 12CaO?7Al2O3 is better as the temperature and concentration of sodium carbonate are higher. The leaching process is the first order reaction, and it can be described by surface chemical reaction. The frequencys factor is 1.089×10-5, and the apparent activation energy is 27.74 kJ/mol.
Key words:12CaO?7Al2O3; dynamics; leaching; apparent activation energy; unreacted core model
近年来,由于铝土矿资源的过度开采,我国可利用的铝土矿资源迅速减少,可利用铝资源范围已经开始从低品位铝土矿转向难处理矿石和非铝土矿资 源[1-3]。因此随着我国铝土矿资源的枯竭,国际铝土矿、铁矿石价格的大幅度上涨以及国内对Al2O3产品需求的不断增加,对于储量丰富和总有价成分含量较高的高铁铝土矿的开采和综合利用指日可待。
三水铝石型高铁铝土矿主要分布在我国广西贵港一带。该矿中Al2O3和氧化铁含量在正常生产工艺条件下均达不到各自的品位要求,极难利用,但总有价成分含量较高。目前,处理该矿的较为可行的方法为“烧结-高炉冶炼-提取Al2O3”工艺,即高铁矿烧结后进高炉冶炼,炉渣(有效成分12CaO?7Al2O3)用于提取Al2O3。东北大学经过十几年的研究,尽管已经基本打通了该工艺的关键性环节,然而还存在一些问题,如在提取Al2O3工艺中如何提高Al2O3溶出率和降低调整液中碳碱浓度等。由于迄今为止国内外缺乏对12CaO?7Al2O3纯体系的研究,其溶出机理尚不清楚,这就使得高铁铝土矿综合利用过程中Al2O3提取工艺的研究缺少理论依据,限制了Al2O3溶出率的进一步提高。因此,本文作者研究12CaO?7Al2O3的溶出动力学,以便找出溶出过程中的控制步骤,为高铁铝土矿的综合利用提供理论基础。此外,由于采用烧结-拜耳工艺从粉煤灰中提取Al2O3的有效成分也是12CaO?7Al2O3,因此该研究对于从粉煤灰中提取Al2O3工艺也具有一定的借鉴意义。
1 实验
1.1 实验原料
实验所用原料为由分析纯Al2O3和CaO(由Ca(OH)2煅烧得到)高温合成而得到的纯12CaO?7Al2O3,其XRD谱如图1所示。调整液由分析纯NaOH、分析纯Na2CO3和工业Al(OH)3调配而成,溶液成分为:Na2O 7 g/L,αk 1.6,Na2OC 0.97~1.94 mol/L。其中,Na2O和Na2OC分别为溶液中以氧化钠表示的苛碱浓度和碳碱浓度;αk为溶液中苛碱与Al2O3的摩尔数之比。

图1 实验原料的XRD谱
Fig.1 XRD pattern of raw material
1.2 实验方法
实验在多孔磁力搅拌器中进行,水浴加热,磨口三角瓶作为溶出容器,瓶口接有循环水冷凝。实验时先将调整液预热到设定的温度,然后加入一定量的12CaO?7Al2O3,计时溶出。到达实验时间后迅速取下冷却,并进行干过滤。用化学成分分析法分析滤液中Al2O3的含量,按下式计算溶出率:

2 结果与讨论
2.1 选择溶出动力学模型
12CaO?7Al2O3的溶出过程为其与调整液中的碳碱发生反应生成铝酸钠和碳酸钙的过程,反应方程式为[4-5]

此反应为液固反应。因反应过程中有不溶物CaCO3生成,且生成物附着在未反应核之外,因此可选择有固相生成的未反应核模型进行描述。此外,在反应过程中,颗粒总体积的变化情况与反应物、产物的密度及化学计量系数有关。已知C12A7的密度为2.7 g/cm3,CaCO3的密度为2.71 g/cm3,由此可以计算反应前后相应的粒径变化之比为0.95。可见,反应前后半径的变化很小,故在反应过程中,可将反应物的总体半径变化忽略,每个炉渣颗粒半径近似地按常数处理,因此最终选择粒径不变的收缩未反应核模型。该模型如图2所示[6-8]。
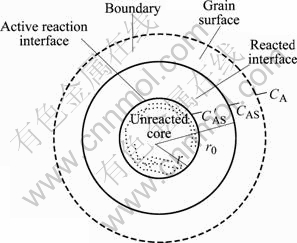
图2 生成固态产物的反应模型
Fig.2 Reactor model of solid product
反应步骤包括:1) 液态反应物或产物通过液体边界层的外扩散;2) 液态反应物或产物通过液体边界层的内扩散;3) 界面化学反应。固态反应物12CaO?7Al2O3近似按球形处理,假设界面化学反应为一级不可逆反应,液态产物的扩散速率足够快,则3个依次发生的动力学方程如下:

在准稳态的情况下,假设液态反应物的浓度保持恒定,通过积分,从上述3个方程可导出该模型包含3个控制步骤方程:表面化学反应控制、固膜内扩散控制以及二者的混合控制[9-13],它们依次为

2.2 搅拌强度对12CaO?7Al2O3溶出过程的影响
在L/S为50的条件下,以前面所说明的实验方法于75 ℃的水浴中用碳碱浓度为1.94 mol/L的铝酸钠溶液溶出12CaO?7Al2O3,溶出时间为60 min,结果如图3所示。

图3 搅拌强度对Al2O3溶出率的影响
Fig.3 Effect of stirring intensity on alumina leaching rate
由图3可以看出,在搅拌速度小于600 r/min时,Al2O3的溶出率随着搅拌速度的增加而快速增加;在转速大于600 r/min时,提高转速则Al2O3溶出率基本不再发生变化,搅拌速度对溶出率已无影响。这说明已经消除了液膜扩散对反应的影响,搅拌作为一个变量可以被忽略。然而扩散作为速率控制步骤是不能被消除的[7],所以此时反应进入了动力学区,溶出过程只可能受化学反应控制(式(6))、固膜内扩散控制(式(7))或二者的混合控制(式(8))。
2.3 温度对12CaO?7Al2O3溶出过程的影响
研究温度对12CaO?7Al2O3溶出过程的影响时,实验条件为:碳碱浓度1.94 mol/L、搅拌速度600 r/min、溶出温度50~80 ℃。实验发现,在同一溶出温度下,随着溶出时间的增加,Al2O3溶出率逐渐增加;同一溶出时间下,温度越高Al2O3溶出率也越高(表1)。
表1 不同溶出温度和溶出时间下Al2O3溶出率
Table 1 Alumina leaching ratio at different temperatures and times

将实验结果用尝试法代入收缩未反应核模型的表面化学控制方程和固膜内扩散方程(式(6)~(7))可知,在溶出过程中反应时间t与1-(1-x)1/3呈线性关系(图4),与1-2x/3-(1-x)2/3不呈线性关系(图5),符合表面化学反应控制模型。

图4 反应时间内1-(1-x)1/3与浸出时间的关系
Fig.4 Relationship between 1-(1- x)1/3 and leaching time
式(8)可以看作是式(6)和(7)分别除以某一常数之后的组合,图5说明t不与1-2x/3-(1-x)2/3呈线性关系,因此t必不与
 呈线性关系。此外根据表1中的实验数据,用最小二乘法求解Ke和Ki无解,这也说明实验过程不符合混合控制。因此,溶出反应受表面化学反应控制。
呈线性关系。此外根据表1中的实验数据,用最小二乘法求解Ke和Ki无解,这也说明实验过程不符合混合控制。因此,溶出反应受表面化学反应控制。

图5 反应时间内1-2x/3-(1-x)2/3与浸出时间的关系
Fig.5 Relationship between 1-2x/3-(1-x)2/3 and leaching time
2.4 碳碱浓度对12CaO?7Al2O3溶出过程的影响
碳碱浓度对12CaO?7Al2O3溶出过程的影响实验条件为:溶出温度85 ℃,搅拌速度600 r/min,碳碱浓度分别为0.97、1.29、1.61、1.94 mol/L。实验结果表明,在同一溶出时间下Al2O3的溶出率随着碳碱浓度的增大而增大,在同一碳碱浓度下Al2O3的溶出率随着溶出时间的增加而增加。将实验结果用表面化学反应模型进行处理,如图6所示。

图6 不同碳碱浓度下的浸出动力学曲线
Fig.6 Leaching dynamics curves of different concentrations of sodium carbonate
根据不同浓度下的动力学曲线可知,图6中各条直线的斜率即为相应浓度下的反应速度v。由于v=k・CAbn,对公式两边取对数,并用lg v对lg CAb作图得图7。
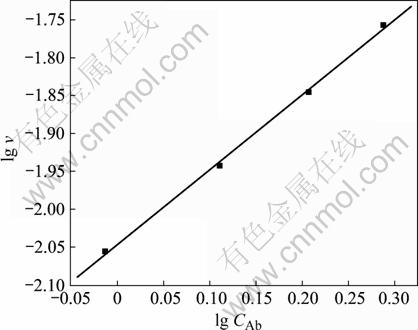
图7 lg v和lg CAb的关系
Fig.7 Relationship between lg v and lg CAb
对图7中直线经线性回归得到的直线斜率 0.990 6,这说明12CaO?7Al2O3溶出过程的反应为一级反应。
2.5 建立宏观动力学方程
根据Arrhenius公式[8] 两边取对数可得,lg K=lg A-Ealg(e/RT)。式中:A为频率因子,Ea为表观活化能,R为摩尔气体常数,T为热力学温度。由图4可以求得不同温度下浸出反应的速率常数Ke,并根据Ke=bKrCAb/(aρr0)计算Kr,结果如表2所列。用lg Kr―1/T作图,见图8:
两边取对数可得,lg K=lg A-Ealg(e/RT)。式中:A为频率因子,Ea为表观活化能,R为摩尔气体常数,T为热力学温度。由图4可以求得不同温度下浸出反应的速率常数Ke,并根据Ke=bKrCAb/(aρr0)计算Kr,结果如表2所列。用lg Kr―1/T作图,见图8:

图8 溶出时间内lg Kr与1/T的关系
Fig.8 Relationship between lg Kr and 1/T during leaching
表2 不同温度下浸出反应的速率常数
Table 2 Rate constant at different temperatures
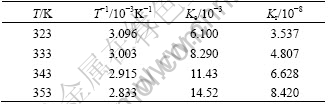
由图8可得直线的斜率为-1.449×103,截距为-4.963。计算得:Ea=27.74 kJ/mol,A=1.089×10-5。
将以上所得的活化能数据和其它参数代入Arrhenius公式和表面化学反应控制方程可得宏观动力学方程具体表达式为 1- (1-x)1/3=[1.878×10-2exp(-3.334×103/T)]t
2.6 优化溶出过程
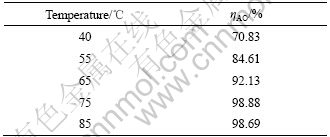
由于溶出过程受表面化学反应控制,温度对溶出过程的影响较大[8],因此提高溶出温度可以优化溶出过程。表3列出在碳碱浓度为1.94 mol/L、液固比为10、溶出时间120 min的条件下,不同溶出温度下的Al2O3溶出率。可以看出,提高反应温度可以大大强化溶出过程。
表3 不同溶出温度下的Al2O3溶出率
Table 3 Aliumina leaching ratio under different temperature
3 结论
1) 搅拌速度对12CaO?7Al2O3的溶出性能影响不大,特别是当转速达到600 r/min之后不再影响Al2O3溶出率,可以消除液膜扩散对溶出过程的影响。
2) 在本实验条件下,溶出温度和碳碱浓度对溶出过程有一定的影响。一般说来在其它条件相同的情况下溶出温度和碳碱越高,溶出性能越好。
3) 在本研究范围之内,12CaO?7Al2O3的溶出过程的反应级数为0.990 6,为一级反应。反应的表观活化能为27.74 kJ/mol,宏观动力学方程为1-(1-x)1/3= [1.878×10-2exp(-3.334×103/T)]t。
REFERENCES
[1] 吴荣庆. 我国矿产资源总体形式及主要短缺矿产的发展趋势[J]. 中国通报, 2006(42): 5-11.
WU Rong-qing. The general form of mineral resources and the development trend of mainly shortage of mineral in China[J]. China Bulletin, 2006(42): 5-11.
[2] 郭鉴镜. 谁来保证国内铝土矿供应[J]. 中国通报, 2006(42): 2-5.
GUO Jian-jing. Who can guarantee Bauxite supply in China[J]. China Bulletin, 2006(42): 2-5.
[3] 谢 群. “十五” 有色金属进出口贸易[J]. 中国有色金属, 2006(10): 60-61.
XIE Qun. The import and export trade of nonferrous metals in the Tenth “Five-year”[J]. China Nonferrous Metals, 2006(10): 60-61.
[4] 杨重愚. Al2O3生产工艺学[M]. 北京: 冶金工业出版社, 1993: 200-210.
YANG Zhong-yu. The process of alumina producing[M]. Beijing: Metallurgical Industry Press, 1993: 200-210.
[5] 毕诗文, 杨毅宏, 李殷泰, 张敬东, 段振瀛. 从高炉铝酸钙渣提取Al2O3的研究[J]. 轻金属, 1992(6): 10-15.
BI Shi-wen, YANGH Yi-hong, LI Yin-tan, ZHANG Jing-dong, DUAN Zhen-ying. Study on alumina leaching from calcium aluminate slag[J]. Light Metals, 1992(6): 10-15.
[6] 莫鼎成. 冶金动力学[M]. 长沙: 中南工业大学出版社, 1987: 93-93.
MO Ding-cheng. Metallurgy kinetics[M]. Changsha: Central South University of Technology Press, 1987: 93-93.
[7] SOHN H, WADSWORTH M E. 提取冶金速率方程[M]. 郑蒂基译. 北京: 冶金工业出版社, 1984: 1-50.
SOHN H, WADSWORTH M E. Rate equation of extractive metallurgy[M]. ZHENG Di-ji transl. Beijing: Metallurgical Industry Press, 1984: 1-50.
[8] 华一新. 冶金过程动力学导论[M]. 北京: 冶金工业出版社, 2004: 188-198.
HUA Yi-xin. Introduction of metallurgy kinetics[M]. Beijing: Metallurgical Industry Press, 2004: 188-198.
[9] 张荣良, 唐淑贞, 佘媛媛, 丘克强, 胡汉祥. HCl-NaCl浸出铅锑合金氧化吹炼渣过程中锑的浸出动力学[J]. 过程工程学报, 2006, 6(4): 544-547.
ZHANG Rong-liang, TANG Shu-zhen, SHE Yuan-yuan, QIU Ke-qiang, HU Han-xiang. Kinetics of antimony leaching from oxidizing-converting slag of Pb-Sb alloy by HCl-NaCl[J]. The Chinese Journal of Process Engineering, 2006, 6(4): 544-547.
[10] 盛灿文, 柴立元, 王云燕, 李 雄, 汪 莉. 铬渣中六价铬水浸动力学研究[J]. 安全与环境工程, 2006(3): 40-44.
SHENG Can-wen, CHAI Li-yuan, WANG Yun-yan, LI Xiong, WANG Li. Study on leaching kinetics of Cr(VI) from Chromium 2 containing slag[J]. Safety and Environmental Engineering, 2006, 13(3): 40-44.
[11] AYDO?AN S, ARAS A, U?AR G, ERDEMO?LU M. Dissolution kinetics of galena in acetic acid solutions with hydrogen peroxide[J]. Hydrometallurgy, 2007, 89(3/4): 189-195.
[12] LI Jin-shan, MILLER J D. Reaction kinetics of gold dissolution in acid thiourea solution using ferric sulfate as oxidant[J]. Hydrometallurgy, 2007, 89(3/4): 279-288.
[13] SOUZA A D, PINA P S, LIMA E V O, SILVAAND C A, LE?O V A. Kinetics of sulphuric acid leaching of a zinc silicate calcine[J]. Hydrometallurgy, 2007, 89(3/4): 337-345.
[14] 佟志芳, 毕诗文, 于海燕, 吴玉胜. 微波作用下铝酸钙炉渣非等温浸出动力学[J]. 中国有色金属学报, 2006, 16(2): 357-362.
Tong Zhi-fang, BI Shi-wen, YU Hai-yan, WU Yu-sheng. Leaching kinetics of norr-constant temperature process of calcium aluminate slag under microwave radiation[J]. The Chinese Journal of Nonferrous Metals, 2006, 16(2): 357-362.
[15] 周秋生, 齐天贵, 彭志宏, 刘桂华, 李小斌. 熟料烧结过程中氧化铁反应行为的热力学分析[J]. 中国有色金属学报, 2007, 17(6): 973-978.
ZHOU Qiu-sheng, QI Tian-gui, PENG Zhi-hong, LIU Gui-hua, LI Xiao-bin. Thermodynamics of reaction behavior of ferric oxide during sinter-preparing process[J]. The Chinese Journal of Nonferrous Metals, 2007, 17(6): 973-978.
基金项目:国家自然科学基金资助项目(50674028);中国铝业股份有限公司资助项目(CHALCO-2007-KJ-03)
收稿日期:2008-03-07;修订日期:2008-06-23
通讯作者:于海燕,副教授,博士;电话:024-83686460;E-mail:haiyan024@yahoo.com.cn
(编辑 陈爱华)