文章编号:1004-0609(2009)12-2237-06
阴离子对嗜酸氧化亚铁硫杆菌生长和硫氧化活性的影响
张成桂,张 倩,王 晶,张瑞永,何 环,夏金兰,邱冠周
(中南大学 资源加工与生物工程学院 生物冶金教育部重点实验室,长沙 410083)
摘 要:以嗜酸氧化亚铁硫杆菌(Acidithiobacillus ferrooxidans, ATCC23270)为对象,研究几种阴离子(NO3-、SO42-、Cl-和PO43-)钾盐对Acidithiobacillus ferrooxidans生长和硫氧化活性的影响。结果表明:不同阴离子对Acidithiobacillus ferrooxidans硫氧化表观活性的影响效应不同,其影响由大到小的顺序依次为Cl-,NO3-,SO42-和PO43-;在高浓度PO43-的胁迫(300 mmol/L)下,细菌所表达蛋白质相对与正常生长情况下的细菌蛋白质的总数量相对减少,质这可可能是正常生长的细菌中一些表达的蛋白质在胁迫条件下收到抑制,同时但在胁迫条件下细菌能表达一些特异性蛋白来调整和适应对无机阴离子胁迫效应。
关键词:嗜酸氧化亚铁硫杆菌;阴离子;胁迫效应
中图分类号:TF18 文献标识码: A
Effect of anions on growth and oxidation activity of Elemental Sulfur by
Acidithiobacillus ferrooxidans
ZHANG Cheng-gui, ZHANG Qian, WANG Jing, ZHANG Rui-yong, HE Huan, XIA Jin-lan, QIU Guan-zhou
(Key Laboratory of Biometallurgy, Ministry of Education, School of Minerals Processing and Bioengineering,
Central South University, Changsha 410083, China)
Abstract: The effects of NO3-, SO42-, Cl- and PO43- on the growth of Acidithiobacillus ferrooxidans and sulfur oxidation activity were investigated. The results show that the anions have different effects on the sulfur oxidation activity, and the inhibition effect sequence from great to little is Cl-, NO3-, SO42-, PO43-. The total proteins of Acidithiobacillus ferrooxidans grown under PO43- threateningthreatening condition (300 mmol/L) are down-regulated, but specific proteins are observed, when compared with normal condition. These specific proteins may take part in the response to the stress effect of anions.
Key words: Acidithiobacillus ferrooxidans; anion; threatening effect
硫化矿分解时产生大量的元素硫和其它含硫化合物,它们经嗜酸硫氧化细菌(包括Acidithiobacillus ferrooxidans)氧化为终产物硫酸。这个过程十分复杂,受各种因素,包括物理、化学和生物因素的影响。Acidithiobacillus ferrooxidans以氧化亚铁离子、元素硫或含还原态硫化合物获得能量而生长嗜酸硫氧化细菌之一,是重要的生物浸出功能菌[1-2]。Acidithiobacillus ferrooxidans生存在极端酸性环境下,属自养革兰氏阴性细菌,最适生长温度为30 ℃左右。其中在一定物理化学条件下,如:在一定的温度、大气压、营养离子和实验菌种的条件下,则Acidithiobacillus ferrooxidans生物硫氧化过程受环境中各种阳离子和阴离子的影响[3-5] 。已有的研究表明,Acidithiobacillus ferrooxidans的硫氧化活性也能被金属离子抑制,相对于Acidithiobacillus ferrooxidans在亚铁氧化过程中的金属离子相互竞争性抑制来说,其机理可能更为复杂,二价金属离子如Mg2+、Zn2+和Cu2+在高浓度时相对于同浓度K+和Na+来说,抑制硫氧化的效果更为显著[4]。TAKEUCHI和SUZUKI[5]研究发现,在不同pH的酸性条件下,嗜酸氧化硫硫杆菌(Acidithiobacillus thiooxidans)的硫氧化活性不同。在研究阳离子对Acidithiobacillus ferrooxidans生长活性的影响时,往往忽略阴离子的影响。因此,有必要了解环境中的各种阴离子对Acidithiobacillus ferrooxidans的生长和硫氧化表观活性影响的一般性规律。
本文作者以嗜酸硫氧化细菌中的模式菌株Acidithiobacillus ferrooxidans ATCC 23270 为研究对象,以细菌生长过程中的一些实时参数如:生长曲线、溶液pH值变化,来反映环境中----典型的阴离子(NO3-、SO42-、Cl- 和PO43-)浓度逐渐增加时对Acidithiobacillus ferrooxidans硫氧化表观活性影响的一般性规律,为获得浸矿细菌的最优生长和硫氧化条件提供依据。
1 实验
1.1 菌株、培养基和培养条件
Acidithiobacillus ferrooxidans ATCC 23270来源于美国模式菌种收集中心,使用9K培养基进行液体培养,对菌种进行活化和传代,在含5.0 g/L元素硫的9K培养基中,成分分别为:(NH4)2S04, 3.0 g/L; MgSO4?7H2O, 0.5 g/L; KCL, 0.1 g/L;K2HPO4, 0.5 g/L和Ca (NO3)2, 0.01 g/L。培养液初始pH值用5 mol/L的H2SO4调整至2.5。
加入不同浓度梯度的各种阴离子(NO3-、SO42-、Cl-和PO43-)钾盐,设置重复3组,细菌用250 mL锥形瓶于30 ℃摇床中以180 r/min振荡培养。
1.2 细菌在不同浓度阴离子溶液中生长行为的观察
用Olympus 生物显微镜(CX-31)通过血球计数板直接计数的方法测定细菌的浓度来比较分析Acidithiobacillus ferrooxidans在不同浓度阴离子溶液中生长呈现的生长曲线。溶液pH值的变化用上海雷磁 pHS-3C pH计测量,间接推测细菌的硫氧化活性。
1.3 Acidithiobacillus ferrooxidans细胞总蛋白质的提取及双向电泳展示
将对数生长期细菌收集后分成两份,一份转入300 mmol/L的磷酸盐环境中静置72 h,一份作为对照。将收集的细菌样品放入预冷的玻璃匀浆管中,加入5倍体积的预冷样品裂解液,套入预冷的匀浆头后,以2 400 r/min的速度将细菌裂解约15 min,然后室温在放置2 h,于4 ℃下16 000 r/min离心40 min后,收集上清液部分冷冻干燥,即为细菌可提取的可溶性总蛋白质。样品经第一向固相pH梯度等电聚焦和第二向SDS-PAGE电泳后进行考马斯亮蓝G-250染料染色。利用Uniscan scanner (清华紫光)扫描仪和2-D Imagemaster 7.2专业分析软件(GE)对着色凝胶图像进行分析,得到凝胶图谱。
2 结果与讨论
2.1 不同浓度NO3-对Acidithiobacillus ferrooxidans生长和硫氧化的影响
在本实验中,低浓度NO3-(10 mmol/L)能延缓细菌的生长速度,在NO3-大于 50 mmol/时对Acidithiobacillus ferrooxidans的生长和硫氧化活性有强烈的抑制作用,其结果如图1所示。有报道1 mmol/L的NO3-就能完全抑制Acidithiobacillus ferrooxidans对亚铁的氧化,NO3-在超过94 mmol/L时能导致细菌死亡;在单质硫中传代生长的Acidithiobacillus ferrooxidans SM-4 能承受100 mmol/L的硝酸根离子[6-7],这些结果和本实验结果相差较大,可能是不同菌株对NO3-的耐受程度不同。也有研究报道,在不同的pH环境中,同一Acidithiobacillus ferrooxidans菌株能耐受的NO3-浓度也不同[7]。但总的趋势是较低浓度的NO3-能抑制细菌的生长,甚至使细菌逐渐死亡。
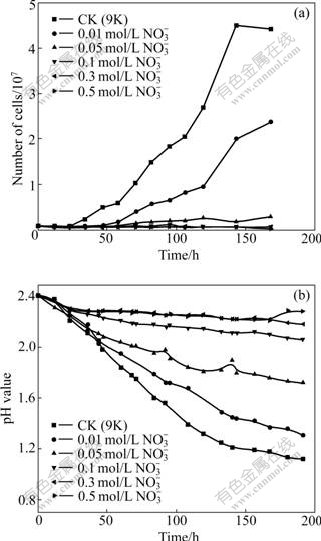
图1 Acidithiobacillus ferrooxidans在含不同浓度NO3-的9K+S培养基中的生长曲线及pH值变化曲线
Fig.1 Growth curves of Acidithiobacillus ferrooxidans and change curves of pH values during cultivation in 9 K medium with different concentrations of NO3-
2.2 不同浓度Cl-对Acidithiobacillus ferrooxidans生长和硫氧化的影响
Acidithiobacillus ferrooxidans在含不同浓度C l-的9K+S培养基中的生长曲线及pH值变化曲线如图2所示。由图2可知,浓度为10 mmol/L的Cl-能就显著延缓细菌的生长,硫氧化活性相对正常生长情况显著降低;当Cl-浓度为50 mmol/L时,细菌在数量上和细菌生活环境的pH值都不再发生变化,表明相对较低浓度的Cl-能成为Acidithiobacillus ferrooxidans生长和硫氧化的抑制剂。研究表明,Cl-对细菌的毒害主要是铁依赖性的细胞色素c有强烈的抑制作用,阻碍电子通过铁依赖性的细胞色素c的传递[7]。

图2 Acidithiobacillus ferrooxidans在含不同浓度Cl-的9K+S培养基中的生长曲线以及pH值变化曲线
Fig.2 Growth curves of Acidithiobacillus ferrooxidans (a) and change curves of pH values (b) during cultivation in 9K medium with different concentrations of Cl-
2.3 不同浓度SO42-对Acidithiobacillus ferrooxidans生长和硫氧化的影响
SO42-是嗜酸氧化亚铁硫杆菌的代谢产物之一,相对Cl-和NO3-来说,细菌能够承受较高浓度的SO42-,(见图3)。由图3可知,SO42-浓度在100 mmol/L时,对细菌的生长起到延缓效应;在SO42-浓度大于300 mmol/L时,完全抑制细菌的生长。通常在酸性矿水或含硫温泉中都含有较高浓度的SO42-,初始研究认为SO42-介导细菌对亚铁离子的氧化利用[6, 8]。FRYI等[9]研究报道,在依赖氧气的电子传递连中,SO42-负责从铁硫族到铜蓝蛋白中的铜原子的电子转运,在铁、铜蓝蛋白氧化还原酶的体外酶活性实验中发现,铜蓝蛋白只有在硫酸根离子存在时才能被亚铁离子还原。

图3 Acidithiobacillus ferrooxidans在含不同浓度SO42-的9K+S培养基中的生长曲线以及pH值变化曲线
Fig.3 Growth curves of Acidithiobacillus ferrooxidans and change curves of pH values during cultivation in 9K medium with different concentrations of SO42-
2.4 不同浓度PO43-对Acidithiobacillus ferrooxidans生长和硫氧化的影响
考察PO43-对Acidithiobacillus ferrooxidans的生长和硫氧化活性的影响结果如图4所示。由图4可知,50和100 mmol/L的PO43-都能促进细菌的生长,提高细胞分裂速度,细菌生长平稳期的细菌浓度显著大于正常生长情况下的细菌浓度。相对于Cl-和NO3-来说,高浓度(大于300 mmol/L)的磷酸盐抑制细菌的生长。磷是细菌体内核酸、磷脂和ATP 的重要组成成分,是细胞的结构物质,参与高能化合物如ATP和ADP的形成,在能量积累和转换过程中发挥作用,能够活化体内蛋白质,调控细菌体的整个代谢过程,在体内信号转导和生理代谢等方面扮演十分重要的角色。在细菌生活在磷酸盐饥饿的情况下时,细菌易形成纺锤体状阻碍细菌分裂。研究发现,Acidithiobacillus ferrooxidans在磷酸盐饥饿状况下,体内至少有25种蛋白质的表达水平发生变化,这说明在Acidithiobacillus ferrooxidans体内可能存在有磷酸盐饥饿的预警应对系统[10-11]。

图4 Acidithiobacillus ferrooxidans在含不同浓度PO43-的9K+S培养基中的生长曲线以及pH值变化曲线
Fig.4 Growth curves of Acidithiobacillus ferrooxidans and change curves of pH values during cultivation in 9K medium with different concentrations of PO43-
从典型阴离子(NO3-、SO42-、Cl-和PO43-)对Acidithiobacillus ferrooxidans硫氧化表观活性影响实验可知,不同阴离子在各个不同浓度情况下,对Acidithiobacillus ferrooxidans硫氧化表观活性影响效应不同,其影响由大到小的顺序依次为:Cl-、NO3-、SO42-和PO43-。50 mmol/L 的NO3-和Cl-能完全抑制细菌的生长,100 mmol/L的SO42-延缓细菌的生长,100 mmol/L的PO43-能促进细菌的生长,但300 mmol/L的PO43-延缓细菌的生长。环境中高浓度阴离子延缓和抑制细菌生长的原因可能是环境中高浓度阴离子改变细菌细胞的渗透势。当外界渗透压改变时,微生物胞内的水活度及各种组分的浓度会发生相应的变化,细胞体积也会缩小或膨胀,导致胞内各种生理代谢活度紊乱,从而引起细菌生长活性降低或逐渐死亡[10]。细菌自身也在长期进化过程中形成了适应渗透压变化的机制,这种机制需要细菌在胁迫环境中进行相当数量的生理反应来保证调节和代谢功能的正常进行[11]。
2.5 PO43-胁迫环境对Acidithiobacillus ferrooxidans总蛋白表达的影响
本实验中选取以PO43-为代表的阴离子,来了解阴离子胁迫环境对Acidithiobacillus ferrooxidans的总蛋白表达的影响,其结果如图4所示。由图4可知,300 mmol/L的PO43-延缓Acidithiobacillus ferrooxidans的生长(将该环境中存在6 d的细菌接种到新鲜培养基中,细菌能恢复生长繁殖),推测细菌在这种胁迫的环境中,是尽可能减小生理代谢活动,转变为细胞本底的代谢活动。比较处于胁迫和正常生长的Acidithiobacillus ferrooxidans的蛋白质表达差异,有助于直接了解细菌对环境胁迫的适应变化,和可能发现与硫氧化相关的硫氧化酶系。图6所示为PO43-胁迫环境72 h后和正常培养Acidithiobacillus ferrooxidans的总蛋白表达差异展示。
已有的研究报道,在磷饥饿的环境下生长的细菌体内有独特的适应应对体系,表现在细菌体内一些特异性的蛋白质表达明显增加,多种基因开始表达或增强表达,包括高亲和力磷转运子、有机酸的分泌等相关基因[12-14]。目前,利用基因转录谱的差异来研究 微生物对环境胁迫的应答反应对是十分有效的研究手 段[11, 15-16]。但从细菌应答反应到细菌维持本底的代谢活动,最终体现为蛋白质效应,即细菌体内一些蛋白质的表达收到抑制或/和应急蛋白质产生[17-18]。在本实验中,如图5和6所示,PO43-胁迫环境和正常培养Acidithiobacillus ferrooxidans的总蛋白表达电泳展示结果表明,正常生长的细菌体内蛋白质表达数量相对较多(见图6(b)),相对在高磷胁下的蛋白展示中相对缺失的蛋白质斑点,推测这些蛋白质可能是正常生长情况下主要参与生理生化反应的酶(包括硫氧化系统中的一些关键酶系)。相对于正常生长的细菌蛋白质展示谱,在高磷胁迫后的特异性蛋白质,可能是参与细菌对无机离子的反应,参与细胞的渗透调节,应对环境胁迫而产生的特异性的蛋白质,达到细菌调整和适应对无机阴离子胁迫效应。以PO43-为代表的阴离子对Acidithiobacillus ferrooxidans生长和硫氧化表观活性影响,以及Acidithiobacillus ferrooxidans对PO43-胁迫环境和正常培养下的差异斑点的具体功能的解析,将有助于更好地了解浸矿细菌的特性,为细菌的最佳生长条件提供依据。

图5 PO43-胁迫环境下和正常培养Acidithiobacillus ferrooxidans的总蛋白表达差异谱展示
Fig.5 Electrophoresis patterns of total protein of Acidithiobacillus ferrooxidans under PO43- threatening condition (a) and normal condition (b)
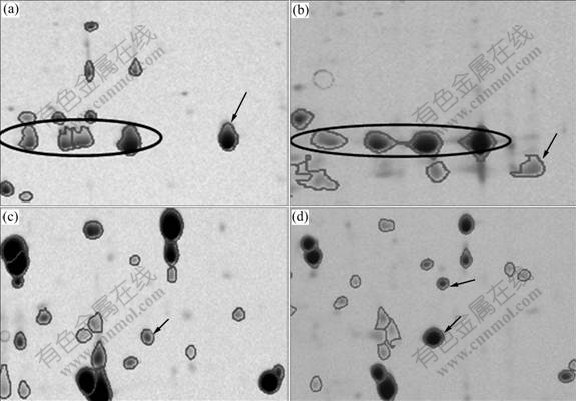
图6 PO43-胁迫环境下和正常培养Acidithiobacillus ferrooxidans总蛋白中表达差异斑点
Fig.6 Differential expressed total protein spots of Acidithiobacillus ferrooxidans under PO43- threatening condition ((a), (c)) and normal condition ((b), (d))
3 结论
1) Acidithiobacillus ferrooxidans-,-,-, -。)高浓度的阴离子抑制Acidithiobacillus ferrooxidans的生长, 100 mmol/L的SO42--延缓细菌的生长,50 mmol/L 的NO3-和Cl-能完全抑制细菌的生长,100 mmol/L的PO43-能促进细菌的生长,但300 mmol/L的PO43-延缓细菌的生长。。)在高浓度PO43-胁迫下细菌表达蛋白的总数量相对减少,但同时表达一些特异性蛋白来调整和适应对无机阴离子胁迫效应。
REFERENCES
[1] RAM?REZ P, GUILIANI N, VALENZUELA L, BEARD S, JEREZ C A. Differential protein expression during growth of Acidithiobacillus ferrooxidans on ferrous iron, sulfur compounds or metal sulfides[J]. Applied and Environmental Microbiology, 2004, 70(8): 4491-4498.
[2] ROHWERDER T, GEHRKE T, KINZLER K, SAND W. Bioleaching review part A: Progress in bioleaching: fundamentals and mechanisms of bacterial metal sulfide oxidation[J]. Applied and Environmental Microbiology, 2003, 63(3): 239-248.
[3] FANG D, ZHOU L X. Effect of sludge dissolved organic matter on oxidation of ferrous iron and sulfur by Acidithiobacillus ferrooxidans and Acidithiobacillus thiooxidans[J]. Water, Air & Soil Pollution, 2006, 171(1): 81-94.
[4] SUZUKI I, LEE D, MACKAY B, HARAHUC L, OH J K. Effect of various ions, pH, and osmotic pressure on oxidation of elemental sulfur by Thiobacillus thiooxidans[J]. Applied and Environmental Microbiology, 1999, 65(11): 5163-5168.
[5] TAKEUCHI TL, SUZUKI I. Cell hydrophobicity and sulfur adhesion of Thiobacillus thiooxidans[J]. Applied and Environmental Microbiology, 1997, 63(5): 2058-2061.
[6] LAZAROFF N. The specificity of the anionic requirements for iron oxidation by Thiobacillus ferrooxidans[J]. Journal of General Microbiology, 1977, 101: 85-91.
[7] LESIA H, HECTOR M L, ISAMU S. Selective inhibition of the oxidation of ferrous iron or sulfur in Thiobacillus ferrooxidans[J]. Applied and Environmental Microbiology, 2000, 66(3): 1031-1037.
[8] LAZAROFF N. Sulfate requirement for iron oxidation by Thiobacillus ferrooxidans[J]. Journal of Bacteriology, 1963, 85(1): 78-83.
[9] FRYI V, LAZAROFF N, PACKER L. Sulfate-dependent iron oxidation by Thiobacillus ferrooxidans: characterization of a new EPR detectable electron transport component on the reducing side of rusticyanin[J]. Archives of Biochemistry and Biophysics, 1986, 246(2): 650-654.
[10] CSONKAL N. Physiological and genetic responses of bacteria to osmotic stress[J]. Microbial Research, 1989, 53(1): 121-147.
[11] ASPEDON A, PALMER K, WHITELEY M. Microarray analysis of the osmotic stress response in pseudomonas aeruginosa[J]. Journal of Bacteriology, 2006, 188(7): 2721-2725.
[12] HE Z, ZHONG H, HU Y, XIAO S, LIU J, XU J, LI G. Analysis of differential-expressed proteins of Acidithiobacillus ferrooxidans grown under phosphate starvation[J]. Journal of Biochemistry and Molecular Biology, 2005, 38(5): 545-549.
[13] SEEGER M, JEREZ C A. Phosphate limitation affects global gene expression in Thiobacillus ferrooxidans[J]. Geomicrobiology Journal, 1992, 10(3/4): 227-237.
[14] WASAKI J, SHINANO T, ONISHI K, YONETANI R, SASAKI T. Transcriptomic analysis indicates putative metabolic changes caused by manipulation of phosphorus availability in rice leaves[J]. Journal of Experimental Botany, 2006, 57(9): 2049-2059.
[15] FIROVED A M, WOOD S R, ORNATOWSKI W, DERETIC V, TIMMINS G S. Microarray analysis and functional characterization of the nitrosative stress response in nonmucoid and mucoid Pseudomonas aeruginosa[J]. Joural of Bacteriology, 2004, 186(12): 4046-4050.
[16] CHEUNG K J, BADARINARAYANA V, SELINGER D W, JANSE D, CHURCH G M. A microarray-based antibiotic screen identifies a regulatory role for super coiling in the osmotic stress response of Escherichia coli[J]. Genome Research, 2003, 13(2): 206-215.
[17] RIEDEL K, LEHNER A. Identification of proteins involved in osmotic stress response in Enterobacter sakazakii by proteomics [J]. Microbiology, 2007, 7(8): 1217-1231.
[18] PETERSOHN A, BRIGULLA M, HAAS S, HOHEISEL J D, V?LKER U, HECKER M. Global analysis of the general stress response of Bacillus subtilis[J]. Journal of Bacteriology, 2001, 183(19): 5617-5631.
基金项目:国家重点基础研究发展计划资助项目(2004CB619201);国家自然科学基金资助项目(50621063; 50674101)
收稿日期:2008-08-21;修订日期:2009-02-12
通信作者:夏金兰,教授,博士;电话:0731-88836944;E-mail: jlxia@mail.csu.edu.cn
(编辑 龙怀中)