文章编号:1004-0609(2008)03-0541-05
碳源和铁源对LiFePO4/C材料的制备及性能的影响
刘旭恒,赵中伟
(中南大学 冶金科学与工程学院,长沙 410083)
摘 要:采用高温固相法合成LiFePO4/C材料,采用XRD和SEM对该材料性能进行表征。结果表明:采用不同原料合成的LiFePO4/C材料都具有规整的橄榄石型结构。原料对比实验表明,葡萄糖为碳源优于碳黑,草酸亚铁优于三价铁源;以葡萄糖为碳源、草酸亚铁为铁源合成的材料形貌规则,分散性好。电化学测试表明,以葡萄糖为碳源、草酸亚铁为铁源得到的LiFePO4/C材料0.1C时首次放电比容量达到152.2 mA?h/g,大电流密度下性能良好,3C时其首次放电比容量为140.8 mA?h/g,20次循环后仅衰减1.2%。
关键词:LiFePO4/C;锂离子电池;正极材料;碳掺杂
中图分类号:TM 912.9 文献标识码:A
Effects of carbon source and iron source on preparation and performance of LiFePO4/C
LIU Xu-heng, ZHAO Zhong-wei
(School of Metallurgical Science and Engineering, Central South University, Changsha 410083, China)
Abstract: LiFePO4/C was synthesized by solid-state reaction. The materials were characterized by XRD and SEM. The results indicate that the performance of the dextrose as carbon source is better than that of carbon black, and the performance of ferrous oxalate as iron source is better than that of ferrate. The materials synthesized with carbon sources and iron source have a standard structure of olive-type phase, and the materials synthesized with dextrose and ferrous oxalate show the regular appearance and good performance of mixture. The material synthesized with the dextrose and ferrous oxalate shows the best electrochemical performance. The initial discharge capacity of this sample reaches 152.2 mA?h/g under the rate of 0.1C, and reaches 140.8 mA?h/g under 3C rate and has a decrease of only 1.2% after 20 cycles.
Key words: LiFePO4/C; Li-ion battery; cathode material; carbon-doped
磷酸铁锂(LiFePO4)的理论容量为170 mA?h/g,具有热稳定性好、充放电效率高、环境友好、价格便 宜[1]的特点,被认为是极有潜力的锂离子电池特别是动力锂离子电池[2-3]的正极材料。但是其电导率低,锂离子扩散速度小,导致其在大电流密度下的容量急剧下降,循环性能也变差[4-9]。因此,如何提高磷酸铁锂的电导率以改善其电化学性能成为当前研究的热点。目前,研究者们广泛采用高温固相法[10]、液相法[11]、共沉淀法[12]和微波加热[13]等方法来合成磷酸铁锂,并采用掺杂[14-15]等方式提高材料的电导率,以期改善其电化学性能,如张宝等[16]合成LiFePO4/C材料,0.1C时放电比容量达到151 mA?h/g。本文作者采用机械化学高能研磨的方式制备得到前驱体,再经高温煅烧合成LiFePO4/C材料,并研究不同原料对材料性能的影响。
1 实验
1.1 LiFePO4/C的合成
将铁源化合物、LiOH?H2O (工业纯99.9%)和磷源化合物按照LiFePO4化学计量比混合,添加5%(质量分数)的碳源物质,置于振动球磨机中研磨15 min,球磨机转速为900 r/min。取研磨后的前驱体直接装入瓷舟,置于高纯氮气保护气氛(流量为0.2 L/min)的管式电炉中,在650 ℃下煅烧8 h;控制降温速度在2~ 10 ℃/min,冷却到室温,所得产物即为LiFePO4/C材料。
1.2 样品分析
采用日本理学D/RAX射线衍射仪进行样品物相分析,Cu Kα辐射源,扫描区间为10?~70?,管电压为50 kV,管电流为100 mA;采用美国KYKY2800扫描电子显微镜观察样品表面形貌。
1.3 电池装配与测试
以涂布法制备电极,将LiFePO4、碳黑和PVDF按质量比为8?1?1的比例配料混合均匀,采用NMP为溶剂调成正极浆液,再将浆液均匀地涂布在预处理过的铝箔上,置于真空干燥箱中,在110 ℃下烘干极片,在氩气保护的手套箱里,以锂片为对电极,以1 mol/L的LiPF6/EC-DMC(1?1)为电解液,采用Celgerd隔膜,组装成2025型扣式电池,在武汉金诺公司的电池检测系统上进行测试。
2 分析和讨论
2.1 不同碳源对材料的影响
图1所示为分别采用碳黑和葡萄糖为碳源、草酸亚铁为铁源所合成的LiFePO4/C材料的XRD谱。从图中可以看出,两个样品的衍射峰均为磷酸铁锂的衍射峰,与标准卡片基本一致,没有出现杂相峰,说明合成的材料主相为磷酸铁锂,而其中碳以无定形的形式存在。
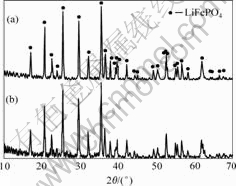
图1 不同碳源合成的LiFePO4/C材料的XRD谱
Fig.1 XRD patterns of LiFePO4/C synthesized with different carbon sources: (a) Carbon black; (b) Dextrose
图2所示为不同碳源合成的LiFePO4/C材料的SEM像。从图可知,用碳黑为碳源的材料粒度相对较大,团聚现象比较严重,呈单体形态存在的颗粒很少,材料呈片状,粒度大都在2 ?m以上;用葡萄糖为碳源的所得LiFePO4/C材料粒度要小,且形貌更加规整,呈现类球形,粒径分布比较均匀,只有少量出现团聚现象,单体粒径为0.5 ?m左右。这可能是由于葡萄糖有良好的可溶性,流动性也优于碳黑,在高能研磨作用下,葡萄糖更加均匀地分散在前驱体中,经高温碳化后,均匀包覆在LiFePO4颗粒表面,阻碍LiFePO4晶粒的长大,有利于晶粒的细化,使材料的分散性更好。

图2 不同碳源合成的LiFePO4/C材料的SEM像
Fig.2 SEM images of LiFePO4/C synthesized with different carbon sources: (a) Carbon black; (b) Dextrose
图3所示为分别用不同碳源所合成的LiFePO4/C材料在0.1C时的首次充放电曲线图。从图3可以看出,采用葡萄糖为碳源所得的LiFePO4/C材料其首次放电比容量达到152.2 mA?h/g,而用碳黑为碳源所合成的样品只有128.8 mA?h/g,且前者的充放电平台更加平坦。结合图2可知,这主要是用葡萄糖所合成的LiFePO4/C材料粒径较小,锂离子的扩散路径短,扩散速度快;同时由于葡萄糖碳化后均匀地包覆在LiFePO4材料上,材料的电子电导率得到提高,减小电极极化,使活性物质能更充分地参与到电化学反应中,从而改善材料的整体电化学性能。因此本研究后续的LiFePO4/C材料合成都采用葡萄糖为碳源物质。
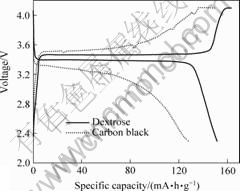
图3 不同碳前驱体制备的LiFePO4/C材料在0.1C时的充放电曲线
Fig.3 Charge-discharge curves of LiFePO4/C synthesized with different carbon sources at 0.1C
2.2 不同铁源对材料的影响
图4所示为以不同铁源合成LiFePO4/C材料的XRD谱。由图可知,采用不同铁源所合成的材料,其XRD谱与磷酸铁锂的标准卡片的衍射图谱一致,不含其他杂相峰,说明生成了LiFePO4/C材料,其中碳以无定形形态存在于材料中。用草酸亚铁为铁源所合成的材料,其衍射峰毛刺较少,峰型更加尖锐;而采用三价铁源通过葡萄糖还原生成的LiFePO4/C材料其衍射峰毛刺较多,结晶程度相对较差。
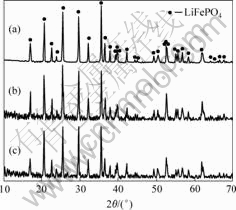
图4 不同铁源合成的LiFePO4/C材料的XRD谱
Fig.4 XRD patterns of LiFePO4/C synthesized with different iron sources: (a) FeC2O4?H2O; (b) FeCl3; (c) Fe2O3
图5所示为以不同铁源合成的LiFePO4/C材料在0.1C时的充放电曲线图。由图可知,对于三价铁源来说,Fe2O3为铁源所合成的LiFePO4/C要优于以FeCl3为铁源所合成的LiFePO4/C材料。用前者合成的材料放电比容量达到133.8 mA?h/g,高于后者的122.5 mA?h/g,而且以Fe2O3为铁源的平台更平坦,在约3.4 V的放电电压下的容量约达到118 mA?h/g,占总放电容量的88.7%;采用二价铁源显著优于三价铁源,以FeC2O4?H2O为铁源所合成的LiFePO4/C的放电比容量达到152.2 mA?h/g,远高于以Fe2O3和FeCl3为铁源所合成的LiFePO4/C的放电比容量。同时,FeC2O4・H2O在反应过程中分解产生气体,阻碍晶粒的长大和团聚,而且从图4中可以看出,用FeC2O4・H2O合成的材料晶型更加完整,这些都有利于FeC2O4・H2O合成的材料比容量的提高。
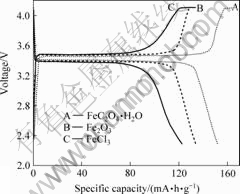
图5 不同铁源合成的LiFePO4/C材料在0.1C时的充放电曲线图
Fig.5 Charge-discharge curves of LiFePO4/C synthesized with different iron sources at 0.1C
2.3 LiFePO4/C材料的电化学性能
将用草酸亚铁为铁源所合成的LiFePO4/C材料组装成电池,在不同倍率下进行充放电循环实验。图6和7所示分别为LiFePO4/C材料在不同倍率下的充放电曲线和循环性能图。
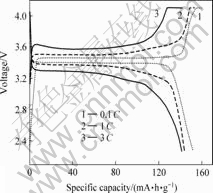
图6 不同倍率下LiFePO4/C材料的充放电曲线
Fig.6 Charge-discharge curves of LiFePO4/C at different rates
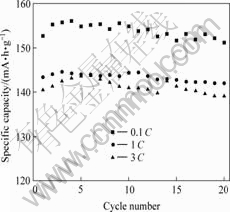
图7 不同倍率下LiFePO4/C材料的循环性能
Fig.7 Cycle performance of LiFePO4/C at different rates
从图6和7可知,用葡萄糖合成的LiFePO4/C材料不仅首次充放电比容量高,充放电循环可逆性能也很好。随着电流密度的增大,比容量的衰减程度不大。
0.1C下的当次放电比容量为152.2 mA?h/g,1C下的首次放电比容量为143.2 mA?h/g,3C下的首次放电比容量为140.8 mA?h/g。循环曲线呈波浪形分布,这有可能是失效的活性物质在后续的循环中重新得到利用所致。20次循环后衰减程度很低,0.1C时仅衰减0.7%,1C时衰减0.77%,在3C时的容量衰减仅为1.2%,循环性能良好。
3 结论
1) 采用高温固相法合成LiFePO4/C材料,所得粉体颗粒具有规整的橄榄石型晶体结构,碳以无定形形态存在于材料中。
2) 在不同的碳源和铁源所合成的LiFePO4/C材料中,以葡萄糖为碳源、草酸亚铁为铁源所合成的LiFePO4/C材料形貌规整,粒度分布均匀,分散性好。
3) 以葡萄糖为碳源、草酸亚铁为铁源所合成的LiFePO4/C材料在0.1C电流密度下放电比容量达到152.2 mA?h/g;材料在大电流密度下也具有优良的电化学性能,在3C倍率下的首次放电比容量为140.8 mA?h/g,20次循环后仅衰减1.2%。
REFERENCES
[1] 卢俊彪, 张中太, 唐子龙, 郑子山. 一种新型的锂离子电池正极材料――LiFePO4[J]. 稀有金属材料与工程, 2004, 33(7): 679-683.
LU Jun-biao, ZHANG Zhong-tai, TANG Zi-long, ZHENG Zi-shan. A novel anode material for lithium ion batteries―LiFePO4[J]. Rare Metal Materials and Engineering, 2004, 33(7): 679-683.
[2] 倪江锋, 苏光耀, 周恒辉, 陈继涛. 锂离子电池正极材料LiMPO4的研究进展[J]. 化学进展, 2004, 16(4): 554-560.
NI Jiang-feng, SU Guang-yao, ZHOU Heng-hui, CHEN Ji-tao. Study of LiMPO4 as cathode material for lithium ion batteries[J]. Progress In Chemistry, 2004, 16(4): 554-560.
[3] WANG G X, YANG L, CHEN Y, WANG J Z, BEWLAY S, LIU H K. An investigation of polypyrrole-LiFePO4 composite cathode materials for lithium-ion batteries[J]. Electrochimica Acta, 2005, 50(24): 4649-4654.
[4] ANDERSSON A S, THOMAS J O. The source of first-cycle capacity loss in LiFePO4[J]. Journal of Power Sources, 2001, 97/98: 498-502.
[5] FRANGER S, LE CRAS F, BOURBON C, ROUAULT H. Comparison between different LiFePO4 synthesis routes and their influence on its physico-chemical properties[J]. Journal of Power Sources, 2003, 119/121: 252-257.
[6] MASQUELIER C, PADHI A K, NANJUNDASWAMY K S, GOODENOUGH J B. New cathode materials for rechargeable lithium batteries: The 3-D framework structures Li3Fe2(XO4)3 (X=P, As)[J]. Journal of Solid State Chemistry, 1998, 135(2): 228-234.
[7] PARK K S, SON J T, CHUNG H T, KIM S J, LEE C H, KIM H G. Synthesis of LiFePO4 by co-precipitation and microwave heating[J]. Electrochemistry Communications, 2003, 5(10): 839-842.
[8] NI J F, ZHOU H H, CHEN J T, ZHANG X X. LiFePO4 doped with ions prepared by co-precipitation method[J]. Materials Letters, 2005, 59(18): 2361-2365.
[9] 赵中伟, 刘旭恒. Li-Fe-P-H2O系热力学分析[J]. 中国有色金属学报, 2006, 16(7): 1257-1263.
ZHAO Zhong-wei, LIU Xu-heng. Thermodynamic analysis of Li-Fe-P-H2O system[J]. The Chinese Journal of Nonferrous Metals, 2006, 16(7): 1257-1263.
[10] TAKAHASHI M, TOBISHIMA S, TAKEI K, SAKURAI Y. Characterization of LiFePO4 as the cathode material for rechargeable lithium batteries[J]. Journal of Power Sources, 2001, 97/98: 508-511.
[11] YANG Shou-feng, Peter Y. Zavalij, M. Stanley Whittingham. Hydrothermal synthesis of lithium iron phosphate cathodes[J]. Electrochemistry Communications, 2001, 3(9): 505-508.
[12] ARNOLD G, GARCHE J, HEMMER R, STR?BELE S, VOGLER C, WOHLFAHRT-MEHRENS M. Fine-particle lithium iron phosphate LiFePO4 synthesized by a new low-cost aqueous precipitation technique[J]. Journal of Power Sources, 2003, 119/121: 247-251.
[13] HIGUCHI M, KATAYAMA K, AZUMA Y, YUKAWA M, SUHARA M. Synthesis of LiFePO4 cathode material by microwave processing[J]. Journal of Power Sources, 2003, 119/121: 258-261.
[14] TAKEUCHI T, TABUCHI M, NAKASHIMA A, NAKAMURA T, MIWA Y, KAGEYAMA H, TATSUMI K. Preparation of dense LiFePO4/C composite positive electrodes using spark-plasma- sintering process[J]. Journal of Power Sources, 2005, 146(1/2): 575-579.
[15] PARK K S, SON J T, CHUNG H T, KIM S J, LEE C H, KANG K T, KIM H G. Surface modification by silver coating for improving electrochemical properties of LiFePO4[J]. Solid State Communications, 2004, 129(5): 311-314.
[16] 张 宝, 李新海, 朱炳权, 王志兴, 郭华军. 沉淀-碳热还原联合法制备橄榄石磷酸铁锂[J]. 中国有色金属学报, 2006, 16(8): 1445-1449.
ZHANG Bao, LI Xin-hai, ZHU Bing-quan, WANG Zhi-xing, GUO Hua-jun. Synthesis of lithium iron phospho-olivines by aqueous precipitation and carbothermal reduction[J]. The Chinese Journal of Nonferrous Metals, 2006, 16(8): 1445-1449.
基金项目:国家自然科学基金重点资助项目(50434010);新世纪优秀人才基金资助项目(NCET-05-0692)
收稿日期:2007-07-06;修订日期:2007-10-12
通讯作者:赵中伟,教授,博士生导师;电话:0731-8830476;E-mail: zhaozw@mail.csu.edu.cn
(编辑 龙怀中)