DOI��10.19476/j.ysxb.1004.0609.2018.02.21
������ֽ���ٿ�����а���ϡ������Ϊ
��������������������������������� ��
(���ϴ�ѧ ұ���뻷��ѧԺ����ɳ 410083)
ժ Ҫ��ͨ������ѧ�������25 ��ʱ������ֽ���ٿ�����а���ϡ��������pHֵ�Լ�����Ũ�ȱ仯������ѧƽ��ͼ��������Щ������������Ѱ��ϡ�������ۺ���ȡ�ļ�������ͨ��ʵ����֤�˼����Ŀ����ԡ����������ϡ�����ӿ������ᡢ������Լ��Ӷ����γ���������������Һ�У���ͬ��pH������ϡ������ϳ������ӻ������ӡ���pH��1ʱ��ϡ�����������ᡢ���������γ������ӣ�����pHԼΪ1~3ʱ��ϡ�����Ӷ�����ϳ�ϡ�������Ӷ������ӣ���Щ��λ�ɴٽ�ϡ������ķֽ⡣ʵ�黹�������Ӷ����ϡ���ֽ��дٽ����ã�����WO3������ϡ�����������ֱ�Ϊ26.11%��0.13%�İ��ٿ����¶�90 �桢��Ӧʱ��5 h������Ũ��1 mol/L������Ũ��2.5 mol/L�����£�ϡ��La��Ce��Nd�����ʿɴ�85.61%��45.68%��47.03%�����⣬����ϡ���������������̬�IJ�������ϡ�����ٷֲ���ͬ����ȡ���ա�
�ؼ��ʣ�ϡ�����ٿ�ϡ�����Ӷ������ӣ���ȡ������ѧ
���±�ţ�1004-0609(2018)-02-0387-10���� ��ͼ����ţ�TF111.31���� ���ױ�־�룺A
����ϡ�����ж��ص���������ѧ���ܣ����㷺Ӧ����ұ�𡢵��ӡ����캽�ա�������������������Ҫ��ս�Խ������й�������ϡ����Դ�ֱ�ռ����ȫ���68%��55%[1]����������Դ�У�Լ70%Ϊ���ٿ�20%Ϊ���ٿ�10%����Ϊ�ڰ��ٻ�Ͽ�[2]����ϡ����Ҫ��3����ʽ�����ڵؿ��У�1) ��������̬���ھ������γɿ������ʯ����̼���ȣ�2) ������������ճ���ʡ���ĸ�ʿ�����棬��绯���ܻ�������ϡ����3) ������Ԫ������ͬ���ɢ�ڿ����У�����������ʯ��[3]�����ڳɿ�����У�������ѧ�������Ƶ�Ԫ�ش��ڹ����Ͱ������������Ԫ�ص�ϡɢ�ֲ���GOLDSCHMIDT[4]���ݳɿ���ɵ������Խ�Ԫ�ط�Ϊ��ʯ����������ͭ������4�����͡�
ϡ���������ٵ�Ԫ��������ʯԪ�أ��������Һ������������������ͬ���û�������ѧ���о����ٿ���ϡ���ķֲ����ɣ���Ϊ�и�����Һ��ƫ���Ի����ٽ���ϡ�����ٿ��еķֲ�[5]��Ԫ�����Ӱ뾶�Ǿ�������ͬ�����Ҫ���أ�GOLDSCHMIDT[4]��Ϊ���ɿ������£��뾶��С��15%�����ӿ���û������ڴˣ�ͼ1(a)�Բ�ͬ��̬����λ����ϡ�����ӺͲ��ֹ��ɽ������ӵİ뾶���бȶԣ����ֶ���ϡ�����Ӱ뾶��Ǧ������С������ϡ���������ʡ��ư뾶�൱����ϡ���������̰뾶Ҳʮ�ֽӽ�������[6-9]���ơ��̡��ʵȿ����е�ϡ���ֲ�״̬�������о�������ϡ��������Ԫ�ش���һ��������Ϊ������������ϡ����ȡ���ٿ��иơ������̵�Ԫ�ط�������ͬ���������
���ɭ[10]���ϡ���������⣬�о����ڲ�ͬ��ʯ�еĸ����̶ȡ��ڳ����Ļ�ʯ����ʯ���������Լ��������У�ϡ����������ʯƽ���������ͣ����ٿ��е�ϡ������ʯ�����߳�2~3��������(��ͼ1(b))���й��ٿ�������������ϡ������Դ�����ģ����ٿ����ϡ����Դ�Ļ��ս�������Ҫ���塣
Ŀǰ�����ְ��ٿ���ü��Էֽ�գ��ڸ���ϵ�У���ת��Ϊ���������Һ�࣬��ϡ�����ɹ�������������δ�ֽ���ʯ�������ࣻͨ����������ֽ����ȡϡ��������ķѴ����Ტ���ӳ��˹������̣�����Ч��Ͷ����¸÷�����о�����[13-14]�����������ᡢ����ֱ�ӷֽ⣬�����������γɹ����Ӱ����ȡ��Ϊ����һ�ָ�Ч���ٿ��ᷨ�ֽ�գ�ZHAO��[15]��������������ϵ������ר����������ʹ�ٱ���Ͻ�����Һ�������������ƽ������ʯ�������࣬�Ӷ�ʵ�����ٿ����Ч�ֽ⣬�����ʸߴ�99%��ʯ�����������Ŀɽ�������Ķѷ����⣬����Һѭ�����ý���˷�ˮ�ŷ����⣬��������������ҵ�ɹ�ʵ�ֲ�ҵ����

ͼ1 ϡ��Ԫ�ص�����ͬ������[10-12]
Fig. 1 Isomorphic property of REE elements[10-12]
�ù��ղ������Խ�����ϵ����Һ�к����ס����ٵĺ�����������Լ����ǵĸ��������ӡ�����ϵ�д���ϡ��Ԫ�أ����п��ܴ��ڸ��Ӹ��ӵ������Ϊ��ʵ���ϣ���HAAS��[16]���о���������ϡ��������ȶ���������Щ���û�������ϡ������ķֽ⣬�Ӷ�Ϊ����ϡ���Ļ��մ����������������������о���������ϵϡ�����ٵ���Ϊ������������ͨ������ѧ�������ۺ�ʵ����֤������������ֽ���ٿ������ϡ�����ٵ����ֱ仯�����ڶ�Ԫ���ۺ������ṩ�����ָ����
1 ����ѧ���ݼ�����
��������ϵ�ֽ���ٿ����ϡ�����ܴ��ڵ�ƽ���ϵ���ɱ�1���С����ڼ�������ϵ���ָ��ӣ������ӻ��ϵ�����ѻ�ã����¼����������Ũ�ȴ����ȡ�ϡ��Ԫ����17�֣����ﻯ�������ƣ����о�������������ڷֽ���ϵ���и����Ӷ���(POM)�γɣ���Ҫ��Keggin�������Ӷ��ᣬҲ������Well-Dawson��Anderson��Waugh��Silverson�ͣ���Ŀǰ����Keggin������ѧ���ݡ������в�������Ϊ��Ӧ����˹�����ܡ�G������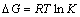 ����Ϊƽ�ⳣ����
����Ϊƽ�ⳣ����
����ʱ����[La]T ��[W]T�ȱ�ʾ��Һ��ϡ�����ٵ���Ũ�ȣ�[WO42-]��[La3+]��Ϊ��Һ�и����ֵ�Ũ�ȣ��������������غ�ԭ������ѧ��Ӧͬʱƽ��ԭ������������ֽ���ϵ�д��ڵĹ�ϵ��
[La]T=[La3+]+[LaOH2+]+[La(OH)2+]+[La(OH)3(aq)]+[La(OH)4-]+[LaH2PO42+]+[La(HPO4)+]+
[La(HPO4)2-]+[La(PO4)23-]+[LaPO4(aq)]+[LaSO4+]+[La(SO4)2-] (1)
[W]T=[WO42-]+[HWO4-]+[H2WO4(aq)]+2[W2O72-]+3[W3O102-]+4[W4O132-]+5[W5O162-]+7[W7O222-]+
7[W7O246-]+7[W7O245-]+8[W8O252-]+10[W10O312-]+11[W11O342-]+12[H2W12O4210-]+
12[H2W12O406-]+[PWO6-]+2[PW2O9-]+3[PW3O12-]+4[PW4O15-]+5[PW5O18-]+
6[PW6O21-]+8[PW8O27-]+10[PW10O33-]+12[PW12O40-] (2)
[P]T=[PO43-]+[HPO42-]+[H2PO4-]+[H3PO4]+[LaH2PO42+]+[La(HPO4)+]+2[La(HPO4)2-]+
2[La(PO4)23-]+[LaPO4(aq)]+CaH2PO4+]+[CaHPO4]+2[Ca(H2PO4)2]+[CaPO4-]+[PWO6-]+
[PW2O9-]+[PW3O12-]+[PW4O15-]+[PW5O18-]+[PW6O21-]+[PW8O27-]+[PW10O33-]+[PW12O40-] (3)
[S]T=[SO42-]+[HSO4-]+[H2SO4]+[LaSO4+]+2[La(SO4)2-] (4)
[Ca]T=[Ca2+]+[CaOH+]+[CaH2PO4+]+[CaHPO4]+[Ca(H2PO4)2]+[CaPO4-] (5)
�����а���ϡ���ĺ����趨Ϊ��Ȼ���ٿ�ϡ��������ƽ��ֵ��ԼΪ�ٿ�������0.5%~1%��������ͬ���La2(WO4)3 Ksp(10-3.9)ԶԶ����CaWO4 Ksp(10-8.8)������Ϊϡ������ٿ�ͬ���ֽ⣬����ʱϡ��ȡ�ֽ���ٿ�Ũ�ȵ�1%(Ħ������)��
��1 �漰��Ӧ�Ļ�ѧ����ʽ����Ӧ��ƽ�ⳣ��(25 ��)
Table 1 Chemical reaction equations and corresponding equilibrium constants of revenant reactions (25 ��)
2 ���������
2.1 La-W-S-P-Ca-H2Oϵ����ѧ����
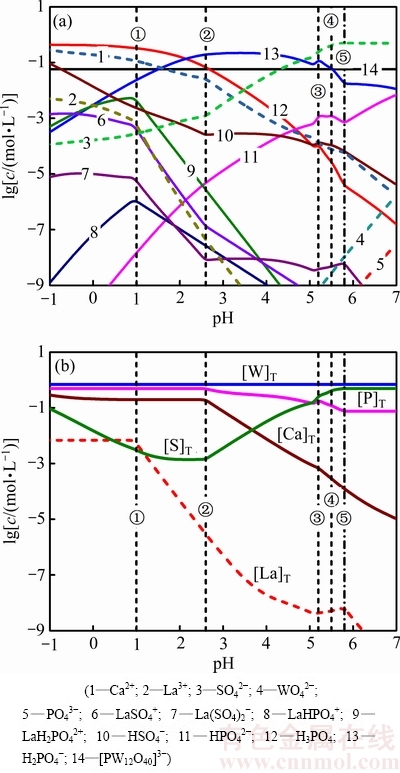
��La-W-S-P-Ca-H2Oϵ�У��Ӷ���������pH�仯�ױ䣬��ϡ������ϼ��临�ӣ�ֻ�ܶ��Է�����δ�����Ӷ������ϡ������£���pHֵ0.1Ϊ����ɼ����Һ�̱�Ϊ5 mL:1 g��������Ũ�Ⱦ�Ϊ0.5mol/L��������Ҫ��ֵ�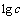 -pHͼ����ͼ2��ʾ��
-pHͼ����ͼ2��ʾ��
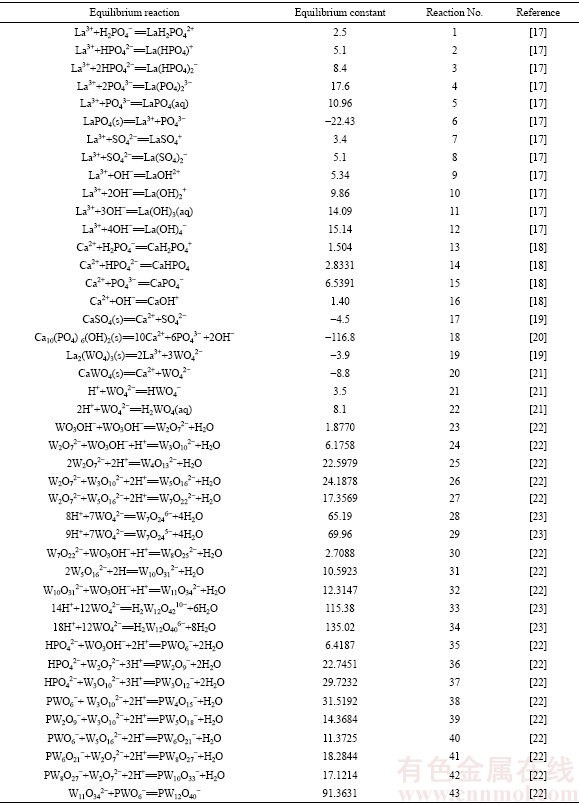
ͼ2 La-W-S-P-Ca-H2O��ϵ��Ҫ�ܽ����lg c-pHͼ�����١��ܸơ����ס����������lg c-pHͼ(25 ��)
Fig. 2 lg c-pH diagrams of main species of La-W-S-P-H2O system(a) and total tungsten, calcium, sulfur, phosphorus and lanthanum(b) (25��)
����ϵ�ﵽƽ��ʱ����Һ����Ҫϡ��������La3+��LaH2PO42+��LaSO4+��La(SO4)2-��������Ϊ[PW12O40]3-��ͼ2�е����ߢ١��ڡ��ۡ��ܡ��ݷֱ�Ϊ����LaPO4(s)��CaHPO4(s)��Ca3(PO4)2(s)��Ca10(PO4)6(OH)2(s)���ٽ��ߺ�CaSO4(s)�ķ����ߡ��ߢ������ٿ�ֽ���ȫ����ʱ����ϡ��ת��Ϊ�������Σ��������γ�ʯ��������ߢ����ң���Һ�е����ת���LaPO4(s)��������ϡ���յ��ʣ��ߢ����ߢ�֮��ΪCaHPO4(s)�ȶ����䣬��ʱ����������ٵ���Ϸֽ⣬������Ƶ����ã������������ģ��ߢ����ߢ�֮��ΪCa3(PO4)2�ȶ������ƿ�ת��Ϊ���������ʶ��ֽ���ٿ����������������ֽ��γɵ�WO42-��ת��Ϊ�Ӷ��ᡣ���ͬʱ����ȥ����ʯ���еĸƶ��ͷų�SO42-������ϡ����������ﺬ����������������pH�������ߢ�ʱ�����ǻ���ʯ���ɣ����ٿ�ֽ�Ĵָ����������ϣ����ߢ�ʱ�ֽ�����CaSO4(s)������������ͼ2�з�����֪������ϡ���Ļ���ֻ�����ߢ�����ĺ�����Һ�ȶ�������У��ڸ����䣬ϡ����Ҫ����ΪLaSO4+��La3+��LaH2PO42+������pH�����ߣ��������H2PO4-Ũ�����ӣ�CaSO4(s)��������SO42-Ũ�Ƚ��ͣ�����La3+���ϱ�������ϣ����ڷֽⷴӦLa2(WO4)3=2La3++3WO42-��ϡ���ֽ��������ƶ���
��ϵ������Ч����ϡ�����������ȡ�����ߢٵ�pHֵ��pHֵԽ��ϡ����Һ���ȶ�����Խ�Ժ�����ϡ���������ȡҲ��������Ϊ�ˣ������˲�ͬ���������ߢ�pHֵ��Ӱ�죬��ͼ3��ʾ����[S]T=0.5mol/Lʱ������[P]T��α仯���ߢٱ���pH=1����(������1��2��3)������[P]T�㶨��[S]TŨ�������ߢ�pHֵҲ��֮����(��������1��4��5)����ͬʱ����[S]T��[P]TŨ��ʱ����ϸù���(��������1��6��7)��

ͼ3 ��ͬ��������Ũ�������������������pH�ı仯 (25 ��)
Fig. 3 Change of total recovery of La with pH at different concentrations of total sulfur and phosphorus(25 ��)
Ϊ��һ������ͼ3�Ĺ��ɣ�������pH=0.5ʱ��ϵ����Ҫϡ���������������ױ仯�ķֲ��Լ����ᡢ����ĵ����������ͼ4��ʾ����ͼ4�ɼ�����[S]T�����ϵ�ʱ����������ں�������(��ͼ2)������ϡ����LaH2PO4+��̬���ڣ�������������������ֱ������ӣ���ʱ����Ϊ��Ҫϡ����ϼ����������������H2PO4-��ͬʱ��������PO43-��Ũ�ȣ������ߢٵ�pHֵ����(��ͼ4(a))����[P]T=0.5mol/Lʱ������[S]T���������ӣ�LaSO4+������������La(SO4)2-����Խ��Խ�ߣ���˵�������ϡ�����������ϣ��ʶ��ߢٵ�pH���������Ũ�����Ӷ�����ͬʱ�����������������������������ͼ4(d)��֪��H2PO4-��SO42-�ĵ�������ʮ�ֽӽ������ӱ�1�����ݿɿ�����ϡ����SO42-��ϳ�����H2PO4-��1~2��������������Ȼ���ڴ�����������£��ײ������ơ�
������ϵ�У�����������γɿ����Ӷ��ᣬ�����˰��ٿ�ķֽ⡣�������������������������£�ϡ����Ҫ�������γ��������ӣ�����λ�ƶ���ϡ����ֽ�������ƶ���ʪ�����������ȡϡ����ʵ��Ҳ��ʾ����������Ũ�ȵ����ߣ���ʯ��ϡ���ķֽ���������[24]�����ٰ���ϡ������ȡ���Դ�Ϊ�������⣬�������ϡ�������н�ǿ����λ����������Ч��������ϡ������Ũ�ȣ������LaPO4(s)��CaHPO4(s)�ij���pHֵ������ϡ����Һ���ȶ�����������ϡ�����ӽ�����Һ�������������������ȼ������ӣ����������������ĵ��룬�Ӷ���������Һ�е�H2PO4-��SO42-��������ϡ�����ܽ⡣WIRTH[25]�о���������������Ũ�ȵ�����ϡ���������ܽ����������С��
ͨ����������ѧ�����Լ��������֪����ֻ����������ϡ������λ����һ�������¶�ϡ���Ľ����������ģ�������ȹ������ϡ���ܽⲻ����Ϊ��Ч��ȡ�������٣�ͬʱ����Ч���հ���ϡ������һ����ȵ�����Ȼ�Ѳ�����Ҫ��ʱ��ֵ��ע����ǣ�������ϵ�в�ֻ������������ϼ������д������Ӷ��������о���ʾ�����Ӷ�����ϡ�����Ӵ�����λ��Ӧ����[26]����ϵ�������Ӷ���Ĵ��ڻ�ɿ˷���ȹ��ߴ����ıˡ�
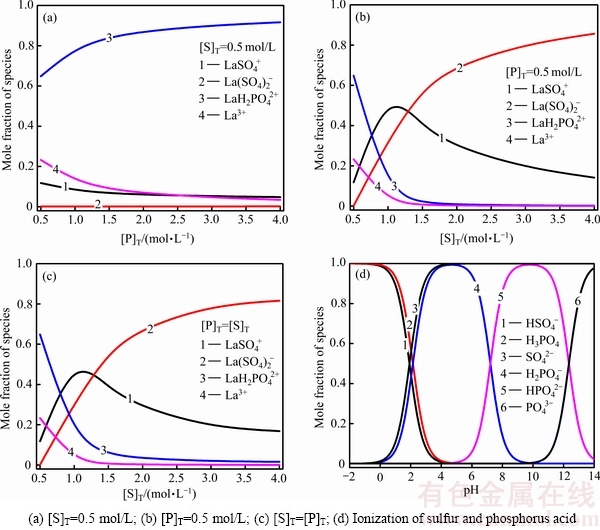
ͼ4 La-W-P-S-Ca-H2Oϵ����Ҫ��ϡ�������ڲ�ͬ��������Ũ�������µ�Ħ�������仯�Լ����ᡢ�����ڲ�ͬpH�����µĵ������(25 �棬pH=0.5)
Fig. 4 Mole fraction of species of lanthanum at different concentrations of total sulfur and phosphorus in La-W-P-S-Ca-H2O system and ionization of sulfur and phosphorus acid at different pH (25 ��, pH=0.5)
2.2 ϡ�������Ӷ������λ�Լ�����ϡ����ȡ����
��������ϵ�ֽ���ٿ�Ļ�����Ӧ���£�
12CaWO4(s)+23H++HPO42-+12SO42-=[PW12O40]3-+12CaSO4(s)+12H2O (6)
��Ȼ���������̽���Ϊ��۲���ı�����������γ��Ӷ����·���ͻ����п��ܼ��临�ӣ�Ŀǰ�����ϵĽ��͡�
KEGGIN[27]����XRD������1:12���Ӷ���ṹ���������������(MO6)�����Թ����Ǻ���ߵ���ʽ���죬�˺�POPE��[28]�ַ�����MO6��ͬ�ѻ�������ʽ�Ľṹ�����¹���ΪWell-Dawson��Anderson��Waugh��Silverson�ṹ��POPE��[29-30]����ϸ��̽�����Ӷ���Ľ�����̣���Ϊ��ԭ����������XO4 (X=P, As, Si��)��ʽ��������MO6 (M=W, Mo��)��������ʽ��������Һ�У�����Һ�¶ȡ�����Լ��Լ�Ũ�ȵ�����ѧ�����ı�ʱ���Ӷ��Ὣ����ԭ����Ϊ�ںˣ�����������Ϊ��Ƿ������ϻ��ۣ��Ӷ���Ӧ�γ�������ȱλ�͵Ȳ�ͬ���֡�
�����Ӷ�����ԣ�����������α仯���������ֲ������Ķ���������ԭ���н�ǿ����λ����ȱλ����ʧȥWO4+���Ӷ�������帺������ӣ���λ������һ����ǿ������Һ�е�ϡ���Ը۵�������̬���ڣ����к�ǿ�����������ã���ͬһϡ�������߷���������õĸ��ʷdz����⣬�Ӷ�������Զ������ߣ�ͨ����Ϊ��ˮ��Һ������������ȫ�����ܽ�������ЧӦ����Щ���ʾ������ڽ���������ϡ�
���ϡ�����Ӷ������λ���⣬PEACOCK��[26, 31]�״ν���ϵͳ�о������ֶ���ȱλKeggin��[SiW11O39]3-��Wells-Dawson��[P2W17O61]10-������ϡ�����Ӷ�������ɷֱ��γ�1:1��1:2����LUO��[32]������ȱλWells-Dawson�Ӷ�����Sm��Eu��Lu�������εļ���������ṹ�Լ�ӫ�������Ϣ������������������λ��ʽ��һЩѧ��[33-35]�о��Ӷ�����ϡ����λ��P��W��O��Ԫ�غ˴Ź������������������϶���ͬ�������������Ҫ���ã������Ӷ���������ϡ������ϳ������2��ʾ��
��2 ����ϡ����POMs����ϳ���(25 ��)
Table 2 Coordination constant of some rare earth ions with POMs (25 ��)

�ӱ�2�п�֪����ϡ�����Ӷ������ϳ������ܴ������Һ��ϡ������ȡ�ṩ������֧�š�Ȼ�������в�ͬ�Ӷ���������ϡ����λ���ڲ��죬��ȱλ����ϳ���Զ���������ͣ���ˣ�Ū�岻ͬ��������µ����ֲַ���������Ҫ��SMITH��[39]Ӧ�ú˴Ź��������pH�����Ӷ������ֺͺ����Ĺ�ϵ�����(��ͼ5)���֣�pH��1ʱ���Ӷ�����Ҫ��Keggin��PW12O403-��ʽ���ڣ�3��pH��8ʱ����ȱλKeggin��PW11O397-ռ��Ҫ��������Wells-Dawson���Ӷ���ֻ����������pHΪ1~3���Ҹ��������������δ��ȷ�ϣ�������[40-41]�пɿ������ڸ��������ȶ����ڦ�1-[P2W17O61]10-���2-[P2W17O61]10-��
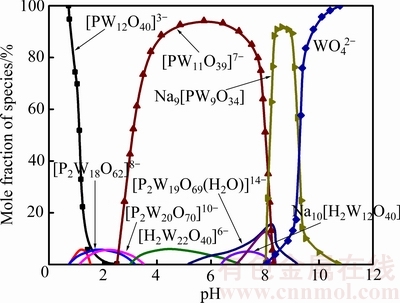
ͼ5 ���Ӷ������ֵĺ�����pH�ı仯[39]
Fig. 5 Change of mole fraction and species of heteropolytungstate with pH [39]
Ϊ̽���Ӷ����ϡ����ʵ�����Ч�����о��˲�ͬ�¶���������������������Ũ�ȱ仯���ܽ����(��ͼ6)��ͼ6(a)��ʾ������ڴ�ˮ��ϵ���ܽ�ȣ�����������������Һ�е��ܽ�����������������������Ũ�ȵ����ӳ��������ơ�Ȼ������2��ʾ�Ӷ�������Բ�ͬ������̬���ڣ��Ӷ�������ϲ��컯��Ϊ�ˣ�����˶�Ӧ������Ũ�������µ�pHֵ(��ͼ6(b))������pH�������Ậ������������ͣ�����ʵ��ֵ�����ӽ�������ֵ�߶��Ǻϣ�˵����������ȫ���룻���ݼ�⣬��������Ũ��Ϊ50 g/Lʱ����ҺpH=1.38����ͼ5֪����Һ����Keggin��Wells-Dawson���Ӷ��ἰ��Ӧȱλ���͵��γɣ���Ũ������100 g/Lʱ��pH=1.02������������ܽ�Ȳ�δ���Ӷ���Ũ�ȷ����ʱ������ӣ���ʱ������(��Keggin��[PW12O40]3-)�����Ậ�������������˲��죻��Ũ�Ƚ�һ������ʱ������Keggin��������Ϊ��Ҫ���֣��ܽ��������Ϊ����������ʵ��������֤ʵ������3�����ۣ�1) �����Ӷ�����ϡ��ȷʵ�н�ǿ����λ���ã�2) ��ͬ����������Ӷ����ϡ������λ���ڲ��죬��ȱλ�������Ӷ�����ϡ����λ��������������ǿ��3) �¶ȶ������Ӷ������ϡ����Ӱ���С��

ͼ6 ��ͬ�¶���������Ũ�������µ��������ܽ����25 ��ʱ��ӦŨ����������Һ��ʵ��������pHֵ
Fig. 6 Solubility of lanthanum sulfate at different temperatures(a) and heteropolytungstate acid concentrations(b) and pH value of heteropolytungstate acid in theory and experiment at 25 ��
��������ѧ������ʵ��������б�Ҫ̽�ְ��ٿ��ʵ�ʷֽ�Ч������ˣ�����WO3������ϡ�����������ֱ�Ϊ26.11%��0.13%�İ��ٿ�Ϊԭ�ϡ�ÿ��ʵ��ȡ��25 g������250 mL��ͬ����Ũ�ȵĽ������С��ֽ��¶�Ϊ90 �棬����Ũ��1 mol/L����Ӧʱ��Ϊ5 h���ֽ�Ч�����3���С���ʵ��Ч���ɼ���ϡ��La��Ce��Nd��߽����ʷֱ�ﵽ��85.61%��45.68%��47.03%�������ڻ�����ϵ��Ҳ���ڷֽ⡣��ͬ�����µ�ʪ����������У�ϡ���������������ʯ�ࣻ��Ȼ���Ӷ����ϡ������Ͽɿ˷����¸���ȵ�Ӱ�졣
��3 ��ͬ�����°��ٿ�����ϡ���ķֽ�ʵ��Ч��
Table 3 Leaching results of tungsten and rare earth of scheelite under different conditions

���⣬���������ֽ�����ѧ������ʵ��������ڷֽ���̬������������ᡢ���Ӷ�����ϡ������λ���ʼ�����죬��ƿ��ܵ���ȡ����·�ߡ�
1) �������ᡢ������γ����������
��������ұ�������������pH��1ʱ���Ӷ�����������[PW12O40]3-��ʽ���ڣ�����[SiW12O40]3-��ϡ������λ�����ƶ����������С�����ᡢ����������ϡ����Ҫ�γ�REH2PO42+��RESO4+ �����ġ���ʱ��������������ȡ��(����֬)��ȡϡ��������������ȡ��(����֬)��ȡ�١�
2) �����Ӷ����γ����������
��Ӧ��̬��pH������1~3֮�䣬��Һ�����Ӷ���ת��Ϊȱλ���͡����ֹ��͵��Ӷ�����ǿ�ҵĸ�����������ϡ�����ӻᱻ��������γ�ϡ�����Ӷ��������ӣ�������λ����Զ�������ᡢ������ġ���ʱ�����ð�����ȡ��(����֬)��ϡ������ͬ����ȡ�����������ᷴ��ϡ���������������Ʒ����١�
3 ����
1) �ӵ���ѧ�ĽǶȼ���ϡ�������ٿ�������ͬ��ȡ�������������Ŀǰ���ٿ�������ֽ��¹��գ�ͨ������ѧ���㣬������25 ��ʱLa-W-P-S-Ca-H2Oϵ��ϡ��������pHֵ��������Ũ�ȱ仯������ѧƽ��ͼ����ָ��Ԫ�ص��ۺ����á�
2) ����ϡ������������ϵ���������ᡢ������γ��ȶ�������Ӷ��ٽ�ϡ����ķֽ⣬���ڸ����������ϡ���ܽ�Ƚ��ͻᵼ������ϡ���ij�����
3) ���ٿ�ֽ��γɵ����Ӷ������ϡ������ϡ�����Ӷ������ӣ�������ʾ��һ�������µ��Ӷ������ϡ������Զ����������������ģ���ɱ���������������ϡ���������⡣
4) ʵ����֤�Ӷ����ڸ��¸���������¶�ϡ����������ã��ڷֽ��¶�90 �桢��Ӧʱ��5 h������Ũ��1mol/L������Ũ��2.5 mol/Lʱ��La��Ce��Nd�ֽ��ʷֱ�Ϊ85.61%��45.68%��47.03%��
5) ͨ�����Ʒ�Ӧ��̬��pHֵ�Լ�������Ũ�ȣ�����ϡ��������������Ӷ��������̬�����ʵ��ϡ�����ٵķֲ���ͬ����ȡ��
REFERENCES
[1] ����Ӣ, �� ƽ, �� ��, ������. �й�ϡ����չ�ſ�[J]. �й���ɫ����, 2010, 20(2): 34-38.
HAN Xiao-ying, LI Ping, WANG Yong, WANG Xin-lin. Development situation of China��s rare earth[J]. China Nonferrous Metals, 2010, 20(2): 34-38.
[2] ������. ���ҹ�������Դ��״���俪������[J]. ��ҵ�о��뿪��, 2003(S1): 69-72.
SUN Yan-mian. On current situation and exploitation of scheelite resources in China[J]. Mining Research and Development, 2003(S1): 69-72.
[3] �����. ϡ����ȡ����[M]. ����: ұ��ҵ������, 2006: 52-88.
HUANG Li-huang. Rare earth extraction technology[M]. Beijing: Metallurgy Industry Press, 2006: 52-88.
[4] Goldschmidt V M. The principles of distribution of chemical elements in minerals and rocks[J]. Journal of the Chemical Society, 1937: 655-673.
[5] ��Ӣ��. �ٵĵ���ѧ[M]. ����: ��ѧ������, 1987: 38-60.
LIU Ying-jun. Geochemistry of tungsten[M]. Beijing: Science Press, 1987: 38-60.
[6] ������. �ٵĵ���ѧ�о���չ[J]. ��У����ѧ��, 2009, 15(1): 19-34.
MA Dong-sheng. Progress in research on geochemistry of tungsten[J]. Geological Journal of China Universities, 2009, 15(1): 19-34.
[7] ��־��, ���, ����ƽ, Ϳ���. �ᶫ�����������ֲ�ͬ�������Ͱ��ٿ��ϡ��Ԫ�ص���ѧ����[J]. ���ʵ���ѧ, 1998, 26(2): 34-38.
ZENG Zhi-gang, LI Chao-yang, LIU Yu-ping, TU Guang-zhi. REE geochemistry of scheelite of two genetic types from Nanyangtian, Southeastern Yunnan[J].Geology-Geochemistry, 1998, 26(2): 34-38.
[8] �ɹ���, ��־��. ������������������ٿ���Ҫ������ϡ��Ԫ�ص�����ص㼰����״̬[J]. ����ѧ��, 1991, 11(2): 122-132.
GAN Guo-liang, CHEN Zhi-xiong. The compositional characteristics and existing state of major, trace and rare-earth elements in wolframite from the Dupanling tin ore-field, Guangxi[J]. Acta Mineralogica Sinica, 1991, 11(2): 122-132.
[9] ���л�. ϡ�����ﻯѧ[M]. ����: �й���ҵ������, 1963.
GUO Cheng-ji. Rare earth minerals chemistry[M]. Beijing: China Industry Press,1963.
[10] ���ɭ. ϡ��Ԫ�ص���ѧ[M]. �� ��, ʩ �R, ��. ����: ���ʳ�����, 1989: 1-69.
HENDERSON P. Rare earth element geochemistry[M]. TIAN Feng, SHI Lang, transl. Beijing: Geological Publishing House, 1989: 1-69.
[11] ����ѧ, ����ï, ��˼��, �����. �ٿ����ϡ������ѧ�������������͵��б��־[J]. ����ѧ, 1990(1): 11-20.
ZHANG Yu-xue, LIU Yi-mao, GAO Si-deng, HE Qi-guang. REE geochemical characteristics of tungsten minerials as the genetic types of ore deposits[J]. Geocheical, 1990(1): 11-20.
[12] ����ʤ. �뻪��ijЩ�ٿ��йصĻ��������ϡ��ģʽ���������������[J]. ����, 1985, 4(1): 49-55.
MAN Fa-sheng. The rare earth patterns and origin of tungsten-related granitic rocks in South China[J]. Mineral Deposits, 1985, 4(1): 49-55.
[13] �캣��, �˺���, �����, ��С��. �������ۺϻ������ü����о���״[J]. �й���ҵ, 2010, 25(4): 15-18.
ZHU Hai-ling, DENG Hai-bo, WU Cheng-hui, HE Xiao-min. The current comprehensive recovery technology of tungsten slag[J]. China Tungsten Industry, 2010, 25(4): 15-18.
[14] ������, ����, �� ��, лӪ��, ��̩Ԫ. �������н��������ֵ������о�[J]. ʪ��ұ��, 2015(2): 114-116.
LIANG Huan-long, LUO Dong-ming, LIU Chen, XIE Ying-bang, HUANG Tai-yuan. Leaching of scandium from tungsten slag[J]. Hydrometallurgy of China, 2015(2): 114-116.
[15] ZHAO Zhong-wei. LI Jiang-tao. Method for extracting tungsten from scheelite: U.S., Patent 8771617[P]. 2014-07-08..
[16] Haas J R, Shock E L, Sassani D C. Rare earth elements in hydrothermal systems: estimates of standard partial molal thermodynamic properties of aqueous complexes of the rare earth elements at high pressures and temperatures[J]. Geochimica et Cosmochimica Acta, 1995, 59(21): 4329-4350.
[17] Spahiu K, Bruno J. A selected thermodynamic database for REE to be used in HLNW performance assessment exercises[M]. Cerdanyola, Spain: MBT. Tecnologia Ambiental, 1995: 24-56.
[18] LU Xiong, YANG Leng. Theoretical analysis of calcium phosphate precipitation in simulated body fluid[J]. Biomaterials, 2005, 26(10): 1097-1108.
[19] Speight J G. Lange��s handbook of chemistry[M]. New York: McGraw-Hill, 2005: 341-352.
[20] Dorozhkin S V. Calcium orthophosphates[J]. Journal of Materials Science, 2007, 42(4): 1061-1095.
[21] Osseo-Asare K. Solution chemistry of tungsten leaching systems[J]. Metallurgical Transactions B, 1982, 13(4): 555-564.
[22] ������, �� ��, ������, ������. ��-Keggin��[PW12O40]3-�γɻ���������ѧ�о�[EB/OL]. [2011-09-02]. http://www.paper.edu.cn/html/releasepaper/2011/ 09/42/.
LANG Zhong-ling, GUANG Wei, YAN Li-kai, SU Zhong-min. Theoretical study on formation thermodynamic of ��-Keggin-type [PW12O40]3- anion[EB/OL]. [2011-09-02]. http://www.paper. edu.cn/html/releasepaper/2011/ 09/42/.
[23] �ż���, ����ΰ, ������, �����. W-Mo-H2O��ϵ������������ѧ����[J]. �й���ɫ����ѧ��, 2013, 23(5): 1463-1470.
ZHANG Jia-liang, ZHAO Zhong-wei, CHEN Xing-yu, LIU Xu-heng. Thermodynamic analysis for separation of tungsten and molybdenum in W -Mo -H2O system[J]. The Chinese Journal of Nonferrous Metals, 2013, 23(5): 1463-1470.
[24] ����ʿ, ��־��, ��С��, ������, ��ҵ��, ����. ʪ���������������п���ϡ��������о�[J]. �й�ϡ��ѧ��, 2008, 26(3): 307-312.
WANG Liang-shi, LONG Zhi-qi, HUANG Xiao-wei, PENG Xin-lin, HAN Ye-bin, CUI Da-li. Rare earth distribution control during wet process of phosphoric acid production[J].Journal of the Chinese Rare Earth Society, 2008, 26(3): 307-312.
[25] Wirth F. Contribution to the chemistry and technology of thor and rare earth[J]. Journal of Inorganic Chemistry, 1912, 76(1): 174-200.
[26] Peacock R D, Weakley T J R. Heteropolytungstate complexes of the lanthanide elements. Part I. Preparation and reactions[J]. Journal of the Chemical Society A: Inorganic, Physical, Theoretical, 1971: 1836-1839.
[27] Keggin J F. Structure of the crystals of 12-phosphotungstic acid[J]. Nature, 1933(3331): 351.
[28] Pope M T, M��ller A. Polyoxometalate chemistry: An old field with new dimensions in several disciplines[J]. Angewandte Chemie International Edition, 1991, 30(1): 34-48.
[29] Pope M T. Polyoxometalates: From platonic solids to anti-retroviral activity: From platonic solids to anti-retroviral activity[M]. New York: Springer Science & Business Media, 1994: 1-40.
[30] Pope M T, M��ller A. Polyoxometalate chemistry from topology via self-assembly to applications[M]. New York: Springer Science & Business Media, 2001: 69-135.
[31] Peacock R D, Weakley T J R. Heteropolytungstate complexes of the lanthanide elements. Part II. Electronic spectra: A metal-ligand charge-transfer transition of cerium (��)[J]. Journal of the Chemical Society A: Inorganic, Physical, Theoretical, 1971: 1937-1940.
[32] LUO Qun-Hui, Howell R C, Dankova M, BARTIS J, WILLIAMS C W, HORROCKS W D, YOUNG V G, RHEINGOLD A L, FRANCESCONI L C, ANTONIO M R. Coordination of rare-earth elements in complexes with monovacant Wells-Dawson polyoxoanions[J]. Inorganic Chemistry, 2001, 40(8): 1894-1901.
[33] ZHANG C, Bensaid L, McGregor D, FANG Xi-kui, HOWELL R C, BURTON-PYE B, LUO Qun-hui, TODARO L, FRANCESCONI L C. Influence of the lanthanide ion and solution conditions on formation of lanthanide Wells�CDawson polyoxotungstates[J]. Journal of Cluster Science, 2006, 17(2): 389-425.
[34] Bartis J, Dankova M, Lessmann J J, LUO Qun-hui, HORROCKS W D, FRANCESCONI L C. Lanthanide Complexes of the ��-1 Isomer of the [P2W17O61]10- heteropolytungstate: Preparation, stoichiometry, and structural characterization by 183W and 31P NMR spectroscopy and europium(��) luminescence spectroscopy[J]. Inorganic Chemistry, 1999, 38(6): 1042-1053.
[35] Fedotov M A, Pertsikov B Z, Danovich D K. 17O, 31P and 183W NMR spectra of paramagnetic complexes with the heteropolytungstate anion [Ln(PW11O39)2]11- and their co[J]. Polyhedron, 1990, 9(10): 1249-1256.
[36] VanPelt C E, Crooks W J, Choppin G R. Stability constant determination and characterization of the complexation of trivalent lanthanides with polyoxometalates[J]. Inorganica Chimica Acta, 2003, 346: 215-222.
[37] Saito A, Choppin G R. Interaction of metal cations with heteropolytungstate ions SiW12O404- and P2W18O626-[J]. Inorganic Chemistry, 1991, 30(24): 4563-4566.
[38] Gschneidner K A, B��nzli J, PECHARSKY V K. Handbook on the physics and chemistry of rare earths(Volume 38)[M]. North-Holland: Elsevier, 2002: 337-375.
[39] Smith B J, Patrick V A. Quantitative determination of aqueous dodecatungstophosphoric acid speciation by NMR spectroscopy[J]. Australian Journal of Chemistry, 2004, 57(3): 261-268.
[40] Massart R, Contant R, Fruchart J M, FRUCHART J M, CIABRINI J P, FOURNIER M. Phosphorus-31 NMR studies on molybdic and tungstic heteropolyanions. Correlation between structure and chemical shift[J]. Inorganic Chemistry, 1977, 16(11): 2916-2921.
[41] Acerete R, Harmalker S, Hammer C F, POPE M T, BAKER L C W. Concerning isomerisms and interconversions of 2:18 and 2:17 heteropoly complexes and their derivatives[J]. Journal of the Chemical Society Chemical Communications, 1979, 17: 777-779.
Behavior of accompanying rare earth during process of decomposing scheelite by sulfuric-phosphoric mixed acid
GUO Fu-liang, CHEN Xing-yu, ZHAO Zhong-wei, HE Li-hua, YANG Kai-hua, YANG Zhen
(School of Metallurgy and Environment, Central South University, Changsha 410083, China)
Abstract: The thermodynamic equilibrium diagrams for the distribution of species of accompanying rare earth(REE) at different pH values, sulfuric and phosphorous acid concentrations were drawn at 25 ��. Using these diagrams, the technical methods for extracting rare earth and tungsten were found theoretically and tested by experiments. It appears that rare earth ions can be coordinated by phosphorous acid, sulfate anion or hereopolytungstate anion at different pH values. When the pH value is less than 1, rare earth ions coordinate with phosphorous acid or sulfate anion preferentially and transform to cation cluster. At the pH range of 1-3, rare earth ions coordinate with hereopolytungstate anion and transform to lanthanide containing anion cluster. These complexations are favorable to decompose rare earth minerals. The heteropoly acid can promote the decomposition of rare earth. When the mass fraction of WO3 and rare earths in scheelite are 26.11% and 0.13%, and the concentration of sulfuric and phosphoric acid are 2.5 and 1 mol/L, respectively, the leaching rates of La, Ce, Nd reach 85.61%��45.68% and 47.03% at 90 �� for 5 h. Besides, rare earth and tungsten also can be extracted separately or simultaneously as the species of complexations difference.
Key words: rare earths; scheelite; lanthanide containing hereopolytungstate anion; extraction; thermodynamics
Foundation item: Project(51334008) supported by the National Natural Science Foundation of China; Project (2015cx001) supported by the Innovation Driven Projects of Central South University, China; Project(2015BAB19B03) supported by the Shenghua Yuying Program of Central South University, China
Received date: 2016-11-29; Accepted date: 2017-04-24
Corresponding author: CHEN Xing-yu; Tel: +86-731-88830476; E-mail: xychen@csu.edu.cn
(�༭ ����)
������Ŀ��������Ȼ��ѧ�����ص���Ŀ(51334008)�����ϴ�ѧ���������ƻ�(2015cx001)�����ϴ�ѧ������Ӣ�ƻ�(2015BAB19B03)
�ո����ڣ�2016-11-29�������ڣ�2017-04-24
ͨ�����ߣ�����������ڣ���ʿ���绰��0731-88830476��E-mail: xychen@csu.edu.cn