WO3掺杂对MnOx/TiO2催化剂低温选择性催化还原NOx的影响
张亚平1, 汪小蕾1, 郑晓红1,宋正兴2,沈凯1,孙克勤1
(1. 东南大学 能源与环境学院 能源热转换及其过程测控教育部重点实验室,江苏 南京,210096;
2. 江苏亿金环保科技股份有限公司,江苏 无锡,214414)
摘要:采用一步浸渍法制备不同WO3含量的MnOx/WO3/TiO2催化剂,并采用XRD, BET, HRTEM, H2-TPR和in situ FTIR等技术进行表征。结果表明:适度添加WO3可以显著提高锰系催化剂的反应活性,其中15% MnOx/5%WO3/TiO2表现出了较好的低温活性,80~240 ℃的温度窗口内NOx转化率超过85%。添加5% WO3可以有效地提高活性物种的分散,大大降低H2的还原温度,有效地增强催化剂的氧化还原能力;增强催化剂的表面酸性,特别是 酸,并且出现活性中间物质―NH2,有利于SCR反应的进行。Mn物种主要以Mn2O3形式存在,但随着钨含量的增加,逐渐出现MnO2。在单独的NO气氛中时,NO会在催化剂表面氧化活性中心形成大量单齿和双齿配位型硝酸盐,占据在氧化活性中心上阻碍NH3的吸附和活化,对后续反应不利。
酸,并且出现活性中间物质―NH2,有利于SCR反应的进行。Mn物种主要以Mn2O3形式存在,但随着钨含量的增加,逐渐出现MnO2。在单独的NO气氛中时,NO会在催化剂表面氧化活性中心形成大量单齿和双齿配位型硝酸盐,占据在氧化活性中心上阻碍NH3的吸附和活化,对后续反应不利。
关键词:MnOx/TiO2;WO3掺杂;低温选择性催化还原;物理化学性质
中图分类号:O643 文献标志码:A 文章编号:1672-7207(2013)12-5165-08
Influence of WO3 doping on properties of MnOx/TiO2 catalyst for low-temperature selective catalytic reduction of NOx by NH3
ZHANG Yaping1, WANG Xiaolei1, ZHENG Xiaohong1, SONG Zhengxing2, SHEN Kai1, SUN Keqin1
(1.Key Laboratory of Energy Thermal Conversion and Control of Ministry of Education,School of Energy and Environment, Southeast University, Nanjing 210096, China;
2. Jiangsu Yijin Environmental Protection Equipment Engineering Co. Ltd., Wuxi 214414, China)
Abstract: Series of MnOx/WO3/TiO2 with different WO3 content were prepared by a one-step impregnation method and BET surface area measurement(BET), X-ray diffraction (XRD), H2-temperature programmed reduction (H2-TPR), High Resolution Transmission Electron Microscope (HRTEM), and in situ Fourier transform infrared spectroscopy (FT-IR) were employed to study their physico-chemisitry properties. It is found that the addition of appropriate amount of WO3 can improve remarkably the catalytic activity of Mn-based catalysts. Particularly, the 15% MnOx/5%WO3/TiO2 exhibites excellent low-temperature catalytic performance with above 85% NO conversion in the wide temperature range of 80-240 ℃. The combination of characterization techques indicate that the addition of 5% WO3 can effectively improve the dispersion of active components and the reducibility as well as enhance the amount and strength of the surface acid sites, especially the  acid sites, and promote the formation of the active intermediate (―NH2). Furthermore, manganese oxide existing in the form of Mn2O3 but MnO2 begin to appear and predominate with the WO3 increasing. A huge amount of monodentate and bidentate coordination nitrates are formed when the 5% WO3-doped catalyst is merely exposed to the pure NO,which occupy the active center of oxidation, thus impeding the absorption and activation of NH3. These materials are irreversible at the low-temperature window, hence blocking the follow-up reaction.
acid sites, and promote the formation of the active intermediate (―NH2). Furthermore, manganese oxide existing in the form of Mn2O3 but MnO2 begin to appear and predominate with the WO3 increasing. A huge amount of monodentate and bidentate coordination nitrates are formed when the 5% WO3-doped catalyst is merely exposed to the pure NO,which occupy the active center of oxidation, thus impeding the absorption and activation of NH3. These materials are irreversible at the low-temperature window, hence blocking the follow-up reaction.
Key words: MnOx/TiO2; WO3 doping; low-temperature SCR; physic-chemical properties
根据目前我国烟气排放状况,采用低温NH3-SCR技术便于和现有的锅炉系统相匹配,且可提高催化剂寿命,高效低废,易于推广。因此,研制开发与之相匹配的低温高效、性能稳定的SCR低温催化剂成为该技术研究领域的一大热点。MnOx中含有大量的晶格氧,有利于氧化-还原反应的进行,使其在低温SCR反应中具有很大的活性[1]。因此,近年来许多研究者致力于以MnOx作为低温SCR催化剂活性组分的研究。目前,低温MnOx基催化剂主要分为3类:一类是负载型锰基催化剂,主要有MnOx/TiO2[2-3],MnOx/Al2O3[4]和MnOx/USY[5](超稳定Y型分子筛),MnOx/AC[6],MnOx/ACF[7]等;一类为非负载型锰基催化剂,即通过某种前驱体直接获得的含锰的氧化物催化剂[8];还有一类双金属氧化物的锰基催化剂,如Cr-Mn[9],Cu-Mn[10],Fe-Mn[11]和Ce-Mn[12]等,利用2种金属氧化物的协同作用,获得低温SCR活性。WO3是中等强度的SCR催化剂,在商业催化剂中常用作助剂来提高催化剂的脱硝活性。研究发现,WO3可以稳定晶体结构,提高晶相转变温度,从而增强催化剂在制备过程中的高温稳定性[13];WO3还具有一定的抗SO2中毒作用[14]。低温催化剂虽然位于脱硫之后,但仍有少量SO2的存在,对MnOx催化剂有很大的毒害作用。本文作者曾对WO3对MnOx/TiO2催化剂的改性作用进行了系列研究,前期研究结果发现,采用一步浸渍法制备的锰钨催化剂显示了最佳的催化活性[15]。本文作者进一步研究不同WO3含量对MnOx/TiO2催化剂改性作用的影响,采用X线衍射(XRD)、比表面积测定(BET)、原位红外(in situ FT-IR)、高分辨率扫描电镜(HRTEM)程序升温还原(TPR)等技术考察不同含量的WO3掺杂对MnOx/TiO2催化剂的微观结构、表面性质和氧化还原特性的影响,并探讨催化剂物性与反应活性的关系。
1 实验
1.1 催化剂制备
按比例加入一定量水合钨酸铵溶于草酸溶液中,再加入一定量的醋酸锰溶解,在搅拌状态下将载体TiO2加入上述混合溶液。所得混合液在35 ℃下均匀搅拌2 h,再升温至85 ℃搅拌浸渍4 h,然后于110 ℃在烘箱中干燥12 h;取出研磨成粉末状,在马弗炉中450 ℃煅烧3 h。本文中MnOx的含量均为15%。
1.2 催化剂的表征
催化剂物相结构分析采用XRD-3型X线衍射分析仪(北京普析),X线波长λ为15 406 nm,Cu靶。催化剂样品在测试前需充分研磨,取适量粉体填充于玻璃载体上并压平,样品粉体厚度约1 mm;催化剂BET比表面积和孔径测定在F-Sorb3400比表面积分析仪(北京金埃谱)上进行,样品在200 ℃下抽真空预处理2 h,以N2为吸附质,在-196 ℃下进行测量;以NH3(或NO)分子作探针采用Nicolet 5700原位红外光谱仪(Thermo Electron 公司, 美国)以获得催化剂表面酸位、活性组分分散性等信息。波数范围为4 000~400 cm-1,分辨率4 cm-1;采用U型石英管反应器结合日本岛津(SHIMADZU) GC214C型气相色谱的TCD进行H2-TPR。在通入H2-Ar气氛之前,样品需要100 ℃下N2气氛中预处理1h,然后从室温开始以10 ℃/min速率加热到400 ℃;催化剂的形貌采用JEM-2100型透射电镜测定。催化剂样品在测试前均需充分研磨,然后放入乙醇溶液中,再将混合物在超声波下分散处理30 min,最后滴在铜网上放入烘箱中将其干燥。
1.3 催化性能测试
性能测试在不锈钢管式固定床SCR反应器中进行,内径为7 mm。催化反应器为外部电加热,由温控仪控制反应温度。试验采用标准钢瓶气模拟电厂烟气,烟气组成为ρ(NO)=ρ(NH3)=0.08%,ρ(O2)=5%,以N2为平衡气。空速比GHSV=24 000 h-1,总烟气流量为100 mL/min。各管路气体经质量流量计(北京汇博隆公司)进入气体混合器混合均衡后再进入反应器。每个工况稳定20 min。采用德国Testo 330-2 LL 烟气分析仪测量NO,NO2和O2的浓度。
2 结果与讨论
2.1 催化剂反应活性
图1所示为不同钨含量催化剂的NH3-SCR反应活性。由图1可看出:钨的添加量对改性催化剂的活性影响很大。随着钨含量的增加,三元复合催化剂的脱硝反应活性显著增加,当WO3的含量(质量分数)达到5%时候,改性后的催化剂反应活性远远高于单一活性组分的催化剂,NOx转化率为80%以上的温度窗口拓宽到了80~240 ℃,而后者仅仅在200 ℃时达到了80%。然而,当WO3含量增加到7.5%,反应活性反而急剧下降,仅仅在240 ℃以上活性达到80%。与前文研究相比[15],一步浸渍法制备的15%MnOx/5%WO3/TiO2催化剂具有最好的反应活性。
根据文献[17]可知:WO3表面有较多的Brφnsted酸位,在高温窗口显示较好的催化活性;而MnOx/TiO2表面有较多的Lewis酸位,比较适合在低温SCR中催化还原NO[3]。少量钨的添加可以增加NH3在催化剂上的吸附活性位及其吸附容量,提高催化剂在高温窗口的催化性能;然而大量添加钨氧化物,则覆盖了催化剂表面的MnOx活性中心,从而导致催化剂在低温阶段的反应活性大大降低,而高温窗口则由于WO3的存在反而增加了反应活性。
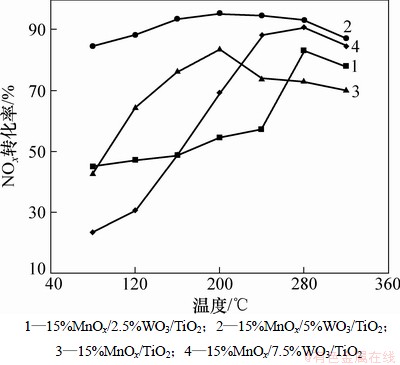
图1 不同锰氧化物催化剂NO+NH3+O2反应的催化活性
Fig. 1 Catalytic activity of MnOx-based catalysts for NO+NH3+O2 reaction
2.2 催化剂的微观结构
图2所示为载体及各种催化剂的XRD谱。相对TiO2载体的XRD谱而言,负载后的催化剂XRD谱中的TiO2特征峰均有弱化现象,可能是由于活性氧化物晶体或无定型晶相形成的杂峰覆盖在TiO2上。单纯添加MnOx与单纯添加WO3相比,XRD谱线比较类似,载体中微弱的金红石特征峰已无法检测出来(36.08°处);此外,前者的XRD谱线中TiO2特征峰弱化更加明显,可能是钨和锰氧化物的添加导致在催化剂表面形成多种钨氧化物无定型态覆盖物,并在载体特征衍射峰左右形成组群衍射峰使其弱化,且WO3对TiO2的改性还体现在稳定晶体结构提高晶相转变温度,故可阻止制备过程中锐钛矿晶相向金红石的转变[16]。
采用一步浸渍法将WO3和MnOx同时负载于载体之上,W对MnOx/TiO2催化剂的改性作用在XRD结果显示上不是特别明显,仅仅是TiO2特征峰的弱化程度稍稍减弱,且随WO3负载量的增加,系列15%MnOx/WO3/TiO2催化剂的衍射线杂乱程度有所提高,36.08°处的金红石峰逐渐显现。此外,谱图中无明显锰氧化物及钨氧化物的晶相存在,说明该二元金属氧化物均以无定形状态分散在TiO2载体上。
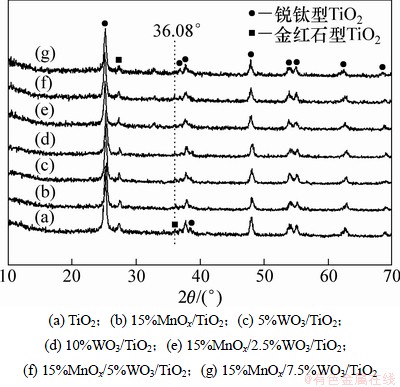
图2 载体和催化剂的XRD谱
Fig. 2 XRD patterns of catalysts and supports
表1显示了不同WO3含量催化剂和载体的比表面积。载体TiO2(P 25)的比表面积为55.3 m2/g,负载Mn以后,比表面积有所降低。结合XRD结果可知:经450 ℃煅烧后,催化剂表面无明显锰氧化物结晶生成,可推测MnOx呈无定形晶相并分散在载体TiO2的表面占据了原有的孔道使其比表面积降低。TiO2中负载5%WO3会使其比表面积增加至58.7 m2/g,继续增加负载量至10%则比表面积发生回落,可见低负载时少量WO3可提高载体结构复杂性并扩展比表面积,而负载量过大则会导致TiO2孔道的堵塞造成比表面积下降。以钨作为催化助剂,通过一步浸渍法与锰同时负载于载体TiO2上,在7.5%WO3负载范围内随负载量增大,其比表面积略有上升,可能由于多元金属氧化物同时负载有拓展表面积的作用。
为进一步研究钨改性对催化剂微观形态的影响,对15%MnOx/5%WO3/TiO2催化剂和TiO2载体进行了HRTEM分析和电子衍射分析,结果如图3和4所示。
表1 催化剂和载体的BET比表面积
Table 1 BET surface area and average diameter measurements of support and catalysts
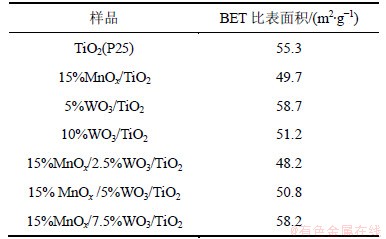

图3 催化剂和载体HRTEM图谱比较
Fig. 3 Comparison of HRTEM graphs of catalyst and support

图4 催化剂和载体电子衍射图像比较
Fig. 4 Comparison of electron diffraction images of catalyst and support
可以看出:15%MnOx/5%WO3/TiO2催化剂基本呈球形颗粒状,平均直径约为17 nm,分散性很好,与XRD分析结果比较接近,故颗粒间基本不存在硬团聚,少部分存在轻微的团聚,但颗粒之间有明显的界限,属于软团聚体。比较而言,TiO2载体粒径较大,平均粒径为24 nm,颗粒间硬团聚较多。
15%MnOx/5%WO3/TiO2催化剂和TiO2载体的电子衍射像见图4。可见二者均呈现为微晶的衍射光斑,但是前者显示了更清晰弥散的同心圆光斑及加深的光晕,表明15%MnOx/5%WO3/TiO2催化剂有着较强的多晶和非晶性质。
2.3 氧化还原分析
图5所示为系列钨改性催化剂H2-TPR谱,表2显示了采用Gaussian-Lorentz方法对催化剂TPR谱各还原峰进行定量化分析的结果。改性前15%MnOx/TiO2催化剂存在2个还原峰,分别位于325 ℃及419 ℃处,前者可能对应于还原过程Mn2O3→ Mn3O4,峰形较弱,后者为Mn3O4→MnO [17]。低温还原峰可归属为表面氧(α氧)脱除,高温为MnOx体相晶格氧(β氧)脱除。文献[18]表明,α氧是氧化-还原过程中主要的活性氧[18]。
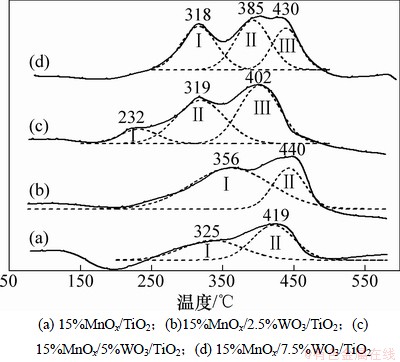
图5 钨改性催化剂H2-TPR谱
Fig. 5 TPR profile of WO3-modified catalyts
改性催化剂MnOx/WO3/TiO2的H2-TPR谱随着钨含量的不同呈现不同的形态。少量的钨添加导致催化剂的还原温度增加,但是仍然呈现出2个还原峰;随着钨含量掺杂到5%,催化剂出现了3个还原峰,分别位于232,319和402 ℃,对应于锰氧化物的3个还原过程,即MnO2→Mn2O3→Mn3O4→MnO[17]。还原峰总面积相对于改性前催化剂大大提高,且还原峰向低温移动;然而,当催化剂中的钨含量达到了7.5%,仍然出现了3个还原峰,但是还原温度均移向了高温,说明添加适量钨的添加可以改变锰系催化剂的锰物种的存在形态和还原行为。通过分析表2显示的各催化剂还原峰的面积和H2/Mn,可以得出,对于低含量的钨改性催化剂和锰钛催化剂,锰物种主要以Mn2O3的形式存在;而对于5%钨改性催化剂,锰物种虽仍主要以Mn2O3为主,但少量存在MnO2;而对于高钨含量的催化剂,锰物质以MnO2形式存在为主。
表2 催化剂 H2-TPR谱分析结果
Table 2 Peak information of H2-TPR results
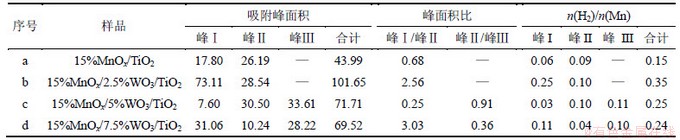
相对于15%MnOx/TiO2,3种改性催化剂的总还原面积均有所增加,说明改性催化剂总体还原能力有所增强,但是,除了15%MnOx/5%WO3/TiO2样品外,第1个还原峰温度均出现在300 ℃以后,表明其他2种改性催化剂的低温还原能力有所降低,但是高温还原性有所增强,这与催化性能测试的结果比较一致。
2.4 表面酸位分析
图6所示为25 ℃时经过N2预处理的2种催化剂对NH3吸附的原位红外谱。由图6可以看出:NH3在酸性催化剂表面吸附后,既出现NH3在Lewis酸中心的吸附峰,又有NH3在 酸中心的吸附峰,2种催化剂的吸附峰大致相同。25 ℃时NH3在MnOx/TiO2上吸附后,在1 614 cm-1处出现相对较强的吸附峰,在1 454和1 168 cm-1处出现较弱的吸收峰,其中1 614和1 168 cm-1处的峰归属于Lewis酸中心吸附的NH3中N―H键的简并伸缩振动,1 454 cm-1处的吸收峰为催化剂表面
酸中心的吸附峰,2种催化剂的吸附峰大致相同。25 ℃时NH3在MnOx/TiO2上吸附后,在1 614 cm-1处出现相对较强的吸附峰,在1 454和1 168 cm-1处出现较弱的吸收峰,其中1 614和1 168 cm-1处的峰归属于Lewis酸中心吸附的NH3中N―H键的简并伸缩振动,1 454 cm-1处的吸收峰为催化剂表面 酸中心的吸附的NH4+中N―H键的变形振动δas(NH4+)[19-21]。
酸中心的吸附的NH4+中N―H键的变形振动δas(NH4+)[19-21]。
当采用一步浸渍法改性后,催化剂MnOx/WO3/TiO2的NH3吸附FT-IR谱图峰位置无变化,但1 614 cm-1和1 454 cm-1吸附峰明显增强,故可初步推测经改性后的催化剂对NH3的吸附活性位点增多,NH3吸附容量增大,其中 酸位发挥主要作用,这与WO3有较强的
酸位发挥主要作用,这与WO3有较强的 酸性相吻合;1 527 cm-1以较小的肩峰形式呈现,属于―NH2活性物种[22]。很多研究表明[23-24],―NH2是锰系催化剂低温SCR反应的重要活性中间物质。在因此,一步浸渍法不仅是对催化剂传统制备工艺进行了简化,而且得到的催化剂表面酸的NH3吸附容量大幅度上升,并且形成了―NH2活性物种,这样预示着其具有较高的SCR活性。
酸性相吻合;1 527 cm-1以较小的肩峰形式呈现,属于―NH2活性物种[22]。很多研究表明[23-24],―NH2是锰系催化剂低温SCR反应的重要活性中间物质。在因此,一步浸渍法不仅是对催化剂传统制备工艺进行了简化,而且得到的催化剂表面酸的NH3吸附容量大幅度上升,并且形成了―NH2活性物种,这样预示着其具有较高的SCR活性。
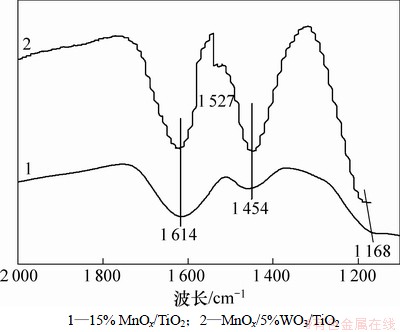
图6 25 ℃时15%MnOx/TiO2 和15%MnOx/5%WO3/TiO2氨气吸附红外光谱
Fig. 6 Ammonia adsorption FT-IR spectra of 15%MnOx/TiO2 and 15% MnOx/5%WO3/TiO2 at 25 ℃
为进一步比较钨改性对锰钛催化剂的低温NH3表面吸附反应情况,分析了随温度变化的NH3吸附的原位红外图谱,结果见图7。对于2种催化剂,随着温度的升高,NH3吸收峰的强度都有所下降,特别是 酸位上的吸收峰(1 454 cm-1)。当温度升高到300 ℃以上时,仅仅能观察到微弱的Lewis酸(1 614和1 168 cm-1处),
酸位上的吸收峰(1 454 cm-1)。当温度升高到300 ℃以上时,仅仅能观察到微弱的Lewis酸(1 614和1 168 cm-1处), 酸位已经完全消失。然而,当温度升高到200 ℃时,在15%MnOx/5%WO3/TiO2催化剂表面检测到了微弱的吸收峰(1 527 cm-1)。由前文分析可知,此吸收峰属于―NH2活性物种。此时,Lewis酸位已经变得极其微弱,几近消失。因此,可以推断,该活性物种是吸附在Lewis酸位的NH3(δs(NH3))的解析产物。
酸位已经完全消失。然而,当温度升高到200 ℃时,在15%MnOx/5%WO3/TiO2催化剂表面检测到了微弱的吸收峰(1 527 cm-1)。由前文分析可知,此吸收峰属于―NH2活性物种。此时,Lewis酸位已经变得极其微弱,几近消失。因此,可以推断,该活性物种是吸附在Lewis酸位的NH3(δs(NH3))的解析产物。
由此可知:低温下NH3在催化剂表面以NH4+和配位态的NH3 2种形式存在,催化剂表面同时存在Lewis酸和 酸位中心;高温下(≥300 ℃)只存在配位态的NH3,表明低温时催化剂表面Lewis酸和
酸位中心;高温下(≥300 ℃)只存在配位态的NH3,表明低温时催化剂表面Lewis酸和 酸对反应同时起作用,而在高温时,只有Lewis酸对反应起作用。
酸对反应同时起作用,而在高温时,只有Lewis酸对反应起作用。
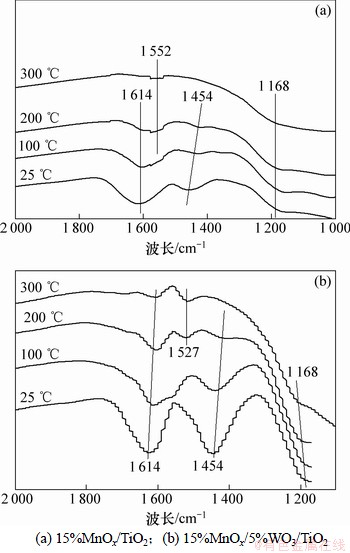
图7 不同温度下NH3 吸附红外光谱
Fig. 7 In situ NH3 adsorption FT-IR spectra at different temperatures
2.5 催化剂的NO吸附性能
图8所示为NO在15%MnOx/5%WO3/TiO2催化剂表面上的吸附时间。原样品在100 ℃下用N2吹扫1 h后,回到室温状态,缓慢通入NO,饱和后用N2吹扫并采集谱图。由图8可见:相比较预处理后的原样品红外谱,吸附NO后的催化剂原位红外谱在1 630 cm-1处附近出现加强吸收峰,1 490~1 330 cm-1处出现较强的宽峰。结合文献[25-26]研究结果,1 630 cm-1处吸收峰归属为桥式硝酸盐物种,而附近1 620 cm-1处被覆盖的吸收峰则属于催化剂表面弱吸附的NO2分子的反对称振动,1 520 cm-1处吸收峰归属为桥式硝基亚硝酸盐物种,NO在催化剂表面形成的双齿硝酸盐则体现在1 530 cm-1处被周边峰平化的吸收峰,1 490~1 330 cm-1处为单齿亚硝酸盐物种吸收峰。说明在常温下,NO在MnOx/WO3/TiO2催化剂上主要存在形式为单齿亚硝酸盐、双齿硝酸盐、桥式硝酸盐、桥式硝基亚硝酸盐和表面吸附。
图9所示为不同温度下15%MnOx/5%WO3/TiO2催化剂表面上的NO吸附谱。逐步升高温度并用N2吹扫,1 630 cm-1及1 620 cm-1处吸收峰很快减弱或消失,验证1 620 cm-1处为弱吸附的NO2物种,而1 630 cm-1处的桥式硝酸盐物种峰随温度上升逐渐减弱,由于原样品在此处存在背景吸收峰,故峰形并未完全消失。1 530 cm-1处代表的双齿硝酸盐物种峰随温度上升强度降低较慢,具有较高的热稳定性,但该峰所属物种不利于催化剂的NH3-SCR反应。1 490~1 330 cm-1处所代表的单齿亚硝酸盐物种吸收峰随温度上升迅速减弱,100 ℃时即大大消弱。1 300 cm-1处吸收峰因温度的上升凸显出来,该峰归属于双齿硝酸盐,200 ℃之后才逐渐消失,可见双齿硝酸盐是主要的不利于催化反应的结合产物,且在低温下难以脱附。
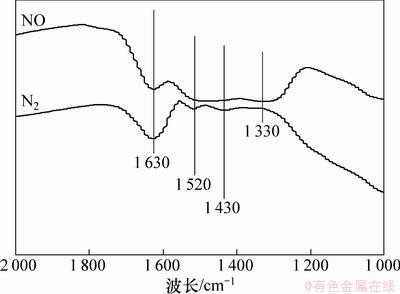
图8 100 ℃时NO在15% MnOx/5% WO3/TiO2催化剂上的吸附状态
Fig. 8 In situ NO adsorption FT-IR spectra of 15%MnOx/5%WO3/TiO2 at 100 ℃
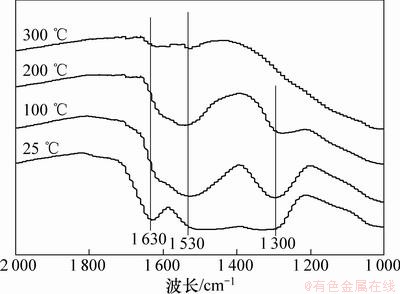
图9 不同温度下的15%MnOx/5%WO3/TiO2催化剂NO吸附原位红外谱
Fig. 9 In situ NO adsorption FT-IR spectra of 15% MnOx/5%WO3/TiO2 at different temperatures
3 结论
(1) 适度添加WO3可以显著提高锰系催化剂的反应活性,其中含有5%WO3的催化剂表现出了较好的低温活性,添加过量和过少均导致催化剂的活性呈现不同程度的下降趋势。
(2) 添加5%WO3可以有效的提高活性物种的分散,催化剂具有较大的比表面积和较小的粒径,催化剂程序球形颗粒,分散良好,有着较强的多晶和非晶性质。
(3) 适量添加WO3不仅大大降低了锰基催化剂的还原温度,有效增强了催化剂的氧化还原能力,并改变了催化剂表面锰物种的存在形式。钨改性和低钨含量的锰催化剂中,Mn物种主要以Mn2O3形式存在,但是在钨中高含量的催化剂中,锰物种逐渐向MnO2转换。
(4) 15%MnOx/5%WO3/TiO2催化剂表面 酸位和Lewis酸位均得到大幅度增加,并且出现了活性中间物种-NH2,有利于SCR反应的进行。NO吸附的红外反应表明,当该催化剂在单独的NO气氛中时,NO会在催化剂表面氧化活性中心形成大量单齿和双齿配位型硝酸盐,此类硝酸盐在低温下不可逆转,占据在氧化活性中心上阻碍NH3的吸附和活化,对后续反应不利。
酸位和Lewis酸位均得到大幅度增加,并且出现了活性中间物种-NH2,有利于SCR反应的进行。NO吸附的红外反应表明,当该催化剂在单独的NO气氛中时,NO会在催化剂表面氧化活性中心形成大量单齿和双齿配位型硝酸盐,此类硝酸盐在低温下不可逆转,占据在氧化活性中心上阻碍NH3的吸附和活化,对后续反应不利。
参考文献:
[1] Morales M R, Barbero B P, Cadus L E. Combustion of volatile organic compounds on manganese iron or nickel mixed oxide catalysts[J]. Applied Catalysis B:Environment, 2007, 74(1/2): 1-11
[2] Ettireddy R P, Ettireddy N, Mamedov S, et al. Surface characterization studies of TiO2 supported manganese oxide catalysts for low temperature SCR of NO with NH3[J]. Applied Catalysis B: Environment, 2007, 76(1/2): 123-134
[3] 黄海凤, 张峰, 卢晗锋, 等. 制备方法对低温NH3-SCR脱硝催化剂MnOx/TiO2结构与性能的影响[J]. 化工学报, 2010, 61(1): 80-85.
HUANG Haifeng, ZHANG Feng, LU Hanfeng, et al. Effect of preparation methods on structures and performance of MnOx/TiO2 catalyst for low-temperature NH3-SCR[J]. Journal of Chemical IndustryandEngineering (China), 2010, 61(1): 80-85.
[4] Kijlstra W S, Poels E K, Bliek A. Characterization of Al2O3-supported manganese oxides by electron spin resonance and diffuse reflectance spectroscopy[J]. Journal of Physical Chemistry B, 1997, 101(3): 309-316.
[5] QI Gongshin, Yang R T, Ramsay C. Low-temperature SCR of NO with NH3 over USY-supported manganese oxide-based catalysts[J]. Catalysis Letters, 2003, 87(1/2): 67-71.
[6] ZHU Zhenping, LIU Zhenyu,LIU Shoujun, et al. Catalytic NO reduction with ammonia at low temperatures on VZOs/AC catalysts: Effect of metal oxides addition and SO2[J]. Applied Catalysis B: Environment, 2001, 30(1): 267-276.
[7] Yoshikawa M, Yasutake A, Mochida I. Low-temperature selective catalytic reduction of NOx by metal oxides supported on active carbon fibers[J]. Applied Catalysis A:General, 1998, 173(2): 239-245.
[8] Kapteijn F, Singoredjo L, Andreini A. Activity and selectivity of pure manganese oxides in the selective catalytic reduction of nitric oxide with ammonia[J]. Applied Catalysis B:Environment,1994, 3 (2/3): 173-189.
[9] CHEN Zhihang,LI Xuehui,GAO Xiang, et al. Selective catalytic reduction of NOx with NH3 on a Cr-Mn mixed oxide at low temperature[J]. Chinese Journal of Catalysis, 2009, 30(1): 4-6.
[10] Kangv M, Park E D, Kim J M, et al. Cu-Mn mixed oxides for low temperature NO reduction with NH3[J]. Catalysis Today, 2006, 111( 3/4): 236-241.
[11] Huang Helen Y, Yang Ralph T. Removal of NO by reversible adsorption on Fe-Mn based transition metal oxides[J]. Langmuir, 2001, 16(17): 4997-5003.
[12] Qi G S,Yang R T. Characterization and FTIR studies of MnOx-CeO2 catalyst for low-temperature selective catalytic reduction of NO with NH3[J]. Journal of Physical Chemistry B, 2004, 108(40): 15738-15747.
[13] Nova L, Lietti E, Tronconi E, et al. Dyanmics of SCR reaction over a TiO2-supported vanadia-tungsta commercial catalysts[J]. Catalysis Today, 2000, 60(1/2): 73-82.
[14] Chen J P, Yang R T. Role of WO3 in mixed V2O5-WO3/TiO2 catalysts for selective catalytic reduction of nitric oxide with ammonia[J]. Applied Catalysis A: General, 1992, 80(1/2): 135-148.
[15] ZHANG Yaping, WANG Xiaolei, SHEN Kai, et al. WO3 Modification of MnOx/TiO2 catalysts for low temperature selectivecatalytic reduction of NO with ammonia[J]. Chinese Journal of Catalysis, 2012, 33(9): 1521-1531.
[16] Kenevey K,Morris M A,Cunningham J, et al. Stabilization of anatase by tungsten introduced to the titania lattice by sol-gel and impregnation techniques[C]//McHugh P E. Frontiers for Engineering Materials. Germany: Trans Tech Publications, 1996: 303-310.
[17] Ettireddy P R, Ettireddy N, Mamedov S, et al. Surface characterization studies of TiO2 supported manganese oxide catalysts for low temperature SCR of NO with NH3[J]. Applied Catalysis B: Environment, 2007, 76(1/2): 123-134.
[18] FENG Shaojie, YI Jianxin. TPD/TPR investigation of the stabilization of Fe doping for SrCoO3-δ[J]. Journal of Anhui Institute of Architecture & Industry, 2006, 14(2): 45-48.
[19] Gutierrez-Alejandre A, Ramirez J, Busca G. A vibration and spectroscopic study of WO3/TiO2-Al2O3 catalyst precursors[S]. Langmuir, 1998, 14(3): 630-639.
[20] Larrubia M A, Ramis G, Busca G. An FT-IR study of the adsorption of urea and ammonia over V2O5-MoO3-TiO2 SCR catalysts[J]. Applied Catalysis B: Environment, 2000, 27(3): 145-151.
[21] Busca G,Ramis G,Amores J M G, et al. An FT-IR study of ammonia adsorption and oxidation over anatase-supported metal oxides[J]. Applied Catalysis B: Environment, 1997, 13(1): 45-58.
[22] Ramis G, Busca G, Bregani F, et al. Fourier transform-infrared study of the adsorption and coadsorption of nitric oxide, nitrogen dioxide and ammonia on vanadia-titania and mechanism of selective catalytic reduction[J]. Applied Catalysis, 1990, 64(1/2): 259-278.
[23] Qi G S,Yang R T,Chang R. MnOx-CeO2 mixed oxides prepared by co-precipitation for selective catalytic reduction of NO with NH3 at low temperatures[J]. Applied Catalysis B: Environment, 2004, 51(2): 93-106.
[24] Kapteijn F, Singoredjo L,Andreini A, et al. Activity and selectivity of pure manganese oxides in the selective catalytic reduction of nitric-oxide with ammonia[J]. Applied Catalysis B:Environment, 1994, 3(2/3): 173-189.
[25] Marbán G, Solís T V, Fuertes A B. Mechanism of low-temperature selective catalytic reduction of NO with NH3 over carbon-supported Mn3O4 role of surfaces NH3 species: SCR mechanism[J]. Journal of Catalysis, 2004, 226(1): 138-155.
[26] Topsoe N Y, Topsoe H, Dumesic J A. Vanadia-Titania catalysts for selective catalytic reduction (SCR) of Nitric-Oxide by ammonia.1.combined temperature-programmed in-situ FT-IR and online mass-spectroscopy studies[J]. Journal of Catalysis, 1995, 151(1): 226-240.
(编辑 陈爱华)
收稿日期:2013-02-15;修回日期:2013-05-09
基金项目:江苏省自然科学基金资助项目(BK2012347);江苏省科技支撑计划项目(BE2012817);国家重点基础研究发展规划项目(2013CB228505)
通信作者:张亚平(1979-),女,河南驻马店人,副教授,从事大气污染控制研究;电话:025-83790667;E-mail:amflora@seu.edu.cn