V(��)/V(��)�����ʯīձ�缫�ϵķ�Ӧ����
�ƿ���1, ̷ ��1, ������1, ������1, ��־��2
(1. ���ϴ�ѧ ��ѧ����ѧԺ, ��ɳ, 410083; 2. ��֦�������о�Ժ, �ɶ� 610000)
ժ Ҫ: ����ѭ�������� �������ߺͽ����迹���ֵ绯ѧʵ�鷽���о���V(��)/V(��)�����ʯīձ�缫�ϵķ�Ӧ����������ܵ��ٶȿ��Ʋ��衣 �о��������: V(��)/V(��)�����ʯīձ�缫�ϵķ�Ӧ���������, ���������̰����к��û�ѧת������; ���ۼ���õ��˵绯ѧ����ͺ��û�ѧת�����̷ֱ�Ϊ���Ʋ���ʱ��Tafelб��ֵΪ0.12��0.06, ʵ��õ���Tafelб��ֵΪ0.124, �����缫���������ܵ绯ѧ���̿���; ��ͬ������λ�µĽ����迹ͼ����Ͻ������, �绯ѧ��Ӧ�迹ֵԶ���������迹ֵ, ˵���绯ѧ��Ӧ�����ǵ缫��Ӧ�Ŀ��Ʋ���, ��ʵ��õ��ļ������߷��������һ�¡�
�ؼ���: �����; ʯīձ; V(��)/V(��); �ٶȿ��Ʋ��� ��ͼ�����: O646.5
���ױ�ʶ��: A
Reaction mechanism of V(��)/ V(��) redox couple at graphite felt electrode
HUANG Ke-long1, TAN Ning1, LIU Su-qin1, LI Xiao-gang1, CHANG Zhi-feng2
(1. School of Chemistry and Chemical Engineering,Central South University, Changsha 410083, China;
2. Steel Institute of Panzhihua, Chengdu 610000, China)
Abstract: The V(��)/V(��) reaction mechanism was investigated on a graphite felt electrode by means of cyclic voltammetry, polarization curve and impedance spectroscopies. Cyclic voltammetry analysis indicates that V(��)/ V(��) redox reaction at graphite felt electrode is quasi reversible. A certain chemical reaction step is suspected to follow the electron transfer step of this reaction. The Tafel slope value (0.124) obtained from the polarization curve agrees well with theoretical value (0.12) when the electron transfer step is supposed to be the rate determining step. Impedance spectroscopies at various potentials were studied and simulated by equivalent circuits. The impedance value of the electron transfer step modified is greatly higher than the others, which shows that the electron transfer step is the rate determining step. This further confirms the conclusion obtained by polarization curve test.
Key words: vanadium redox battery; graphite felt; V(��)/V(��); rate determining step
��Skyllas-Kazacos��[1]�о�����һ����������ԭҺ�������֮��, ��ɫ��Һ�����������صļ�������[2-4]�����ڶ��ѧ�о��ߵĹ�ע�� Ŀǰ, ��������ԭҺ������Ѿ��ڷ��ܡ� ̫���������Լ��������巽��ȡ���˳ɹ�Ӧ��[5-7]�� �����ڵ������Һ�����Ӵ�����̬�ĸ����ԺͲ��ȶ���, �Լ����Ӵ�����̬��绯ѧ�Ĺ����Ե�������δ��ʶ���, ���Թ��ڵ缫��Ӧ�Ļ����о��Ժܱ����� Sum[8]����ѭ������������תԲ�̵缫������V(��)/V(��)����ڲ�̼�缫�ͽ�缫�ϵĵ绯ѧ��Ϊ�� Zhong��[9]�о���V(��)/V(��)�����ʯī�缫�ϵĵ绯ѧ��Ϊ, ָ��V(��)���������̺�V(��)�Ļ�ԭ�����кܴ�IJ�ͬ, �õ���V(��)����ɢϵ���Լ������ʯī�缫��ʯīձ�缫�ϵIJ��ֶ���ѧ������ ���Oriji��[10]���ö��ֵ绯ѧ�����о���V(��)/V(��)����ڲ�̼�缫�ϵ���Ϊ, ָ���õ�Ե������ͻ�ԭ���̶����Ǽ�ɴ��ݷ�Ӧ, �������漰����ԭ�Ӵ��ݵĺ��û�ѧת�����̡� Gattrell��[11]��������������ϸ�о���V(��)/V(��)�ķ�Ӧ����, ָ�����ڵ���λ������CECģ��, �߹���λ������ECCģ�͡� ������V(��)/V(��)��Ӧ�����п��ܵĿ��Ʋ����Լ��÷�Ӧ�Ľ����迹���Եȷ�����о����١� ��������ǰ���о�[12, 13]��Ҫ��������V(��)/V(��)�ڸ���缫�ϵĵ绯ѧ����, �������о��õ缫��Ӧ�Ķ���ѧ����, ��Ϊ��һ����ߵ缫�����ṩ�������ݡ� Ϊ��, �������߽���ѭ�������� �������ߺͽ����迹3�ֵ绯ѧ���Է�����V(��)/V(��)�����ʯīձ�缫�ϵķ�Ӧ����������ܵĿ��Ʋ���������о���
1 ʵ��
ʵ������Ϻ�����̼������˾�ľ۱�ϩ���(PAN)ʯīձ, �ȼ�Ϊ��������
���������ʯīձ�ü���ͬ����С����Ʒ, ��������ˮ������ϴ, ��������ո������ں��, ȡ����һ����ʯ���ܷ�, �����缫��Ӧ���Ϊ1cm��1.5cm, �Ƴ�ʵ���õ缫��
��������V2O5��һ�������Ũ������, ͨ�������ܽ⡢ ����, �õ������VOSO4������Һ�� V(��)��Һ���Ʊ����õ�ⷨ�õ��� ��ʯīձ���缫�� ���ӽ���Ĥ����Ĥ�� ����VOSO4��ҺΪ���Һ, ��װ�ɵ�ؽ��г��, ������ʱ�������õ�����Һ��Ϊ�ϴ���V(��)��Һ�� ���������õ�V(��)��V(��)�Ĵ���Һ��������ϲ�ϡ�͵õ�����ĵ��Һ��
���Һ�з�����Ũ�ȵķ��������Զ���λ�ζ���������-�ɼ��ֹ��ȷ������ֶν��в��ԡ� ��λ�ζ������Ƚ�������ȫ��������V(��), �ٵμӻ�ԭ�����л�ԭ, ��V(��)��V(��)�ĵ�λͻ���Ϊ�ζ��յ㡣 �ֹ��ȷ�������ͨ����������V(��)��V(��)������ȡ�Ũ�ȵı�����, �ٸ��ݴ�����Һ�������, �ɱ�������������ӵ�Ũ�ȡ� ������Ƚ�, ������5%��
�Բ��缫Ϊ�Ե缫, ���ʹ��缫Ϊ�αȵ缫, ͨ��³��ëϸ��������缫��ϵ����ѭ�������� �������ߺͽ����迹�ĵ绯ѧ���ԡ�
ѭ���������Ե�ɨ���ٶȷ�ΧΪ10~0.2mV/s, �绯ѧ�������߲��Ե�ɨ���ٶ�Ϊ1mV/s, ���������þ�Ϊ10-6, �����迹����ǰ, ����5��ѭ������ɨ�衣
���еĵ绯ѧ���Ծ���CHI660B�͵绯ѧ����վ�Ͻ���, �����迹���ݵ���Ͻ���ZsimpWin 3.20 Demo�������С�
2 ���������
2.1 ѭ����������
��ͬɨ��������, V(��)/V(��)�����ʯīձ�缫�ϵ�ѭ������������ͼ1��ʾ�� ���ڲ��õ�ʯīձ�缫����Һ�����γɵ�˫�����ݽϴ�, ������ϡ�ķ���Һ��, ��ɨ�����ʳ���10mV/sʱ, ����ɨ�����ᷢ�����䵼������÷����ֵ�ͷ����ֵ�� ��˱�ʵ���ɨ�����ʷ�Χ��10~0.2mV/s֮��, ����һ��ʵ��IJ�����Χ�� ��ͼ1 �ɿ���, �õ缫��Ӧ������ȫ���淴Ӧ, ��Ϊ������ԭ���λ��(��pa-��pc)����60mV, ��ʹ��ɨ��������СΪ0.2mV/sʱ, ���λ������100mV�� �ӱ����Ͽ�, ��������״�϶Գ�, Ҳ������ȫ��������ϵ��
ͼ2��ʾΪѭ���������ߵ������������ɨ�����ʵĹ�ϵ�� ��ͼ�ɼ�, ������ֵ������ɨ�����ʵ����Ӷ�����, ����v1/2�����ϸ�ı�����ϵ, ��
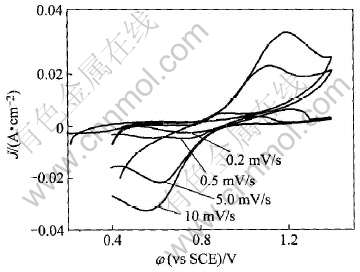
ͼ1 ��ͬɨ��������ʯīձ�缫��0.0087mol/L V(��)+ 0.0087mol/L V(��)+1mol/L H2SO4���Һ�е�ѭ������ͼ
Fig.1 Cyclic voltammograms for V(��)/V(��) reaction on graphite felt electrode in 0.0087mol/LV(��) +0.0087mol/L V(��)+ 1mol/L H2SO4 solution at various scan rates
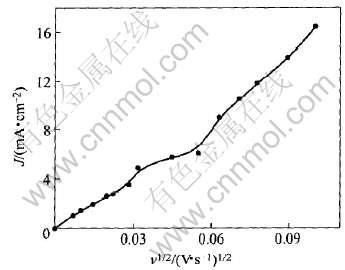
ͼ2 �����������ɨ�����ʵĹ�ϵ
Fig.2 Peak current density as function of square root of scan rate for V(��) oxidation
�����ӽ��������, �������ӽ������������ �����ж�V(��)/V(��)�����ʯīձ�缫�ϵķ�Ӧ����Ϊ������̡�
ɨ����Ʒ����жϰ����л�ѧת���ĸ��ӷ�Ӧ���͵���֮��Ч�ķ���֮һ�� �������߶�ѭ���������ݽ��д���, �õ�ɨ������������ƺ���(����1/2/��lgv)�Ĺ�ϵ(ͼ3), ��ͼ3��ʾ�� ��ͼ�ɿ���, ��������ɨ�����ʵ����ӳ���������, ���ݰ����о���ת����Ӧ�ĵ缫��Ӧ����[14], ��֪�õ缫��Ӧ����EC����, �����˺���ת������, ����Oriji��[10]�ı���һ�¡�
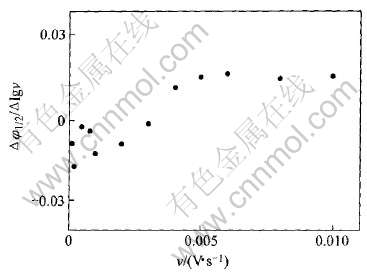
ͼ3 V(��)���������λ��ɨ�����ʵĹ�ϵ
Fig.3 Half wave potential density as function of scan rate for V(��) reaction
2.2 �������߷���
��ʵ��ⶨ��̬�������߷����õ��ĵ缫���ƺ͵����ܶ�֮��Ĺ�ϵ�Ƿ�����ȷ���缫��Ӧ���Ʋ����һ�ּ�����Ч�ķ����� ��������ѭ�������ķ���, V(��)/V(��)��������Ӧ������һ���ĺ��û�ѧת������, ���Gattrell��[11]���о�����, ��д����������Ӧ��������:
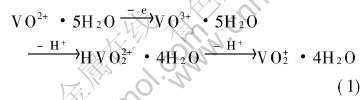
�ٶ���V(��)�����Ĺ�����, �绯ѧ����Ϊ������Ӧ���ٶȿ��Ʋ���, ʯīձ��缫�ϴ���绯ѧ����ʱ����̬�������߹�ʽΪ

����ʽ(2)��д����Ia��i0ʱ�Ķ���ѧ����Ϊ
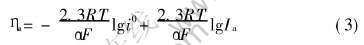
��ͬ�缫��Ӧ�Ĵ���ϵ���������в�ͬ��ֵ, ��һ��Ӧ�Ц���0.5�� ����ʽ����������Ե绯ѧ����Ϊ�ٶȿ��Ʋ����V(��)������Ӧ�ļ������ߵ�б��ԼΪ
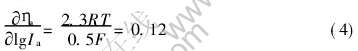
ʵ��õ���ʯīձ�缫�ڷ���Һ�еļ���������ͼ4��ʾ�� �ûع鷽��[15]�õ�����Tafelб��Ϊ0.124, ��һ��ֵ�����������Ʋ�Ľ�����������
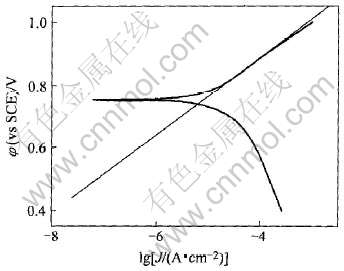
ͼ4 ʯīձ�缫����Һ�еļ�������(1mV/s)
Fig.4 Polarization curve at graphite felt electrode in 0.03mol/L V(��)+ 0.03mol/L V(��)+3mol/L H2SO4
����ٶ����õĻ�ѧת������Ϊ�ٶȿ��Ʋ���, �Ҽ���ʱ�绯ѧ�����ƽ��δ���ƻ�, ��ǰ������Nernst��ʽ�������缫������缫���淴Ӧ����Ũ��֮��Ĺ�ϵ�� ������ѧת��������κ�һ��Ϊ���Ʋ���ʱЧ������ͬ, �����Ե�һ��ת��Ϊ����
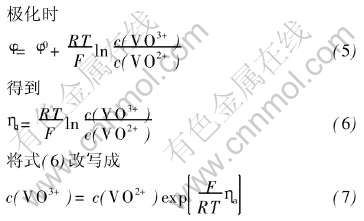
����ѧת�����̳�Ϊ������Ӧ�Ŀ��Ʋ���ʱ, ������Ӧ�ٶȿɱ�ʾΪ
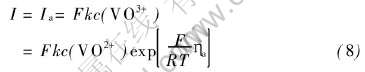
ʽ�� kΪ��Ӧ�ٶȳ����� ���ڻ�ѧת�����̲��漰��ɴ���, ��˷�Ӧ�ٶȳ���kӦ��缫�����ء� ʽ(8)�ɸ�дΪ
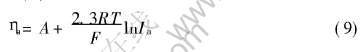
ʽ�� AΪ������
�ڴ�����µ缫����������ܶȵ�Tafelб��Ϊ0.06, ��V(��)������Ӧ������������ߵ�ʵ��б��ֵ���ϴ�
�����Ϸ������Կ���, ֻ�мٶ��绯ѧ����Ϊ�ٶȿ��Ʋ���, �������İ�����������ߵ�б�ʲ���ʵ�����ֵ�Ƚ����, ����V(��)��ʯīձ��缫�ϵ�������Ӧ�������ٶȿ��Ʋ������п�����VO2+����ֱ�Ӳ���ĵ绯ѧ���衣
2.3 �����迹����
ͼ5��ʾΪʯīձ�缫�ڲ�ͬ������λ�µĽ����迹�ס� ��ͼ�ɼ�, �ڲ�����Χ�ھ�������������С��ͬ�İ�Բ����һ��ֱ�ߡ� �ڲ�ͬ�ļ�����λ��, ��Ƶ���İ�Բ�仯����, ���迹���ɶ�缫�ڵ�ŷķ���������; ��Ƶ����Բ���漫����λ�����Ӷ���С, ���迹ΪV(��)������Ӧ�ĵ绯 ѧ�����迹�� ������λ�ϵ�ʱ�迹�װ�Բֱ���ϴ�, ����������Ӧ�Ľ��������ܶ�(i0)��Խ�С�йء�
�Բ�ͬ��λ�µ��迹�ײ�����С���˷�������Ϸ���, ������1����, ��ϵĵ�Ч��·ͼ��ͼ6��ʾ��
��1��: RsΪ�缫�����Ͳαȵ缫֮�����Һ����; RmΪʯīձ�缫ŷķ��������; RtΪ������ԭ��Ӧ�ĵ绯ѧ�����迹, ����ɴ��ݵ���; Qm���������м����йصij���λԪ��(CPE); Qt���뷨���ڷ�Ӧ�����йص���һ������λԪ�� (CPE); W����Warbrug�迹, ��Ũ����迹��
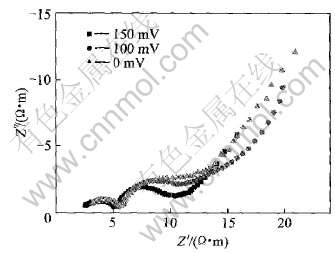
ͼ5 ʯīձ�缫�ڲ�ͬ��λ�µĽ����迹ͼ��
Fig.5 Impedance spectra of graphite felt electrode at some potentials
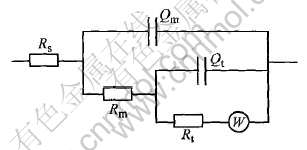
ͼ6 ʯīձ�缫�ڲ�ͬ��λ�µĵ�Ч��·ͼ
Fig.6 Equivalent circuits of graphite felt electrodes at different potentials
��1 ��ͬ��λ��ģ���Ч��·����ѧ����
Table 1 Electrode kinetic parameters modified by equivalent circuit at different potentials
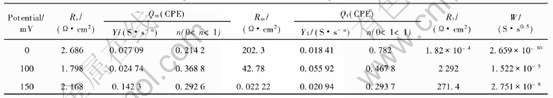
CPE�ľ������������в����, ֻ��Ϊ����迹���ݶ������һ��ʵ������� һ����ΪCPE��ֵ��缫����Ĵֲڶ��й�, �ֲڵĵ缫���治�������伸�α����, �����ɴ�Ӱ�������ڱ���ĵ��衢����ֵ, �������ڵ����ܶȵķǾ�һ�ֲ��������ɢ����[16, 17]��
��ģ���Ч��·����(��1)�ɿ���, ��3����λ��, �����绯ѧ�����迹��Rpֵ�����, �����绯ѧ��Ӧ�п���Ϊ�����缫��Ӧ�Ŀ��Ʋ��衣
3 ����
ͨ���о�V(��)/V(��)�����ʯīձ�缫�ϵ�ѭ����������, �ó�, V(��)��V(��)��������Ӧ�����������, ���������̰����˺��û�ѧת�����衣 �������߷����������������������, VO2+����ֱ�Ӳ���ĵ绯ѧ���������������Ӧ�Ŀ��Ʋ��衣 �����迹��Ͻ�������绯ѧ��Ӧ�����ǵ缫��Ӧ����Ҫ���Ʋ���, �뼫�����߷��������һ�¡�
��л
��л��֦�������о�ԺΪ�������ṩ�ʽ����, ��Ŀ���Ϊ02-09-01��
REFERENCES
[1]Skyllas-Kazacos M, Rychcik M, Robins R G, et al. New all-vanadium redox cell[J]. J Electrochem Soc, 1986, 133: 1057-1058.
[2]Rydh C J. Environmental assessment of vanadium redox and lead-acid batteries for stationary energy storage[J]. J Power Sources, 1999, 80: 21-29.
[3]Kazacos M, Cheng M, Skyllas-Kazacos M. Electrolyte optimization of vanadium redox cell[J]. J Appl Electrochem, 1990, 20: 463-467.
[4]Skyllas-Kazacos M, Menictas C. Thermal stability of concentrated V(V) electrolytes in the vanadium redox cell[J]. J Electrochem Soc, 1996, 143: 86-88.
[5]Menictas C, Hong D R, Yan Z H, et al. Status of the vanadium battery development programme[A]. Proceedings of Electrical Engineering Congress[C]. Sydney: Sydney University Press, 1994, 033: 1-4.
[6]The vanadium redox battery, UNSW, http: //www.ceic.unsw.edu.au/centers/vrb/
[7]Skyllas-Kazacos M, Kazacos M, McDermott R. Vanadium Charging Cell and Vanadium Dual Battery System[P]. Australia: PCT/AU88/00473, 1988.
[8]Sum E, Rychcik M, Skyllas-Kazacos M. Investigation of the V(��)/V(��) system for use in the positive half-cell of a redox battery[J]. J Power Source, 1985, 16: 85.
[9]Zhong S, Skyllas-Kazacos M. Electrochemical behaviour of vanadium(V)/vanadium(IV) redox couple at graphite electrodes[J]. J Power Sources, 1992, 39: 1.
[10]Oriji G, Katayama Y, Miura T. Investigations on V(IV)/V(V) and V(II)/V(III) redox reactions by various electrochemical methods[J]. J Power Sources, 2005, 139: 321-324.
[11]Gattrell M, Park J, MacDougall B, et al. Study of the mechanism of the vanadium 4+/5+ redox reaction in acidic solutions[J]. J Electrochem Soc, 2004, 151: 123-130.
[12]�ƿ���, ������, ������, ��. ��������ԭҺ�����ʯī-̿�ڸ��ϵ缫����[J]. ��Դ����, 2004, 2: 91-93.
HUANG Ke-long, WU Qiu-mei, LIU Su-qin, et.al. Performance of graphite powder-carbon black composite electrodes for the vanadium redox flow battery[J]. Chinese Journal of Power Source, 2004, 2: 91-93.
[13]̷��, �ƿ���, ������. ȫ��Һ����ظ�Ĥ�ڷ���Һ�е�����[J]. ��Դ����, 2004, 12: 775-778.
TAN Ning, HUANG Ke-long, LIU Su-qin. Studies on ion exchange membrane performance in vanadium solution for all vanadium flow battery[J]. Chinese Journal of Power Source, 2004, 12: 775-778.
[14]���ٰ�, ������. �缫���̶���ѧ�����̳�[M]. �人: �人��ѧ������, 1989. 276.
CHEN Zhong-bai, CHEN Yong-yan. Basic Tutorial of Electrode Kinetics[M]. Wuhan: Wuhan University Press, 1989. 276.
[15]ZHOU De-bi, HUANG Ke-long, ZHANG Shi-min. Oxygen reduction on Teflon bonded carbon electrode[J]. Trans Nonferrous Met Soc China, 2004, 14(4): 817-823.
[16]�ܳ���, �ż���. �绯ѧ�迹����[M]. ����: ��ѧ������, 2002. 26.
CAO Chu-nan, ZHANG Jian-qing. Impedance Guide[M]. Beijing: Science Press, 2002. 26.
[17]�����, ����, �Ծ�ï. ����������Ĥ��NaCl��Һ�еĵ绯ѧ����[J]. �й���ɫ����ѧ��, 2004, 14(4): 562-567.
ZHAO Xu-hui, ZUO Yu, ZHAO Jing-mao. Electrochemical properties of anodized aluminum films in sodium chloride solution[J]. The Chinese Journal of Nonferrous Metals, 2004, 14(4): 562-567.
(�༭��ѧ��)
�ո�����: 2005-07-11; ������: 2005-11-14
ͨѶ����: �ƿ���, ����; �绰: 0731-8879850; E-mail: klhuang@mail.csu.edu.cn