Acidiphilium属菌DX-A的分离鉴定及其浸矿功能
王秀美1, 2,王乾芬1,赵兰1,高金昌2,郝福来2,张谷平2,朱建裕1,柳建设1, 3,邱冠周1
(1. 中南大学 资源加工与生物工程学院,湖南 长沙,410083;
2. 长春黄金研究院,吉林 长春,130012;
3.东华大学 环境科学与工程学院,上海,201620)
摘要:从江西德兴铜矿酸性矿坑水中分离得到1株嗜酸细菌(命名为DX-A),该菌株为革兰氏阴性菌,短杆状,菌体宽×长为 (0.45~0.55) μm×(1.1~2.1) μm,最适生长pH为3.5,最适生长温度为30 ℃。该菌能利用FeCl3及多种硫化矿和葡萄糖等多种有机物进行生长,但是不能利用FeSO4进行生长,因而该菌为兼性异养型细菌。构建该菌的系统发育树,研究表明:菌株DX-A与Acidiphilium sp. PK46(AY765995)位于系统发育树的同一分支中,相似度为99%;菌株DX-A分别浸出黄铁矿和铁闪锌矿28 d后,含菌摇瓶中Fe2+与Zn2+的质量浓度分别可达到2.36 g/L和2.47 g/L,而对照组中Fe2+与Zn2+的质量浓度分别为0.60 g/L 和0.39 g/L;菌株DX-A和 A. ferrooxidans ATCC23270混菌分别浸出黄铁矿和铁闪锌矿比A. ferrooxidans ATCC23270单菌浸出效果分别高2.7%和10.3%,表明该菌能够浸出黄铁矿和铁闪锌矿并能促进自养菌的浸矿,为进一步研究异养菌促进自养菌浸矿提供了依据。
关键词:Acidiphilium sp.;分离鉴定;生物浸出;黄铁矿;铁闪锌矿
中图分类号:Q939 文献标志码:A 文章编号:1672-7207(2013)07-2637-07
Isolation and identification of Acidiphilium strain DX-A and function of its bioleaching
WANG Xiumei1, 2, WANG Qianfen1, ZHAO Lan1, GAO Jinchang2, HAO Fulai2, ZHANG Guping2, ZHU Jianyu1, LIU Jianshe1, 3, QIU Guanzhou1
(1. School of Minerals Processing and Bioengineering, Central South University, Changsha 410083, China;
2. Changchun Gold Research Institute, Changchun 130012, China;
3. School of Environmental Science and Engineering, Donghua University, Shanghai 201620, China)
Abstract: An Acidiphilium strain named DX-A was isolated from acid mine drainage of Dexing mine, Jiangxi Province, China. Strain DX-A is rod-shaped in (0.45-0.55) μm×(1.1-2.1) μm and Gram negative. The optimum temperature and pH for cultivation of DX-A are 30 ℃ and 3.5. FeCl3, and other kinds of sulfide ores and organics(such as glucose), except FeSO4, can be utilized to help strain DX-A grow. Strain DX-A has the closest relativity to the Acidiphilium sp. PK46(AY765995), with 99% sequence similarity based on the phylogenetic tree,which was constructed according to the published 16S rDNA gene sequences of the relative bacteria species. After cultivating strain DX-A in the flask respectively containing pyrite and marmatite for 28 d, the mass concentrations of the Fe2+ and Zn2+ reach to 2.36 g/L and 2.47 g/L, respectively, while those of the controls are only 0.60 g/L and 0.39 g/L. After strain DX-A and A. ferrooxidans ATCC23270 together leached pyrite as well as marmatite, the mass concentrations of Fe2+ and Zn2+ are 2.7% and 10.3% respectively higher than only A. ferrooxidans ATCC23270 did. The results show that the strain can leach pyrite and marmatite and promote the leaching ability of autotrophic bacteria. All of these provide some evidences for further study on the promotion effects of bioleaching, which are caused by heterotrophic bacteria.
Key words: Acidiphilium sp.; isolation and identification; bioleaching; pyrite; marmatite
当前,矿产资源日益贫乏,能源和资源是全球共同面临的难题。生物冶金具有成本低、能耗低、环境污染小等优点,因此,特别适合处理低品位矿、尾矿、废矿和难处理矿[1-4]。与其他的技术相比,生物浸矿具有一些优势,但是生物浸出效果不理想,这主要与浸矿微生物的种类有关系。不同酸性矿坑废水(AMD)中的微生物种类及比例呈现显著的多样性,研究表明:Acidithiobacillus ferrooxidans,Leptospirillum ferrooxidans和Acidiphilium spp等细菌几乎存在于所有酸性矿坑水中,这些微生物在矿物氧化分解中起重要作用[5-7]。因此,有必要分离鉴定出性能不同的专属高效菌种并提高其浸矿能力[8-10]。近些年,一些异养菌在浸矿环境中被分离,这些异养菌对促进浸矿效率的提高和自养菌的生长有所帮助,这种促进作用主要是消化细菌代谢有机产物及残体(它们对自养菌有抑制作用)[11-12]。随着异养菌在浸矿体系中的作用越来越受关注[13-15],对异养菌进行分离鉴定并分析其在浸矿中的作用及在浸矿体系中的群落结构很有必要。本文作者从江西德兴铜矿酸性矿坑水中分离得到1株嗜酸兼性异养细菌DX-A,对其进行生理生化特性及浸矿性能的研究,以便为其在生物冶金应用中提供依据。
1 材料和方法
1.1 菌种分离
样品采自江西德兴铜矿区的矿坑水,取样时矿坑水温度为30 ℃,pH为2.50左右。分离步骤是:将采到的矿坑水样首先使用9K+1%(质量分数)葡萄糖液体培养基进行富集培养,待细菌培养至对数期,用梯度稀释法进行9K+1%葡萄糖固体培养基涂布,最后使用平板划线法分离,并将得到的菌株命名为DX-A。
1.2 培养基
富集培养采用9K培养基(不加FeSO4・7H2O)+1%葡萄糖,即:(NH4)2SO4,3 g/L;KCl,0.1 g/L;K2HPO4,0.5 g/L;MgSO4・7H2O,0.5 g/L;Ca(NO3)2,0.01 g/L;葡萄糖,10 g/L;蒸馏水,1 L;用稀H2SO4调节pH至3.0。
固体培养基在富集培养基的基础上加1.2%(质量分数)琼脂粉,用稀H2SO4调pH 至3.0。
浸矿所用培养基为9K培养基,不加FeSO4・7H2O,以黄铁矿或铁闪锌矿作为唯一能源,矿浆质量浓度为3 g/(100 mL),用稀H2SO4调节pH至2.0。
1.3 菌株形态观察
将处于对数生长期的菌液5 000 r/min离心20 min收集细菌,部分细菌经革兰氏染色后在光学显微镜下观察,另外部分用4%戊二醛固定,经制样处理后在扫描电子显微镜下进一步观察菌体形态,并拍照记录。
1.4 生理生化特性测定
1.4.1 最适生长温度的测定
以相同的接种量接种于9K+1%葡萄糖液体培养基中,分别置于不同的温度下摇床培养,每隔一段时间用血球计数板计数,测定不同温度下细菌生长情况。
1.4.2 最适初始pH的测定
用稀H2SO4将9K+1%葡萄糖液体培养基调至不同pH,接种量相同,摇床培养,每隔一段时间用血球计数板计数,测定不同初始pH下细菌生长情况。
1.4.3 底物利用情况
无机底物利用方面,在9K基础盐培养基中分别加入FeSO4・7H2O,FeCl3以及黄铜矿、黄铁矿、铁闪锌矿各质量浓度分别为1 g/(100 mL);有机底物利用方面,在9K基础培养基中分别加入葡萄糖、半乳糖、乳糖、糊精、柠檬酸各质量浓度分别为1 g/(100 mL)。菌株DX-A按照10%接种量接种,置于30 ℃摇床培养,4 d后在显微镜下观察细菌的生长情况。若是没有细菌生长则表示菌株不能利用该种物质作为营养物质生长;有细菌生长则传代3次,镜检观察细菌的生长情况,若是经过3次传代还有细菌生长则表明细菌可以利用该培养基中的营养物质进行生长。
1.5 基因组提取、16S rDNA基因扩增、测序与分析
采用离心柱型细菌基因组DNA提取试剂盒(TIANGEN,DP302)提取DX-A的基因组DNA。PCR(聚合酶链反应)引物采用通用引物63F和1387F来扩增16S rDNA片段。PCR产物经0.8%琼脂糖凝胶电泳分离,切胶回收,经E.Z.N.A Gel Extraction Kit(OMEGA)纯化, 后用PBS-T载体(BBI)连接后转入E.coil DH5α感受态细胞中,经蓝白筛选后挑选出阳性克隆子,送上海生物工程公司测序。
把测序的菌株DX-A的16S rDNA序列提交到GenBank,并将该菌株16S rDNA序列于Genbank核酸序列数据库中已有的序列进行比对,用Clustal X软件进行同源性分析,并用MEGA 3.1构建系统发育树。
1.6 浸矿实验
1.6.1 浸矿条件
实验所用的矿样为黄铁矿和铁闪锌矿,粒度≤74 μm。浸矿实验条件如下:250 mL摇瓶装液100 mL,矿样质量浓度3 g/(100 mL),温度为35 ℃,初始pH值均为2.00,转速为170 r/min,浸矿菌株为菌株DX-A和 A. ferrooxidans ATCC23270,初始接种浓度为2.1×107 个/mL(混菌浸矿时,各菌接种浓度相同,总菌浓度保持为2.1×107 个/mL)。对照组不加任何菌,其他条件与实验组完全一样。
为排除矿物表面的氧化层对浸矿过程中pH变化的影响,在接菌前,先用无机盐预浸。每隔几个小时用稀硫酸调节体系的pH至初始值,直至pH稳定。
1.6.2 pH和电位的测定
浸出液中pH用PHSJ-4A型酸度计的复合玻璃电极测定,其电位用PHSJ-4A型酸度计的Pt电极与参比饱和甘汞电极一起测定。
1.6.3 浸出液的测定
浸出液采用日立公司Z-8000原子吸收光谱仪测定离子浓度,其中黄铁矿测铁离子的浓度、铁闪锌矿测锌离子的浓度。
2 结果和讨论
2.1 菌株形态特征
经过5 d培养,9K培养基平板上长出单菌落,如图1所示。菌落呈边缘光滑、凸起的圆形,乳白色半透明,直径约为1.0~2.5 mm;经革兰氏染色后在光学显微镜下观察,菌株为革兰氏阴性;扫描电镜显示,菌体为短杆状,宽×长为(0.45~0.55) μm×(1.1~2.1) μm。
2.2 菌株生理生化特性
实验表明DX-A最适生长温度为30 ℃,最适生长pH为3.5,如图2所示。菌株DX-A不仅能利用FeCl3、黄铜矿、黄铁矿、铁闪锌矿进行自养生长,而且可以利用葡萄糖、半乳糖、乳糖、糊精、柠檬酸进行异养生长,但不能利用FeSO4进行生长,如表1所示,因而该菌为兼性异养型细菌。
2.3 16S rDNA序列与系统发育树构建
PCR产物经0.8%琼脂糖凝胶电泳分离,为单一条带。测序结果表明:菌株DX-A的16S rDNA序列长度为1309 bp。Genbank核酸序列登录号为EU710758。以16S rDNA序列同源性为基础构建系统发育树(图3)。菌株DX-A与嗜酸杆菌属(Acidiphilium sp.)细菌的16S rDNA基因相似性最高,与Acidiphilium sp. PK46(AY765995)最为相似,相似度为99% 。据此初步判定DX-A属于Acidiphilium sp.。
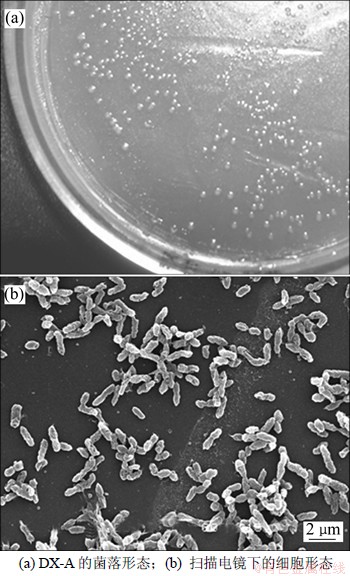
图1 DX-A的菌落形态和扫描电镜下的细胞形态 (10 000×)
Fig.1 Colony of DX-A and cell morphology under scanning electron microscopy (10 000×)
表1 DX-A菌株能源利用特性
Table 1 Characteristics of strain DX-A with different substrates
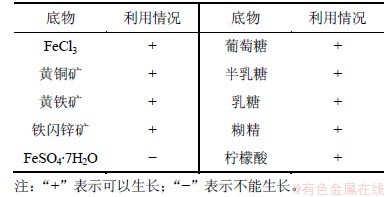
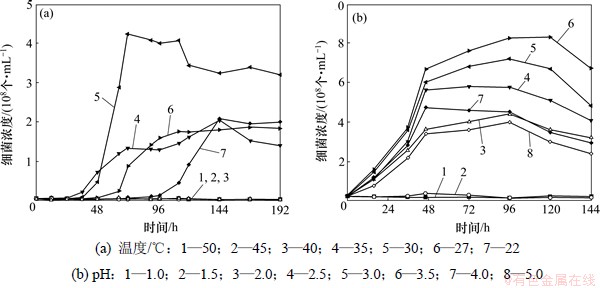
图2 菌株DX-A的生长与温度和pH的关系图
Fig.2 Cell concentration in different phases under different temperatures and different initial pH values
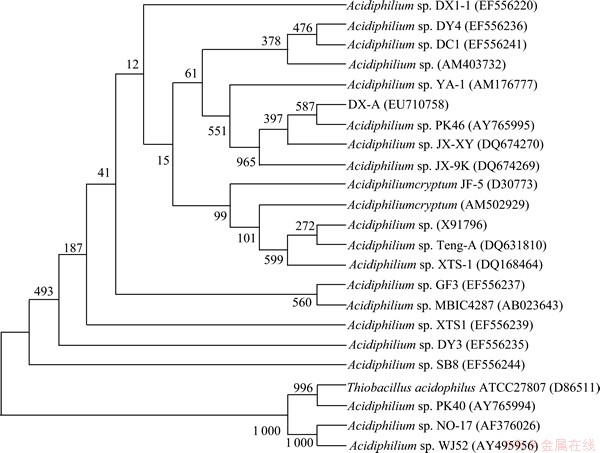
图3 依据16S rDNA基因序列构建的菌株DX-A和相关属菌种的系统发育树
Fig.3 Phylogenetic tree of strain DX-A and related bacterial species constructed according to 16S rDNA gene sequence
2.4 浸矿实验
2.4.1 黄铁矿和铁闪锌矿浸出液的pH和电位变化
2种菌单独浸出黄铁矿过程中溶液的pH整体的变化趋势是先快速下降,在第10天时变化开始缓慢,第20天左右逐渐趋于平缓,到实验结束时,下降到1.15左右;而对照组pH只下降到1.77。因为黄铁矿的氧化是产酸反应,细菌参与后,溶液中生成的Fe2+会很容易被氧化成为Fe3+,而随着溶液中Fe3+浓度增加并参与到黄铁矿的氧化反应中,溶液pH明显下降。
接种菌株DX-A体系液相Eh值(氧化还原电位)在短暂滞后期后快速上升,而接种A. ferrooxidans ATCC23270体系液相Eh值不呈现滞后期;而对照组Eh值上升幅度不大,如图4(a)所示。
2种菌单独浸出铁闪锌矿过程中溶液的pH变化明显。其中接种菌株DX-A所在的浸出体系pH在经过一个很短的小幅上升期后,开始显著下降,在第12天已降到1.50,在18~20 d时达到最低值1.33,随后开始缓慢上升,至反应结束达到1.82。接种A. ferrooxidans ATCC23270体系pH显著升高,可达到3.60;而对照组pH先是大幅度升高然后有一段平稳期最后下降至3.63。铁闪锌矿的完全氧化理论上应该是一个产酸过程,若加上Fe2+氧化为Fe3+的过程中消耗的酸和极其缓慢的硫氧化,则A. ferrooxidans ATCC23270所在的体系pH不断升高。而菌株DX-A能进行铁呼吸并且不能氧化Fe2+,所以,其所在体系pH会下降。
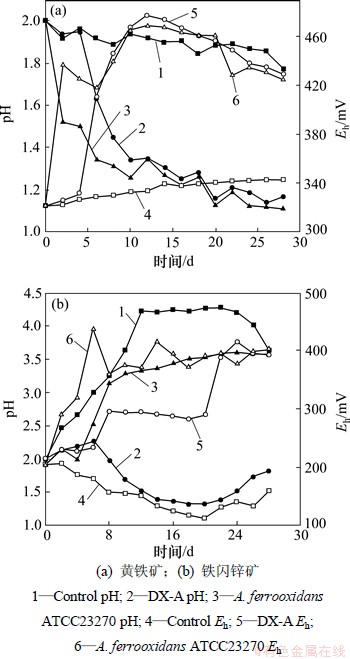
图4 黄铁矿与铁闪锌矿浸出液的pH和Eh变化
Fig.4 Variations of pH and Eh of solutions in leaching of pyrite and marmatite
接种菌株DX-A体系Eh值开始时升高很快,但是在第8~20天,电位基本保持在相对稳定水平,此后又开始显著上升;接种A. ferrooxidans ATCC23270体系液相Eh值开始就显著升高,到第6 d达到440 mV,之后一直都保持较高水平;而对照组Eh值开始是小幅度下降然后小幅度上升至159 mV,如图4(b)所示。
2.4.2 黄铁矿和铁闪锌矿的单菌浸出
在单菌浸出黄铁矿的实验中,菌株DX-A的浸出率比A. ferrooxidans ATCC23270的浸出率稍低,对照组只是酸浸的结果比2种菌单独浸出效果低很多。因为A. ferrooxidans ATCC23270可以氧化Fe2+、元素硫和还原态硫化物;而Acidiphilium sp. DX-A不能利用Fe2+作为能源生长,所以在黄铁矿的环境中,Acidiphilium sp. DX-A比A. ferrooxidans ATCC23270浸出效果稍差。
在铁闪锌矿浸出的前20 d菌株DX-A的浸出率较高,在第16天的时候A. ferrooxidans ATCC23270的浸出效率快速提高,之后超过菌株DX-A的浸出效率,对照组只是酸浸的结果比2种菌单独浸出效果低很多。铁闪锌矿的浸出过程是以Fe3+的化学浸出为主。A. ferrooxidans ATCC23270已经在实验室用Fe2+培养了至少2 a,有很好的亚铁氧化能力,所以Acidiphilium sp. DX-A比A. ferrooxidans ATCC23270的浸出效果稍差。如图5所示。
2.4.3 黄铁矿和铁闪锌矿的混菌浸出
图6所示为2种细菌混菌浸出黄铁矿和铁闪锌矿的浸出曲线。由图6可见:菌株 DX-A和 A. ferrooxidans ATCC23270混菌浸出黄铁矿和铁闪锌矿均比单菌浸矿的效果好;对照组只是酸浸的结果比混菌浸矿效果低很多。混菌浸出黄铁矿和铁闪锌矿比A. ferrooxidans ATCC23270单菌浸出效果分别高2.7%和10.3%,这表明菌株DX-A可以促进自养菌浸矿,并且混菌浸矿中菌株DX-A对促进A. ferrooxidans ATCC23270在铁闪锌矿中的浸出比其在黄铁矿中的浸出明显。
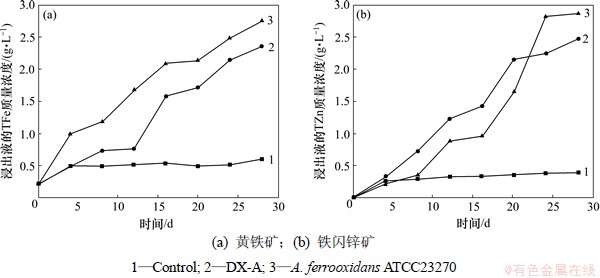
图5 2种细菌单独浸出黄铁矿与铁闪锌矿的浸出曲线
Fig.5 Leaching curves of pyrite or marmatite in presence of either A. ferrooxidans ATCC23270 or strain DX-A
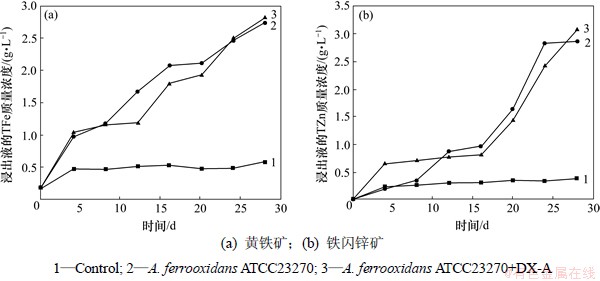
图6 2种细菌混菌浸出黄铁矿与铁闪锌矿的浸出曲线
Fig.6 Leaching curves of pyrite or marmatite in presence of A. ferrooxidans ATCC23270 and strain DX-A
3 结论
(1) 从江西德兴铜矿的酸性矿坑水中分离得到1株嗜酸细菌,该菌为革兰氏阴性菌,短杆状,菌体宽×长为 (0.45~0.55) μm×(1.1~2.1) μm,,最适生长温度为30 ℃,最适生长pH为3.5。该菌不仅能利用多种硫化矿生长,也可以利用多种有机物进行异养生长, 但是不能利用FeSO4进行生长,因而为兼性异养型细菌。
(2) 菌株DX-A的16S rDNA序列长度为1 309 bp,Genbank核酸序列登录号为EU710758。16S rDNA系统发育树的构建表明,DX-A菌株与Acidiphilium sp. PK46(AY765995)位于系统发育树同一个分支中,相似度为99%,初步判定菌株DX-A属于Acidiphilium sp.。
(3) 菌株DX-A分别浸出黄铁矿和铁闪锌矿28 d后,含菌的摇瓶的Fe2+和Zn2+的质量浓度分别可达到2.36 g/L和2.47 g/L,菌株 DX-A和 A. ferrooxidans ATCC23270混菌浸出黄铁矿和铁闪锌矿分别比A. ferrooxidans ATCC23270单菌浸出效果高2.7%和10.3%,这表明该菌能够浸出黄铁矿和铁闪锌矿并能促进自养菌浸矿。若对该菌进一步驯化,则有望更好地促进自养菌的浸矿。
参考文献:
[1] Akcil A. Potential bioleaching developments towards commercial reality: Turkish metal mining’s future[J]. Minerals Engineering, 2004, 17(3): 477-480.
[2] 陈勃伟, 温建康, 刘文彦. 浸矿微生物鉴定研究进展[J]. 中国矿业, 2007, 16(9): 103-106.
CHEN Bowei, WEN Jiankang, LIU Wenyan. Progress in identification of bioleaching microorganisms[J]. China Mining Magazine, 2007, 16(9): 103-106.
[3] 彭艳平, 余水静. 我国生物冶金研究的发展概况[J]. 矿业快报, 2006, 25(12): 8-10.
PENG Yanping, YU Shuijing. Progress of research on biologic metallurgy in China[J]. Express Information of Mining Industry, 2006, 25(12): 8-10.
[4] Rohwerder T, Cehrke T, Kinzler K, et al. Bioleaching review part A: Progress in bioleaching: fundamentals and mechanisms of bacterial metal sulfide oxidation[J]. Applied Microbiology and Biotechnology, 2003, 63(3): 239-248.
[5] Johnson D B, Hallberg K B. The microbiology of acidic mine waters[J]. Research in Microbiology, 2003, 154(7): 466-473.
[6] YANG Yu, WAN Minxi, SHI Wuyang, et a1. Bacterial diversity and community structure in acid mine drainage from Dabaoshan Mine, China[J]. Aquatic Microbial Ecology, 2007, 47(2): 141-151.
[7] 杨宇, 张帅, 徐爱玲, 等. 隐藏嗜酸菌 DX1-1和氧化亚铁硫杆菌CMS的紫外诱变育种及浸矿研究[J]. 中南大学学报: 自然科学版, 2010, 41(2): 393-399.
YANG Yu, ZHANG Shuai, XU Ailing, et al. UV-induced mutagenesis and bioleaching of Acidiphilium cryptum and Acidithiobacillus ferrooxidans[J]. Journal of Central South University: Science and Technology, 2010, 41(2): 393-399.
[8] 顾国华, 孙小俊, 李建华, 等. 嗜铁钩端螺旋菌对黄铁矿浸出的影响[J]. 中南大学学报: 自然科学版, 2010, 41(4): 1223-1228.
GU Guohua, SUN Xiaojun, LI Jianhua, et al. Bioleaching of pyrite by L. ferriphilum[J]. Journal of Central South University: Science and Technology, 2010, 41(4): 1223-1228.
[9] Olson G J, Brierley J A, Brierley C L. Bioleaching review part B: Progress in bioleaching: Applications of microbial processes by the minerals industries[J]. Applied Microbiology and Biotechnology, 2003, 63(3): 249-257.
[10] Brierley J A , Brierley C L. Present and future commercial applications of biohydrometallurgy[J]. Hydrometallurgy, 2001, 59(2/3): 233-239.
[11] 刘艳阳, 陈志伟, 姜成英, 等. 一株嗜酸化能异养菌Acidiphilium sp. 的分离鉴定及其对Fe(Ⅲ)代谢的研究[J]. 微生物学报, 2007, 47(2): 350-354.
LIU Yanyang, CHEN Zhiwei, JIANG Chengying, et al. Isolation and characterization of Acidiphilium strain Teng-A and its metabolism of Fe(Ⅲ) during pure and mixed cultivation[J]. Acta Microbiologica Sinica, 2007, 47(2): 350-354.
[12] Watling H R. The bioleaching of sulphide minerals with emphasis on copper sulphides-A review[J]. Hydrometallurgy, 2006, 84(1/2): 81-108.
[13] Johnson D B, Bridge T A M. Reduction of ferric iron by acidophilic heterotrophic bacteria: Evidence for constitutive and inducible enzyme systems in Acidiphilium spp.[J]. Journal of Applied Microbiology, 2002, 92(2): 315-321.
[14] Baker B J, Banfield J F. Microbial communities in acid mine drainage[J]. FEMS Microbiology Ecology, 2003, 44(2): 139-152.
[15] 邹俐宏, 钱林, 张燕飞, 等. 源自硫化矿区的Acidiphilium属菌的分离及其浸矿性能[J]. 中国有色金属学报, 2008, 18(2): 336-342.
ZOU Lihong, QIAN Lin, ZHANG Yanfei, et al. Isolation and identification of Acidiphilium strain DY from complex sulfide mines and its bioleaching characterization[J]. The Chinese Journal of Nonferrous Metals, 2008, 18(2): 336-342.
(编辑 邓履翔)
收稿日期:2012-06-26;修回日期:2012-08-18
基金项目:国家自然科学基金资助项目(30700008,50874032,41073060);国家重点基础研究发展计划(“973”计划)项目(2010CB630900)
通信作者:朱建裕(1975-),男,湖南湘乡人,博士,副教授,从事资源综合利用和生态环境研究;电话:0731-88836944;E-mail: zhujy@csu.edu.cn