DOI�� 10.11817/j.issn.1672-7207.2020.11.024
�⾧ʯLiMn2O4���װ��ĺϳɺʹ������
�ܸ�1�������2�����鲨1
(1. ��ݸ����ѧԺ ��̬�����뽨������ѧԺ���㶫 ��ݸ��523808��
2. ���ϴ�ѧ ��ĩұ������ص�ʵ���ң����� ��ɳ��410083)
ժҪ��Ϊ�˸���LiMn2O4����������ӵ��Ӧ���б��ʷŵ����ܺ�ѭ�����ܽϲ�����⣬���������ߴ���Ʒ������Զ�άLiMn2O4���װ��Ĵ��Ӧ�ý����о���ͨ��ˮ�ȷ��ϳɵĦ�-MnO2��������LiOH��H2O���й����ս��Ʊ��⾧ʯ�ṹ��LiMn2O4���װ���̽��ˮ�ȷ�Ӧʱ�䡢�¶Ⱥͷ�Ӧ�����ʵ����ȶ�ǰ�����-MnO2��ò�ṹ�����ܵ�Ӱ�졣�о�����������Ʊ���LiMn2O4���װ��ȱ����������������Li+��ɢ���룬�ϴ�ij����ȿɼ���ѭ�������в��ϵ��žۣ��Ӷ�����LiMn2O4�����ѭ�����ܡ�LiMn2O4���װ���1C���ʳ�ŵ�ʱ��ʼ�ŵ�����Ϊ104.8 mA��h/g��ѭ��150Ȧʱ���ɿ��Ա��ֳ�ʼ������84.4%������3C���ʳ�ŵ�ʱ���Ա��ֳ�ʼ������75%����ʾ�˽ϸߵĵ绯ѧ������ܡ�
�ؼ��ʣ�ˮ�Ⱥϳɣ������ս��������װ�������ӵ�أ��������
��ͼ����ţ�TB321 ���ױ�־�룺A
���±�ţ�1672-7207��2020��11-3211-09
Synthesis and lithium storage performance of spinel LiMn2O4 nanorods
ZHOU��Gang1, CHEN��Yuejiao2, FAN��Hongbo1
(1. School of Environment and Civil Engineering, Dongguan University of Technology, Dongguan 523808, China;
2. State key Laboratory of Powder Metallurgy, Central South University, Changsha 410083, China)
Abstract: To improve attenuation of electrical performance for LiMn2O4, the application of two-dimensional LiMn2O4 nanorods in lithium storage was studied by using the nano-size improvement scheme. LiMn2O4 nanorods were synthesized by solid phase sintering method using LiOH��H2O and single-crystal ��-MnO2 nanowires obtained by hydrothermal method. And the effect of hydrothermal time, temperature and the ratio of reactant and salt on the morphology and structure were investigated. The results show that the prepared LiMn2O4 nanorods have large specific surface area and large aspect ratio, which benefits the diffusion distance of Li+, and reduces the agglomeration of materials during cycling, thus endowing the superior cycling performance of LiMn2O4. The electrochemical test demonstrates that LiMn2O4 nanorods can maintain 84.4% of the initial discharge capacity which is 104.8 mA��h/g after 150 cycles at 1C rate, and 75% of the initial discharge storage can be maintained at 3C rate, which displays a better performance of electrochemical lithium storage.
Key words: hydrothermal synthesis; solid phase sintering; lithium manganese oxide nanorods; lithium ion battery; lithium storage performance
����ӵ�ؾ��������ܶȡ������ܶȽϸߣ�ʹ���������Լ������Ѻõ��ص㣬���㷺Ӧ���ڵ��Ӳ�Ʒ��[1-3]�����⾧ʯ�ṹ�������(LiMn2O4)�ɱ��͡���Դ�ḻ�������Ѻã������DZ����﮵���������֮һ[4]��LiMn2O4����AB2O4�ͻ�����ռ�ȺΪFd3m�����У���ԭ�ӳ������������ܶѻ��Ų��������ռ����1/8���������϶�������ӽ���λ����ԭ���ܶѻ��İ������϶λ��[2,5]����һ�־�����άͨ����Ƕ�뻯������нϸߵĴ����������(148 mA��h/g)��Ȼ���������������������ȣ��������ܶ���Խ�С����ѧ�ȶ��Խϵͣ������Ǵ��������¼������⣺1) Mn3+��Jahn-TellerЧӦ������ɾ�����䣬�ƻ��ṹ������ѭ�����ܱ�2) �ŵ�ĩ��Mn3+���绯��Ӧ�����ɵ�Mn2+���ڵ��Һ�У���ɻ������ʼ��٣����͵�ص�����[6-8]��Ϊ�˸���LiMn2O4�ĵ绯ѧ���ܣ����õķ����а����������Ӳ��ӡ������ߴ��[4-5,9-14]��Ŀǰ�������Ʊ�����﮵ķ�����ˮ�ȷ�[11]��ģ�巨[10, 15]������ϳɷ�[16]�ȡ���ͳ�Ĺ��෨�Ʊ���LiMn2O4һ��������Ϊ�˺ϳɳ����׳ߴ��LiMn2O4����������ѡ��ˮ�ȷ��Ʊ��Ħ�-MnO2��Ϊǰ���壬��LiOH��H2O�����ս�ϳ����װ���ò��LiMn2O4���о�ˮ�ȷ�Ӧʱ�䡢�¶Ⱥͷ�Ӧ�����ʵ����ȶ�ǰ�����-MnO2��ò�ṹ�����ܵ�Ӱ�졣
1 ʵ�鲿��
1.1���������ϵ��Ʊ�
ˮ�Ⱥϳɦ�-MnO2��Ȼ������LiOH��H2O������½��й����ս��Ʊ������װ�״�ṹ������ﮡ�
1.1.1����-MnO2���Ʊ���
��-MnO2����ò�ṹ��Ҫ�ܵ�ˮ�ȷ�Ӧ�¶ȡ�ʱ�估��Ӧ�����ʵ����ȵ�Ӱ�졣���ʵ������˷�Ӧ�¶ȡ���Ӧʱ�䡢��Ӧ�����ʵ�����3����������̽���ϳɦ�-MnO2�����ߵ����ʵ��������
ˮ�ȷ�Ӧ��Ӧ����ʽΪ

�������ʵ�����Ϊ1:1:2��Mn(CH3COO)2��4H2O,(NH4)2S2O8��(NH4)2SO4�����ձ��У�����60 mLȥ����ˮ����������ȫ�ܽ⡣����Ͼ��ȵ���Һ����100 mL�ķ�Ӧ���ڽ���ˮ�ȷ�Ӧ����Ӧ������õĦ�-MnO2�ֱ���ȥ����ˮ���Ҵ���Һ��ϴ�Ӳ�����(100 �棬12 h)��
1.1.2���⾧ʯLiMn2O4�ĺϳɡ�
����-MnO2��������LiOH��H2O�ڹ�ʽ¯�й����սᣬ�Ʊ����⾧ʯ�ṹ��������װ���
�����սᷴӦ����ʽΪ
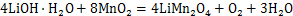
�����ʵ�����Ϊ1:2��LiOH��H2O�ͦ�-MnO2����С�ձ�����140 �淴Ӧ12 h����ˮ�����̡���������李�����淋����ʵ�����Ϊ1:1:4���μ�5 mL��ˮ�Ҵ����ڽ������Ͻ������Ҵ���ȫ�ӷ���Ȼ����Ʒ�ڹ�ʽ¯�У���480 ������ս�10 h����������Ϊ1 ��/min��
1.2�����ϱ���
���ó�����ɨ��羵(SEM��NOVA NANO SEM230)�����������(TEM��TECNAI G2 F20)������ò�ͽṹ������X�������������(XRD���ձ�Rigaku��˾)�����������࣬����Դ����Cu K�� (��=1.540 56��10-10 m)��ɨ�跶ΧΪ10��~85�㡣
1.3���绯ѧ���ܲ���
��������7:2:1��ȡ�Ʊ���LiMn2O4���װ���Super-P(�����)��PVDF(��ƫ����ϩ�����)����ĥLiMn2O4��Super-P�Ļ�����������PVDF��N-��������ͪ(NMP)�У�����12 h��Ϳ����������60 ������ո���12 h���ڳ�ѹ���ϳ��ֱ��Ϊ12 mm��Բ�μ�Ƭ���������������װ�ڳ���������������н��У�ˮ����������������0.5��10-6���ң�����Celgard 2400��Ϊ﮵��Ĥ�������Ƭ�����������ø�ѹ���Һ(̼����ϩ��(EC)+̼�������(DMC))����װ��CR2025�Ͱ��ء�
ѭ�����ܡ��������ܺͳ�ŵ��������������ϵͳ(LANHE CT2001A���人�����������˾����)�Ͻ��У�ѭ����������(CV)�ڵ绯ѧ����վ����0.1 mV/s���ʲ���(��ѹΪ3.5~4.3 V)��
2 ���������
2.1����ͬʵ���������Ʊ���-MnO2��Ӱ��
2.1.1����Ӧʱ��Ժϳɦ�-MnO2��Ӱ�졡
�̶���Ӧ�¶�(120 ��)�ͷ�Ӧ�����ʵ�����(��ˮ�����̡���������李�����淋����ʵ�����Ϊ1:1:2)������8�鷴Ӧʱ��(4��6��8��10��12��24��36��48 h)����ˮ�ȷ�Ӧ�����ò����SEM��òͼ��ͼ1��ʾ��
��ͼ1���Կ���������ˮ�ȷ�Ӧʱ����ӳ�����-MnO2����ò�ṹ�����ϴ�仯����Ӧ4 hʱ���֦�-MnO2��������״��̬���ڣ�ֻ�к�Сһ����Ϊ�����ߣ�˵���ڴ�ʱ�������Ѿ���ʼ�γɡ�����Ӧ���е�8 hʱ���Ѿ����Կ�����������״�ṹ�����������߱Ƚ϶̣�˵����ʱ�������Ѿ��γɣ����ǻ�û�г�ȫ����Ӧ10~12 hʱ�����Է����������䳤��ϸ����Ӧ12 hʱ���������Ѿ���ȫ���á�����Ӧʱ�䳬��24 hʱ�����Է��������߱�֣������žۡ����ŷ�Ӧʱ���һ���ӳ������ž�����������ء��ɴ˿�֪���Ʊ���-MnO2��ѷ�Ӧʱ��Ϊ12 h��

ͼ1����ͬˮ�ȷ�Ӧʱ���Ʊ��Ħ�-MnO2��SEM��Ƭ
Fig. 1��SEM images of ��-MnO2 obtained with different reaction time
ͼ2��ʾΪ��ͬ��Ӧʱ���XRDͼ�ס���ͼ2���Կ�������Ӧʱ��Ϊ4��6��8��10��12 h�ķ�Ӧ���ﶼ�ܽϺõض�Ӧ��-MnO2�ı�PDF��Ƭ��������20��~30��֮��������С�ӷ壬��Щ�ӷ����ŷ�Ӧʱ�������������ʧ����Щ�ӷ�����Ƿ�Ӧ���м�������Ӧ���е�12 h����ʱ���ӷ��Ѿ�������ʧ����˵����ʱ��Ӧ�Ѿ�������ȫ����ˣ�ѡ��12 h��Ϊ��Ӧʱ����Ի�æ�-MnO2�Ĵ��ࡣ���⣬���ŷ�Ӧʱ����ӳ�����ǿ����������˵����-MnO2�Ľᾧ����������
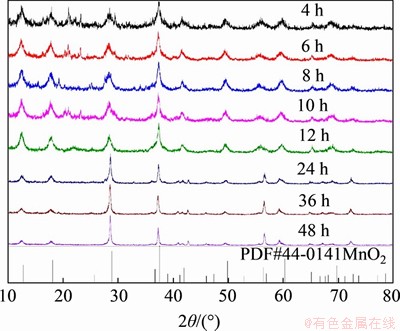
ͼ2����ͬˮ�ȷ�Ӧʱ���XRDͼ��
Fig. 2��XRD patterns of ��-MnO2 obtained with different reaction time
2.1.2����Ӧ�¶ȶԺϳɦ�-MnO2��Ӱ�졡
�̶���Ӧʱ��(12 h)�ͷ�Ӧ�����ʵ�����(��ˮ�����̡���������李�����淋����ʵ�����Ϊ1:1:2)������3�鷴Ӧ�¶�(80��140��180 ��)����ˮ�ȷ�Ӧ�����ò����SEM��òͼ��ͼ3��ʾ��

ͼ3����ͬ��Ӧ�¶��Ʊ��Ħ�-MnO2��SEM��Ƭ
Fig. 3��SEM images of ��-MnO2 obtained at different reaction temperatures
��ͼ3�ɿ�����ˮ�ȷ�Ӧ�¶�Ϊ140 ��ʱ�õ��������߽ṹ��ã������ߵij���Ϊ1~3 ��m������Ϊ25~30 nm������Ӧ�¶�Ϊ80 ��ʱ�������ߴ�ϸ���Ȳ����ȣ���Ϊ���ң���˵����80 ��/12 h�������£�������û����ȫ���á����ڷ�Ӧ�¶�Ϊ180 ��ʱ�������߽ṹ�Ѿ����ƻ�����˵����Ӧʱ��12 h��180 ��ķ�Ӧ�¶ȹ��ߡ��ڷ�Ӧ�¶�Ϊ140 ��ʱ�õ��������߳����ȴ�ϸ���ȣ���ˣ�ˮ�ȷ�Ӧ���¶�Ӧ���趨��140 �����ҡ�
2.1.3����Ӧ�����ʵ����ȶԺϳɦ�-MnO2��Ӱ�졡
�̶���Ӧʱ��(12 h)�ͷ�Ӧ�¶�(140 ��)��������ˮ�����̡���������李�����淋����ʵ����ȷֱ�Ϊ1:1:0��1:1:1��1:1:3��1:1:4��4�����飬����ˮ�ȷ�Ӧ�����ò����XRDͼ����ͼ4��ʾ��
��ͼ4��֪���������������ʱ(���ʵ�����Ϊ1:1:0)��MnO2�ľ���Ϊ���͡������������ʱ���õ��˦����͵�MnO2����-MnO2���ɰ�����[MnO6]Ϊ������Ԫ��ɵ�2��2�;��壬����-MnO2���ɰ�����[MnO6]Ϊ������Ԫ��ɵ�1��1�;��壬��˦�-MnO2Ҫ�Ȧ�-MnO2�����ȶ�����û�����Ӱ�����صĸ���ʱ����-MnO2���Է���ת��Ϊ��-MnO2�������ξ���Ϊ����ֹ�������ķ������������������ӣ���K+��NH4+��H3O+��Ba2+��Na+ʱ����Щ������Ũ���㹻��ʱ�ͻ��кܴ�ĸ��ʽ��뵽2��2�;�����У�ʹ�æ�-MnO2������ȶ����ڡ����⣬��������Ҫ�ǿ���MnO2�ľ��ͣ�����������Ҫ�ǿ���MnO2����ò��
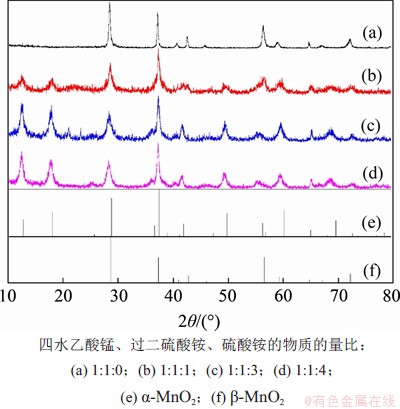
ͼ4����ͬ����隣��������XRDͼ��
Fig. 4��XRD patterns of products obtained with different ratios of reactants
ͼ5��ʾΪ��ͬ��Ӧ�����ʵ����ȵ�SEM��Ƭ����ͼ5(a)���Կ�����MnO2Ϊ���װ�״�ṹ����������F-��SO42-��ʹ�������߽ṹ���γɣ���������£�����F-���к�ǿ�ĵ縺�ԣ������������ڦ�-MnO2��(100)��(200)���棬������2��������������裬�Ӷ��γ���������״�ṹ��������SO42-�����Ӱ뾶��F-�Ĵ����SO42-������������Mn2+Ũ�Ƚϵ͵�(100)�棬��Ҫ������(100)�������������ˣ���������ΪSO42-�õ���MnO2Ϊ����Ϊ���ε������߽ṹ(ͼ5(b)~(d))�����⣬����SO42-�����Ӱ뾶�ϴ������ή�����ӵ���ɢ���ʣ�ʹ�ü��������εõ��IJ���ȼ��������εIJ���С����ͼ5�����Է��֣���ˮ�����̡���������李�����淋����ʵ�����Ϊ1:1:4ʱ�õ��������߽ṹ���á���ˣ���ˮ�����̡���������李�����淋�������ʵ�����Ϊ1:1:4��

ͼ5����ͬ��Ӧ�������SEM��Ƭ
Fig. 5��SEM images of products obtained with different ratios of reactants
ͨ������ʵ������飬����ȷ����ˮ���¶�140 �棬ˮ�ȷ�Ӧʱ��12 h����ˮ�����̡���������李�����淋����ʵ�����1:1:4ʱ���Եõ���ѵĦ�-MnO2�����߽ṹ���Դ������ºϳɵĦ�-MnO2�����߽���TEM��������ͼ6��ʾ��
ͼ6(a)�б�ǵľ�����Ϊ0.690 nm�����PDF��Ƭ��(110)��������������������������Ĺ����У�(100)����������ܵ����ƣ�������<110>������������ǰ��������������������SO42-������(100)���������ƾ���������һ�¡���ͼ6(b)��(c)�ɵã������߽ṹֱ��Ϊ10~30 nm������Ϊ1~2 ��m����ͼ6(d)�ɼ�����������仨��Ϊ������������㣬˵����-MnO2�ᾧ�Է�������

ͼ6����-MnO2 TEM��Ƭ��ѡȡ���仨��
Fig. 6��HRTEM, TEM and SAED of ��-MnO2
2.2��LiMn2O4���װ��ı���
2.2.1��LiMn2O4��������
ͼ7��ʾΪ�Ʊ���LiMn2O4 SEM��Ƭ����ͼ7���Կ�����LiMn2O4Ϊ���װ�״�ṹ����Ϊ��ɢ�Ҿ��ȡ����װ���1~4 ��m����Լ125 nm����ǰ�����-MnO2�Ŀ��ȴ����װ�������С������ͬʱ����һЩϸС����ά���Ʋ������ս�����������߱��նϲ����ġ�

ͼ7���⾧ʯ�����SEM��Ƭ
Fig. 7��SEM images of spinel LiMn2O4
ͼ8��ʾΪLiMn2O4���߷ֱ���ͼ��ѡ���������仨������ͼ8(a)��֪����þ�����Ϊ0.294 nm�����ݱ�PDF��ƬPDF#35-0782��֪���⾧ʯ����﮵�(220)������Ϊ0.291 45 nm����˿����ж��˾���Ϊ(220)���档��ͼ8(b)�ɼ������仨��Ϊ�����Ĺ�ߣ�˵���Ʊ���LiMn2O4�������õĽᾧ�ṹ��

ͼ8��LiMn2O4 HRTEM��Ƭ��ѡ���������仨��
Fig. 8��HRTEM image and SAED of LiMn2O4
2.2.2��LiMn2O4��XRD����
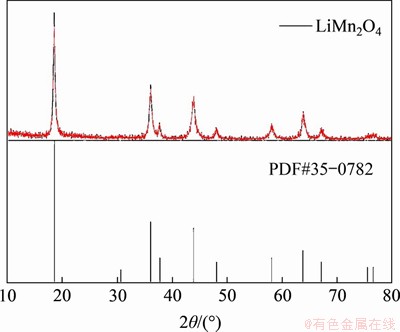
ͼ9��LiMn2O4���װ���XRDͼ��
Fig. 9��XRD pattern of LiMn2O4 nanorods
ͼ9��ʾΪLiMn2O4���װ���XRDͼ�ס���ͼ9��֪�����з���ܺͱ�����ﮱ�PDF��Ƭ��Ӧ������û�������ӷ���ڣ�˵���Ʊ����˽ϴ��ļ⾧ʯ�ṹ����ﮡ�
2.2.3��LiMn2O4�ĵ绯ѧ���ܡ�
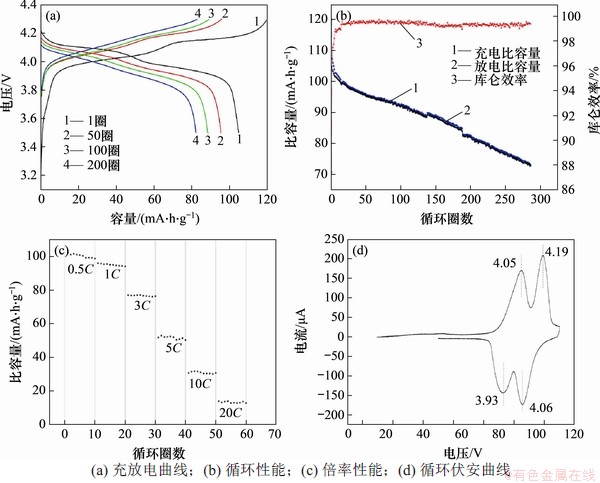
ͼ10��LiMn2O4�ĵ绯ѧ����
Fig. 10��Electrochemical properties of LiMn2O4
ͼ10(a)��ʾΪLiMn2O4�ŵ�����1C��ѭ��1Ȧ��50Ȧ��100Ȧ��200Ȧʱ�ij�ŵ����ߡ���ͼ10(a)���Է���2�����Ե���4 V���ҵķŵ�ƽ̨���ֱ������ŵ�����е�2�������̣���LiMn2O4/Li0.5Mn2O4��Li0.5Mn2O4/��-MnO2��
ͼ10(b)��ʾΪLiMn2O4��3.5~4.3 V�ĵ�ѹ��������1C���ʳ�ŵ��ѭ�����ܣ�ѭ��Ȧ��Ϊ287Ȧ���ɼ�����Ȧ�ij�������Ϊ119.9 mA��h/g���ŵ������Ϊ104.8 mA��h/g����ȦЧ��Ϊ87%���ڵ�һȦ��������Ч�ʿ��������ӽ�100%���״β�������������Ϊ11%����ѭ��100Ȧʱ���ŵ������Ϊ91.8 mA��h/g������������Ϊ87.6%����ѭ��150Ȧʱ���ŵ������Ϊ88.5 mA��h/g������������Ϊ84.4%����ѭ��Ȧ����250Ȧʱ���ŵ������Ϊ77.2 mA��h/g������������Ϊ73.7%��
ͼ10(c)��ʾΪLiMn2O4�ı������ܡ��ɼ���LiMn2O4�ڷŵ�����0.5C��1Cʱ�������źܺõ����������У��ŵ�����1C�£��ŵ����ʱ��������93%�����������ǵ��ŵ�����������3C����ʱ������˥���ܿ졣���ŵ�����3Cʱ����ر���75%��������5Cʱ������49%�����������ŵ�����10C��20Cʱ���ֱ�ֻ��30%��13%����������˵���Ʊ��õ���LiMn2O4���װ������������ڳ����ʷŵ硣����ԭ��������ڽϴ��ʵij�ŵ�����У�����������������������λ�����뵽�������λ�������γ���Li2Mn2O4����ʱ��������Ҫ�����۴��ڣ�Jahn-TellerЧӦ�dz����ԣ��⾧ʯ����﮵ľ���ṹ�����ı�Ϊ�ķ���ϵ������ӵ���ά��ɢͨ���ܵ��谭�����²��ϵ������½������⣬����ŵ����ʹ���ʱ���ᵼ������﮷����žۣ��Ӷ������������ɢ���ѣ������½���
ͼ10(d)��ʾΪLiMn2O4��CV���ߣ�ɨ���ٶ�Ϊ0.1 mV/s����ѹ��ΧΪ3.5~4.3 V����ͼ10(d)�ɼ�2�Էdz����Ե�������ԭ�壬˵��������ڼ⾧ʯ������е�Ƕ�����Ƕ��2�����С�����ŵ�����1Cʱ�ij�ŵ������������һ��������ԭ����4.05/3.93 V��������һ�������Ӵ��������λǶ�������Ƕ���ڶ���������ԭ����4.19/4.06 V����������һ�������Ӵ��������λǶ�������Ƕ��ͼ�е�������ԭ�嶼�dz������ҷ������ã���˵���Ʊ��õ�������﮾������õĽᾧ�ȡ������븺����������ԭ��ĵ�ѹ������˵�صļ����̶ȡ���ѹ��(0.12 V)С˵����������װ����н�С�������Ǩ���迹�������ڸò��ϵı��ʷŵ����ܡ�
3 ����
1) ��ˮ�ȷ��ϳ��˦�-MnO2������ǰ���壬����ȷ���Ʊ���-MnO2�����߽ṹ����ѷ�Ӧ����Ϊˮ���¶�140 �棬ˮ�ȷ�Ӧʱ��12 h����ˮ�����̡���������李���������ʵ�����1:1:4������������Ʊ��Ħ�-MnO2��������Ϊģ�壬�ɹ����Ʊ��˼⾧ʯ�ṹ��LiMn2O4���װ���
2) �Ʊ���LiMn2O4���װ����нϺõĽᾧ�Ժͽϴ�ij����ȣ�����������Li+��ɢ���룬�ɼ���ѭ�������в��ϵ��žۡ�
3) �Ʊ���LiMn2O4���װ�������Ǩ�ƹ����о��нϵ͵��迹�ͼ�������������Ƕ﮹����еĵ绯ѧ����ѧ����ŵ���Թ����б��ֳ������õı������ܺ�ѭ�����ܡ�
�ο����ף�
[1] YI Tingfeng, ZHU Yanrong, ZHU Xiaodong, et al. Erratum to: a review of recent developments in the surface modification of LiMn2O4 as cathode material of power lithium-ion battery[J]. Ionics, 2009, 15(6): 785.
[2] TANG Wei, HOU Yuyang, WANG Faxing, et al. LiMn2O4 nanotube as cathode material of second-level charge capability for aqueous rechargeable batteries[J]. Nano Letters, 2013, 13(5): 2036-2040.
[3] SAHU B B, KIM S H, KIM S, et al. Plasma diagnostic in LiMn2O4 thin film process for Li-ion battery application[J]. Surface and Coatings Technology, 2020, 397: 126066.
[4] SHAJU K M, BRUCE P G.A stoichiometric nano-LiMn2O4 spinel electrode exhibiting high power and stable cycling[J]. ChemInform, 2008, 39(48): 5557-5562.
[5] LUO Jiayan, WANG Yonggang, XIONG Huanming, et al. Ordered mesoporous spinel LiMn2O4 by a soft-chemical process as a cathode material for lithium-ion batteries[J]. ChemInform, 2007, 38(48): 4791-4795.
[6] TANG C Y, LEUNG K, HAASCH R T, et al. LiMn2O4 surface chemistry evolution during cycling revealed by in situ auger electron spectroscopy and X-ray photoelectron spectroscopy[J]. ACS Applied Materials & Interfaces, 2017, 9(39): 33968-33978.
[7] MAINO G, DHAEN J, MATTELAER F, et al. Effect of annealing atmosphere on LiMn2O4 for thin film Li-ion batteries from aqueous chemical solution deposition[J]. Journal of Materials Chemistry, 2016, 4(47): 18457-18469.
[8] MARINCAS A H, GOGA F, DORNEANU S A, et al. Review on synthesis methods to obtain LiMn2O4-based cathode materials for Li-ion batteries[J]. Journal of Solid State Electrochemistry, 2020, 24(3): 473-497.
[9] LEE H W, MURALIDHARAN P, RUFFO R, et al. Ultrathin spinel LiMn2O4 nanowires as high power cathode materials for Li-ion batteries[J]. Nano Letters, 2010, 10(10): 3852-3856.
[10] LI Xiaoxia, CHENG Fangyi, GUO Bing, et al. Template-synthesized LiCoO2, LiMn2O4, and LiNi0.8Co0.2O2 nanotubes as the cathode materials of lithium ion batteries[J]. The Journal of Physical Chemistry B, 2005, 109(29): 14017-14024.
[11] LEE S, CHO Y, SONG H K, et al. Carbon-coated single-crystal LiMn2O4 nanoparticle clusters as cathode material for high-energy and high-power lithium-ion batteries[J]. Angewandte Chemie International Edition, 2012, 51(35): 8748-8752.
[12] SELVAMANI V, PHATTHARASUPAKUN N, WUTTHIPROM J, et al. High-performance spinel LiMn2O4@carbon core�Cshell cathode materials for Li-ion batteries[J]. Sustainable Energy & Fuels, 2019, 3(8): 1988-1994.
[13] DING Yuanli, XIE Jian, CAO Gaoshao, et al. Single-crystalline LiMn2O4 nanotubes synthesized via template-engaged reaction as cathodes for high-power lithium ion batteries[J]. Advanced Functional Materials, 2011, 21(2): 348-355.
[14] HAN Chenggong, ZHU Chunyu, SAITO G, et al. Improved electrochemical performance of LiMn2O4 surface-modified by a Mn4+-rich phase for rechargeable lithium-ion batteries[J]. Electrochimica Acta, 2016, 209: 225-234.
[15] BORHANIHAGHIGHI S, KHARE C, TROCOLI R, et al. Synthesis of nanostructured LiMn2O4 thin films by glancing angle deposition for Li-ion battery applications[J]. Nanotechnology, 2016, 27(45): 455402.
[16] AHN D S, SONG M Y. Variations of the electrochemical properties of LiMn2O4 with synthesis conditions[J]. Journal of the Electrochemical Society, 2000,147(3):874-879.
(�༭ �Կ�)
�ո����ڣ� 2020 -08 -01; �����ڣ� 2020 -09 -14
������Ŀ(Foundation item)��������Ȼ��ѧ����������Ŀ(51901043) (Project(51901043) supported by the National Natural Science Foundation of China)
ͨ�����ߣ����鲨�����ڣ����²��Ͽ�ѧ�о���E-mail��fhb666666@126.com