DOI: 10.11817/j.issn.1672-7207.2016.08.004
Na2CO3-NaCl二元共晶熔盐的热稳定性
叶龙刚,唐朝波,陈永明,杨声海,唐谟堂
(中南大学 冶金与环境学院,湖南 长沙,410083)
摘要:考察Na2CO3-NaCl共晶熔盐在熔点温度至1 000 ℃的热稳定性,从高温下的质量损失,循环使用性能,高温处理后的成分、结构和形貌等方面进行评价。研究结果表明:共晶成分的挥发性介于纯NaCl和纯Na2CO3之间,当温度超过800 ℃后,挥发量急剧增加,挥发量与时间成线性关系。共晶成分在多次循环过程中保持熔化温度、结晶温度及熔化时间、结晶时间基本不变。XRD研究表明:熔盐的组成在长时间高温处理后保持不变,NaCl和Na2CO3的相对含量也不发生变化,同时经高温处理后混合物的结晶性和溶合更好,液相成分更均匀。
关键词:熔盐;热稳定性;共晶成分;热循环
中图分类号:TF8 文献标志码:A 文章编号:1672-7207(2016)08-2563-06
Thermal stability of eutectic composition in Na2CO3-NaCl binary system
YE Longgang, TANG Chaobo, CHEN Yongming, YANG Shenghai, TANG Motang
(School of Metallurgy and Environment, Central South University, Changsha 410083, China)
Abstract: The thermal stability of the eutectic Na2CO3-NaCl molten salt was investigated from the melting point to 1 000 ℃. The mass loss at high temperatures, the cycle performance, the component, structure and morphology after the heat treatment were evaluated. The results show that the volatility of eutectic composition is between pure NaCl and pure Na2CO3. The volatility of molten salt is sharply increased after 800 ℃, and the amount of volatility has a linear relationship with time. The temperature of melt and crystal and the time of melt and crystal of eutectic salt are almost invariant during the cycle times. XRD studies show that the composition of the molten salt is unchanged after high-temperature treatment is prolonged, and the relative contents of NaCl and Na2CO3 have no change. While the crystallinity and mutual dissolution of mixture are better after high temperature treatment, the constituent of liquid phase is more uniform.
Key words: molten salts; thermal stability; eutectic; thermal cycle
熔盐是盐的熔融态液体,最常见的熔盐由碱金属或碱土金属的卤化物、碳酸盐、硝酸盐以及磷酸盐等组成。熔盐具有高温稳定性好、蒸汽压低、黏度低、导电性能良好、离子迁移快、热容量高[1-2]等优点,使其在太阳能电池、核工业、冶金工业、环保领域和材料制备等工程技术中有着广泛的应用[3-8]。目前关于熔盐的研究多关注在太阳能熔盐储热,集中在开发更低熔点和更好稳定性的多元熔盐,具有良好的流动性和导热性的LNK熔盐已有大量研究和应用[3-4],但其在较高的温度下使用时也分解[5]。另外,因为熔盐具有高于水溶液的沸点和电极电位,可作为反应的介质,用于进行在水溶液中无法完成的反应[6]。在冶金领域,熔盐主要用于金属及其合金的电解生产与精炼,熔盐电解已成为金属铝生产的唯一方法。近些年来,碱性(NaOH,Na2CO3-NaCl,K2CO3-KCl)的熔盐还用于熔炼重金属硫化矿[7]和二次资源[8],以取代传统熔炼的FeO-SiO2-CaO高温渣,显著效果在于大幅降低了熔炼温度和SO2排放,取得了很好的环保效果,在常见重金属中的铅、锌、锡、锑、铋等熔点都低于800 ℃,均可用低温熔盐冶金方法提取和分离,是一种清洁绿色的冶炼工艺。但熔盐体系的稳定性是需要关注的问题,相对于FeO-SiO2-CaO渣高达1 000~1 400 ℃的熔点[9]和0.02~1 Pa・s的黏度[10],碱性熔盐的熔沸点和黏度都要小得多,因而,在较高温度下使用时也易挥发,同时在高温下和还原性气氛中也可能分解和转变[15]。为此,有必要研究用于熔炼的熔盐体系的热稳定性,以免出现因熔盐挥发或分解引起的二次污染。Na2CO3和NaCl都是廉价易得的盐类,作为熔炼介质或合成其他材料时具有成本优势,因此,本文作者研究了共晶成分的Na2CO3-NaCl熔盐的热稳定性,以考察其用于重金属硫化矿低温熔炼或作为基础体系用于合成材料的可能性。
1 实验
本实验所用Na2CO3和NaCl都为分析纯级,在270 ℃的温度下烘干24 h后存放在干燥器中。本实验研究共晶成分Na2CO3-NaCl的稳定性,图1所示为Factsage中该二元体系的相图。从图1可以看出:纯Na2CO3和NaCl的熔点分别为858 ℃和801 ℃,共晶点在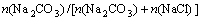 =0.423处,共晶温度为635 ℃。
=0.423处,共晶温度为635 ℃。
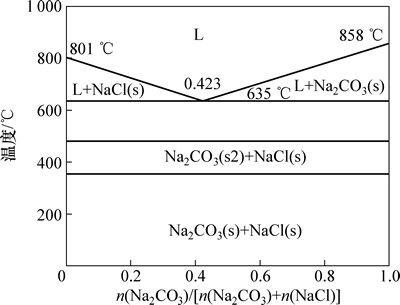
图1 Na2CO3-NaCl二元系相图
Fig. 1 Phase diagram of Na2CO3-NaCl binary system
取干燥后的NaCl和Na2CO3,按共晶成分的组成配成均匀的混合物后装入刚玉坩埚,升温到700 ℃,待物料完全熔化后再保温10 min,冷却后粉碎,置于干燥器中储存。分别取样进行同步热重-差热分析和质量挥发损失实验,进行质量损失实验时每次取20 g熔盐置于20 mL刚玉坩埚中,保温一段时间后冷却并称量,并对最后的样品进行XRD和SEM分析。所有的实验都在氩气保护下进行。
热循环实验的装置如图2所示,电炉带有程序控温系统,100 g混合熔盐装入200 mL刚玉坩埚中后置于电炉中,热电偶插于其中。实验开始时设置电炉以5 ℃/min的速度从室温升到800 ℃,同时打开测温仪和联机测温软件开始记录,800 ℃保温20 min后,以相同速度冷却,进行步冷曲线测量。待温度降到500 ℃时,重复升温过程,进行多次循环测量。运用图3所示的切线法计算样品的开始熔化温度、完全熔化温度和开始结晶温度、完全结晶温度以及熔化时间和结晶时间。

图2 热循环实验装置图
Fig. 2 Schematic diagram of thermal cycle equipment

图3 切线法测定开始熔化和结束熔化温度的示意图
Fig. 3 Schematic diagram of “Tangent intersection method” to determine melting (solidification) start and end temperature
2 结果与讨论
2.1 熔盐的熔点
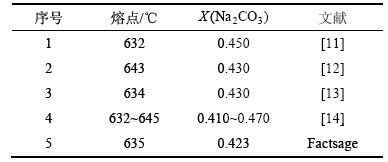
图4所示为纯Na2CO3和NaCl和共晶熔盐的差示量热扫描的曲线。从图4可以看出:纯Na2CO3和纯NaCl的峰值温度为858.64 ℃和811.44 ℃,与Factsage相图中的858 ℃和801 ℃相近,其中氯化钠的实测温度偏高,可能与升温速度和气流有关。共晶混合物的峰值温度在644.51 ℃,比相图中温度要高。表1记录了相关文献中Na2CO3-NaCl共晶熔盐的共晶点的温度和组成,共晶温度在632~645 ℃的范围内,共晶成分中 在0.41至0.47之间,与实测温度较为符合。
在0.41至0.47之间,与实测温度较为符合。
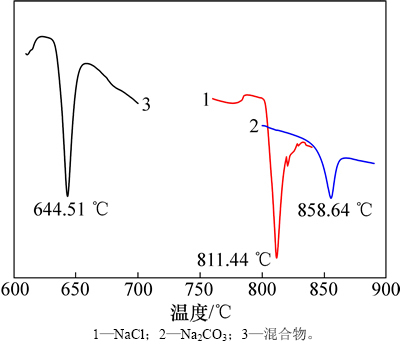
图4 Na2CO3,NaCl和共晶成分的差热曲线
Fig. 4 The DSC curve of Na2CO3, NaCl and eutectic composition
表1 文献中Na2CO3-NaCl体系的共晶点
Table 1 Eutectic point of Na2CO3-NaCl in reference
2.2 熔盐的挥发损失
图5所示为纯Na2CO3、纯NaCl和共晶成分的热重图。从图5可以看出:三者在700 ℃以前的挥发都很少,能稳定地存在。因为氯化钠的蒸汽压较高,在800 ℃已达66.69 Pa[20],当温度升到804 ℃以后,质量减小变得十分明显,挥发损失加剧,到温度上升到1 000 ℃时,质量约损失了90%。对纯Na2CO3,因其熔点较NaCl高,同时蒸汽压又比NaCl低,因此,质量损失并不明显,质量减小的速度也较氯化钠慢得多,当温度上升到1 000 ℃时也只减小了15%。而共晶成分熔盐的质量减少量和速度都介于二者之间,但开始挥发温度降低,在638 ℃以后就有显著挥发,这也接近混合物的熔点,在超过此温度后混合物转变为液相,体系中离子迁移速度加快,离子动能增加,变得比离子间吸引力大得多,因而挥发加快。随着温度的进一步升高,挥发速率加快,到1 000 ℃时质量已经减少了60%。
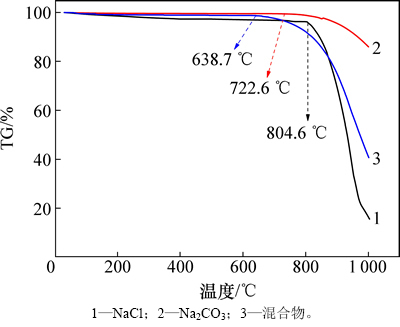
图5 Na2CO3,NaCl和共晶成分的热重曲线
Fig. 5 TG curve of Na2CO3, NaCl and eutectic composition
为宏观定量反映持续时间和温度对挥发量的影响,进行了不同温度下熔盐质量随持续时间延长而变化的实验,其结果如图6所示。从图6可以看出:温度较低时,挥发量很小,在700 ℃时50 h只挥发了3.618 5%,但随着温度升高,明显加快,800 ℃是一个较为明显的转变点,超过此温度后,挥发急剧加快,这是因为超过此温度,分子运动的动能已大于逸出能,再升高温度,蒸汽压会呈指数增加,在850 ℃和900 ℃时50 h的挥发量分别达到了27.939 4%和37.463 7%,且挥发量与时间基本呈线性关系。
2.3 热循环稳定实验
利用在线测温装置测得了熔盐在10次循环过程中的升温和降温曲线,图7所示为Na2CO3-NaCl共晶熔盐循环10次的升降温曲线。从图7可以看出:在一次升降温过程中有2个拐点,一个为熔盐熔化吸热引起的升温滞后,另一个为冷却过程中熔盐结晶时所释放的结晶热,使温度下降速度减慢。在10次循环过程中曲线形状和趋势相同,说明曲线热稳定性好,没有突变发生。
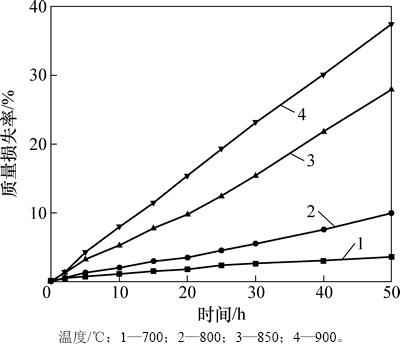
图6 在不同时间和温度下熔盐的质量损失率
Fig. 6 Mass loss rate of eutectic composition at different temperatures and time
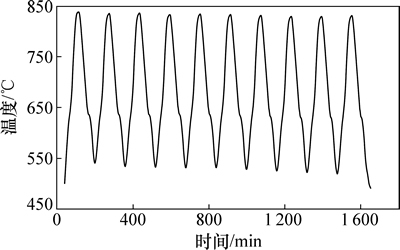
图7 Na2CO3-NaCl共晶熔盐循环10次的升降温曲线
Fig. 7 Heating and cooling curve of NaCl-Na2CO3 eutectic system in 10 times recycling
根据测得的熔体温度随时间变化曲线,运用相变切线法获得开始熔化温度TSS和结束熔化温度TSE,及开始凝固温度TCS和结束凝固温度TCE,同时获得熔化时间△ts和凝固时间△tc,如图8所示。从图8可以看出:Na2CO3-NaCl二元熔盐熔化过程起始温度为612.11 ℃,终止温度为642.783 ℃,其中首次循环的开始熔化温度比后几次循环的温度都要高,这是因为待物料变成熟料后,再熔化的开始温度就稍低,所以,开始熔化温度有下降的趋势。样品的凝固过程起始温度为631.643 ℃,终止温度为619.872 ℃,在10次循环中,试样的熔化起始温度和凝固终止温度有小幅波动,最大波动均在10 ℃之内。可见:Na2CO3-NaCl二元熔盐在多次热循环过程中,相变转化温度基本稳定,符合冶炼过程炉况稳定的要求。
根据图3的方法计算了循环过程中试样的相变时间,如图9所示。从图9可以看出:样品每次熔化时间和凝固时间有局部波动,但总体变化不大,完全熔化和完全凝固所需时间的平均值为16.025 min和14.484 min,误差在5 min以内,呈现稳中有降的趋势,同时样品完全熔化时间较凝固时间要长,因为块状样品由外及内的熔化使内部完全融化所需时间较长。
2.4 XRD分析
图10所示为700~900 ℃的范围内保温50 h后样品的XRD谱。从图10可以看出:图谱基本没有变化,全部为NaCl和Na2CO3的峰,峰的位置和强度较没有热处理时都没有变化,说明共晶成分混合物在高温下成分能保持稳定,各熔盐在高温下能保持较好的化学相容性,同时不发生反应。
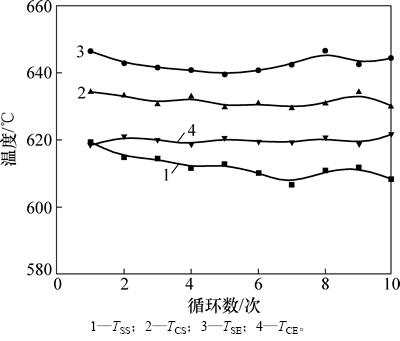
图8 NaCl-Na2CO3二元共晶系开始熔化温度和结束熔化温度随着循环数的变化
Fig. 8 Variations of starting temperature and end temperature about NaCl-Na2CO3 binary system with thermal cycling number
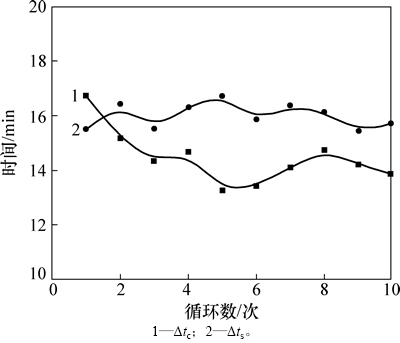
图9 NaCl-Na2CO3二元共晶系熔化时间和凝固时间随着循环数的变化
Fig. 9 Phase change time of melting and freezing about NaCl-Na2CO3 binary system with thermal cycling number
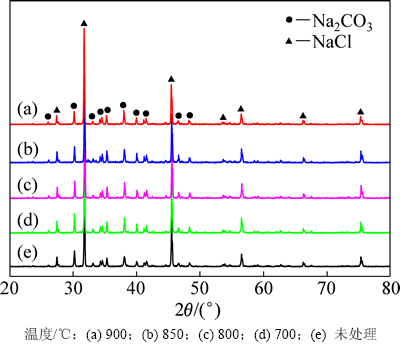
图10 熔盐在不同温度下保温50 h后的XRD谱
Fig. 10 XRD patterns of molten salt insulation for 50 h at different temperatures
2.5 熔盐中Na2CO3和NaCl相对含量的变化
采用滴定法测定了混合盐中的CO32-质量分数,进而推导Na2CO3和NaCl的质量分数,图11所示为在850 ℃下混合物中Na2CO3和NaCl的质量分数随着保温时间的变化。从图11可以看出:Na2CO3和NaCl的质量分数随着保温时间延长变化不大,考虑分析误
差的影响可近似认为其质量分数近似不变,这是因为所选熔盐为相图上的共晶点,混合物为恒沸物,其上方蒸汽的组成与液相组成相同,同步挥发,同时在850 ℃碳酸钠的稳定性较好[1],几乎不分解,组成不会因分解而改变,因而熔融盐中Na2CO3和NaCl的质量分数也会保持不变。
2.6 熔盐的形貌
图12所示为新制熔盐粉末和850 ℃时分别保温20 h和50 h后的样品的SEM像。图12(a)可以看出:
没有经高温处理的熔盐结晶性较好,颗粒多具有规则的形状和不规则的棱角,颗粒堆积在一起较为致密。图12(b)可以看出:颗粒溶合得较好,颗粒之间有明显的界面,形貌较为均匀。

图11 850 ℃时熔盐中Na2CO3和NaCl质量分数随着保温时间的变化
Fig. 11 Variations of mass fraction of Na2CO3 and NaCl with time at 850 ℃

图12 新制熔盐和保温20 h和50 h后熔盐的SEM像
Fig. 12 SEM images of freshly prepared eutectic mixture of Na2CO3-NaCl system at different magnifications
比较保温20 h和50 h后的SEM像可以发现:颗粒间出现了较多的连结,液相表面明显。从图12(e)可以看出:颗粒的结晶性较没有保温时的结晶性更好,同时也比保温20 h后的结晶性好,颗粒的棱角更针锐,多呈长条形。从图12(f)可以看出:颗粒之间连结更多,可见在高温是均匀的液相,Na2CO3和NaCl完全溶合,保温50 h比保温20 h后的颗粒间的连结更多,无明显的界面而形成更大的颗粒,因此,在保温较长时间后熔盐结构变得更均匀,Na2CO3和NaCl相互溶解的更好。
3 结论
1) Na2CO3-NaCl共晶熔盐在高温下容易挥发,其挥发性介于纯NaCl和纯Na2CO3之间,在熔点温度至800 ℃时挥发量很少,但当温度超过800 ℃后,挥发量急剧增加; 共晶熔盐在多次升温和降温循环过程中保持开始熔化温度、完全熔化温度、开始结晶温度和完全结晶温度及熔化时间、结晶时间基本不变。
2) 熔盐的物相在长时间高温处理后保持不变,熔盐成分之间无化学反应发生。熔盐中NaCl和Na2CO3的含量在高温处理后也不发生变化,同时经高温处理后混合物的结晶性和溶合更好,液相成分更均匀,颗粒之间的联结更多。
3) NaCl-Na2CO3共晶熔盐在一定温度范围内是较稳定的体系,使用温度不宜超过800 ℃,其熔点、成分、组成和结构在长时间高温处理后基本保持不变。
参考文献:
[1] JUN Y, DAISUKE M, KOICHI A, et al. Strength of salt core composed of alkali carbonate and alkali chloride mixtures made by casting technique[J]. Materials Transactions, 2007, 48(5): 1034-1041.
[2] NUNES V M B, LOURENCO M J V, SANTOS F J V, et al. Viscosity of molten sodium nitrate[J]. International Journal of Thermophysics, 2006, 27(6): 1639-1648.
[3] CHEN G Z, FRAY D J, FARTHING T W. Direct electrochemical reduction of titanium dioxide to titanium in molten calcium chloride[J]. Nature, 2000, 407(9): 361-364.
[4] ZHAO C Y, WU Z G. Thermal property characterization of a low melting-temperature ternary nitrate salt mixture for thermal energy storage systems[J]. Solar Energy Materials & Solar Cells, 2011, 96(12): 3341-3346.
[5] OLIVARES R I. Thermal stability of molten nitrite/nitrates salt for solar thermal energy storage in different atmospheres[J]. Solar Energy, 2012, 86(9): 2576-2583.
[6] L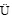 W Y, ZENG C L. Praparation of cohesive graphite films by electroreduction of
W Y, ZENG C L. Praparation of cohesive graphite films by electroreduction of 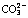 in molten Na2CO3-NaCl[J]. Surface & Coatings Technology, 2012, 206(19/20): 4287-4296.
in molten Na2CO3-NaCl[J]. Surface & Coatings Technology, 2012, 206(19/20): 4287-4296.
[7] 叶龙刚, 唐朝波, 唐谟堂, 等. 硫化锑精矿低温熔炼新工艺[J]. 中南大学学报(自然科学版), 2012, 43(9): 3338-3343.
YE Longgang, TANG Chaobo, TANG Motang, et al. Separation antimony from stibnite concentrate through a low temperature smelting[J]. Journal of Central South University(Science and Technology), 2012, 43(9): 3338-3343.
[8] MARGULIS E V. Low temperature smelting of lead metallic scrap[J]. Erzmetall, 2000, 53(2): 85-89.
[9] GUTIERREZ J, ROMERO-SERRANO A, PLASCENCIA G. Thermodynamic model for ternary silicate system[J]. ISIJ International, 2000, 40(7): 664-669.
[10] SEETHARAMAN S, MUKAI K, SICHEN D. Viscosities of slags: an review[J]. Steel Research International, 2005, 76(4): 267-278.
[11] JUN Y, KATSUNARI O, KOICHI A. Thermodynamic assessment of the KCl-K2CO3-NaCl-Na2CO3 system[J]. Computer Coupling of Phase Diagrams and Thermochemistry, 2007, 31(2): 155-163.
[12] KOKORO I, MASAFUMI M. Phase diagram study for the alkali metal-oxychloride[J]. Metallurgical and Materials Transaction B, 2000, 31(4): 795-799.
[13] KOKORO I, SHU Y, MASAFUMI M. Phase relation and thermodynamic properties of NaCl-Na2CO3 system as a basic system for secondary fly ash in incineration processes of municipal wastes[J]. Materials Transaction, 2001, 42(12): 2480-2486.
[14] DESSUREAULT Y, SANGSTER J, PELTON A D. Coupled phase diagram-thermodynamic analysis of the 24 binary systems, A2CO3-AX and A2SO4-AX where A=Li, Na, K and X=Cl, F, NO3, OH[J]. Journal of Physical Chemistry Reference Data, 1990, 19(5): 1149-1178.
[15] KUBASCHEWSKI O, ALCOCK C B. Metallurgical thermochemistry[M]. London: Pergamon Press Ltd, 1979: 25-50.
(编辑 陈爱华)
收稿日期:2015-09-11;修回日期:2015-12-18
基金项目(Foundation item):国家自然科学基金资助项目(51104128,51234009)(Projects(51104128, 51234009) supported by National Natural Science Foundation of China)
通信作者:唐朝波,博士,副教授,从事火法清洁冶金新工艺研究;E-mail:tangchaobo9043@163.com