DOI��10.19476/j.ysxb.1004.0609.2019.09.05
�����\����Կ���������Դ���õĴ���
����ܣ���ѧ��
(���ϴ�ѧ ��Դ�ӹ������﹤��ѧԺ������ұ��������ص�ʵ���ң���ɳ 410083)
ժ Ҫ������ұ����Ӧ����ȫ��50������Һ͵������й��ڹ��������罨���˻��ڻ�����ѧ��ұ�����ﶨ����������ʵ�������������Ϊ�о��ɱ������������ת�䣻��������ֲ��������ۻ�ѧ��Ӧģ�ͣ�ʵ��������ұ���о��Ӻ�۵��۵Ŀ�Խ������ұ�����ǿ���������ں�����õ����ģ��ҵ��Ӧ�ã��������괦����ʯ����6000��t������ͭ�����γ��˾�������֪ʶ��Ȩ��CCGRI����������������������й��ƽ���ҵ�ĵ�һ��������ҵ��ʾ�����̣�����������˿���˽����������96%��ʹ�˿�Ʒλ��ǧ��֮һ���͵����֮�����й�����ұ���Ѵ����������ȵ�λ����ʹ�����Դ�����ʴ�33%��ߵ�96%����������й������Դ��ʹ�����ޡ�
�ؼ��ʣ����\��������ұ�𣻿����Դ��������Ϊ
���±�ţ�1004-0609(2019)-09-1848-11���� ��ͼ����ţ�TF18���� ���ױ�־�룺A
���й�������������ʪ��ұ��ļ����ǹ�Ԫǰ�������͵ġ�ɽ���������ɹ�֮ɽ���Cˮ���ɣ�����ע��μ�����ж�ͭ����������������д�ġ���������������С��������������Ϊͭ���ĵ�ˮ��ͭ���أ��ơ���������йٰ��ʪ����ͭ��������ʱ���ͭ�����ﵽ100�����ÿ��[1]��
1670���й��������������͢�п������Կ��ˮ������ͭ��ʯ�ı�����1947�꣬�״η��������ϸ����������������˾���1958�꣬��һ������ʪ��ұ��ר���ɹ�����[2]�����ͬʱ�����Ͽ�ұѧԺ(�����ϴ�ѧǰ��)�θ���������1958����ѡ��¥����������ұ��ʵ���ҡ��й���ѧԺ�����о�����1960���ͭ��ɽͭ�����ͭ������ұ��ҵ�����о���1970�꣬���ǽ����˴�����Ϊ700 tƶ�˿�ʯ��ϸ���ѽ��������顣1976�꣬��һ���������ʪ��ұ�����ٿ�(��������23��)��1995�꣬���Ϲ�ҵ��ѧ(�����ϴ�ѧ)��ʼ���н�������ͭ�������ʯ������������飬����1997�꽨�������2000 t������ʪ����ͭ��[1]��
1999�꣬���ϴ�ѧ���������������ʵ���Һ�����ʼ���н���������̬�������о���2004�꣬���������״������ұ������ģʽ������������������˾�23270��ȫ���������2007�꣬���ϴ�ѧ�ƶ��ͷ����ˡ���������������˾�������ԵĻ���оƬ��ⷽ�����Ĺ��ұ���ʵ���˸�Ч������ֵĿ��١�ȷɸѡ[3]��2005�������ϴ�ѧ�ͱ�����ɫ�����о�Ժ������ָ���£��й��Ͻ��ҵ����3��t����ͭ������ȡ�����ɣ�����ͭ���ȴﵽ����A������2011�꣬���ϴ�ѧ�а�ĵ�19���������ʪ��ұ���ᣬ�λ���Ա����500�����������˹�������ʪ��ұ��ѧ�ᣬ�ܲ����ڳ�ɳ[1]��
1 ����ұ����й���ɫ������ҵ��չ������
�����й���ҵ�����̵ļӿ죬ͭ�����˵���ɫ�������Ѽ������ӣ��ҹ������Դ�����ı�֤�̶������Ͼ�����ͭ����������֤������20�꣬����15�ꡣ����������ɫ������Դ��70%������Ʒλ���Ѵ������Ӷ�������ô�ͳѡұ�������ܾ�����Ч�����ò��ֿ����Դ��ʹ���ҹ����������Դ�����������ض�ȱ��״������Ϊ��Լ�ҹ����÷�չ����Ҫ����֮һ��
����ұ������������(ϸ������������)����ʯ�е��м۽����ܽ������ͨ��֮�����ȡ��������Ʊ��ߴ����������ͼ�����������ұ������ȣ�����ұ��������гɱ��ͣ������Ѻ�(��ͼ1)��������Ч���յ�Ʒλ�������Ѵ��������Դ�����ơ�Ŀǰ���Ѿ�ȫ��50������Һ͵���ʵʩ��ҵӦ�á�
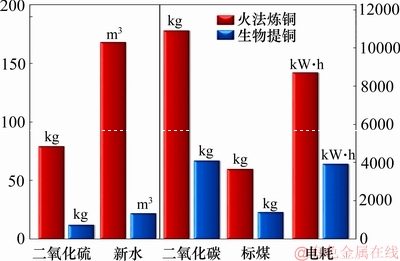
ͼ1 ������ͭ�����ͭ���ܺ����ŷűȽ�
Fig. 1 Comparison of energy consumption and pollutants emission between copper biohydrometallurgy and copper pyrometallurgy
��ͭ��Դ���棺�й����ֽ������һ��ͭ���ѹ�����Ŀǰ�й���ɽ�Բ�ͭ��ռʹ������20%���ң���������ʪ��ұ����������Ʒλ��ͭ��Դ������ʹ�ɾ�������ͭ��Ʒλ��ͽ���0.1%���й�ͭ��Դ������2000��t���ϣ���Ӧ���ڷ����������ҵĵ�Ʒλ��Դ�Ŀ������á�
�ڽ����Դ���棺�ҹ�Ŀǰ�Ѵ��������ԴԼռ��̽���ƽ�����2/3���ϣ����������Ѷȷdz�������Ԥ������������Ч�����ⲿ���Ѵ��������Դ����������Ԥ���������ķ�չ���й��ƽ�������������Ϊ�����һ����������ƹ�Ӧ�ã��Ա����й��ƽ��������������ˮƽ�Ͳ�����ʾ���������Ҫ�����塣
������Դ���棺����ұ������ʹ�ҹ��������û����������������˿���Դ�õ���Ч���ã�������ʹ�˿���Դ����Ʒλ��Ŀǰ��ǧ��֮һ���͵����֮�����Ӷ�ʹ�˿�ɾ��ÿ��ɴ���������ӡ�
2 �й�����ұ���о���չ
2.1 �Ӻ�۵���
1999��֮ǰ���ҹ�����ʪ��ұ���о���ͣ���ں�۵IJ�Ρ���Чұ�������ɸѡ��Ҫͨ�������жϣ�ѡ�������ɫ�Ŀ��ˮ����ȡ��Ʒ(��ͼ2)��Ȼ���ں��ʵ����������½��н�����������������������¹۲�ϸ������(��ͼ3)����һ��ͨ����������ⶨ��ͬϸ�����������ԺͿ��Ե�����(��ͼ4)������ҺpH�½�(������������������)������Һ��ɫ��ɺ�ɫ(��������������������)ʱ����������˽Ϻõ�ұ������ڵ�ʱȴ����֪Ϊʲôұ�����������Ӧ�������������������ȱ���������Ķ����оݡ�

ͼ2 ����ɫ�����Կ��ˮ
Fig. 2 Acid mine drainage with liver-coloured
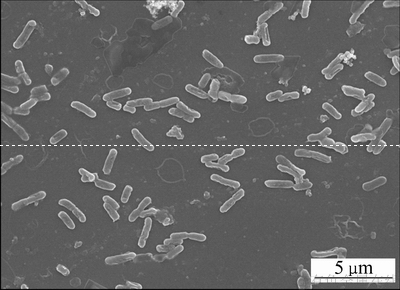
ͼ3 ɨ��羵�¹۲쵽��ϸ��
Fig. 3 Bacteria observed under SEM
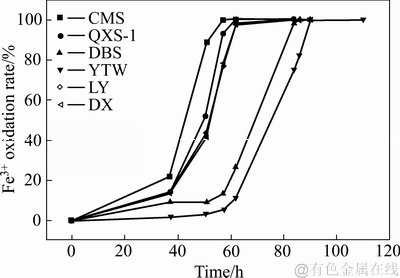
ͼ4 ��ͬA.f �������������ԺͿ��Եȷ���IJ���
Fig. 4 Bioleaching performance of A. f. strains with different oxidation activity and resistance activity and resistance of different A.f strains lead to different leaching effects
2004�꣬���ϴ�ѧ�μ������ϵ�һ������ұ��������������������˾�23270��ȫ����������о�����(��ͼ5)�����ڻ�øþ�ȫ��3217��������Ϣ�Ļ����ϣ�������ȫ������оƬ��ͨ���Ƚϻ�����ѧ����320�����������ԵĻ������а���135�������������������Լ�������ػ���(��ͼ6)[4]��Ȼ���ƶ��ˡ���������������˾�������ԵĻ���оƬ��ⷽ�������ұ�(GB/T 20929��2007)��ʵ���˸�Ч������ֵĿ���ȷɸѡ����������������˾�ȫ������ͼ����ע��Ϊ�ӻ���ˮƽ��չ��������춨�˻�����ʵ�������������Ϊ�о��ɱ������������ת��[4]��
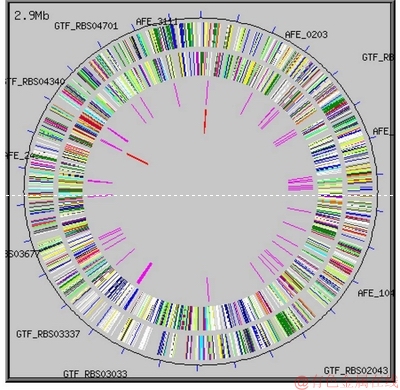
ͼ5 A. f ATCC 23270ȫ������ͼ��
Fig. 5 Whole genomic spectrum of A. f. ATCC 23270
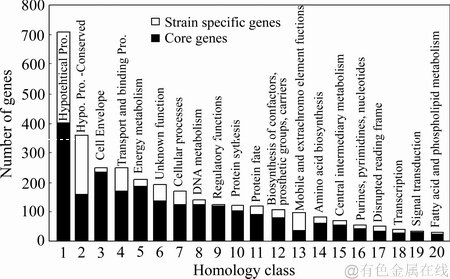
ͼ6 ��ͬA .f���깲�к����л����ֲܷ�
Fig. 6 Common and specific gene function distribution of different A. f. strains
��������ı������������ʯ����ú��ʯ�ֲ������ֽ⣬�����ַ�Ӧ��Ҫ�����ڿ���-��Һ-�����������ϡ���ˣ���ʾ����ұ����ϵ����������õ��ۻ��ƾ�����Ҫ�����塣��2008�꿪ʼ�����ϴ�ѧ����ͬ��������Ƚ�������̽����ԭ����ͭ��������������еĶ����м���P����Ӧ�Ļ�ѧ��Ӧ����������ֲ�����ģ��(��ͼ7)�������˸ù��̵Ķ���ѧ����[5]��ȷ����Fe�����ܽ��Ǻ�����ͭ�����ܽ�ij�ʼ���裬������Cu2S��������ԭ����ͭ���ܽ�Ĺؼ����裬�͵�λ����ת��ΪCu2S�Ĺؼ�����[6-7]������������ϵ������Ũ�ȼ�Fe3+/Fe2+��ֵ��ά�ֽ�����ϵ�ĵ͵�λ((430��20) mV)������ͭ�Ľ������ʿ������1������(��ͼ8)��
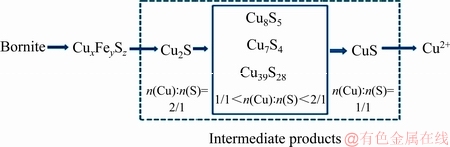
ͼ7 ������ͭ����������̵ķֲ�����ģ��
Fig. 7 Stepwise oxidation model for bioleaching of copper sulfide containing iron
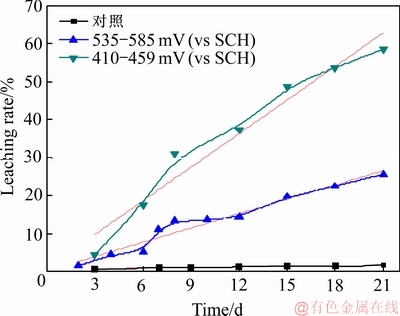
ͼ8 ��ͬ��λ������ͭ�������ʵı仯
Fig. 8 Copper bioleaching rate under different potential conditions
2.2 �Ӷ��Ե�����
������������У�������������ࡢ��״�빦�ܲ��������ù�ϵ���ӣ����Ҵ������������Ŀǰ�в����˹���������ͳ���Է�������Ϊ�����ķ����������ԶԽ���������ж���������ʵʱ��ء����⣬��������Ĺ��ܻ��һ�ַdz��۵����ã���ͳ�����ﻯѧ��Ӧ�ⶨ������������������������ѧ�����ķ��ٷ�չ������ͻ����顢�������ȼ���Խ��Խ�౻Ӧ��������ұ�����������ǻ����鼼����Ӧ�ã�ʹ��ұ������Ķ��������˸����Եı仯���Ӷ�ʹұ�������о�ˮƽ�ӵ����ĵ�һ�����������������幦�ܺ;�Ⱥ���幦��(��ͼ9)��
���û�����ѧ������ʵʱ�������ѽ��������������̬�����ԣ��Ӷ�Ϊ���ܾ�Ⱥ�ĵ����ṩ����ָ�������ϴ�ѧ��2008���ڹ㶫÷����ˮ��ͭ�����ȿ�չ��Ʒλͭ��ĵ�������ѽ��о�������Ⱥ��������о������ͨ������������������ʱ���ֵȷ������ֹ��ܾ�Ⱥ�Ļ��ԣ�������������˽���Ч��(��ͼ10)[8]��
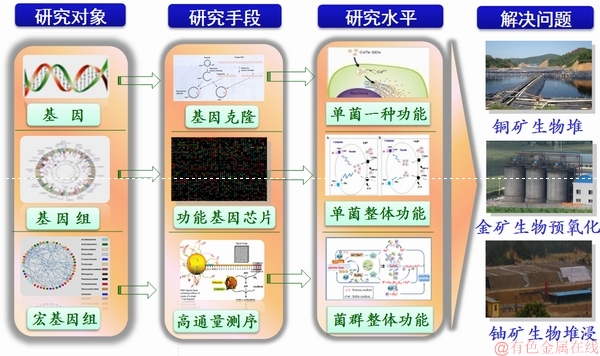
ͼ9 ����ұ��ķ�������ѧ����
Fig. 9 Molecular biological technique of biohydrometallurgy
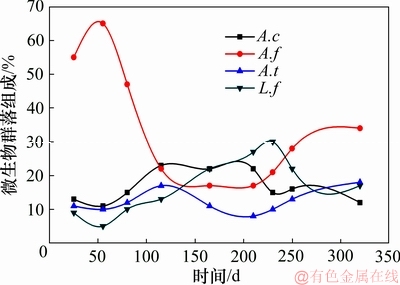
ͼ10 ����ѽ�����������Ⱥ��ṹ����仯����
Fig. 10 Microbial community structure and its change trend during heap bioleaching process
ұ������Ķ�����ˮƽ�������ú������ѧ��������������أ������Բ���OUT����ˮƽ�������������ߡ����ϴ�ѧ�Խ�������ͭ������ѽ���ϵ��������Լ����(��ͼ11~13)���������ô�ͳ�Ŀ�¡�Ŀⷨ�ⶨ������30~60��������454����⣬��OUT��Ϊ200~300��������MiSeq������OTU����1000~2000��[9]��
����оƬ����������Ⱥ��ṹ�빦�ܶ�����������Ч�ֶΣ����ϴ�ѧ�Ⱥ�չ��4��ұ���������оƬ����(����1)[10]���ֱ��ǿ���ʵʱ��⸴����ϵұ��������Ⱥ�ṹ�붯̬��Ⱥ�������оƬ���������������ȴ�0.1 ng������DNA[11]����ȷ��������ұ���������������Ȼ��ԵĹ��ܻ�����оƬ���������������ȴ�5 ng������DNA[12]���ܿ���ɸѡ�ض�Ŀ�����/����ص�ұ������������оƬ�����������øü��������˴���δ֪��������ܻ���[13]������ϵ�л���оƬ�����Ŀ�����ʵ����ұ������Ⱥ��ṹ�빦�ܵĶ�������ȷ�Ϳ��ٷ�����ͻ�������������ܽ�����о��ļ���ƿ����
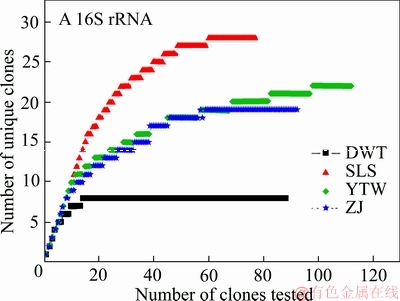
ͼ11 ��¡�ĿⷨOUT 30~60(��¡��100~200)
Fig. 11 Clone library method OTU 30-60 (clone number 100-200)
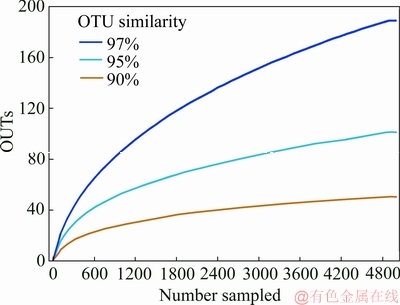
ͼ12 454����OUT 200~300(Reads��5000~8000)
Fig. 12 454 sequencing OUT 200-300 (Reads number 5000- 8000)
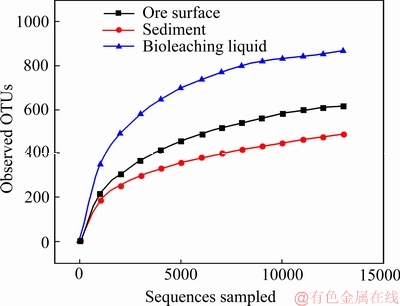
ͼ13 MiSeq����OTU1000~2000(Reads��20000~30000)
Fig. 13 MiSeq sequencing OTU 1000-2000 (Reads number 20000-30000)
2.3 �����۵�ʵ��
2.3.1 ͭ����Դ������ұ��
ͭ��������ұ����Ӧ����Ϊ�㷺�Ķ���֮һ���ѽ���ͭ������ұ�����ҪӦ�����͡���1995~2015���30��䣬ͭ������ѽ��Ĺ�ģ�Ѵ��ҹ��Ͻ�ɽͭ��������5��t/a�������ޱ���¬���ĵ�6000��t/a(��ͼ14)����ֹ��Ŀǰ������ʪ��ұ������ͭ���ѳ���ȫ��ͭ������20%[14-15]��
1) ��������ͭ��Ʒλͭβ�������ʪ��ұ����Ӧ��
�й���������ͭ�������ѽ�����������ұ�����ɹ�Ӧ�õĵ䷶������ͭҵ��˾����ͭ���ڼ�ʮ���¶�ɹ����У������˴�����ͭԼ0.05%~0.25%�ķϿ�ʯ��������������3.5��t����ͭ����ԼΪ60��t�����ڸ÷Ͽ�ʯ�е�ͭ��Ҫ��ԭ����ͭ��ʽ���ڣ����ô�ͳ��ѡұ�������ѻ������е�ͭ��Դ��20����90������ù�˾�����ϴ�ѧ������չ�����˵�Ʒλ���˹�ϸ����������ȡ��������η����о����롰����ͭ���Ʒλϸ���������ָ����ʹ��������乤ҵ��Ӧ���о�����ͨ�����ϴ�ѧ�Ƚ��ľ��ֶ���������������ɸѡ������������Ըߡ����ж���������ǿ�ĸ�Ч���֣����������ͭ�Ľ����ʺͽ������ʡ���������һ���������Ϊ2000 t��ͭ�����������ȡ�������(��ͼ15)[16-17]��
��1 ��Ҫұ���������оƬ�����Ƚ�[10]
Table 1 Comparison of microarray characteristics of major bioleaching microorganisms[10]


ͼ14 ͭ������ѽ���ҵ��Ӧ��
Fig. 14 Industrial application of heap bioleaching for copper ore

ͼ15 ��������ͭ������ұ��ҵӦ��
Fig. 15 Application of biohydrometallurgy in Dexing copper mine, Jiangxi province
2) �����Ͻ�ɽͭ���Ʒλ����������ұ��������Ӧ��
�Ͻ�ɽͭ��λ�ڸ���ʡ�Ϻ��أ��õ���̽����ͭ����2.4��t��ͭ��ƽ��ƷλΪ0.063%����ʯ��ͭ�����Դ�����Ϊ������Ҫ������ͭ��ͭ��������ͭ��ȡ�����ͭƷλ�dz��ͣ���ͳ�ĸ�ѡ���������ղ��ܾ�����Ч�ش������ֿ�ʯ��������ʪ��ұ������һ������֮·���봫ͳ������ȣ�����ұ������������������Դ������������Դ���ģ����һ����Լ����ữ������ЧӦ�����нϴ�ľ��á���ἰ��̬Ч��(����2)���Ͻ�ɽͭ����½�����ɲ���1��t��2��t��5��t/a�ĵ�Ʒλ����������ұ��������[18-19]��
3) �ޱ���ǫ��ϣͭ��
����ұ���о��ɹ������ڹ���ȡ���˽Ϻõ�Ч��������һ���ƹ㵽�˹��⡣2010���ޱ��ǿ�ҵ�������ϴ�ѧǩ��ս�Կ�ܺ���Э�飬�����ˡ��й���ɫ���š����ϴ�ѧ�ޱ�������ұ������ҵ��ʾ�����ء�����������ұ���������ù������ı����β����Դ��
2011��3�£��ޱ���ǫ��ϣʪ��ұ����˾ͬ���ϴ�ѧ������չ��Ʒλͭ�Ͽ�ʯ������ѽ���ҵ�о���ͨ��ɸѡ��������ѱ�����ؽ������ʹ����Ͽ���Ӧ�˶ѳ���������������������[20]����Ը�������Ⱥ�����������ٶ�����Ⱥ��ṹ�ȶ��Բ���ģ�ѳ�ϸ����ֳ�ѵ����⣬�������Թ�ҵ����Ϊ�������ʵľ�Ⱥ��Ч��������ٶ�ֳ�����η�����������ģ��5 L��50 L��1 m3��20 m3��ߵ�150 m3(��ͼ16)����������ľ��ֽ��ֵ�����У���ʹ�����ѽ���ϵϸ��Ũ��������ߣ��Ӷ����̶ѽ�ʱ�䣬���ͭ�������ʺͽ�����[21]��
��2 ������ͭ�����볣������¯��ͭ�Ա�
Table 2 Comparison of copper bioleaching process with conventional copper flash smelting

ͼ16 �ޱ���ǫ��ϣͭ����������������������
Fig. 16 Expanded culture process of microorganisms from Chambishi copper mine in Zambia
��60��t��Ʒλͭ��ʯ������ѽ���ҵ�����У� 2������ͭ�Ľ����ʴﵽ50%������Һͨ����������ȡ-������գ���ô���99.99%������ͭ���ڲ��ı�ԭ�����������Ļ����ϣ����е�����ұ������ʹǫ��ϣʪ����ͭ���ѽ�ͭ���������20%����Ľ���35%���ϣ�������ǰ���ܻ��յ�ͭ��Դ�õ�����Ч����(����3)[22]��
4) �ޱ���������ϣͭ��
������������ϵ�й���������������ѧ���غ�����Ⱥ��ṹ�빦��ƥ���ѵ����⣬���ϴ�ѧ����ɫ¬����ͭҵ��˾������ϣ�ѽ���Ϊ�о�����չ�����������ǿ�������о������ú������ѧ�������Զ��ڵ�����Ⱥ��ṹ�빦�ܽ���ʵʱ��⣬��ȷ��Ͷ�Ÿ�Ч�����Ⱥ����ڽ��������е����ã������˽������̲�ͬ��Ⱥ��������ɣ�����ǰ���������¾�Ϊ�����������ʶ����Ⱦ�Ϊ���������Ը��¾�Ϊ����ͬʱ���ֶ����¶��������ͬʱ�����ߣ��ɽ������ڵ���Ȼ�¶�������� 65 �����ϡ���һ��ͨ�������������ϵpHֵ��������ԭ��λ(ORP)���о������ֽ���������ƽ����Ժ���ϵ������ǿ��pH�½����¶������ߣ�ORP�������������¶ȵ����ӿ������Ӧ����λ�����������˻�ͭ��ת��Ϊ��ͭ��Ľ��У��Ӷ������˽���Ч��[23-24]�����������ɵĻ����ϣ��������ԡ���Ⱥ�ֶ�Ͷ�š���λ���غ�ά�ֽϵ�pH��Ϊ���ĵĽ�����ϵ�Ż����ؼ���(��ͼ17)���ü���Ӧ����������ϣ6000��t��ʯ�ѽ�����ͨ��5���µĽ�����ͭ�����ʴ�85%������Ȼ������ϵ��ȣ�ͭ���������25%��
��3 ����ұ���ԭ������������̲���������ָ��Ա�
Table 3 Comparison of technological parameters and indicators between bioleaching and original acid leaching process
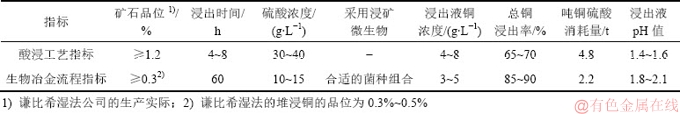
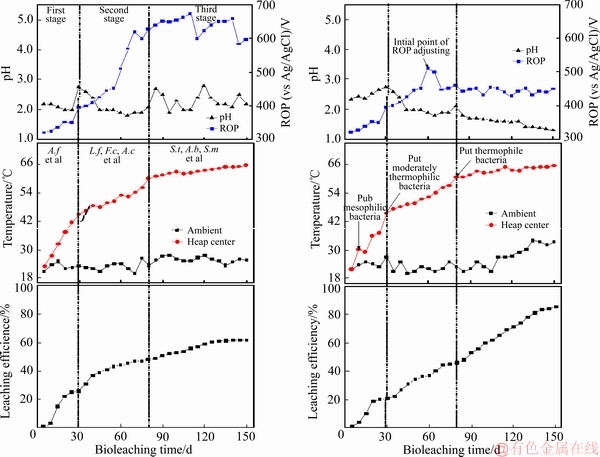
ͼ17 ��Ȼ������ϵ��Эͬ�Ż����ؼ�����ϵ�����Ա�
Fig. 17 Comparison of parameters between natural leaching system and collaborative optimal control technology system
2.3.2 �������Ԥ��������
�ҹ�Ŀǰ�Ѵ��������ԴԼռ��̽���ƽ�����2/3���ϣ����������Ѷȷdz�������Ԥ������������Ч�����ⲿ���Ѵ��������Դ[25]����������Ԥ���������ķ�չ���й��ƽ��������12���Ϊ�����һ(��ͼ18)����������ƹ�Ӧ�ã��Ա����й��ƽ��������������ˮƽ�Ͳ�����ʾ���������Ҫ�����塣
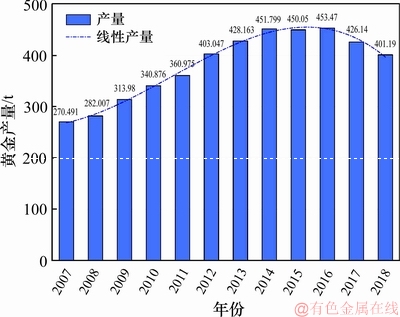
ͼ18 �й��ƽ����
Fig. 18 Gold production in China
�й��ƽ�����������ҵ��˾�Ժ����ѽ���Ϊ����Ŀ�꣬Χ������������-�軯�����·�ߣ�����������������������������£��γ��������ġ���������֪ʶ��Ȩ��CCGRI�����������������ʵʩ���ƹ���ʾ�����������ڵضԽ�����Ķ����� ����ѱ��������������BIOX���պ�BACOX���ղ�ͬ�Ľ��̾�(����ΪHY-ϵ�о�)���Ըþ���Ϊ���Ľ�����ع��յļ����������γ���CCGRI����ϵ�С������˹��ڻƽ���ҵ�ĵ�һ��������ҵ��ʾ�����̣���2003��7��Ͷ���������ȶ�������10����[26]��
2.3.3 �˿�������ȡ����
����ұ������ʹ�ҹ��������û����������������˿���Դ�õ���Ч���ã��˽����ʿɸߴ�96%(��ͼ19)[27]��������ʹ�˿���Դ����Ʒλ��Ŀǰ��ǧ��֮һ���͵����֮�����Ӷ�ʹ�˿�ɾ��ÿ��ɴ���������ӡ�
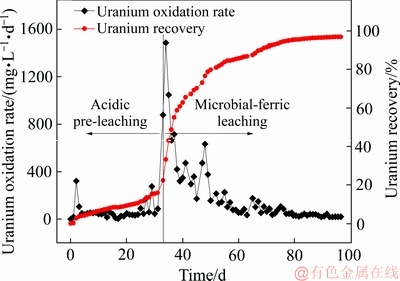
ͼ19 �˿���������������������
Fig. 19 Oxidation and recovery rate of uranium ore by bioleaching
3 չ��
���ϴ�ѧ����ұ���ص�ʵ����ͨ����30��Ŀ��й��أ��ѷ�������ұ����ѧ������700��ƪ����BioleachingΪ�ؼ�����Web of Science���ݿ���м������֣����ϴ�ѧ����ұ��������������λ��ȫ���һ������ѧ����������ϴ�ѧ����ұ�������Ĺ��������˽ϸ����ۡ����������ƻ�����ϯGeorge Weinstock������Forward for 24th International Mineral Processing Congress (IMPC)�����ۡ�û���뵽���������ұ���о��Ѿ��ﵽ�˻����Σ����ܻ����о��ɹ��Ѹ��ҵӦ�á�������������̬ѧѧ��������ϯ��������ѧ����ϯJames TiedjeԺʿ���ۡ�ʹ����ұ���о������˻������ͻ�����ˮƽ�������﹦�ܻ�����ѧ�о����������ǰ��ͬ����[28]����Hydrometallurgy����־����David Muir���ۡ���������������Ϊ����ұ�������ش��ס���
���⣬�ޱ�������ұ���ҵ��ʾ�����صĽ��裬��Ϊ����ұ���ں���ijɹ�Ӧ������һ�����ġ�����ұ�������ޱ��ǵ��ƹ�Ӧ��ʹ�������ͭ��Դ������һ�������Դ�������ͭ��Դ�Ŀ��������ʣ������ޱ����µ�ͭ��ҵ���������ͭ����ĵ�λ��ͬʱҲΪ�ҹ���������Ľ���ͭ��Դ���ڹ��ڣ���ͳ�IJ�-ѡ-ұ-�������켼������Դ�����ʽ�Ϊ33%���ң�����������������ѧ������Ϊ�����Ŀ����Դ���ﴦ����������ʹ��Դ������ߵ�96%���ң��������3�����ҡ���Դ�����ʵ���߿���Ч��߿����Դʹ�����ޣ��Ӷ����Ϲ��ÿɳ�����չ(��ͼ20)������ұ��������������Ӧ������ؿ����Դ���ɡ����п�ɽ��Դ�����Լ������ؽ�����Ⱦ�����ȶ�������䷢չǰ��ʮ�ֹ�����
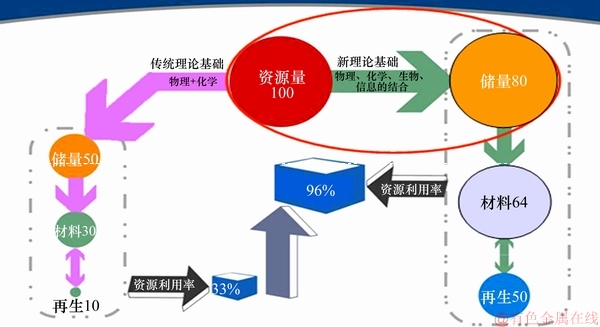
ͼ20 �����Դ�����ʱ��Ϲ��ÿɳ�����չ
Fig. 20 Improving utilization rate of resources to ensure sustainable development of national economy
��л
��л���ҷ���ί����ʾ������([2001]1907��)�������ص�����о���չ�ƻ�������Ŀ(2004CB619200��2010CB630900)�����Ҹ����о���չ�ƻ�������Ŀ(2007AA060900��2012AA061500)��������Ȼ��ѧ����ί����Ⱥ��(50321402��50621063)����ʺ����ص�(������Ȼ��ѧ����ί����Ⱥ��(50321402��50621063)����ʺ����ص�)�����ҽ�����111�ƻ�(B07043)����Ŀ�Ĵ�����������л������ɫ�����о���Ժ���й���ѧԺ��������ɽ����ѧ��������ұ�о���Ժ���й���ҵ��ѧ���ϻ���ѧ��������ѧ�ȵ�λ�ĺ����뽻������л�й���ɫ��ҵ��������˾���й��ƽ�������˾���й��˹�ҵ��������˾����ұ��ɫ�������ſع�����˾�����Կ�ұ�������ι�˾������ͭҵ���Ź�˾���㶫��ɽ��ҵ��˾���㶫����ͭҵ��˾����ҵ��֧�֡�
REFERENCES
[1] WANG D Z, QIU G Z, LIU X D. The progress of biohydrometallurgy in China[C]//Proceedings of 19th International Hydrometallurgy Symposium, 2011: 13-20.
[2] BRIERLEY J A, BRIERLEY C L. Present and future commercial applications of biohydrometallurgy[J]. Hydrometallurgy, 2001, 59(2/3): 233-239.
[3] �� ��, ��ѧ��, �����. ���ڻ���оƬ�������������Ⱥ��ṹ�������������������[J]. ���﹤��ѧ��, 2008, 24(6): 968-974.
SHEN Li, LIU Xue-duan, QIU Guan-zhou. Gene function and microbial community structure in sulfide minerals bioleaching system based on microarray analysis[J]. Chinese Journal of Biotechnology, 2008, 24(6): 968-974.
[4] LUO H L, SHEN L, YIN H Q, LI Q, CHEN Q J, LUO Y J, LIAO L Q, QIU G Z, LIU X D. Comparative genomic analysis of Acidithiobacillus ferrooxidans strains using the A. ferrooxidans ATCC 23270 whole-genome oligonucleotide microarray[J]. Anadian Journal of Microbiology, 2009, 55(5): 587-598.
[5] FANG C J, YU S C, WANG X X, ZHAO H B, QIN W Q, QIU G Z, WANG J. Synchrotron radiation XRD investigation of the fine phase transformation during synthetic chalcocite acidic ferric sulfate leaching[J]. Minerals, 2018, 8(10): 461.
[6] GU G H, HU K T, ZHANG X, XIONG X X, YANG H S. The stepwise dissolution of chalcopyrite bioleached by Leptospirillum ferriphilum[J]. Electrochimica Acta, 2013, 103: 50-57.
[7] GU Guo-hua, XIONG Xian-xue, HU Ke-ting, LI Shuang-ke, WANG Chong-qing. Stepwise dissolution of chalcopyrite bioleaching by thermophile A. manzaensis and mesophile L. ferriphilum[J]. Journal of Central South University, 2015, 22(10): 3751-3759.
[8] �� ��, ������, �����. ��Ʒλ������ͭ���������������ʵ��[M]. ��ɳ: ���ϴ�ѧ������, 2015: 110-129.
WANG Jun, QIN Wen-qing, QIU Guan-zhou. Theory and practice of bioleaching of low grade complex copper sulfide[M]. Changsha: Central south university press, 2015: 110-129.
[9] ZHANG X, NIU J J, LIANG Y L, LIU X D, YIN H Q. Metagenome-scale analysis yields insights into the structure and function of microbial communities in a copper bioleaching heap[J]. BMC genetics, 2016, 17(1): 21.
[10] YIN, H Q, LIU X D. Bioleaching microarrays for profiling microbial communities in acid mine drainage and bioleaching ecosystems[M]. Microarrays: Current Technology, Innovations and Applications, Book Chapter, 2014: 181-193.
[11] CHEN Q J, YIN H Q, LUO H L, XIE M, QIU G Z, LIU X D. Micro-array based whole-genome hybridization for detection of microorganisms in acid mine drainage and bioleaching systems[J]. Hydrometallurgy, 2009, 95(1/2): 96-103.
[12] YIN H Q, CAO L H, QIU G Z, WANG D Z, KELLOGG L, ZHOU J Z, DAI Z M, LIU X D. Development and evaluation of 50-mer oligonucleotide arrays for detecting microbial populations in Acid Mine Drainages and bioleaching systems[J]. Journal of Microbiological Methods, 2007, 70(1): 165-178.
[13] GUO X, YIN H Q, CONG J, DAI Z M, LIANG Y L, LIU X D. RubisCO gene clusters found in a metagenome microarray from acid mine drainage[J]. Applied and Environmental Microbiology, 2013, 79(6): 2019-2026.
[14] YIN S H, WANG L M, KABWE E, CHEN X. YAN R F, AN K, ZHANG L, WU A X. Copper Bioleaching in China: Review and Prospect[J]. Minerals, 2018, 8(2): 32.
[15] YANG S R, XIE J Y, QIU G Z, HU Y H. Research and application of bioleaching and biooxidation technologies in China[J]. Minerals Engineering, 2002, 15: 361-363.
[16] WU A X, YIN S H, WANG H J, QIN W Q, QIU G Z. Technological assessment of a mining-waste dump at the Dexing copper mine, China, for possible conversion to an in situ bioleaching operation[J]. Bioresource Technology, 2009, 100(6): 1931-1936.
[17] LIU Q M, YU R L, QIU G Z, FANG Z, CHEN A L, ZHAO Z W. Optimization of separation processing of copper and iron of dump bioleaching solution by Lix 984N in Dexing Copper Mine[J]. Ransactions of Nonferrous Metals Society of China, 2008, 18(5): 1258-1261.
[18] RUAN R M, WEN J K, CHEN J H. Bacterial heap-leaching: Practice in Zijinshan copper mine[J]. Hydrometallurgy, 2006, 83: 77-82.
[19] RUAN R M, LIU X Y, ZOU G, CHEN J H, WEN J K, WANG D Z. Industrial practice of a distinct bioleaching system operated at low pH, high ferric concentration, elevated temperature and low redox potential for secondary copper sulfide[J]. Hydrometallurgy, 2011, 108: 130-135.
[20] NGOM B, LIANG Y L, LIU X D. Cross-comparison of leaching strains isolated from two different regions: Chambishi and Dexing Copper Mines[J]. BioMed Research International, 2014, 2014: 11.
[21] HAO X D, LIANG Y L, YIN H Q, MA L Y, XIAO Y H, LIU Y Z, QIU G Z, LIU X D. The effect of potential heap construction methods on column bioleaching of copper flotation tailings containing high levels of fines by mixed cultures[J]. Minerals Engineering, 2016, 98: 279-285.
[22] �� ��, ������, �����. ��Ʒλ������ͭ���������������ʵ��[M]. ��ɳ: ���ϴ�ѧ������, 2015: 199-207.
WANG Jun, QIN Wen-qing, QIU Guan-zhou. Theory and practice of bioleaching of low grade complex copper sulfide[M]. Changsha: Central South University Press, 2015: 110-129.
[23] ������, ��ΰ��, ���ü�, �� ��, ������, ����Ⱥ, �����, ��ѧ��. ��ͨ��������������ͬ�¶����ޱ��ǵ�Ʒλͭ��������������е����������[J]. �й���ɫ����ѧ��, 2015, 25(9): 2558-2564.
HAO Xiao-dong, ZENG Wei-min, PENG Tang-jian, HU Qi, LIANG Yi-li, YIN Hua-qun, QIU Guan-zhou, LIU Xue-duan. Analysis of microbial diversity during bioleaching of low grade copper ore from Zambia using high-throughput sequencing technology at different temperatures[J]. The Chinese Journal of Nonferrous Metals, 2015, 25(9): 2558-2564.
[24] ������, ���Ӣ, �¹���, ١����, ������, Ф����. �Ѵ�����Ʒλͭ�ܿ���������[J]. ������ұ��ѧ��, 2016, 15(2): 92-96.
LIU Yuan-yuan, YANG Hong-ying, CHEN Guo-bao, TONG Lin-lin, JIN Zhe-nan, XIAO Fa-xin. Bioleaching of refractory low grade copper-cobalt ore[J]. Journal of Materials and Metallurgy, 2016, 15(2): 92-96.
[25] BRIERLEY C L, BRIERLEY J A. Progress in bioleaching: part B: Applications of microbial processes by the minerals industries[J]. Applied Microbiology and Biotechnology, 2013, 97(17): 7543-7552.
[26] �¸���, �Ź�ƽ, �ձ���, �߽��. �������������ں�������Ĺ�ҵӦ��[J]. �ƽ�, 2011, 3(11): 46-51.
HAO Fu-lai, ZHANG Gu-ping, SU Ben-chen, GAO Jin-chang. Industrial application of biological oxidation process in cold regions[J]. Gold, 2011, 3(11): 46-51.
[27] QIU G Z, LI Q A, YU R L, SUN Z X, LIU Y J, CHEN M A, YIN H Q, ZHANG Y G, LIANG Y L, XU L L, SUN L M, LIU X D. Column bioleaching of uranium embedded in granite porphyry by a mesophilic acidophilic consortium[J]. Bioresource Technology, 2011, 102(7): 4697-4702.
[28] TIEDJE J. Foreword[J]. Transactions of Nonferrous Metals Society of China, 2008, 18(6): 1-2.
Biotech key to unlock mineral resources value
QIU Guan-zhou, LIU Xue-duan
(School of Minerals Processing and Bioengineering, Key Laboratory of Biohydrometallurgy, Ministry of Education, Central South University, China)
Abstract: Biohydrometallurgy has been applied in more than 50 countries and regions around the world. At present, the study of biometallurgy in China has entered the era of genomics. China firstly established the quantitative technology of bioleaching microorganisms based on genomics, which realized the transformation of the study on bioleaching behavior from phenotype to genotype. Meanwhile, stepwise oxidation model of sulfide ore was established at the microscopic level of chemical reaction, which realized the biohydrometallurgy from the macroscopic to the microscopic leap. Besides, the intensification technology of bioleaching process was applied industrially in the world on a large scale, and a bioleaching copper mine plant with an annual processing capacity of 60 million tons was established. CCGRI bio-oxidation gold extraction technology with independent intellectual property rights was formed, and the first high-tech industrialization demonstration project in China��s gold industry was built. The leaching rate of sulphide coated uranium ore increased to 96%, and the grade of uranium ore reduces from 1/1000 to 3/10000. The study on biohydrometallurgy in China has been in the world leading level, which can improve the utilization rate of mineral resources from 33% to 96%, greatly improving the service life of China��s mineral resources.
Key words: biotech; biohydrometallurgy; mineral resources; bioleaching behavior
Foundation item: Projects(2004CB619200, 2010CB630900) supported by the National Basic Research and Development Program of China; Projects(2007AA060900, 2012AA061500) supported by the National High-tech Research and Development Program of China; Projects(50321402, 50621063) supported by the National Natural Science Foundation of China
Received date: 2019-07-10; Accepted date: 2019-08-22
Corresponding author: QIU Guan-zhou; Tel: +86-731-88879815��E-mail: qgz@csu.edu.cn
(�༭ ������)
������Ŀ�������ص�����о��ƻ�������Ŀ(2004CB619200��2010CB630900)�����Ҹ����о���չ�ƻ�������Ŀ(2007AA060900��2012AA061500)��������Ȼ��ѧ����ί����Ⱥ��������Ŀ(50321402��50621063)
�ո����ڣ�2019-07-10�������ڣ�2019-08-22
ͨ�����ߣ�����ܣ����ڣ���ʿ���绰��0731-88879815��E-mail��qgz@csu.edu.cn