文章编号:1004-0609(2014)04-1014-06
微弧氧化对常规和超细TiNi合金表面性能的影响
朱利华,许晓静,刘 敏,牛小丫,陈婷卓
(江苏大学 先进制造与现代装备技术工程研究院,镇江 212013)
摘 要:研究微弧氧化-水热处理对常规TiNi合金和超细晶TiNi合金表面形貌、膜-基结合力和抗微动摩擦磨损性能的影响。结果表明:与常规TiNi合金微弧氧化涂层相比,超细晶TiNi合金微弧氧化涂层表面具有较高的n(Ca)/n(P)(0.85)、较低的摩擦因数(0.027)、较高的膜基结合力(10 N)、较高的抗微动摩擦磨损性(磨痕宽度0.27 mm);在经过48 h的水热处理后,超细晶TiNi合金微弧氧化涂层表面具有较高的n(Ca)/n(P)(1.79),接近标准HA的n(Ca)/n(P)(1.67);TiNi合金的组织超细化能大幅度提高TiNi合金微弧氧化-水热处理涂层表面的抗微动摩擦磨损性和表面活性。
关键词:超细晶TiNi合金;微弧氧化;水热处理;表面形貌;微动摩擦;磨损;膜-基结合力
中图分类号:TG 174.4 文献标志码:A
Effects of micro-arc oxidation on surface properties of conventional and ultrafine-grained TiNi alloy
ZHU Li-hua, XU Xiao-jing, LIU Min, NIU Xiao-ya, CHEN Ting-zhuo
(Engineering Institute of Advanced Manufacturing and Modern Equipment Technology,
Jiangsu University, Zhenjiang 212013, China)
Abstract: The surface morphology, adhesion of film and substrate, fretting friction and wear properties and bioactivity of conventional TiNi alloy and ultrafine-grained TiNi alloy treated by micro-arc oxidation and heat-treatment were investigated. The results show that, compared with the conventional TiNi alloy, the mircro-arc oxidiation coating surfaces of ultrafine-grained TiNi alloy have higher surface activity (the n(Ca)/n(P) is 0.85), lower friction coefficient (0.027) with higher fretting wear resistance, narrower wear scar width (0.27 mm), better adhesion of film-substrate adhesion (10 N) and much higher surface activity with the n(Ca)/n(P)(1.79) (which is closer to the standard n(Ca)/n(P) of HA (1.67)) after heat-treatment for 48 h. The present results illustrate that the ultrafinement processing of microstructure is an effective way to improve fretting wear resistance and bioactivity.
Key words: ultrafine-grained TiNi alloy; micro-arc oxidation; hydrothermal treatment; surface morphology; fretting friction; wear; film-substrate adhesion
TiNi合金以其形状记忆效应、超弹性、良好的生物相容性、耐磨性及耐腐蚀性而在临床和医疗器械等方面得到了广泛关注,已被广泛用于牙科和骨科矫形等领域[1]。大量的研究证明,纳米尺度形貌能有效提高生物医用材料的生物活性[2-5]。通过等通道转角挤 压制备的超细晶TiNi合金具有更高的超弹性、更低的弹性模量等性能,是一种很有应用前景的新型生物医用金属材料[6]。
但作为骨替代材料,TiNi合金表面性质和结构与骨组织差异太大,不能与骨组织形成化学骨性结合,也就是没有骨传导、骨整合作用,严重阻碍了钛合金在骨替代领域中的推广, 同时,由于TiNi合金中Ni含量较高[7-8],对热处理的敏感性[9-11]以及TiNi植入体形态的复杂性,因此,必须对医用TiNi合金进行表面改性处理。
微弧氧化是将A1、Ti、Mg等阀金属置于电解质水溶液中,用电化学方法在材料的表面产生火花放电斑点,然后在热化学、等离子体化学和电化学的共同作用下生成陶瓷层[12]。已有研究证明微弧氧化方法在TiNi 形状记忆合金表面所制备的膜层与基体具有很高的结合强度和很好的耐腐蚀性。微弧氧化制备的氧化陶瓷膜具有多孔表面,有利于与其他改性方法复合而制备各种所需的膜层[13]。HA的合成方法有水热法[14]、溶胶-凝胶法、机械化学法、共沉淀法等水热合成法是指在一个密闭压力容器内,以水溶液为反应介质,通过对反应容器加热,使得在一般情况下难溶或者不溶的物质溶解并重新结晶。
晶粒细化是提高材料综合性能的一种有效方法。因此,将微弧氧化技术和后续水热合成法引用到常规TiNi合金和超细晶TiNi合金表面改性中,研究TiNi合金组织超细化对其微弧氧化涂层表面的形貌、膜-基结合力、摩擦磨损性能以及后续水热合成对超细晶TiNi合金微弧氧化表面性能的影响,以期为生物医用金属材料的发展提供实验依据。
1 实验

图1 超细晶TiNi合金的TEM形貌
Fig. 1 TEM morphology of ultrafine-grained TiNi
试验所用TiNi合金为市购常规TiNi合金和经过大塑性变形制取的超细晶TiNi合金。超细晶Ti合金的TEM形貌如图1所示。合金经砂纸打磨、抛光后,再用丙酮和酒精进行超声波清洗。接着采用成都普斯特电气有限公司生产的MAO-I微弧氧化电源制备涂层,采用恒电压方式在含有0.04 mol/L的磷酸二氢钠和0.02 mol/L乙酸钙的电解液中采用电压为 370 V,脉冲频率为60 Hz,占空比为±45%,实验时间为5 min。最后将经微弧氧化处理后的试样放入高压反应釜中,氨水调节PH值为13~14,在190 ℃的条件下保温48 h。
采用带有X射线能谱仪(EDS)的JEOL JSM-7001F型场发射扫描电子显微镜 (SEM)观察分析合金微弧氧化表面及水热处理后的涂层表面的表面形貌。采用D/max-2500PC型X衍射仪(日本理学产)对合金微弧氧化表面及水热处理后的涂层表面进行物相分析,扫描速度为7 (°)/min、步宽0.01°、Cu靶、管流200 mA,扫描角度为10°~90°。采用MGW-01型高频往复微动摩擦磨损试验机测试微弧氧化涂层表面摩擦磨损性能,摩擦对偶件采用直径为4 mm的Si3N4球,载荷1 N,时间10 min,频率20 Hz,位移幅值0.4~0.5 mm,室温Kokubo模拟体液。Kokubo人体模拟体液的成分为7.996 g NaCl, 0.35 g NaHCO3, 0.224 g KCl, 0.278 g K2HPO4・3H2O, 0.228 g MgCl2・6H2O, 0.278 g CaCl2, 0.071 g Na2SO4, 6.057 g (CH2OH)3CNH2,其余为 H2O[用HCl调整 pH至 7.4 (36.5 ℃)] [15]。采用MFT-4000型涂层附着力自动划痕仪测量维护养护涂层与基体之间的界面结合力。试验载荷30N,加载速率10 N/min,金刚石压头的锥角120°,划痕长度3 mm。
2 结果与分析
2.1 微弧氧化
2.1.1 表面形貌与化学成分
图2所示为恒定电压、脉冲频率、n(Ca)/n(P)、反应时间和占空比分别为370V、60Hz、5:1、5min、45%时,常规TiNi合金和超细晶TiNi合金微弧氧化膜层的SEM形貌和EDS谱。从图2(a)和(b)可以看出,与常规TiNi合金微弧氧化涂层表面相比,超细晶TiNi合金微弧氧化涂层表面表现出较明显的微弧氧化多孔特征,孔洞较为致密。从热力学角度考虑,微弧氧化反应加速的驱动力是由于含有大量晶界、亚晶界等晶体缺陷储存有大量额外能量。而由于组织的超细化一方面使得晶界等晶体缺陷增多、自由能和扩散能增强,为微弧氧化提供了更多的能量和扩散通道,导致放电通道增多;另一方面组织的超细化有利于增加材料表面的化学反应速度和元素的扩散能力,从而在表面形成了更多的孔洞。而从EDS分析谱中可以看出,超细晶TiNi合金微弧氧化涂层表面Ca、P含量略多于常规TiNi合金微弧氧化涂层表面Ca、P含量,其对应的n(Ca)/n(P)分别为0.85和0.5。
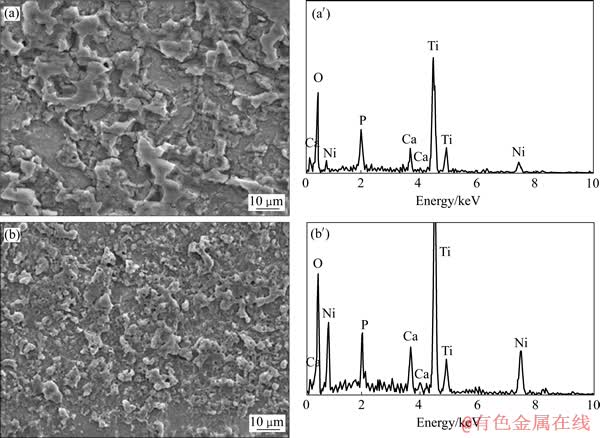
图2 微弧氧化表面SEM像和成分EDS谱
Fig. 2 SEM images and EDS spectra of MAO coatings of conventional((a), (a′)) and ultrafine-grained((b), (b′)) TiNi
图3所示为氧化膜的XRD谱。由图3可以看出,常规TiNi合金和超细晶TiNi合金表面均出现TiO2衍射峰,未出现晶态羟基磷灰石(HA)。
2.1.2 膜-基结合力
图4所示为输出电压、反应时间、n(Ca)/n(P)、脉冲频率和占空比分别为370 V、5 min、5:1、60 Hz和45%时常规TiNi合金和超细晶TiNi合金表面氧化膜的划痕测试谱。测定膜基结合力的关键是临界载荷的确定。本实验中采用摩擦力曲线法来判断临界载荷。由图4可以看出,与常规TiNi合金相比,超细晶TiNi合金与其微弧氧化涂层之间具有较高的膜基结合力,前者约为9 N,后者约为10 N。这可能是TiNi合金组织的超细化使得晶体缺陷显著增多、自由能和扩散能力显著增加,从而给表面涂层改性层的形核、生长提供了额外的能量和扩散通道,具有提高表面涂层改性层性能与界面结合的作用。
2.1.3 摩擦磨损性能
图5所示为在微弧氧化参数分别为370 V、5 min、60 Hz、n(Ca)/n(P)=5时,常规TiNi合金和超细晶TiNi合金微弧氧化表面的摩擦因数随磨损时间变化关系。
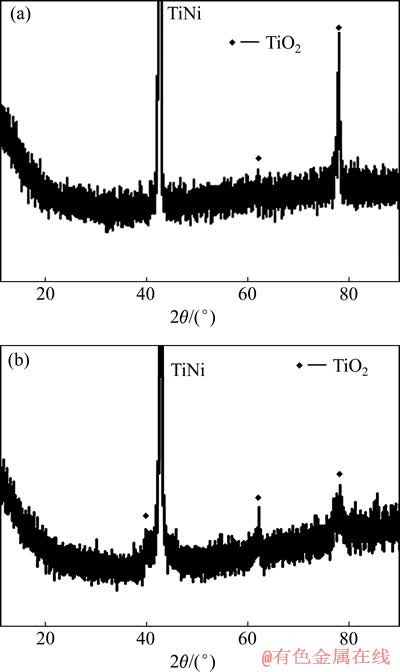
图3 TiNi合金和超细晶TiNi合金微弧氧化涂层XRD谱
Fig. 3 XRD patterns of MAO coatings on conventional(a) and ultrafine-grained(b) TiNi
由图5可知,在载荷1N、时间为10 min、频率为20 Hz、对磨球件为Si3N4、室温SBF润滑条件下常规TiNi合金和超细晶TiNi合金微弧氧化表面均表现出来很好的抗微动摩擦磨损性能,其对应到平均摩擦因数分别为0.0297和0.027。但与常规TiNi合金表面微弧氧化膜相比,超细晶TiNi合金表面氧化膜具有更低的摩擦因数。这可能是因为超细晶TiNi合金表面存在更多的孔洞,贮存模拟体液也较多,因此降低了粘着磨损倾向。
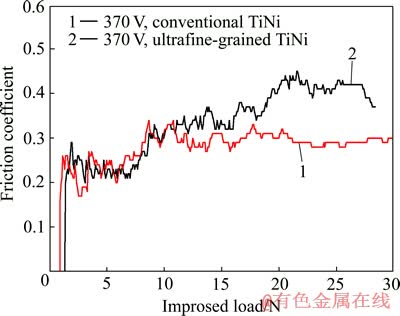
图4 微弧氧化涂层的划痕测试谱
Fig. 4 Scratch testing spectra of MAO coatings of conventional and ultrafine-grained TiNi
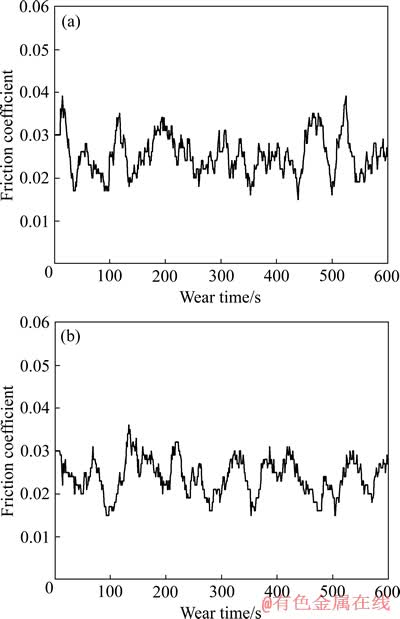
图5 常规TiNi合金和超细晶TiNi合金微弧氧化表面的摩擦因数随磨损时间变化曲线
Fig. 5 Variation curves of friction coefficient with wear time of MAO coatings of conventional (a) and ultrafine-grained (b) TiNi
图6所示为恒定电压、脉冲频率、n(Ca)/n(P)、反应时间和占空比分别为370 V、60 Hz、5:1、5 min、45%时常规TiNi合金和超细晶TiNi合金微弧氧化涂层表面磨痕的SEM像。从图6中可以看出,超细晶TiNi合金比常规TiNi合金具有较好的耐磨损性能(即磨痕宽度为0.27 mm)。
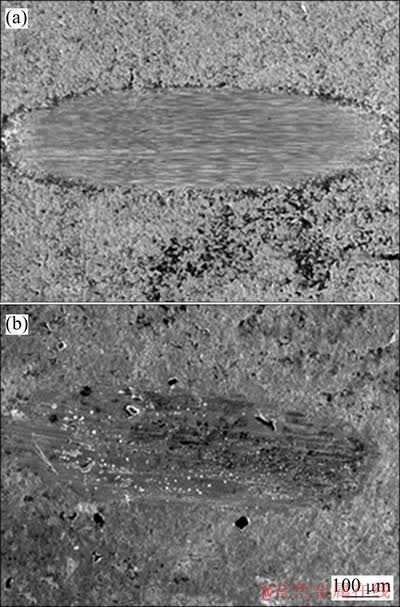
图6 微弧氧化涂层表面磨痕的SEM像
Fig. 6 SEM images of worn tracks of MAO surfaces of conventional(a) and ultrafine-grained(b) TiNi
2.2 水热处理对微弧氧化涂层表面性能的影响
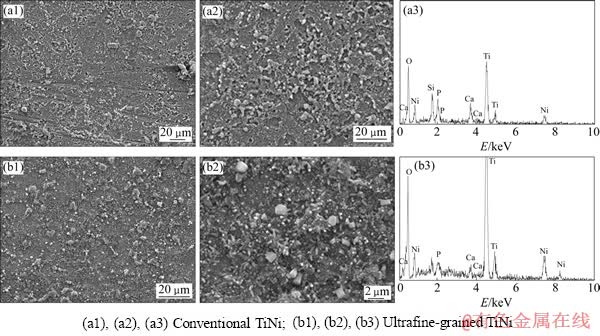
图7 水热处理48h后微弧氧化表面SEM像和EDS成分
Fig. 7 SEM images and EDS spectra of MAO coatings after hydrothermal treatment for 48 h
表1 微弧氧化后涂层中与水热处理后微弧氧化涂层中n(Ca)/n(P)
Table 1 n(Ca)/n(P) of anodic oxidized surface

图7所示为常规TiNi合金和超细晶TiNi合金微弧氧化表面在高温高压反应釜中浸泡48 h的SEM像和EDS谱。由图7可以看出,常规TiNi合金和超细晶TiNi合金涂层表面均有不同形态的晶态羟基磷灰石(HA)析出,但是超细晶TiNi合金表面所沉积的羟基磷灰石(HA)更多。表1列出了微弧氧化表面和经水热处理后的微弧氧化表面的n(Ca)/n(P)的变化情况。从表1中得知,经水热处理后的涂层n(Ca)/n(P) 明显提高,其中超细晶TiNi合金的n(Ca)/n(P)比TiNi合金的要大得多,且超细晶TiNi合金的n(Ca)/n(P)=1.79,接近标准HA的n(Ca)/n(P)(1.67)。因此,超细晶TiNi合金微弧氧化涂层更利于Ca、P的沉积,这可能是由于组织的超细化使得晶界等晶体缺陷增多、自由能和扩散能增强,为微弧氧化提供了更多的能量和扩散通道,使得反应更充分,溶解在涂层表面的Ca、P也越多,当放入高温高压反应釜后,涂层中游离出更多的Ca、P,重新溶解形成更多的HA。
图8所示为经水热处理48 h后的微弧氧化表面涂层的XRD谱。从图8中可以看出,常规TiNi合金和超细晶TiNi合金微弧氧化涂层表面除来自氧化表面的衍射峰外,均出现了磷灰石衍射峰,说明钙-磷层的相有晶态磷灰石相。但是超细晶TiNi合金比常规TiNi合金微弧氧化涂层表面的磷灰石衍射峰多,这说明超细晶TiNi合金钙-磷层出现晶态磷灰石的概率高、含量多,这与其水热处理后涂层表面具有较高n(Ca)/n(P)是一致的。
以上实验结果说明,TiNi合金组织超细化显著提高了微弧氧化涂层的表面活性(即n(Ca)/n(P))、孔洞的密度和耐摩擦磨损性能,其机理讨论如下。
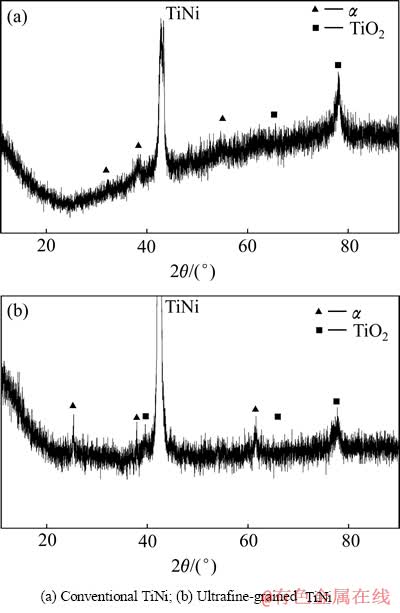
图8 水热处理48 h后的微弧氧化表面涂层的XRD谱
Fig. 8 XRD patterns of MAO coatings after hydrothermal treatment for 48 h
TiNi合金组织超细化显著提高了微弧氧化涂层的表面活性(即n(Ca)/n(P))和孔洞的密度,这可能是由于组织的超细化使得晶界等晶体缺陷增多、自由能和扩散能增强,为微弧氧化提供了更多的能量和扩散通道,从而在表面形成了更多的孔洞。而自由能的增多也提供了更多的能量,使得反应加剧,更多的Ca、P参与到反应中来,从而使得游离在膜层中的Ca、P含量增多,n(Ca)/n(P)增大。
TiNi合金组织超细化显著提高了微弧氧化涂层的耐摩擦磨损性能,这可能一方面是因为材料组织超细化后其硬度提高,另一方面是因为超细晶TiNi合金微弧氧化表面表现出显著的微弧氧化多孔特征,即存在更多的孔洞,因此贮存模拟体液也较多,降低了粘着磨损倾向[16]。
3 结论
1) 当恒定电压、脉冲频率、n(Ca)/n(P)、反应时间和占空比分别为370 V、60 Hz、5、5 min、45%时,与常规TiNi合金微弧氧化涂层相比,超细晶TiNi合金微弧氧化涂层表面具有更高的n(Ca)/n(P) (0.85)、较高的膜基结合力(10 N)、更低的摩擦因数(0.027)、较高的抗微动摩擦磨损性(磨痕宽度0.27 mm)。同时,超细晶TiNi合金微弧氧化涂层表面具有明显的微弧氧化多孔特征。
2) 常规TiNi合金和超细晶TiNi合金微弧氧化涂层表面在经过49 h的水热处理后,涂层表面均析出了羟基磷灰石(HA),但是超细晶TiNi合金的n(Ca)/n(P)比TiNi合金的要大得多(1.79),超细晶TiNi合金的n(Ca)/n(P)接近标准HA的n(Ca)/n(P)。
REFERENCES
[1] MACHADO L G, SAVI M A. Medical applications of shape memory alloys[J]. Brazilian Journal of Medical and Biological Research, 2003, 36(6): 683-691.
[2] VENKATSURYA P, THEIN-HAN W W, MISRA R. D K, SOMANI M C, KARJALAINEN L P. Advancing nanograined/ ultrafine-grained structures for metal implant technology: Interplay between grooving of nano/ultrafine grains and cellular response[J]. Materials Science and Engineering C, 2010, 30(7): 1050-1059.
[3] PARK J W, KIM Y J, PARK C H, LEE D H, KO Y G, JANG J H, LEE C S. Enhanced osteoblast response to an equal channel angular pressing-processed pure titanium substrate with microrough surface topography[J]. Acta Biomaterialia, 2009, 5(8): 3272-3280.
[4] TRUONG V K, LAPOVOK R, RUNDELL S, WANG J Y, FLUKE C J, CREWFORD R J, IVANOVA E P. The influence of nano-scale surface roughness on bacterial adhesion to ultrafine-grained titanium[J]. Biomaterials, 2010, 31(13): 3674-3683.
[5]  F J L, COOPER L F. Advancing dental implant surface technology- from micron- to nanotopography[J]. Biomaterials, 2008, 29(28): 3822-3835.
F J L, COOPER L F. Advancing dental implant surface technology- from micron- to nanotopography[J]. Biomaterials, 2008, 29(28): 3822-3835.
[6] VALIEV R, GUNDEROV D, PROKOFIEV E, PUSHIN V, ZHU Yun-tian. Nanostructuring of TiNi alloy by SPD processing for advanced properties[J]. Materials Transactions, 2008, 49(1): 97-101
[7] MCKAY G C, MACNAIR R, MACDONALD C, GRANT M H. Interactions of orthopaedic metals with an immortalized rat osteoblast cell line[J]. Biomaterials, 1996, 17(17): 1339-1344.
[8] CHENG F T, SHI P, MAN H C. A preliminary study of TiO2 deposition on NiTi by a hydrothermal method[J]. Surf Coat Tech, 2004, 187(1): 26-32.
[9] RONDELLI G. Corrosion resistance tests on NiTi shape memory alloy[J]. Biomaterials, 1996, 17(20): 2003-2008.
[10] SHABALOVSKAYA S A. Surface, corrosion and biocompability aspects of Nitinol as an implant material[J]. Bio-medicinal Material Engineering, 2002, 12(1): 69-109.
[11] BOGDANSKI D M, KOLLER M, MULLER D, MUHR G, BRAM M, BUCHKREMER H P, STOVER D, CHOI J, EPPLE M. Easy assessment of the biocompatibility of Ni-Ti alloys by in vitro cell culture experiments on a functionally graded Ni-NiTi-Ti material[J]. Biomaterials, 2002, 23(23): 4549-4555.
[12] 钟涛生, 蒋百灵, 李均明. 微弧氧化技术的特点、应用前景及其研究方向[J]. 电镀与涂饰, 2005(6): 47-50.
ZHONG Tao-sheng, JIANG Bai-ling, LI Jun-ming. Characteristics, applications and research direction of micro-arc oxidation technology[J]. Electroplating & Finishing, 2005(6): 47-50
[13] 刘 福, 徐吉林, 王福平, 赵连城, 孙德智. 医用NiTi 合金的表面改性研究进展[J]. 稀有金属材料与工程, 2008, 37(4): 748-752.
LIU Fu, XU Ji-lin, WANG Fu-ping, ZHAO Lian-cheng, SUN De-zhi. Progress on surface modification of biomedical NiTi alloy[J]. Rare Metal Materials and Engineering, 2008, 37(4): 748-752.
[14] 廖其龙, 徐光亮, 尹光福, 周大利, 郑昌琼, 李晓东. 纳米羟基磷灰石的水热合成[J]. 功能材料, 2002, 33(3): 338-340.
LIAO Qi-long, XU Guang-liang, YIN Guang-fu, ZHOU Da-li, ZHEN Chang-qiong, LI Xiao-dong. Hydrothermal synthesis of nano-hydroxyapatite crystals[J]. Journal of Functional Materials, 2002, 33(3): 338-340.
[15] KOKUBO T, KUSHITANI H, SAKKA S, KITSUGI T, YAMAMURO T. Solutions able to reproduce in vivo surface- structure changes in bioactive glass-ceramic A-W[J]. Journal of Biomedical Materials Research, 1990, 24(6): 721-734.
[16] 许晓静,张体峰,凌智勇,盛新兰,刘 敏,牛小丫,朱利华.超细晶TiNi合金电化学抛光表面生物相容性研究[J].中国有色金属学报, 2013, 23(7): 1931-1936.
XU Xiao-jing, ZHANG Ti-feng, LING Zhi-yong, SHENG Xin-lan, LIU Min, NIU Xiao-ya, ZHU Li-hua. Biocompatibility of electrochemical polished ultrafine-grained TiNi alloy[J]. The Chinese Journal of Nonferrous Metals, 2013, 23(7): 1931-1936.
(编辑 李艳红)
基金项目:江苏省高校自然科学基金重大项目(11KJA430004);江苏大学优秀学术青年骨干培养对象基金资助项目(1211110001)
收稿日期:2013-07-18;修订日期:2013-10-28
通信作者:许晓静,教授,博士;电话:0511-88792058;传真:0511-88792058;E-mail: xjxu67@ujs.edu.cn