用P507萃取分离钴及草酸反萃制备草酸钴
张阳,满瑞林,王辉,梁永煌
(中南大学 化学化工学院,湖南 长沙,410083)
摘要:研究锂电池浸出液中钴、镍、锂的P507萃取分离方法,通过直接采用草酸反萃富钴有机相得到草酸钴产品。实验对含有53.8 g/L钴的料液进行萃取。研究结果表明最佳萃取条件如下:有机相组成(体积分数)为25% P507+5% TBP+70%磺化煤油,萃取剂皂化率为70%,水相初始pH为3.5,常温下萃取10 min,有机相与水相的相比φ(O)/φ(A)为1.5:1.0,通过3级错流萃取,钴的萃取率达99.5%,锂和镍的萃取率仅为4.9%和3.1%;P507萃取分离钴、镍、锂过程的焓变分别为:-2.043,-0.812和1.586 kJ/mol;直接使用草酸反萃富钴有机相,得到分相良好的油―水―固3相,最优反萃工艺为:0.03 g草酸/mL富钴萃取剂,温度为40 ℃,φ(O)/φ(A)=1.0:2.5,钴的反萃率达99.5%,反萃后的萃取剂和水相均可再生循环利用。
关键词:P507萃取;草酸反萃;草酸钴
中图分类号:TG146.1 文献标志码:A 文章编号:1672-7207(2011)02-0317-06
Extraction of cobalt with P507 and preparation of cobalt oxalate powders by ethane diacid stripping
ZHANG Yang, MAN Rui-lin, WANG Hui, LIANG Yong-huang
(School of Chemistry and Chemical Engineering, Central South University, Changsha 410083, China)
Abstract: The extraction and separation of Co, Ni and Li from Li-ion batteries powders leaching solution was carried out using P507, and cobalt oxalate was directly prepared by stripping with oxalic acid. The initial concentration of cobalt in feed solution was 53.8 g/L. The results show that the optimal extraction condition is as follows: organic phase composition of 25% P507+5% TBP+70% sulfonated kerosene; saponification rate is 70%, ambient temperature equilibration time is 10 min, phase ratio φ(O)/ φ(A) is 1.5:1.0 and aqueous phase pH is 3.5. In this condition, 99.5% of Co in the solution is extracted by three-stages extraction, while the extraction efficiency of Li and Ni is only 4.9% and 3.1%, respectively. The enthalpy of P507 extraction Co, Ni and Li is determined as -2.043, -0.812 and 1.586 kJ/mol, respectively. Oil, water and solid with good three-phase are separated by oxalic acid stripping. The optimum back extraction process is as follows: at 40 ℃, 0.03 g oxalic acid/mL co-rich extractant, andφ(O)/φ(A) is 1.0:2.5. The stripping efficiency of Co reaches 99.5%. The extractant and aqueous can be recycled after stripping.
Key words: P507 extraction; ethane diacid stripping; cobalt oxalate
锂电池是当今使用量最大的二次电池,全球各类锂电池年产量达15~20亿只,大量锂电池使用一定年限后被废弃,但其中仍含有相当含量的钴等有价金属,将其综合回收具有重要的环保意义和经济价值。如何将钴与电池芯粉中的锰、锌等其它金属元素分离是当前的研究热点之一。采用水解沉淀法可将钴与铁、铝、铜分离[1-2],采用氧化沉淀法或P204萃取法可将钴与锰分离[3-4],分离钴、镍、锂一般采用萃取法。Cyanex 272 是分离钴、镍、锂最常用的萃取剂,使用该萃取剂可从废旧锂电池浸出液中分离出几乎不含镍和锂的钴液[5-7]。通常使用Cyanex 272分离钴时需要将Cyanex 272皂化[8],以提高萃取效果。Kumbasar[9]使用PC-88A成功地将钴与镍分离。Reddy[10] 等使用TOPS99和TIBPS联合萃取分离钴与镍,以增强分离效果;Darvishi[11]等分别使用Cyanex 272和D2EHPA的混合体以及Cyanex 302和D2EHPA的混合体对钴、镍进行分离。几种萃取剂对钴、镍的选择性系数β依次为:β(Cyanex 272)>β(PC-88A)>β(D2EHPA)。上述研究很少涉及钴的反萃过程。反萃钴的传统方法是通过强酸对负载钴的有机相进行洗脱、电积或调洗脱液pH后加入草酸铵沉淀得钴产品,但采用这些方法不仅成本较高,且污染环境。本文作者采用P507萃取法分离电池芯粉浸出液中的钴、镍、锂,并提出采用草酸替代草酸铵直接反萃富钴有机相回收草酸钴的方法。反萃后油-水-固3相分相清晰,所得的有机相可再生作为萃取剂循环使用,水相作为溶剂补充草酸后可循环使用,固相所得草酸钴中的钴含量达30.8%。
1 实验
1.1 试剂药品及萃取液制备方法
(1) 试剂药品:氢氧化钠(分析纯,汕头市西陇化工有限公司生产);磺化煤油(工业级,上海有机所萃取化工剂厂生产);P507萃取剂(2-乙基己基磷酸-2-乙基己基酯,工业级,上海有机所萃取化工剂厂生产);TBP(磷酸三丁酯,工业级,上海有机所萃取化工剂厂生产);草酸(分析纯,湖南师范大学化学试剂厂生产);蒸馏水。
(2) 萃取料液制备方法为:将预处理后的废旧锂电池芯粉用硫酸和双氧水浸出,并分离铁、铝、铜、锰4种金属元素,即成为料液,料液pH为5.8,其成分见表1。
1.2 仪器
ICP-AES,为PS-6型电感耦合等离子体发射光谱仪(美国贝尔德公司生产);AA320型原子吸收分光光度计(上海精密科学仪器有限公司分析仪器总厂生产);pH计,为PHS-3C型数显pH/mv仪(上海分析仪器厂生产)。
表1 料液金属元素的质量浓度
Table 1 Mass concentration of solutionmetal elements g/L

2 结果与讨论
2.1 萃取
2.1.1 有机相的组成
选用磺化煤油稀释后的P507为萃取剂,它类似于国外PC-88A,用于钴、镍分离。当萃取剂中φ(P507)≥30%时,萃取体系乳化现象严重,分相时间长,有机相中夹水相较多,实验选择φ(P507)为25%。为了防止萃取过程形成第3相,添加TBP(磷酸三丁酯)为改质剂,表2所示为实验料液萃取时TBP的质量浓度对分相的影响。
表2 TBP质量浓度与萃取分相
Table 2 Effect of mass concentration of TBP on phase separation g/L

加入TBP可显著提高萃取体系的分相能力,最终有机相组成(体积分数,下同)为25% P507+5% TBP+ 70%磺化煤油。P507为磷酸酯类萃取剂,适当地皂化可增强P507的萃取能力。皂化率对萃取率和分离因素的影响分别见图1和图2。由图1和图2可知:在温度为25 ℃、初始pH为3.5时,随着皂化率的升高,萃取剂对钴、镍、锂的萃取能力均升高;当皂化率达70%~80%时,钴/镍、钴/锂的分离因数最大,但皂化率增高的同时,萃取剂的黏度随即急剧增大,不利于工艺操作,故萃取剂皂化率选择为70%。
2.1.2 水相初始pH对萃取的影响
表1中的料液初始pH为5.8,为了达到最优分离效果,需将pH调至最适合萃取的范围,实验使用的有机相组成为25% P507+5% TBP+70%磺化煤油,皂化率为70%,水相pH对萃取率和分离因素的影响分别见图3和图4。图3和图4表明:随着水相初始pH升高,钴、镍、锂的萃取率亦升高,在pH为3.5时,钴/镍分离因数最大;当pH高于3.5时,镍将大量被萃至有机相,选择性系数因数较低,所以,萃取前应将料液pH调节至3.5,以达到最优的分离效果。
2.1.3 温度对萃取的影响
通过考察萃取温度确定萃取过程的焓变。图5和图6所示为温度对萃取效果的影响,根据克劳修斯-克拉贝龙方程[15]作图,求得萃取过程的焓变,见图7。
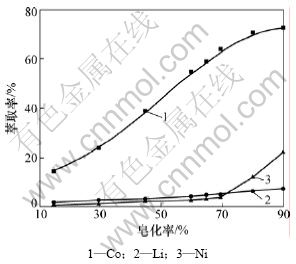
图1 皂化率对萃取率的影响
Fig.1 Effects of extraction efficiency on different saponifications
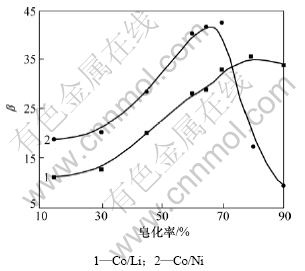
图2 皂化率对分离因数β的影响
Fig.2 Effects of separation factor on different saponifications
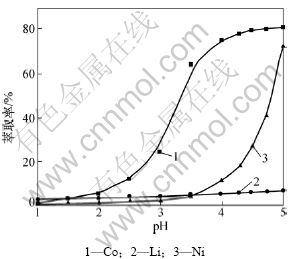
图3 水相pH对萃取率的影响
Fig.3 Effects of extraction efficiency on different aqueous pH
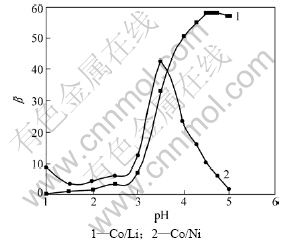
图4 水相pH对分离因数β的影响
Fig.4 Effects of separation factor on different aqueous pH
由图5和图6可以看出:温度升高有利于钴的萃取;但镍和锂的萃取率几乎不受温度变化的影响,有利于萃取选择性的提高。P507的萃取原理为:
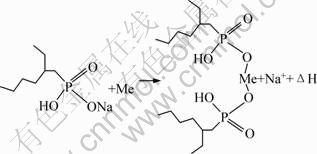
该化学式中:Me代表金属离子,本文中为Co2+,Li+和Ni2+。可见P507萃取是一种典型的螯合萃取,每2 mol皂化后的萃取剂可螯合1 mol的金属离子。
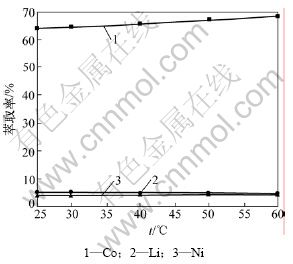
图5 温度对萃取率的影响
Fig.5 Effects of extraction efficiency on different temperatures
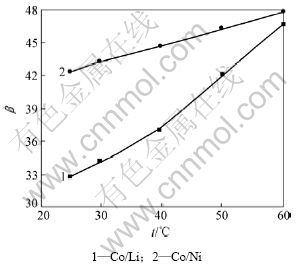
图6 温度对分离因数β的影响
Fig.6 Effects of separation factor on different temperatures
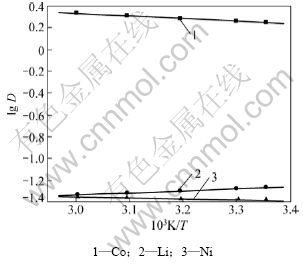
图7 萃取热力学回归线
Fig.7 Thermodynamic regression line of extraction
通过热力学回归线计算出P507萃取钴和镍为吸热反应,ΔHCo=-2.043 kJ/mol,ΔHNi=-0.812 kJ/mol;萃取锂为放热反应,ΔHLi=1.586 kJ/mol。温度升高有利于钴的萃取,但磺化煤油的闪点仅为65 ℃[15],高温易使萃取剂损失,故实验萃取温度选择常温。
2.1.4 时间对萃取的影响
萃取时间对萃取率和分离因素的影响分别见图8和图9。从图8和图9可见:萃取率随萃取时间的延长而增大,萃取时间大于10 min后,钴的萃取率几乎不变,而镍、锂的萃取率缓慢增加;当萃取时间为10 min时,钴/镍、钴/锂的分离因数达到极值,故选择萃取时间为10 min。
2.1.5 料液的多级错流萃取
选择有机相组成为25% P507+5% TBP+70%磺化煤油,萃取剂皂化率为70%,调节水相料液初始pH为3.5,常温下萃取10 min,相比φ(O)/φ(A)为1.5:1, 三级错流萃取,结果见表3。
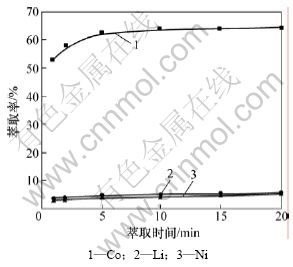
图8 萃取时间对萃取率的影响
Fig.8 Effects of extraction efficiency on different reaction time
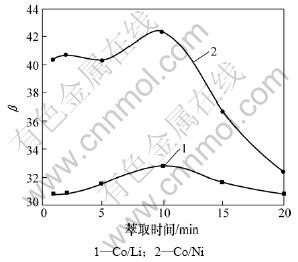
图9 萃取时间对分离因数β的影响
Fig.9 Effects of separation factor on different reaction time
通过测定P507萃取钴的饱和容量,计算出钴的饱和质量浓度为18.64 g/L, 有机相中P507与Co2+物质的量比为2:1。
表3 萃余液中钴、锂、镍质量浓度
Table 3 Mass concentration of raffinate metals contents g/L
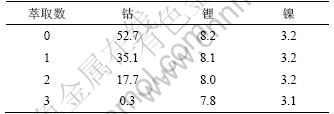
由实验结果发现:在最优条件下钴、镍、锂分离效果明显;料液中99.4%的钴进入有机相,锂、镍的萃取率仅为4.9%和3.1%,3次萃取水相钴质量浓度递减量分别为17.6,17.4和17.4 g/L,说明萃取过程有机相几乎成饱和状态。将3次萃取后的萃余液补充酸后可作为电池芯粉酸性浸出溶剂循环使用。
2.2 反萃
2.2.1 草酸量对反萃的影响
根据络合在有机相中的Co2+与H+的反应计量比,确定反萃1 mL富钴有机相需要26 mg固体草酸,表4所示为不同草酸用量的反萃液(40 ℃,φ(O)/φ(A)=1:2)对20 mL富钴有机相反萃的结果。从表4可见:当草酸用量少时,钴沉淀率低,分相不明显;当用量过多时,则沉淀的草酸钴易反溶,故选择反萃20 mL富钴有机相草酸用量为0.6~0.7 g。
表4 草酸用量与反萃效果
Table 4 Stripping efficiency and different oxalic acid amounts

2.2.2 温度对反萃的影响
温度对反萃的影响主要表现在分相时间和沉淀的稳定性方面。表5所示为不同反萃温度时的实验现象(0.03 g草酸/mL富钴萃取剂,φ(O)/φ(A)=1:2.5)。
由表5可知:反萃温度升高有利于沉淀颗粒长大和反应速率加快;但温度过高会加速沉淀溶解和溶剂挥发,故选取适宜的反萃温度为40 ℃。
2.2.3 相比对反萃的影响
相比对反萃的影响主要体现在分相上,表6所示为不同相比的反萃现象(0.03 g草酸/mL富钴萃取剂、40 ℃),从表4可见:当φ(O)/φ(A)>1:1.5时,分相慢,乳化明显,水相不清晰。当φ(O)/φ(A)达到1:2时,开始出现油相、水相和沉淀;当φ(O)/φ(A)<1:2.5时,3相分界非常明显。实验最终选择φ(O)/φ(A)=1:2.5。
根据以上分析,确定最优的反萃工艺条件为:0.03 g草酸/mL富钴萃取剂,温度为40 ℃,φ(O)/φ(A) =1:2.5。经对萃取制得的富钴有机相作反萃取实验,获得钴的反萃效率为99.5%;沉淀的草酸钴中,钴含量为30.8%。反萃后有机相可再生利用,反萃水相可作为配反萃剂的溶剂循环使用,减少外排污水。
表5 温度与反萃效果
Table 5 Stripping efficiency and different temperatures

表6 相比与反萃效果
Table 6 Stripping efficiency and different phase ratios

3 结论
(1) 从锂电池酸浸出处理液中萃取钴、镍、锂的最佳工艺条件为:有机相组成25% P507+5% TBP+70%磺化煤油,萃取剂皂化率70%,水相初始pH为3.5,相比φ(O)/φ(A)为1.5:1.0,常温下萃取时间10 min,对该条件下经3级错流的电池芯粉浸出液进行萃取,钴的萃取率达99.4%,锂和镍的萃取率仅为4.9%和3.1%。
(2) 采用P507萃取分离钴、镍、锂的热力学参数为:ΔHCo=-2.043 kJ/mol,ΔHNi=-0.812 kJ/mol,ΔHLi= 1.586 kJ/mol。
(3) 通过直接使用草酸反萃富钴有机相的方法,得到分相良好的油―水―固3相,最优反萃工艺为:0.03 g草酸/mL富钴萃取剂,温度为40 ℃,φ(O)/φ(A)为1.0:2.5,钴的反萃率为99.5%,反萃后的萃取剂和水相均可再生循环利用。
参考文献:
[1] Dorella G, Mansur M B. A study of the separation of cobalt from spent Li-ion battery residues[J]. Journal of Power Sources, 2007, 170(1): 210-215.
[2] Sayar N A, Filiz M, Sayar A A. Extraction of Co(II) and Ni(II) from concentrated HCl solutions using Alamine 336[J]. Hydrometallurgy, 2009, 96(1/2):148-153.
[3] 王艳, 周春山. 含钴废渣硫酸化焙砂浸出液中钴、铁、锰分离研究[J]. 化学世界, 2001(6): 289-290.
WANG Yan, ZHOU Chun shan. Study on the separation of cobalt, iron and manganese from the leach solution of sulphated calcined cobalt residue[J]. Huaxue Shijie (Chemical World), 2001(6): 289-290.
[4] 吴芳. 从废旧锂离子二次电池中回收钴和锂[J]. 中国有色金属学报, 2004, 14(4): 697-701.
WU Fang. Recovery of cobalt and lithium from spent lithium-ion secondary batteries[J]. The Chinese Journal of Nonferrous Metals, 2004, 14(4): 697-701.
[5] Swain B, Jeong J, Lee J C, et al. Development of process flow sheet for recovery of high pure cobalt from sulfate leach liquor of LIB industry waste: A mathematical model correlation to predict optimum operational conditions[J]. Separation and Purification Technology, 2008, 63: 360-369.
[6] Swain B, Jeong J, Lee J, et al. Hydrometallurgical process for recovery of cobalt from waste cathodic active material generated during manufacturing of lithium ion batteries[J]. Journal of Power Sources, 2007, 167(2): 536-544.
[7] Mantuano D P, Dorella G, Elias R C A. Analysis of a hydrometallurgical route to recover base metals from spent rechargeable batteries by liquid-liquid extraction with Cyanex 272[J]. Journal of Power Sources, 2006, 159(2): 1510-1518.
[8] Swain B, Jeong J, Lee J C, et al. Separation of cobalt and lithium from mixed sulphate solution using Na-Cyanex 272[J]. Hydrometallurgy, 2006, 84(3/4): 130-138.
[9] Kumbasar R A. Selective extraction and concentration of cobalt from acidic leach solution containing cobalt and nickel through emulsion liquid membrane using PC-88A as extractant[J]. Separation and Purification Technology, 2009, 64(1): 273-279.
[10] Ramachandra R B, Venkateswara R S, Kyung H P. Solvent extraction separation and recovery of cobalt and nickel from sulphate medium using mixtures of TOPS 99 and TIBPS extractants[J]. Minerals Engineering, 2009, 22(5): 500-505.
[11] Darvishi D, Haghshenas D F, Keshavarz Alamdari E, Sadrnezhaad T S K, Halali M. Synergistic effect of Cyanex 272 and Cyanex 302 on separation of cobalt and nickel by D2EHPA[J]. Hydrometallurgy, 2005, 77(3/4): 227-238.
[12] 谢福标. 钴废料中有价元素综合回收的生产实践[J]. 矿冶, 2001, 10(3): 61-64.
XIE Fu-biao. Practice on comprehensive recovery of valuable metals from cobalt-bearing wastes[J]. Mining and Metallurgy, 2001, 10(3): 61-64.
[13] 张学锋, 王海北, 蒋开喜, 等. 钴废料生产草酸钴实践[J]. 矿冶, 2007, 16(1): 43-45.
ZHANG Xue-feng, WANG Hai-bei, JIANG Kai-xi, et al. Practice for production of cobalt oxalate from cobalt waste materials[J]. Mining and Metallurgy, 2007, 16(1): 43-45.
[14] 梁妹. 从废弃炉渣中分离回收钴、镍[J]. 湿法冶金, 2007, 26(3): 157-162.
LIANG Mei. Separation and recovery of cobalt and Nickel from waste slag [J]. Hydrometallurgy of China, 2007, 26(3): 157-162.
[15] 杨佼庸, 刘大星. 萃取[M]. 北京: 冶金工业出版社, 1988: 50-150.
YANG Jiao-yong, LIU Da-xing. extraction[M]. Beijing: Metallurgical Industry Press, 1988: 50-150.
(编辑 张曾荣)
收稿日期:2009-12-07;修回日期:2010-03-15
基金项目:湖南省科技计划项目(2008GK3111);中南大学米塔尔学生创新创业项目(08MX06)
通信作者:满瑞林(1955-),男,湖南长沙人,教授,从事环境化工、二次资源加工研究;电话:0731-88836237;E-mail:rlman@mail.csu.edu.cn