文章编号:1004-0609(2014)11-2906-08
高铁闪锌矿赤铁矿法除铁中锌离子和镁离子的影响及存在机理
杨 凡1, 2,邓志敢1, 2,魏 昶1, 2,李兴彬1, 2,李存兄1, 2,邱伟佳1, 2,朱如龙1, 2
(1. 昆明理工大学 冶金与能源工程学院,昆明 650093;
2. 昆明理工大学 复杂有色金属资源清洁利用国家重点实验室,昆明 650093)
摘 要:研究赤铁矿法处理高铁闪锌矿浸出液过程中ZnSO4和MgSO4浓度对除铁率及赤铁矿渣性质的影响,讨论元素Zn、Mg和S在赤铁矿渣中的存在形态及形成机理。结果表明,除铁率随ZnSO4浓度的升高而增加,随MgSO4浓度的升高而降低。增加硫酸盐的浓度可以得到结晶形态更好的晶体。赤铁矿的粒度和S含量随硫酸盐浓度的升高而降低,比表面积随硫酸盐浓度的升高而增加。Zn浓度和Mg浓度的合理存在范围分别为80~100 g/L和小于10 g/L;Zn以ZnSO4的形式存在于赤铁矿表面,少量的Mg以夹带的方式存在于赤铁矿渣中。
关键词:赤铁矿;除铁;高铁闪锌矿;硫酸锌;硫酸镁
中图分类号:TF813 文献标志码:A
Effect and existence mechanism of zinc ion and magnesium ion in iron removal from high iron sphalerite by hematite process
YANG Fan1, 2, DENG Zhi-gan1, 2, WEI Chang1, 2, LI Xing-bin1, 2, LI Cun-xiong1, 2, QIU Wei-jia1, 2, ZHU Ru-long1, 2
(1. Faculty of Metallurgical and Energy Engineering, Kunming University of Science and Technology, Kunming 650093, China;
2. State Key Laboratory of Complex Nonferrous Metal Resources Clear Utilization in Yunnan Province,
Kunming University of Science and Technology, Kunming 650093, China)
Abstract: The effects of ZnSO4 and MgSO4 concentrations on the iron removal rate and the properties of residues for treating the leaching liquor of high iron sphalerite by hematite process were investigated, the existent form and formation mechanism of Zn, Mg and S in hematite were discussed. The results show that the iron removal rate increases with increasing the ZnSO4 concentration and decreases with increasing the MgSO4 concentration. Better crystal morphology of precipitates can be obtained by increasing the sulfate concentration. Higher sulfate concentration produced precipitates with finer particle sizes, lower S contents and bigger specific surface area. A reasonable existence range of Zn and Mg are 80~100 g/L and <10 g/L, respectively. Zn exists in hematite surface as ZnSO4, low levels of Mg in the precipitates present as tiny liquid inclusions in the hematite particles.
Key words: hematite; iron precipitation; high iron sphalerite; zinc sulfate; magnesium sulfate
随着锌矿资源的不断开发利用,高品质锌资源逐渐枯竭,高铁闪锌矿的开发利用引起人们的广泛关注。因其在选矿过程中无法将铁分离导致产出的锌精矿含铁高(>10%)、含锌低(<45%)[1]。在湿法炼锌过程中,铁以各种化合物形式进入渣中被除去。选择不同的除铁方法会影响到锌的总回收率,采用常规法炼锌工艺产出的浸出渣含锌高(约20%)、渣量大,需要火法处理回收渣中的锌[2]。采用热酸浸出-黄钾铁矾法处理高铁闪锌矿时产出大量铁矾渣(渣率约30%),渣含锌 4%~6%,不利于锌的回收[3]。针铁矿法在处理高铁闪锌矿时产出的渣量也较大,渣含锌8%。针铁矿渣需要火法处理回收锌,实现铁渣无害化。相比之下采用赤铁矿法处理高铁闪锌矿时产出的渣量小,含锌低。谢里特公司、秋田锌业和鲁尔电锌厂采用赤铁矿法得到的铁渣中含锌分别为0.6%、1.3%和1%[4-6]。在国内锌价较低的情况下,进一步提高锌及其他有价金属的回收率,减轻后续渣处理负担,充分利用资源,减排污染物,降低成本成为各锌厂的关注点。
ZnSO4是高铁溶液中重要的共存硫酸盐,溶液中Zn浓度的控制是赤铁矿除铁的关键环节。MgSO4是 高铁溶液中不可避免的硫酸盐,含量过高时要考虑到结晶带来的管道结垢的问题。硫酸盐含量的升高会改变高温氧压下溶液的性质,对赤铁矿的渣型产生影响。研究ZnSO4与MgSO4在氧压酸性条件下对赤铁矿法除铁的影响,探明硫酸盐的合理存在范围,对进一步提高除铁率及赤铁矿渣的商业用途具有重大意义。
本文作者选取高铁闪锌矿浸出液为原料,考察不同Zn离子和Mg离子浓度对除铁效果及渣的性质产生的影响,研究Zn离子和Mg离子在赤铁矿渣中的存在机理。
1 实验
1.1 实验原料
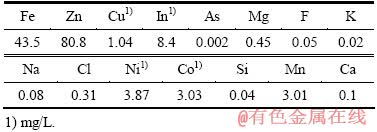
实验所用高铁闪锌矿取自云南,高铁溶液分别回收In和Cu后作为除铁原料,其主要化学成分如表1所列。溶液中大部分Fe以Fe(II)形式存在,Zn浓度为80.8 g/L,Mg浓度为0.452 g/L,有价金属Cu和In等含量低。
表1 浸出液主要化学成分分析
Table 1 Chemical compositions of leach liquor (g/L)
1.2 实验方法
添加分析纯七水硫酸锌(ZnSO4・7H2O)和分析纯七水硫酸镁(MgSO4・7H2O)配制不同浓度的Zn离子和Mg离子。采用2L-GSH型高压釜(材质为1Cr18Ni9Ti-TA2)作反应容器。将1 L浸出液加入高压釜内,添加晶种(分析纯Fe2O3),连接供氧设备后检查高压釜的气密性。调节氧分压0.3 MPa,搅拌转速600 r/min,维持反应温度的变化范围在±2 ℃。到达反应时间后快速降温,用旋片型真空泵(型号2XZ-4)取出矿浆抽滤过滤,滤液量后保存,取等滤液体积的去离子水洗渣。滤渣在101-I型电热鼓风干燥箱内干燥(温度55 ℃,时间48 h)后制样。
1.3 分析与检测
采用X射线衍射仪(D/max-2200)分析赤铁矿渣的物相成分。采用X射线光电子能谱仪(型号PHI5500)分析元素Zn、Mg和S在赤铁矿渣表面的存在形态。采用马尔文激光粒度仪(型号ZEN3690)分析赤铁矿渣的粒度。采用氮吸附比表面仪(BET)(型号Autosorb-1-C)分析赤铁矿颗粒的比表面积。采用红外光谱仪(型号Bruker TENSOR27)对渣中S的吸附含量进行表征。取赤铁矿渣和滤液送云南分析测试中心测定相关元素含量。
1.4 实验原理
已有研究表明,增加物料中的Zn浓度不仅可以扩大赤铁矿的热力学稳定区域[7],而且对Fe2+的氧化具有促进作用[8]。但随着ZnSO4和MgSO4浓度的增加会不同程度的降低高温下FeSO4的溶解度[9],导致除铁溶液中Fe(II)浓度升高,阻碍除铁反应的进行。饭岛冶炼厂的实际运行情况发现,沉淀物的颗粒尺寸随溶液中ZnSO4浓度的增加而降低,造成沉降和过滤的困难[10]。
S是赤铁矿渣中的主要污染物,Zn2+离子和Mg2+离子的引入必然导致溶液中SO42-含量的增多,考察Zn2+、Mg2+对除铁的影响时必须考虑到渣中S含量的变化。麦吉尔大学研究表明,S的来源除了铁矾以外还包括部分含硫化合物[11],DUTRIZAC[12]在研究铁矾渣向赤铁矿转化时发现,溶液中有Zn离子存在时,少量Zn以化合物形态进入赤铁矿中,不能通过水洗或酸洗除去。为此,本文作者结合高温氧压酸性体系下溶液的性质,研究硫酸盐的合理存在范围,产出更纯净的赤铁矿渣。
2 结果与讨论
2.1 Zn2+离子浓度对除铁的影响
实验条件如下:初始Fe2+浓度为43.5 g/L,Mg2+离子浓度为0.45 g/L,反应温度为190 ℃,反应时间为3 h,氧分压为0.3 MPa,晶种用量为15 g/L,搅拌速度为600 r/min,初始溶液pH为3.2,改变初始Zn2+离子的浓度,考察Zn2+离子对除铁的影响。实验结果如图1所示。
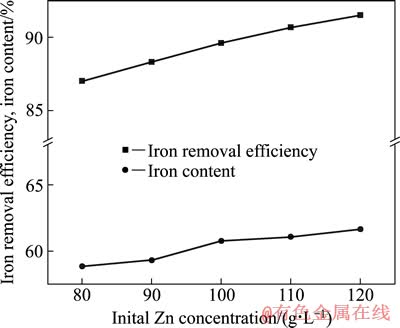
图1 初始锌离子浓度对除铁率及渣中铁含量的影响
Fig. 1 Effect of initial Zn2+ concentration on iron removal efficiency and iron contents in precipitate
由图1可见,增加初始溶液中Zn2+离子的浓度可以有效提高除铁率和渣中铁含量。Zn2+离子浓度由80 g/L升高至120 g/L时,除铁率由87.02%升高至91.50%;渣中铁含量由58.84%升高至61.67%;除铁溶液的Fe由6.78g/L降低至4.15g/L,Fe3+离子由6.18 g/L降低至3.19g/L。除铁率的升高与Fe2+离子的氧化能力密切相关。由同离子效应可知,硫酸盐体系下存在以下平衡关系:
H2SO4=H++HSO4-(完全电离) (1)
HSO4-=H++SO42-(部分电离) (2)
增加Zn2+的浓度可以降低式(2)的电离程度,改变反应初期溶液中自由H+的活度。根据PANANGELAKIS[13]模拟计算得到185 ℃下的物种平衡相图可知,自由H+浓度的降低可增加SO42-的浓度,提供更多的FeSO4离子对,FeSO4离子对的氧化能力较Fe2+离子的氧化能力强[8]。反应初期以Fe2+离子的氧化为主,H+活度的降低可促进氧化反应的进行,提高除铁率。初始Zn2+浓度为80和120 g/L条件下得到的赤铁矿渣的XRD如图2所示。

图2 不同初始Zn2+离子浓度下得到赤铁矿渣的XRD谱
Fig. 2 XRD pattern of hematite residues produced at various initial Zn2+ concentrations
由图2可见,Zn2+浓度对渣型有显著影响,初始Zn2+浓度低于100g/L时产物以赤铁矿和针铁矿为主。Zn2+浓度下降,针铁矿衍射峰(2θ=21.3°)的强度由372降低至270,半峰宽由0.469增加至0.735;赤铁矿衍射峰(2θ=33.24°)的强度由627增加至786,半峰宽由0.355降低至0.315。已有研究表明[14]:赤铁矿从高铁溶液中的析出顺序为
Fe(III)→FeOOH・H2Oamorphous→α-FeOOH or β-FeOOH→α-Fe2O3 (3)
实验结果表明,增加ZnSO4的浓度可以有效地转化亚稳态相(FeOOH),这主要依赖于增加ZnSO4的浓度可以提高FeSO4离子对的氧化能力。体系中Fe2+离子浓度的降低及Fe3+离子浓度的升高可以增加溶液的Eh。TINDALL等[15]的研究表明,当溶液的Eh较高时,针铁矿向赤铁矿转化的推动力是溶液中H+的浓度。初始Zn2+浓度由80 g/L升高至120 g/L时,除铁溶液的H+浓度由0.417 mol/L升高至0.676 mol/L。反应后期H+浓度的增加可破坏针铁矿的晶格,转化更多的针铁矿,增加赤铁矿渣中的Fe含量。ZnSO4含量的增加可以加速针铁矿陈化的过程,缩短亚稳态相的存在时间,作为晶型转化的推动力。因此,采用赤铁矿法处理高铁溶液(>40 g/L)时Zn2+的浓度宜高于80 g/L。
2.2 Mg2+离子浓度对除铁的影响
实验条件如下:初始Fe2+浓度为25 g/L,Zn2+浓度为80 g/L,反应温度为190 ℃,反应时间为3 h,氧分压为0.3 MPa,晶种用量为15 g/L,搅拌速度为600 r/min,初始溶液pH为3.2,改变MgSO4的浓度,考察MgSO4对除铁的影响。实验结果如图3所示。
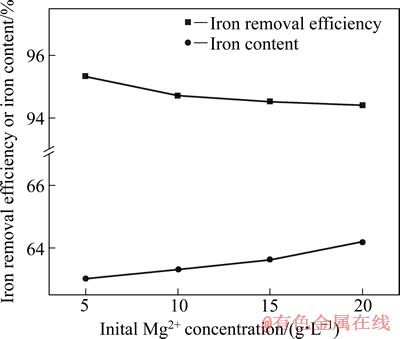
图3 初始Mg2+离子浓度对除铁率及渣中铁含量的影响
Fig. 3 Effect of initial Mg2+ concentration on iron removal efficiency and iron contents in precipitate
由图3可见,Mg2+离子浓度由5g/L升高至20g/L时,渣中的铁含量由63.02%升高至64.18%,除铁率由95.33%降低至94.40%。图4所示为不同初始Mg2+离子浓度下除铁溶液中Fet和Fe2+离子的浓度曲线。

图4 初始Mg2+离子浓度对除铁溶液的影响
Fig. 4 Effect of initial Mg2+ concentration on Fe concentration of purified solution
由图4可见,除铁溶液中全铁(Fet)与Fe2+离子的浓度均随初始溶液中Mg2+离子浓度的升高而增加,这主要是由于MgSO4的存在降低了FeSO4的溶解度。MgSO4和ZnSO4在高温酸性体系中会引起FeSO4溶解度线性降低的规律。HASEGAWA[9]给出了两种硫酸盐对FeSO4溶解度的影响:在200 ℃,30 g/L H2SO4的条件下,体系中的ρ(Zn2+)由0 g/L增加至20 g/L时,平衡液相中的ρ(Fe2+)由14.56 g/L降低至7.26 g/L;体系中的ρ(Mg2+)由0 g/L增加至7 g/L时,平衡液相中的ρ(Fe2+)由14.52 g/L降低至4.74 g/L。MgSO4浓度的升高更容易降低FeSO4的溶解度,导致除铁溶液中Fe2+离子浓度逐渐升高。由于ZnSO4浓度的升高而导致的FeSO4溶解度的降低不足以制约除铁反应的进行,但MgSO4浓度的升高会对除铁率产生负面影响。初始Mg2+离子浓度为5和20 g/L条件下得到的赤铁矿渣的XRD谱如图5所示。

图5 不同初始Mg2+离子浓度下得到赤铁矿渣的XRD谱
Fig. 5 XRD pattern of hematite residues produced at various initial Mg2+ concentrations
由图5可见,渣中的物相主要是赤铁矿和少量针铁矿。随初始Mg2+浓度的升高,除铁溶液的H+离子浓度分别为0.309、0.331、0.339和0.355 mol/L,当溶液中Fe2+离子浓度降低时,H+浓度的升高有利于破坏针铁矿晶格,得到铁含量更高的赤铁矿渣。为了减少MgSO4对FeSO4溶解度降低带来的影响,以及避免Mg2+浓度过高造成管道结垢的问题,Mg2+离子浓度不宜高于10 g/L。
2.3 Zn、Mg和S在渣中的分布
不同初始Zn2+浓度条件下得到的赤铁矿渣中Zn、Mg和S含量见表2和表3。
由表2和表3可见,赤铁矿渣中Zn和Mg的含量与初始溶液中Zn2+离子和Mg2+离子的浓度无关。渣中的Zn含量稳定在0.5%~1%、Mg含量稳定在0.015%左右、S含量随ZnSO4和MgSO4浓度的升高逐渐降低。
2.4 粒度和比表面积分析
表2 不同初始Zn2+离子浓度条件下赤铁矿渣中主要化学元素组成
Table 2 Chemical compositions of hematite residues at different initial Zn2+ concentrations
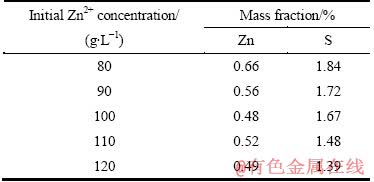
表3 不同初始Mg2+离子浓度下赤铁矿渣主要化学元素组成
Table 3 Chemical compositions of hematite residues at different initial Mg2+ concentrations
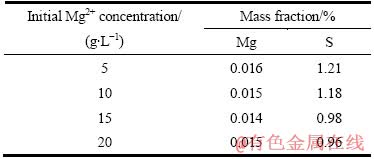
表4 初始Zn2+离子浓度对赤铁矿渣的平均粒度和比表面积的影响
Table 4 Effect of initial Zn2+ concentration on average particle size and specific surface area of hematite residues
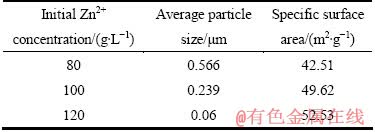

图6 不同初始Zn2+离子浓度下得到赤铁矿渣的粒度分布图
Fig. 6 Size distribution of hematite residues obtained at various initial Zn2+ concentrations
表4所列为不同初始Zn2+离子浓度下得到的赤铁矿渣的平均粒度和比表面积,图6所示为不同初始Zn2+离子浓度下得到赤铁矿渣的粒度分布图。
结合表4及图6可见,随Zn2+离子浓度的升高,赤铁矿渣的颗粒变细,颗粒的分布范围变窄,粒度大小更为集中。赤铁矿颗粒的减小与Fe2+离子的氧化能力以及溶液的性质有关,增加Zn2+离子浓度时,FeSO4离子对的氧化能力变强,溶液中Fe3+离子的饱和度增加,当Fe3+离子的饱和度(S)大于临界饱和度(Scr)时,更多的颗粒从溶液中析出。溶液的物理性质随ZnSO4浓度的升高而变化,Zn2+离子浓度由80 g/L升高至120 g/L时,溶液密度由1.27 g/L升高至1.37 g/L,体系中颗粒更容易发生聚合[16],聚合体系下均相成核占主导,更多的沉淀以均相成核的方式从溶液中析出。同时,硫酸盐浓度的升高会导致溶液的粘度增大,反应过程中颗粒的碰撞程度相应降低,也会一定程度减小赤铁矿的颗粒大小。赤铁矿渣中的S含量随颗粒尺寸的减小而降低,这与RUIZ等[17]采用水热法沉淀赤铁矿时得出的结论一致。
由表4可见,结晶析出的赤铁矿具有较大的比表面积,约是晶种比表面积(24.09 m2/g)的两倍,且随初始Zn2+浓度的升高有小幅增加的趋势。相对于赤铁矿平均粒度的减小而言,比表面积的增加趋势较小,假设样品中的颗粒以球状形貌为主,则考虑低硫酸盐浓度下氧化水解得到的颗粒具有较高的孔隙度。由于SO42-会以双配位络合的方式吸附于赤铁矿表面[18],故孔隙度的降低有助于减少渣中S含量。
2.5 红外光谱分析
为直观反映赤铁矿渣中吸附的S含量的变化,对初始Zn2+离子浓度分别为80和120 g/L得到的赤铁矿渣和晶种进行红外光谱分析,结果如图7所示。
由图7可见,在SO42-的吸收峰(900~1300 cm-1)范围内存在4个红外波段,对应着―SO42-的拉伸振动。随初始ZnSO4浓度的升高,4个波段的透过率明显升高。结合渣中的S含量可知,SO42-在颗粒表面的配合反应减弱。已有研究表明,赤铁矿渣中S的双配位络合反应随H+浓度的升高而降低[18]。故随着Zn2+离子浓度的升高,除铁溶液中H+浓度的升高也会在一定程度上降低渣中的S含量。
2.6 XPS分析
为确定赤铁矿渣中Zn、Mg和S的存在形态,分别对初始Zn2+离子浓度为80g/L和初始Mg2+离子浓度为20g/L条件下得到的赤铁矿渣进行XRS分析。结果如图8所示。

图7 晶种及不同初始Zn2+离子浓度下得到赤铁矿渣的红外光谱
Fig. 7 Infrared spectra of seed and hematite residues produced at various initial Zn2+ concentrations
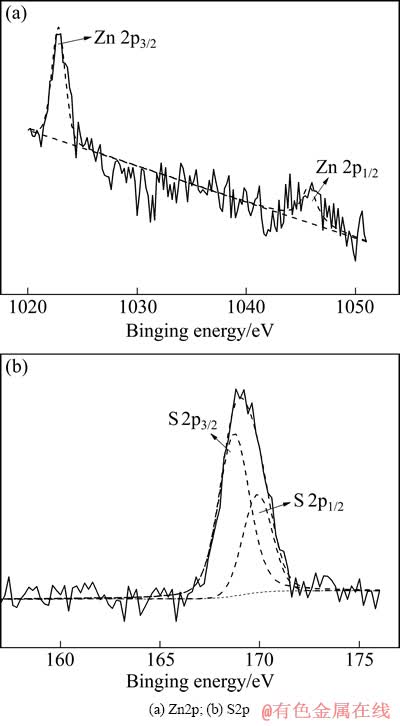
图8 赤铁矿渣的XPS谱
Fig. 8 XPS pattern of hematite residues
由图8可见,Zn的2p3/2峰和2p1/2峰对应的结合能分别为1022.80和1045.77 eV,S的2p3/2峰和2p1/2峰对应的结合能分别为168.7和167.52 eV,实验未能检测出Mg的峰值。结合有关物质的结合能数据[19]可知,渣中0.5%~1.0%的Zn以ZnSO4的形式存在于赤铁矿的表面;S以SO4的形式存在;渣中Mg的含量不随初始Mg2+离子浓度的增加而升高,始终低于0.02%。因此,Mg极有可能以夹带的方式存在于赤铁矿渣中。
赤铁矿渣中ZnSO4的来源与高温氧压酸性条件下ZnSO4的溶解度有关,已有研究表明,ZnSO4与FeSO4在水中的溶解度有相似的特性[20],随温度的升高溶解度急剧下降,高温下以一水硫酸盐的形式结晶析出,ZnSO4的溶解度随酸度的升高而减小。图9所示为 190 ℃和0.3 MPa氧分压条件下,不同时刻高铁闪锌矿浸出液中Zn2+离子的溶解度曲线图。

图9 反应时间对Zn溶解度的影响
Fig. 9 Effect of reaction time on zinc solubility
由图9可知,在高温氧压酸性条件下Zn2+离子浓度低于80 g/L,因为赤铁矿除铁反应不断产生酸液,所以随着反应的进行,ZnSO4的溶解度逐渐降低。日本秋田冶炼厂测量了不同温度下浸出液中Zn2+离子的溶解度,温度由187升高至200 ℃时,Zn2+离子的浓度由105 g/L降低至70 g/L[10],低于LIU等[20]测量的190 ℃时Zn2+离子在水中的溶解度(>120 g/L)。说明渣中少量ZnSO4的存在与ZnSO4的溶解度降低有关。DUTRIZA等[21]采用赤铁矿法处理Fe2(SO4)3溶液时发现,溶液中Zn2+离子浓度由0升高至100 g/L时,渣中Zn的含量均小于0.1%。说明当溶液中同时存在ZnSO4和FeSO4时,两种硫酸盐在高温下会同时结晶析出,FeSO4的溶解度随酸度的升高而增加[17],故除铁反应对FeSO4结晶的再溶解有促进作用,但会抑制ZnSO4结晶的再溶解。少部分未溶解的ZnSO4留在赤铁矿渣中,导致Zn含量高于0.5%,因ZnSO4的存在而引入的杂质S占渣中全S的20%。
综合考虑,为得到颗粒较大、比表面积较小、Zn和S含量较低的赤铁矿渣,高铁闪锌矿浸出液中Zn2+离子的浓度不宜高于100 g/L。
3 结论
1) 采用赤铁矿法处理高铁闪锌矿浸出液时,当Fe2+离子浓度过高(>40 g/L),渣相中会有针铁矿生成,增加初始溶液中Zn2+离子和Mg2+离子的浓度有利于针铁矿向赤铁矿转化。
2) 增加初始溶液中ZnSO4的浓度可以提高除铁率,增加初始溶液中MgSO4的浓度会降低FeSO4的溶解度,使除铁溶液中Fe2+离子的浓度升高。
3) 增加初始溶液中Zn2+离子和Mg2+离子的浓度均会减小赤铁矿的粒度,降低渣中S含量。
4) ZnSO4和FeSO4在高温酸性氧压条件下溶解度相似的特性,导致0.5%~1.0%的Zn以ZnSO4的形式存在于赤铁矿渣的表面。Mg以夹带的方式存在于渣中,其含量低于0.02%,不会污染赤铁矿渣。
5) 为获得高除铁率的同时得到过滤性良好的矿浆和结晶形态较好、颗粒较大、比表面积较小的赤铁矿渣,高铁闪锌矿浸出液中Zn2+离子的浓度不宜高于100 g/L、Mg2+离子的浓度不宜高于10 g/L。
REFERENCES
[1] 王吉坤, 李存兄, 李 勇, 张红耀, 黄 卉, 阎江峰, 刘 露, 魏 昶.高铁闪锌矿高压酸浸过程中ZnS-FeS-H2O系的电位-pH图[J]. 有色金属: 冶炼部分, 2006, 2: 2-5.
WANG Ji-kun, LI Cun-xiong, LI Yong, ZHANG Hong-yao, HUANG Hui, YAN Jiang-feng, LIU Lu, WEI Chang. The ε-pH figure of ZnS-FeS-H2O system during acid leaching under pressure of high iron sphalerite[J]. Nonferrous Metal: Extractive Metallurgy, 2006, 2: 2-5.
[2] 王纪明, 彭 兵, 柴立元, 李 密, 彭 宁. 锌浸渣还原焙烧-磁选回收铁[J]. 中国有色金属学报, 2012, 22(5): 1455-1461.
WANG Ji-ming, PENG Bing, CHAI Li-yuan, LI Mi, PENG Ning. Recovery iron from zinc leaching residues by reduction roasting and magnetic separation process[J]. The Chinese Journal of Nonferrous Metals, 2012, 22(5): 1455-1461.
[3] 何 静, 罗 超, 唐谟堂, 鲁君乐, 王小能, 王 涛. 采用铅黄铁矾去除硫酸体系中的铁[J]. 中国有色金属学报, 2012, 22(10): 2890-2895.
HE Jing, LUO Chao, TANG Mo-tang, LU Jun-yue, WANG Xiao-neng, WANG Tao. Technique of ferrum-removal by lead jarosite from sulfuric acid solution[J]. The Chinese Journal of Nonferrous Metals, 2012, 22(10): 2890-2895.
[4] COLLINS M J, CHALKLEY ME, MASTERS I M, OZBERK E. The sherritt two-stage zinc pressure leach process with hematite precipitation[C]//ROBSON A D. Proceedings of the International Symposium on Zinc. Parkville: Australasian Inst of Mining & Metallurgy, 1993: 315-323.
[5] ONOZAKI A, SATO K, KURAMOCHI S. Effect of some impurities on iron precipitation at the Iijima Zinc Refinery[J]. Iron Control in Hydrometallurgy, 1986: 742-752.
[6] OZBERK E, MAKWANA M, MASTERS I M,  R, BAHL W. Zinc pressure leaching at the Ruhr-Zink refinery[J]. Hydrometallurgy, 1995, 39(1): 53-61.
R, BAHL W. Zinc pressure leaching at the Ruhr-Zink refinery[J]. Hydrometallurgy, 1995, 39(1): 53-61.
[7] UMETSU V, TOZAWA K, SASAKI K. The hydrolysis of ferric sulfate solutions at elevated temperatures[J]. Canadian Metallurgical Quarterly, 1977, 16(1): 111-117.
[8] DREISINGER D B, PETERS E. The oxidation of ferrous sulfate by molecular oxygen under zinc pressure-leach conditions[J]. Hydrometallurgy, 1989, 22(1): 101-119.
[9] HASEGAWA F, TOZAWA K, NISHIMURA T. Solubility of ferrous sulfate in aqueous solutions at high temperatures[J]. Journal of the Mining and Materials Processing Institute of Japan(Japan), 1996, 112(12): 879-884.
[10] ARIMA H, AICHI T, KUDO Y, SARUTA K, KANNO M, TOGASHI R. Recent improvement in the hematite precipitation process at the Akita Zinc Company[J]. Iron Control Technologies, Canadian Institute of Mining, Metallurgy and Petroleum, Montreal, Canada, 2006: 123-134.
[11] CHENG T C, DDEMOPOULOS G P, SHIBACHI Y, MASUDA H. The precipitation chemistry and performance of the akita hematite process―An integrated laboratory and industrial scale study[C]//Hydrometallurgy 2003: 5th International Symposium Honoring Professor Ian M. Ritchie, 2003: 1657-1674.
[12] DUTRIZAC J E. Converting jarosite residues into compact hematite products[J]. JOM, 1990, 42: 36-39.
[13] PAPANGELAKIS V G, BLAKEY B C, LIAO H. Hematite solubility in sulfate process solutions[M]. Hydrometallurgy’94. Springer Netherlands, 1994: 159-175.
[14] VOIGT B;GOBLER A. Formation of pure hematite by hydrolysis of iron(III) salt solutions under hydrothermal conditions[J]. Crystal Research and Technology, 1986, 21(9): 1177-1183.
[15] TINDALL G P, MUIR D M. Effect of Eh on the rate and mechanism of the transformation of goethite into hematite in a high temperature acid leach process[J]. Hydrometallurgy, 1998, 47(2): 377-381.
[16] CHENG T C M, DEMOPOULOS G P. Analysis of the hematite precipitation process from a crystallization point of view[C]//MISHRI B. Proceedings of EPD Congress. Warrendale: TMS, 1997: 599-617.
[17] RUIZ M C, ZAPATA J, PADILLA R.Effect of variables on the quality of hematite precipitated from sulfate solutions[J]. Hydrometallurgy, 2007, 89(2): 32-39.
[18] CHENG T C M. Production of hematite in acidic zinc sulfate media[D]. Canada, Materials Engineering McGill University, 2002: 246-252.
[19] WAGNER C D. Handbook of X-ray photoelectron spectroscopy[M]. Perkin-Elmer, 1979.
[20] LIU H, PAPANGELAKIS V G. Thermodynamic equilibrium of the O2-ZnSO4-H2SO4-H2O system from 25 to 250 ℃[J]. Fluid Phase Equilibria, 2005, 234(1): 122-130.
[21] DUTRIZAC J E, CHEN T T. Behavior of various impurities during the precipitation of hematite from ferric sulfate solutions at 225 ℃[C]//T T Chen Honorary Symposium on Hydrometallurgy, Electrometallurgy and Materials Characterization. John Wiley & Sons, Inc., 489-499.
(编辑 龙怀中)
基金项目:国家重点基础研究发展计划资助项目(2014CB643404);国家自然科学基金资助项目(51364022)
收稿日期:2014-01-02;修订日期:2014-05-21
通信作者:魏 昶,教授,博士;电话:0871-65188819;E-mail:weichang502@sina.cn