��������������Ľ�������
�����꣬����⣬�� ������ ��
(���ϴ�ѧ ұ���ѧ�빤��ѧԺ������ ��ɳ��410083)
ժ Ҫ��Ϊ�Ʊ��ߴ����������Ը���������Ϊԭ�ϣ�����Һ�̱ȡ��¶ȡ�ʱ��������������������ʵ�Ӱ�졣�о�ȷ������������̵Ĺ��������������������̵Ķ���ѧ������ȷ������������۵���ѹ�������Ϊ��Һ�̱�3?1���¶�100 �棬ʱ��6.0 h����������Ϊ��������1.25�����ڴ��Ż����������£�������Fe��ƽ��������Ϊ91.69%������ѧ�о�������������۵�������������ڶ���ѧ����������ģ�ͣ�������1/2(1-at)-2/3-1/2=Kt���ܻ�ѧ��Ӧ�Ŀ��ƣ���Ӧ���Ϊ70.40 kJ/mol��
�ؼ��ʣ����ۣ��������������ѧ
��ͼ����ţ�O642.4��TQ136.1 ���ױ�ʶ�룺A ���±�ţ�1672-7207(2009)04-0874-05
Leaching process of millscale from steel plant
PENG Chang-hong, HU Zhen-guang, DAI Jin, FU Feng
(School of Metallurgical Science and Engineering, Central South University, Changsha 410083, China)
Abstract: For preparation of high-purity iron oxide, a study on the leaching of millscale from steel plant and the effects of the liquid-solid ratio, the reaction temperature, the leaching time and the sulfuric acid excessive times was investigated. The best technical conditions of the leaching process were ascertained, and the kinetics of leaching was studied. The results show that when liquid-solid ratio is 3?1, the sulfuric acid excess is 1.25 times, reaction temperature is 100 �� and the leaching time is 6.0 h, the average leaching rate of Fe in the three comprehensive experiments is 91.69%. The leaching process is controlled by chemical reaction and can be described by the shrinking core model with activation energy of 70.40 kJ/mol.
Key words��millscale; sulfuric acid leaching; kinetics
������ҵ������������Ʒ�Ĺ����У������ԼΪ�ֲ���1.0%�����������׳ơ����ۡ����ҹ����и�������Լ5��t/a��������Լ500��t/a[1]���仯ѧ���������ܴ���һ������[2-4]�������ɷ�����������Ŀǰ������������۵Ĵ��������������Ʊ�Fe2O3[5]�����������ռ���Ʒ�ĸ���ֵ�ͣ�������Fe2O3��������ʵ�ָ��������۵ĸ�ֵ���������ش����մɷ������Ʊ���п���������壬�ߴ�Fe2O3����ռ70%����[6]����ǰ����Mn-Zn��������ܲ���ԼΪ23��t��ȥ��������ҵ�IJ���5.87��t��ʵ��������ҵ������IJ���Լ17.13��t��Լ��Fe2O3 12��t�������������Ʊ�Mn-Zn�������Fe2O3�IJ���Լ8��t��ȱ��Լ4��t������Ӿ�����ڲ��䡣���Ӧ����Ҫ�У��ձ���JFE��������EG��DONGBU���¹���Thyssen-krupp���ҹ�̨��ʡ���иֵȡ����ܽ������Ƴ���п�������õĸߴ�Fe2O3��������������۵����ü�ֵ��Ϊ�ˣ���������������ø���������Ϊԭ���Ʊ���������п�������������������ǣ����������۵����ʳɷָ��ӣ������ϸ�[7]�����ݶ���п��������������Ʊ��Ĵ����о�[8-10]��֪��ʵ�ָ����������Ʊ���������п��������Fe2O3��ǰ��ؼ���ʵ��������Fe�Ľ����ͽ���Һ������ʹӰ����п���������ܵ����ʳɷֽ� ��[11]�����������о��˸�������������������̵Ĺ���������̽���������̵Ķ���ѧ������
1 ʵ ��
1.1 ʵ��ԭ��
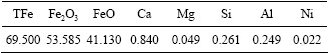
����ȡ�Ժ��Ϻ����ֹܳ�������ĥ������С��0.18 mm���仯ѧ�ɷּ���1��
��1 ���۵Ļ�ѧ�ɷ�
Table 1 Chemical composition of millscale
��������/%
1.2 ������������
��������������������۷��Ϲ����У���Ҫ��Ӧʽ���£�
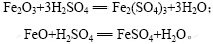
�������۷��ϵĻ�ѧ�ɷֺ������������������������۽��������е�����������
1.3 ʵ�鷽��
���õ�����ʵ���о��������ֱ�Һ�̱ȡ���Ӧ�¶ȡ���Ӧʱ����������������ض�������Fe�����ʵ�Ӱ����ɡ������ٶȳ��������Ϊ400 r/min����Ӧ��500 mL��������ƿ�н��С�
1.4 ���ķ���
��ȡһ��������Ʒ��ŨHCl�ܽ������SnCl2��ԭ������HgCl2��������Ͷ�����������ָʾ�������ظ���ر���Һ�ζ����յ㡣
2 ���������
2.1 Һ�̱ȶ�������Fe�����ʵ�Ӱ��
�ڹ̶�����ʱ��Ϊ3.0 h����Ӧ�¶�Ϊ90 ������������������������������£�����Һ�̱�(Һ��������������֮��)��������Fe�����ʵ�Ӱ����ɣ������ͼ1��
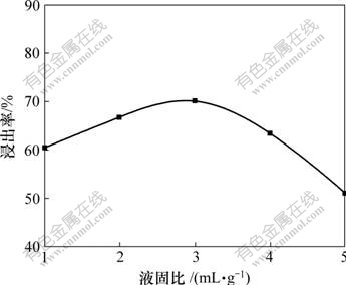
ͼ1 Һ�̱ȶ�Fe�����ʵ�Ӱ��
Fig.1 Effect of liquid-solid ratio on leaching rate of Fe
��ͼ1��֪������Һ�̱ȵ�����Fe�Ľ�������������С����Һ�̱�Ϊ3?1ʱ��Fe�Ľ����ʴﵽ70.04%���������������ԭ���ǣ���Һ�̱�̫Сʱ����Һ����ȸߣ�FeSO4��Fe2(SO4)3Ũ�Ƚϴ�������Һ��H+�Ļ�ȣ�������������Fe�Ľ���������Һ�̱�������Һ��H+�Ļ������������������Fe�Ľ���������Һ�̱ȳ���һ��ֵ֮����Һ��Ƚ��ͣ�Fe�Ľ����ʿ�ʼ�����½�����ˣ�ȡ��������������̵����Һ�̱�Ϊ3?1��
2.2 �¶ȶ�Fe�����ʵ�Ӱ��
�ڹ̶�Һ�̱�Ϊ3?1����������������������������ʱ��Ϊ3.0 h�������£����췴Ӧ�¶ȶ�������Fe�����ʵ�Ӱ����ɣ������ͼ2��
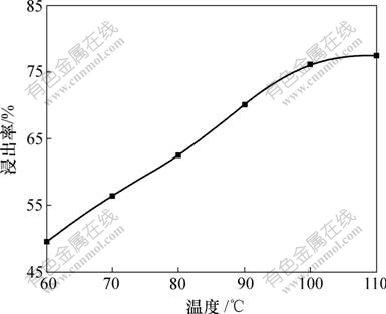
ͼ2 ��Ӧ�¶ȶ�Fe�����ʵ�Ӱ��
Fig.2 Effect of reaction temperature on leaching rate of Fe
��ͼ2�ɿ�����������Fe�Ľ��������¶ȵ��������������¶���60 �����ߵ�100 ��ʱ��������Fe�Ľ�������49.62%��ߵ�76.18%���¶�ÿ���� 10 �棬Fe�Ľ�����ƽ�����6.64%�����ǣ����¶���100 �����ߵ�110 ��ʱ��������Fe�Ľ����ʽ����0.25%�����ǵ��¶ȹ���ʱ��Һ��ˮ��������̫���Լ��豸����Ҫ��ߣ�ȡ��������������̵��¶�Ϊ100 �档
2.3 ��Ӧʱ��Խ����ʵ�Ӱ��
�ڹ̶�Һ�̱�Ϊ3?1�������¶�Ϊ100 �棬���������������������������£��������ʱ���������Fe�����ʵ�Ӱ����ɣ������ͼ3��
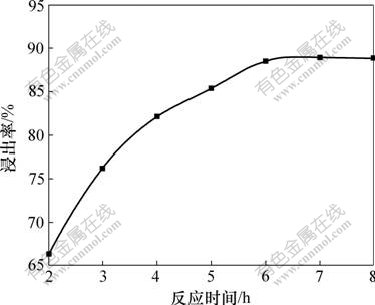
ͼ3 ��Ӧʱ���Fe�����ʵ�Ӱ��
Fig.3 Effect of reaction time on leaching rate of Fe
��ͼ3��֪��������Fe�Ľ����������ʱ����ӳ���������Ӧʱ����1 h���ӵ�6 hʱ��Fe�Ľ�������66.42%����88.49%��Fe�Ľ����������22.07%�������������Ͽ죻����Ӧʱ���ӳ���7.0 hʱ��Fe�Ľ����ʽ����0.42%���ӳ���8 h��Fe�Ľ����ʼ���û�б仯�����������Ѿ�ƽ�⣬������������Ϊ88. 91%�����ǵ��������أ�ȡ�����������������ʱ��Ϊ6.0 h��
2.4 ����������Fe�����ʵ�Ӱ��
�ڹ̶�Һ�̱�3?1��ʱ��6.0 h�ͷ�Ӧ�¶�100 ��������£���������������������Fe�����ʵ�Ӱ����ɣ������ͼ4�����У� Ϊ����ʵ����������������֮��(mol/mol)��
Ϊ����ʵ����������������֮��(mol/mol)��
��ͼ4��֪������������������Fe�Ľ�����Ӱ��ϴ������������������ӣ�������Fe�Ľ�������������С������������Ϊ��������1.25��ʱ��������Fe�Ľ����ʴﵽ91.36%�����������������Ľ�һ�����ӣ�������Fe�Ľ����ʷ������ּ�С�����ơ��������������ԭ�����ڣ�������������Сʱ����Һ����ȵͣ�������Fe������Ҳ�ͣ������������������ӣ���Һ��������ӣ�������Fe�Ľ�������������������Ϊ������1.3��ʱ����Ӧ��ϵ��Һ�̱�ʵ���Ѵﵽ2?1�����������Һ��ȹ��ߺ�������������Һ��H+�Ļ�ȣ����������Fe�Ľ����ʽ��͡�
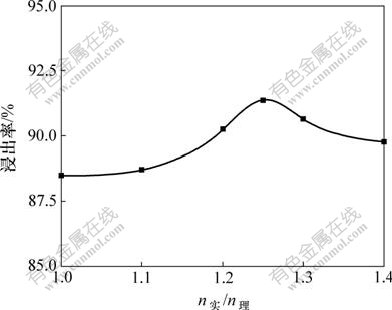
ͼ4 ����������Fe�����ʵ�Ӱ��
Fig.4 Effect of different sulfuric acid excessive times on leaching rate of Fe
2.5 ���۽������̵��ۺ�����ʵ��
����������������ʵ�������ۺϿ����豸���ʺ�����Ч�ʵ����أ�ȷ����������������̵����Ź����������£�Һ�̱�Ϊ3?1����Ӧ�¶�Ϊ100 �棬��Ӧʱ��Ϊ6.0 h����������Ϊ������1.25�����������Ż����������£�������3���ۺ�����ʵ�飬�������2��
��2 �ۺ�����ʵ����
Table 2 Result of experiments under comprehensive condition
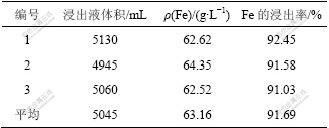
�ӱ�2��֪���������Ż����������£������������������Fe�����нϸߵĽ����ʣ���ƽ�������ʴ�91.69%��
3 �������̶���ѧ����
�������������෴Ӧ�����۵Ľ������̾������۷�����������Һ����ɵĹ�-Һ���෴Ӧ���������̿��Ʋ����ɻ�ѧ��Ӧ���ƻ�Ӧ����ɢ����[12]�����۷��ϵ�����������ʿ�������ҺĤ��ɢ���ƻ�ѧ��Ӧ���ơ�
�����ٶȶ�ҺĤ��ɢ���Ƶķ�Ӧ������Ӱ��dz�����߽���ǿ�ȣ���ɢ���Ƶķ�Ӧ�����ʿ����40%~70%[13]��Ϊ�ˣ��������Ż����������£���������ٶȶ�Fe�����ʵ�Ӱ�죬�����ͼ5��
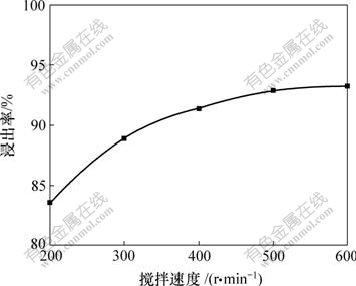
ͼ5 �����ٶȶ�Fe�����ʵ�Ӱ��
Fig.5 Effect of stirring speed on leaching rate of Fe
����ͼ5���֣��������ٶ���200 r/min��ߵ�600 r/minʱ�����������9.68%��ֻ���ֳ�һ�������ϵ��Һ���г�ַ�ɢ�������Ľ�������ߵ�Ч�����ݴˣ��ж����۷������������Ӧ�Ŀ��Ʋ��費����ɢ����[12-13]��
����ѧ��Ӧ����Ϊ���Ʋ��裬�ҷ�Ӧû�������µĹ���ʱ���÷�Ӧ�Ķ���ѧģ�Ϳ���������ģ�����������������ٶȷ���[14]��
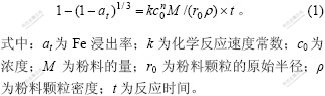
����Ũ��c�ı仯��������ģ�ͽ�������[12]���õ���
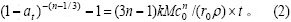
��n=1��ʽ(2)��Ϊ��
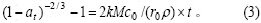
����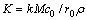 ����ʽ(3)��Ϊ��
����ʽ(3)��Ϊ��
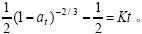
�����ܻ�ѧ��Ӧ���Ƶ����������Ӧ�Ľ������뷴Ӧʱ��ɱ�����ϵ��
����ʵ��������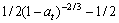 ��ʱ��t��ͼ�������ͼ6��
��ʱ��t��ͼ�������ͼ6��
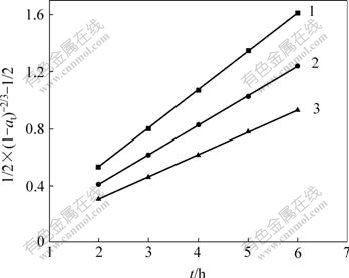
�����¶�/��: 1��100; 2��90; 3��80
ͼ6 �¶Ȳ�ͬʱ��ѧ��Ӧ����������ģ��
Fig.6 Shrinking core model controlled by chemical reaction procedures at different temperatures
��ͼ6��֪����������������̷��ϻ�ѧ��Ӧ���Ƶķ�Ӧģ�ͣ��ʿ��жϽ�����Ӧ�Ŀ��Ʋ���Ϊ��ѧ���ơ�
���ݰ�������˹��ʽ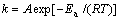 �ɵã�
�ɵã�

����ͼ6��ò�ͬ�¶�ʱ���ٶȳ������ó�lg k��1/T�Ĺ�ϵ����ͼ7��
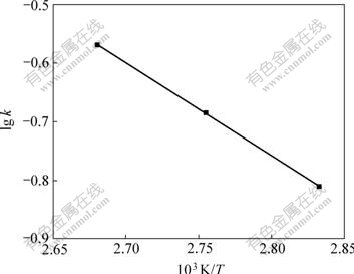
ͼ7 lg k��103 K/T�Ĺ�ϵ
Fig.7 Relationship between lg k and 103 K/T
��ͼ7�������Ea/(2.303��103R)= 3.68�������ۻ��Ea=70.40 kJ/mo1��
4 �� ��
a. ��Һ�̱ȴﵽ3?1ʱ���������ʴﵽ���Һ�̱�������ʱ�������ʼ�С������������Ϊ����������1.25��ʱ���������ʴﵽ���ֵ��������ʱ��ﵽ6.0 h���������������ȶ���
b. �¶ȶ���������Ӱ��ϴ���Һ�̱�Ϊ3?1����Ӧ�¶�Ϊ100 �棬��Ӧʱ��Ϊ6.0 h����������Ϊ��������1.25�����Ż����������£�������Fe��ƽ��������Ϊ91.69%��
c. ���������۵�����������̷���Һ-�̷�Ӧ��������ģ�ͣ�Fe���������ܻ�ѧ��Ӧ���Ƶ�������ģ��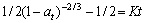 �Ϸ��ϣ���Ӧ�Ļ��Ϊ70.40 kJ/mol��
�Ϸ��ϣ���Ӧ�Ļ��Ϊ70.40 kJ/mol��
�ο����ף�
[1] �����. ����������������ҵ��չΪ���Բ��ϲ�ҵ׳���ṩ֧��[J]. ���Բ��ϼ�����, 2005, 36(6): 45-49.
LI Ba-yu. Iron oxide: The rapid development of iron and steel companies in China: Providing supports to Chinese magnetic material industry[J]. Journal of Magnetic Materials and Devices, 2005, 36(6): 45-49.
[2] Koros P J. Dusts, scale, slags, sludges�� not wastes, but sources of profits[J]. Metallurgical and Materials Transactions B, 2003, 34B(6): 769-779.
[3] Heino J, Laitila L, Hiltunen A, et al. Optimisation of steel plant recycling in Finland: Dusts, scales and sludge[J]. Resources, Conservation and Recycling, 2002, 35(1/2): 77-84.
[4] Nolasco-Sobrinho P J, Espinosa D C R, Tenorio J A S. Characterisation of dusts and sludges generated during stainless steel production in brazilian industries source[J]. Ironmaking and Steelmaking, 2003, 30(1): 11-17.
[5] ������. ������ӹ������������������е�Ӧ��[J]. ���Բ��ϼ�����, 2002, 33(4): 44-45.
XU Xiu-sheng. Further processing of millscale and its application in permanent ferrite materials[J]. Journal of Magnetic Materials and Devices, 2002, 33(4): 44-45.
[6] ������, ������, ������, ��. �ߴ����צ�-2Fe2O3������Ʊ�������[J]. ���ϴ�ѧѧ��: ��Ȼ��ѧ��, 2006, 37(3): 487-492.
YANG Zheng-hui, GONG Zhu-qing, MA Yu-tian, et al. Preparation and characterization of high-purity ��-2Fe2O3 nanoparticles[J]. Journal of Central South University: Science and Technology, 2006, 37(3): 487-492.
[7] ������, �� ��. �������������������Բ���[J]. ���Բ��ϼ�����, 2001, 32(5): 56-61.
YIN You-xiang, SUN Yan. Iron oxides and ferrite magnetic materials[J]. Journal of Magnetic Materials and Devices. 2001, 32(5): 56-61.
[8] ������, Ľ˼��, ������, ��. ���ø������̳��Ʊ���п�����干������[J]. ���ϴ�ѧѧ��: ��Ȼ��ѧ��, 2006, 37(1): 31-35.
PENG Chang-hong, MU Si-guo, TANG Mo-tang, et al. Mn-Zn ferrite co-precipitation powders made from steel plant dust[J]. Journal of Central South University: Science and Technology, 2006, 37(1): 31-35.
[9] ������, ������, ������, ��. ֱ�ӷ��Ʊ�������������������ʵ���о�[J]. ʪ��ұ��, 2003, 22(3): 142-146.
PENG Chang-hong, TANG Mo-tang, YANG Sheng-hai, et al. Research of enlarge experiments to fabricating low cost soft magnetic ferrite by using direct method[J]. Hydrimetallurgy, 2003, 22(3): 142-146.
[10] ��С��, ������. �����̿���п����мֱ����ȡ��п���������Ų����¹����о�[J]. �й���ҵ, 1996, 14(1): 42-44.
HUANG Xiao-zhong, TANG Mo-tang. The novel process of manufacturing Mn-Zn ferrites from pyxrolusite, sphalerite and steel scraps[J]. China��s Manganese Industry, 1996, 14(1): 42-44.
[11] �� ��, ������, Ǯ����. ��п��������������������Ҫ��[J]. ���Բ��ϼ�����, 2004, 35(4): 42-43.
SHAO Feng, LI Xiao-qing, QIAN Qiong-hui. Requirements for properity of ferric oxide for MnZn ferrites[J]. Journal of Magnetic Materials and Devices, 2004, 35(4): 42-43.
[12] ����. ʪ��ұ��ѧ[M]. ��ɳ: ���ϴ�ѧ������, 2002: 83-85.
LI Hong-gui. Science of hydro-metallurgy[M]. Changsha: Central South University Press, 2002: 83-85.
[13] �����, ������, Ԭ����. ʪ����п����������������Ķ���ѧ[J]. �й���ɫ����ѧ��, 2001, 11(5): 933-937.
HU Tian-jue, ZENG Guang-ming, YUAN Xin-zhong. Leaching kinetics of silver extracted by thiourea from residue in hydrometallurgy of zinc[J]. The Chinese Journal of Nonferrous Metals, 2001, 11(5): 933-937.
�ո����ڣ�2008-09-02�������ڣ�2008-11-22
������Ŀ�����Ҹ�����չ�о��ƻ�(863)��Ŀ(2006AA06Z373)���㶫ʡ-��������ѧ��ר�����������Ŀ(2006D904032)���й���ʿ���ѧ����������Ŀ(20060400884)���㶫ʡ�Ƽ��ƻ���Ŀ(2008A080403007-03)
ͨ�����ߣ�������(1966-)���У����ϳ�ɳ�ˣ���ʿ�������ڣ�����ֱ�ӷ��Ʊ���п�����幦�ܲ��ϼ���������Һ��ϳ���Ӧ���о����绰��0731-88836724��E-mail: Peng9103@163.com