��ɢ����Fe3O4���滯ѧ���Ե�Ӱ��
��ϲ��,������
(���ϴ�ѧ ұ���ѧ�빤��ѧԺ,���� ��ɳ,410083)
ժҪ: ��Zeta��λ�͵�����ܶ�Ϊ����ָ��,�о��˲�ͬ��ɢ����ʮ����������ơ����Ҷ������������Fe3O4���滯ѧ���Ե�Ӱ�졣�о��������:Fe3O4�ȵ���pHֵΪ6.4~6.8,��pH��6.4ʱ,����������,��pH>6.8ʱ,����������;ʮ����������ƺ�������ͨ��������������ʹFe3O4�ı����ɷ����dz������ı仯,�ȵ�����������Է����ƶ�,Fe3O4������С,��ɢ�ȶ�����Խǿ;���Ҷ�����Fe3O4�γ���λ��,�ṩλ������ı�Zeta��λ�͵�����ܶ�,��Fe3O4�������ͷ�ɢ����������Ӱ�졣
�ؼ���: Fe3O4; Zeta��λ; ������ܶ�; ��ɢ��
��ͼ�����:O647.2 ���ױ�ʶ��:A ���±��: 1672-7207(2005)02-0243-05
Effect of Dispersants on Surface Chemical Properties of Magnetite
YANG Xi-yun, GONG Zhu-qing
(School of Metallurgical Science and Engineering, Central South University, Changsha 410083, China)
Abstract: Surface chemical properties of magnetite were investigated by measuring Zeta potential and surface charge density. The effects of different dispersants,such as sodium lauryl sulfate,polyethylene glycol and citric acid on surface charge of magnetite were discussed. The results show that the zero point of charges (ZPC) for magnetite in KNO3 solution is determined to be 6.4~6.8, the surface acquires a positive charge at pH value below 6.4 and a negative charge at pH value above 6.8. In the presence of sodium lauryl sulfate and citric acid, surface charge of magnetite powder changes significantly and ZPC shifts toward acidic environment probably due to electrostatic adsorption, and as a result, the diameter of Fe3O4 is decreased and dispersing property is improved. In a solution containing polyethylene glycol, the change of Zeta potential and surface charge is considered to be brought about by complex bond and position obstruction repulsion, which has no obvious effect on the diameter and dispersing property of Fe3O4.
Key words: magnetite; Zeta potential; surface charge density; dispersants
Fe3O4�ڴ��Բ��ϡ����������ﻯѧ�ȴ�ͳ����õ��㷺Ӧ��,���ֳ�Ϊ����Һ�塢��ˮ������������ҩ������Ͳ��ϵ���Ҫ��ɲ���[1-7]�����ڴ�������֮��Ĵ�������������֮��ķ��»���,Fe3O4�������Ʊ��������ѷ�ɢ�����žۡ�Ҫ�Ʊ���ϸFe3O4���ӵĹؼ���ѡ����ʵķ�ɢ��[8]��һ��ѡ���ɢ���ķ�����:�ȷֱ���벻ͬ��ɢ���Ʊ���Fe3O4,Ȼ�����������,���������Ĵ�С��ѡ����ʷ�ɢ�������ַ�����ʱ,�ɱ��ߡ���ʵFe3O4�����Ƿ��ž��ںܴ�̶���������滯ѧ���ʵ�Ӱ�졣P.P.OSCAR�Ȳ�����Fe3O4��[CM(22] KNO3,CaSO4��Al(NO3)3�е�Zeta��λ��pHֵ�Ĺ�ϵ,�õ��˵ȵ��ֵ[9];M.S.SYED�о���Fe3O4��KNO3��Һ�еĽ�������[10];�̺�����о�������Fe3O4�ĦƵ�λ�ͷ�ɢ�ȶ��ԵĹ�ϵ[11]�������ڷ�ɢ����Fe3O4���滯ѧ����Ӱ����о��ͱ������١��ڴ�,������Zeta��λ��������ܶ�Ϊָ��,�о��˲�ͬ��ɢ����pHֵ��ˮ��Һ��Fe3O4���ӵı��滯ѧ���ʵ�Ӱ�졣
1 ʵ ��
1.1 ʵ��ԭ��
���������������Ʊ�Fe3O4[1],��ȱ����Ϊ12.59 m2/g,ƽ������ԼΪ0.30 ��m,���Ʊ���Fe3O4�����ɨ��羵(SEM)��Ƭ��ͼ1��ʾ��

ͼ 1 Fe3O4�����SEM��Ƭ
Fig. 1 SEM image of Fe3O4 powder
���÷�ɢ����:ʮ�����������(SDS);���Ҷ���(PEG),��ƽ����Է�������Ϊ4 000;�����ᡣʵ���õ�HNO3,KNO3��KOH��Ϊ��������
1.2 Fe3O4��Zeta��λ�������IJⶨ
Fe3O4��Zeta��λ(�Ƶ�λ)��������Brookhavan��˾��Zeta Potential Analyzer�ⶨ,Fe3O4����������Ϊ0.01%,��0.001 mol/L KNO3��������ǿ��,��������������ص���pHֵ��Fe3O4����������MS-2000�������ȷ����Dz��ԡ�
1.3 Fe3O4������ܶȵIJⶨ
Fe3O4������ܶȵIJⶨ����Ϊ:��һ������Fe3O4���뵽20 mL��֪Ũ�Ⱥ�pHֵ�ķ�ɢ����Һ��(����0.001 mol/L KNO3),������20 min,ͨ��N210 min�Գ�ȥFe3O4�������������O2,Ȼ�����pHֵ����Fe3O4������Һǰ������pHֵ�ı仯���Ѳ�õıȱ����,�������ͬpHֵ������Fe3O4�ĵ�����ܶ�,���ɴ˵õ��ȵ��[10]���������ܶȵļ��㹫ʽΪ:
��=[F/(mA)]��(��H+-��OH-)
��������ϵ��:
��=[F/(mA)]��(��H+-��OH-)��[F/(mA)]����H+=[F/(mA)]��(10-pHǰ-10-pH��)��0.02;
�ڼ�����ϵ��:
��=[F/(mA)]��(��H+-��OH-)��-[F/(mA)]����OH-=-[F/(mA)]��(10-(14-pHǰ)-10-(14-pH��))��0.02��
����:��Ϊ������ܶ�,C/cm2;FΪ�����ڳ���;mΪFe3O4������, g;AΪFe3O4���ӵıȱ����,cm2/g;��H+ΪFe3O4����������H+����;��OH-ΪFe3O4����������OH-����; pHǰΪ����Fe3O4ǰ��Һ��pHֵ;pH��Ϊ����Fe3O4����Һ��pHֵ��
1.4 �������ܵIJⶨ
��ȡ0.5 g Fe3O4����100 mLˮ��,�ڳ������з�ɢ30 min,����100 mL������Ͳ��,�۲���Һ�����������ʱ�䡣ʱ��Խ��,��ɢЧ��Խ�á�
2 ���������
2.1 Fe3O4���滯ѧ����
Fe3O4��0.001 mol/L KNO3��ϵ������ˮ�е�Zeta��λ��pHֵ�Ĺ�ϵ��ͼ2��ʾ��
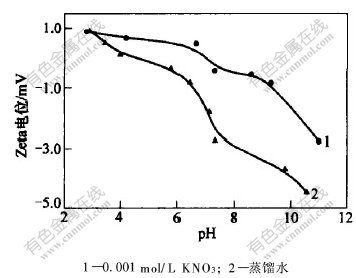
ͼ 2 Fe3O4��Zeta��λ��pHֵ�Ĺ�ϵ
Fig. 2 Relationship between Zeta potential of Fe3O4 and pH value
��ͼ2�ɼ�,��0.001 mol/L KNO3��ϵ��,Fe3O4���ӵĵȵ��λ��pH=6.8����,��������[12,13]�ı���һ��;����ˮ��ϵ����ȵ��λ��pH=5.6������Fe3O4����������ˮ��KNO3�е�Zeta��λ����pHֵ�����Ӷ���С����������������ɢ��ˮ�������ڱ����γ�һ��ˮ��Ĥ,����������H+��OH-������,�ڲ�ͬ��pHֵ��,��ɢ��ˮ�еķ����������ܶ������������������H+��OH-���������,ˮ��Һ�е�H+��OH-���������������ı����ɾ�������,��ˮ����Ӧ����:
MeOH+2[FY(Z]H+[FY)]Me(OH)[FY(]OH-[FY)]
MeO-+H2O��(1)
Fe3O4�����ڵȵ�㴦����������H+��������OH-��Ŀ���,�ʲ���������ɺ������Ŀ��ȡ����,����治�����,��ʱ���������žۡ�ͼ3��ʾΪ�ڲ�ͬpH������Fe3O4�ĵ�����ܶ����ߡ�
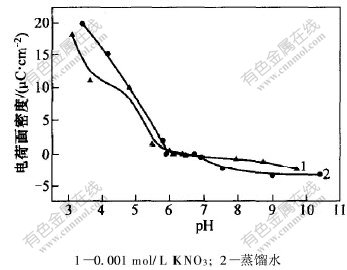
ͼ 3 Fe3O4������ܶ���pHֵ�Ĺ�ϵ
Fig. 3 Relationship between surface charge density of Fe3O4 and pH value
��ͼ3�ɼ�,Fe3O4������ˮ��0.001 mol/L KNO3��ϵ�еĵ���ܶȱ仯������ͬ,��ֵ�ӽ�,�ȵ���Ϊ6.4,pH��6.4,����������;pH>6.4,���������硣
2.2 SDS��Fe3O3�����������Ե�Ӱ��
���Ʊ�Fe3O4�Ĺ����г�ѡ�ñ�����Լ����������ɢ�ȶ����ܡ�ͼ4��ʾΪ����SDS��Fe3O4���ӵ�Zeta��λͼ����ͼ4�ɼ�,����SDS��,Fe3O4�ĵȵ�����������Է����ƶ�,Zeta��λ������pHֵ��Χ�ڶ�Ϊ��ֵ��
ͼ5��ʾΪ����SDS��Fe3O4 �ĵ�����ܶ���pHֵ�Ĺ�ϵ���ߡ���ͼ5��֪,SDS�ļ���ʹFe3O4�ĵ�����ܶ������Եı仯,������pHֵ��Χ�ڶ�Ϊ��ֵ����������SDS��һ���������ͱ�����Լ�,��ˮ��Һ�л�������,SDS������Ĵ�����Ļ��ŷdz����������ڴ������Fe3O4���ӱ�����,ʹFe3O4������ִ����������,���,��ȵ�����������Է����ƶ����䷴Ӧ����ʽΪ:
CH3(CH2)11OSO3Na��CH3(CH2)11OSO-3+Na+;(2)
CH3(CH2)11OSO-3+H++MeOH��MeOH+2��CH3(CH2)11OSO-3��(3)
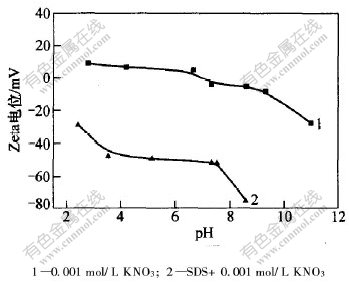
ͼ 4 ����SDS�� Fe3O4���ӵ�Zeta��λ��pHֵ�Ĺ�ϵ
Fig. 4 Relationship between �� potential of Fe3O4with addition of SDS and pH value
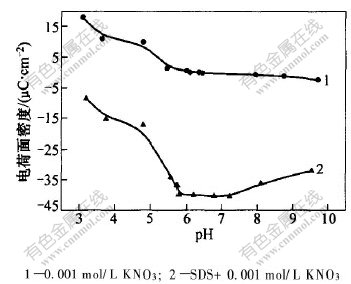
ͼ 5 ����SDS�� Fe3O4 �ĵ�����ܶ���pHֵ�Ĺ�ϵ
Fig. 5 Relationship between surface charge density of Fe3O4 with addition of SDS and pH value
��ͼ5�ɿ���,������ϵFe3O4�������������pHֵ�ı仯������Zeta��λ�еı仯��һ�¡�����Ҫ�Ǽ�����ϵ���н϶��OH-, OH-��MeOH �е����,������CH3(CH2)11OSO-3��MeOH�е����,�������˷�Ӧ(3)���ҽ���,������Fe3O4�������ܶȡ�
2.3 PEG��Fe3O4�����������Ե�Ӱ��
ͼ6��ʾΪ����PEG��Fe3O4���ӵ�Zeta��λ����ͼ6�ɼ�,����PEG��,Fe3O4�ĵȵ��ΪpH=5.5,�봿KNO3��ϵ�е�����������Է���ƫ��,�Ҵ�pHֵ��Χ��Zeta��λ�ľ���ֵ�ȴ�KNO3��ϵ�еĴ���������PEG��һ�ַ����ӱ�����Լ�, PEG�����Ѽ�����ԭ�ӡ�O����Fe3O4���γ���λ��[14]������PEG�Ǹ������,���ṩһ��λ�����,�Ӷ�������Fe3O4�����Zeta��λ��
ͼ7��ʾΪ����PEG��Fe3O4�ĵ�����ܶ���pHֵ�Ĺ�ϵ���ߡ���ͼ7��֪, PEG��Fe3O4�ĵ�����ܶȵ�Ӱ�첻��,�봿KNO3��ϵ�еĽӽ�,�ȵ��Ϊ5.7��
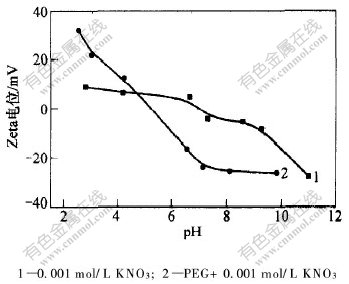
ͼ 6 ����PEG��Fe3O4��Zeta��λ��pHֵ�Ĺ�ϵ
Fig. 6 Relationship between �� potential of Fe3O4with addition of PEG and pH value
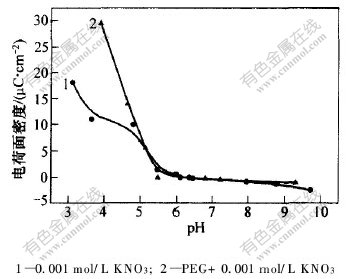
ͼ 7 ����PEG��Fe3O4�ĵ�����ܶ���pHֵ�Ĺ�ϵ
Fig. 7 Relationship between surface charge density of Fe3O4 with addition of PEG and pH value
2.4 �������Fe3O4���滯ѧ���Ե�Ӱ��
��������һ�ֺ����ǻ��Ķ�Ԫ����,��ˮ�е�������Ȼ���������Fe3O4������,�ı�Fe3O4�������ܡ�ͼ8��ʾΪ�����������Fe3O4���ӵ�Zeta��λ��pHֵ�Ĺ�ϵ���ߡ�
��ͼ8�ɼ�,������ļ������Ըı���Fe3O4�ĵȵ��,����pH=2.6����;�ںܴ��pHֵ��Χ��,Fe3O4��������ɡ���Fe3O4������ܶ���pHֵ�ı仯����(ͼ9)�ɼ�,����������Fe3O4��������pHֵ����;��pH>4.0ʱ,�������ܶȾ���ֵ������KNO3��ϵ�е�ֵ����Ϊ��������ˮ�е���,���������������,������Fe3O4����,ʹFe3O4���������,����pHֵ������,������������ĵ���,����������,ʹpH>4.0ʱ,������ܶȾ���ֵ������KNO3��ϵ�е�ֵ��
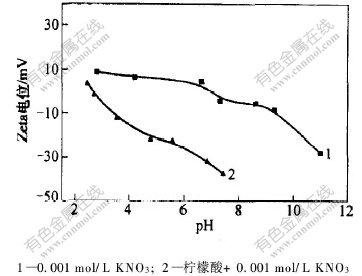
ͼ 8 �����������Fe3O4���ӵĦƵ�λ��pHֵ�Ĺ�ϵ
Fig. 8 Relationship between �� potential of Fe3O4with addition of citric acid and pH value
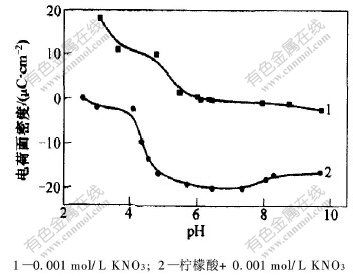
ͼ 9 �����������Fe3O4������ܶ���pHֵ�Ĺ�ϵ
Fig. 9 Relationship between surface charge density of Fe3O4 with addition of citric acid and pH value
2.5 ��ɢ����Fe3O4��ɢ���ܵ�Ӱ��
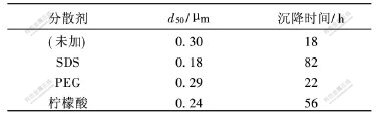
���Ʊ�Fe3O4�����зֱ����PEG,SDS��������3�ַ�ɢ��,���Բ�Ʒ�������ͳ�������,��������1��
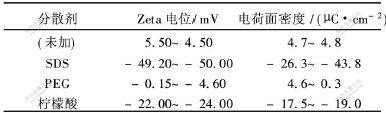
�ӱ�1�ɿ���,�����ɢ����,������С,����ʱ���ӳ�,��SDS����ɢ������Fe3O4��������С����Fe3O4�Ʊ�������,����pHֵΪ5.2~5.8,����ͼ2~9�Ľ����pHֵΪ5.2~5.8��Zeta��λ�͵�����ܶȵ�ֵ���ڱ�2�С��ɱ�2��֪,pHֵΪ5.2~5.8ʱ,��SDS����ɢ��,Fe3O4��Zeta��λ�͵�����ܶȵľ���ֵ���;Zeta��λ�͵�����ܶȼ�С��˳������������ɢ���ܱ���˳��һ��,˵��Zeta��λ�͵�����ܶ�Խ��,��ɢ�ȶ���Խǿ,����ԽС����Zeta��λ�ͱ������ܶ��ܱ�����ɢ����ɢ���ܡ�
�� 1 ��ɢ����Fe3O4��ɢ���ܵ�Ӱ��
Table 1 Effects of dispersants on dispersing property of Fe3O4
�� 2 ��ɢ����Zeta��λ�͵�����ܶȵ�Ӱ��
Table 2 Effects of dispersants on Zeta potential and surface charge density
3 �� ��
a. Zeta��λ�͵�����ܶ��DZ�����ɢ����ɢ���ܵ�һ����Ч������
b. Fe3O4�ĵȵ��Ϊ6.4~6.8,��pH��6.4ʱ,����������,��pH>6.8ʱ,���������硣ʮ����������ƺ�������ͨ��������������ʹFe3O4�ı������������ı仯,�ȵ�����������Է����ƶ���PEG�����Ѽ�����ԭ�ӡ�O����Fe3O4�γ���λ���ṩһ��λ�����,�Ӷ�����Fe3O4�����Zeta��λ�͵�����ܶȡ�
c. ��ʮ���������������ɢ������Fe3O4��������С,��Zeta��λ�͵�����ܶȵľ���ֵ���
�����:
[1]��ϲ��,������. �����������ϵ��Ʊ�[J].Ϳ�Ϲ�ҵ,2001,21(3):21-24.
YANG Xi-yun, GONG Zhu-qing. Preparation of Iron Oxide Black Pigment[J]. Paint & Coatings Industry,2001,21(3):21-24.
[2]�λ���,ׯ��,���½�. Fe3O4 �������ı������[J].��ѧ�о�,2003,14(1):11-15.
REN Huan-yu,ZHUANG Hong,LIU Yong-jian. Surface Modification of Fe3O4 Nanoparticles[J]. Chemical Research,2003,14(1):11-15.
[3]������,��ƼƼ, ����ɭ,��. ������״Fe3O4 �������ӵ��Ʊ�[J].������ѧѧ��,1990,6(1):88-90.
CHENG Long-wu,ZHANG Ping-ping,JIANG Ji-sen, et al. Preparation of Uniform Spherical Magnetite Particles[J]. Acta Physico-Chimica Sinica, 1990, 6(1): 88-90.
[4]�α���,��ҫ��,������,��. ��Fe3O4 �������ӵ��Ʊ�[J].����ұ��,1995,16(2):165-166.
SONG Bao-zhen,GAN Yao-kun,LIU Jing-ling, et al. Manufacture of Ultrafine Magnetite Colloidal Particles[J].Engineering Chemistry & Metallurgy, 1995,16(2):165-166.
[5]����ҵ,���ʾ�,ʩչ,��. Ӱ��Fe3O4 �������������ص��о�[J].�ߵ�ѧУ��ѧѧ��,1991,12(5):684-685.
KANG Hong-ye, WANG Yun-jun, Shi Zhan, et al. A Study on Factors Affecting the Properties of Fe3O4 Ultrafine Particles[J]. Chemical Journal of Chinese University, 1991,12(5): 684-685.
[6]ULRICH M. Manufacture of Toner-grade Magnetite by Precipitation and In-situ Oxidation[P].Germany: EP1048619, 2000-11-02.
[7]DIAMANDESCU C L, TARBASANU D E,BARB D, et al. Production of Ultrafine Magnetite Powder[P]. Romania: RO111444, 1996-10-31.
[8]JIWON L, TERSUHIKO I, MAMIRU S. Preparation of Ultrafine Fe3O4 Precipitation in the Presence of PVA at High pH[J]. Journal of Colloid and Interface Science, 1996, 177: 490-494.
[9]OSCAR P P, YOSHIAKI U, HIROSHI S. Electrokinetic Characteristic of Magnetite Produced at Ambient Temperature[J]. Shigen to Sozai, 2000, 116(4): 297-301.
[10]SYED M S. Studies of the Dissociation of Oxide Surfaces at the Liquid-Solid Interface[J]. Canadian Journal of Chemistry, 1966, 44: 1663-1670.
[11]�̺���, ������, ������, ��. ����Fe3O4�ĦƵ�λ�ͷ�ɢ�ȶ���[J]. �人������ѧѧ��,2003,25(5):4-7.
CHENG Hai-bin, LIU Gui-zhen, LI Li-chun, et al. �� Potential and Stability of Fe3O4 Nanoparticles[J]. Journal of Wuhan University of Technology, 2003, 25(5): 4-7.
[12]PLAZA R C, ARIAS J L, ESPIN M, et al. Aging Effect in the Electrokinetics of Colloids Iron Oxides[J]. Journal of Colloid and Interface Science, 2002, 245: 86-90.
[13]AHEMD S M, MAKSIMO D. Studies of the Oxide Surface at the Liquid-Solid Interface Part�� Fe Oxides[J]. Canadian Journal of Chemistry, 1968, 46: 3842-3850.
[14]����÷,¬����. ���Ҷ���-Fe3O4���ӵ��Ʊ�[J].��ѧ�о���Ӧ��,2002,14(5):563-565.
WEN Yan-mei, LU Ze-qin. Studies on the Preparation of Fe3O4 Parceliked PEG[J]. Chemical Research and Application, 2002,14(5): 563-565.
�ո�����:2004-06-12
�����:��ϲ��(1974-),Ů,�����۶���,��ʦ,��ʿ�о���,���¹��ܲ����о�
������ϵ��: ��ϲ��,Ů,��ʿ�о���;�绰:0731-8830752(O); E-mail:yxy7412@mail.csu.edu.cn