���±�ţ�1004-0609(2008)S1-0422-06
��TiCl4ͭ˿��������ˮ�����ཬ�ۺϻ��չ���
��ѧ��1������Ƽ1��Ф����1���Ź���1��Ԭ��ά2�����˳�2
(1. ���ϴ�ѧ ұ���ѧ�빤��ѧԺ����ɳ410083��
2. ������ҵ�ɷ�����˾������563004)
ժ Ҫ��������һ�ִ�TiCl4ͭ˿��������ˮ�����ཬ�ۺϻ����¹��ա��ù����ɳ����ཬ����������ϴ���ȡ�������һ�������������ͭ��һ��������մ����ᷰ���ᷰ���������5����Ҫ������ɡ�ʵ������������TiCl4ͭ˿��������ˮ�����ཬ�ڿ��������������������ཬ�ڿ����жѷ�1���£��ӽ�90%�Ľ���ͭ���CuCl2��2H2O��Cu2Cl(OH)3��Cu2(OH)3Cl����Щͭ�������������ڼ�����Һ������ת����Cu(OH)2���ڿ���Һ�̱�4?1��pHֵΪ 11���¶�Ϊ80 ��������½���1 h��ת���ʴ�96%�������Һ��pHֵΪ2.0~2.5ʱ��Fe��V��Ti�������������У�����Һ����Ũ�����ܶ�Ϊ1.38 g/cm3����ȴ�ᾧ�õ�������ͭ��Ʒ���Ϲ���GB437��93������Ҫ�����������ѧ������2.5�����մ����700 �決��3 h�����պ�Һ�̱�3?1��ˮ��70 �����1 h������ˮ��Һ����ѧ������3�����Ȼ�麟���ƫ����泥�ƫ�������550 ���Ƚ�2 h�õ�����Ϊ98.61%��V2O5���ᷰ���پ�����������������չ���ͭ�ͷ����ܻ����ʷֱ�ﵽ98.63%��95.65%��
�ؼ��ʣ���TiCl4���ƣ�ͭ˿���������ۺϻ���
��ͼ����ţ�TQ 134.1; TF 841 ���ױ�ʶ�룺A
Comprehensive recovery of precipitate of wastewater in removing vanadium from raw TiCl4 with copper-wire
WANG Xue-wen1, ZHANG Li-ping1, XIAO Lian-sheng1, ZHANG Gui-qing1, YUAN Ji-wei2, GONG Shi-cheng2
(1. School of Metallurgical Science and Engineering, Central South University, Changsha 410083, China;
2. Zunyi Titanium Industry Co. Ltd, Zunyi 563004, China)
Abstract: A new method was presented to recover copper and vanadium from the precipitate formed in the waste water after vanadium removal from raw TiCl4 with copper-wire. The recovery process consists of five major procedures, namely, the self-oxidization of precipitate, the removal of chlorine with sodium hydroxide solution, the first-stage leaching of copper with sulphuric acid and recovering vanadium by roasting the first leached residue with sodium carbonate, the leaching with water and the leaching copper with sulphuric acid once again. It is found that the precipitate can self-oxidize in air. After stacking for one month in air, about 90% metallic copper contained in the precipitate turns into CuCl2��2H2O, Cu2Cl(OH)3 and Cu2(OH)3Cl. The copper oxychlorides can easily convert to Cu(OH)2, and the conversion rate is over 96% under liquid-to-solid ratio 4?1 and pH 11 at 80 �� by stirring for 1 h. When pH value is maintained in the range of 2.0-2.5 during the leaching of sulfuric acid, the impurities of Fe, Ti and V are remained in the leached residue. And then the leaching liquor is concentrated to 1.38 g/cm3 by evaporation and cooled to obtain the product of CuSO4��5H2O, which is in accordance with the standard of GB437��93. After adding sodium carbonate under the stoichiometric proportion of 2.5 the residue is roasted at 700 �� for 3 h. The calcined product is leached with water under liquid-to-solid ratio 3?1 at 70 �� by stirring for 1 h. NH4Cl is then added in the leaching liquor containing vanadium according to the stoichiometric proportion of 3 to obtain the precipitate of NH4VO3. When NH4VO3 is thermolysized at 550 ��for 2 h, V2O5 with the purity grade of 98.61% is produced. After vanadium removal, the residue is leached once again with sulfuric acid. The total recoveries of copper and vanadium are 98.63% and 95.65%, respectively.
Key words: raw TiCl4 purifying; copper wire; vanadium removal; comprehensive recovery
TiCl4����ұ���һ����Ҫ�м��Ʒ����Ҫ���ں����Ѻ��Ѱ�����[1-2]����ҵ�϶���ý��ʯ���������̼�Ȼ���ȡTiCl4�����ַ����õ��Ĵ�TiCl4����FeCl3��AlCl3��TiOCl2��SiCl4��VOCl3��Cl2��HCl��VCl4������[3]����TiCl4����ͨ�������ᴿ�������ں����Ѻ��Ѱ�����������ɽ���TiCl4�е�SiCl4��Cl2��HCl�ȵͷе����ʳ�ȥ�������ܷ���FeCl3��TiOCl2�ȸ߷е����ʣ���VOCl3��TiCl4������ѹ�ӽ���ֻ�ܲ��û�ѧ�������ѳ�[4]�����õij��������У�������������л�������������۳�������ͭ˿�����������������Ч���ã���ԭ���۸���ˣ������ɱ��ͣ������սϸ��ӣ����������ж����壬�Ͷ�������ҹ���ҵ��δ���á��л������Ч���ã����̼������ɱ��ͣ��������ȴ��������մ������ѣ����ַ���Ŀǰ���ҹ����������ýΡ����۳���Ч���ã����̼������ɱ��ͣ��������������Ƚ����ѣ����Գ��������γɵ�AlCl3���벻�����Բ�Ʒ������Ӱ�졣ͭ˿����Ч���ã����̽ϼ���Ʒ�����ȶ�����Ҫ���Ĵ����۸�ߵ�ͭ������ϴͭ˿�γɵķ�ˮ�Ի�������Ⱦ���Ͷ�ǿ�ȴ�ͭ˿�������ҹ��� �е�һ�ֳ������������ձ�Ӧ�����ҹ�TiCl4������ҵ[5-6]��
�ڳ���������ͭ˿�μӻ�ԭ��Ӧ�������ģ��γ�VOCl2��CuCl������ͭ˿�����ʹ��һ��ʱ���ͭ˿�Ļ��Ա����С�����������½�����ʱΪ��ȷ��TiCl4�з����������꣬������ˮ��ϴͭ˿����ij������Իָ��仹ԭ����[7]����ϴͭ˿���õ��ķ�ˮpHֵΪ1.0~2.0��TiCl4������ҵһ�����Ƚ����ַ�ˮ�ռ��ڵؿ��м���м�û���Ȼ���������ؿ��еij����ཬ���ռ��õ��ij����ཬͨ�����û�-ʪ�����Ϲ��ջ������е�ͭ�����м۽�������ɢ��������¯���������ա������ཬ�к��д����Ȼ���ڻ����������Ȼ�������ӷ�������صĻ�����Ⱦ����ˣ�����������Դ�TiCl4ͭ˿��������ˮ�����ཬ�������մ��ڵ����⣬�����������ཬ����������ͭ�����롪�ۺϻ��յĴ����¹��գ�������������Ȼ�������ӷ��Ի�����ɵ���Ⱦ�������ཬ�е�ͭ�ͷ����õ�����Ч���գ����й��ռ��������㡢���������ʸߡ������ɱ��͡������Ѻõ��ŵ㡣
1 ʵ��
1.1 ʵ��ԭ��
ʵ��ԭ��Ϊ�����ѳ���TiCl4ͭ˿��������ˮ����м�û��õ��ij����ཬ���ཬ������ɫ�����к��д�����м�û�������ͭ�����ͭ˿�������ཬ�ѷ��ڿ����������ɫ���ɷ�״�����Ҫ��ѧ�ɷ����1��ʾ��
��1 �����ཬ��������Ļ�ѧ�ɷ�
Table 1 Chemical compositions of precipitate after self- oxidization (mass fraction, %)

1.2 ʵ���������Լ�
��Ҫ���������ͷ���Ƚ�����(CJJ-931����̳�о���ʵ��������)��ԭ�����չ�����(AAnalyst100������)��pH��(Orion Model 410A������)��
�Լ����������ơ�̼���ơ��Ȼ�李����ᣬ��Ϊ��������
1.3 ʵ�鷽��
�����ཬ������ͼ1��ʾ�Ĺ��մ��������ؿ����ͳ����ཬ��Ȼ���ɺѷ��ڿ����У�������Ȼ�������������ɫ��״�����NaOH������ҺpHֵ����11���ȣ����Ƚ��衣����Һ�����к���м�û�Һ������������ѧ����1.0~1.2����ϡ������70 �����1 h��ͭ����ͭҺŨ�����ܶ�Ϊ1.38 g/cm3����ȴ�ᾧ�õ�����ͭ���塣����ͭ�ᾧĸҺ������м�û��������������ѧ������2.5�����մ��գ������ϰ�Һ�̱�3?1ˮ���ᷰ��ˮ��Һ����ѧ������3�����Ȼ�麟���ƫ����泥�ˮ���������ٻ���ͭ��

ͼ1 �����ཬ�ۺϻ��չ�������ͼ
Fig.1 Flowsheet of vanadium and copper recovery from precipitate
1.4 ��������
ʵ����Ʒ�з������IJⶨ���÷����ı���������������������淋ζ�����ͭ�����ķ�����ԭ�����շֹ��ȷ���������Ũ�Ȳ�����������Һ�ζ�������Һ��pHֵ��pH�Ʋⶨ��
2 ���������
2.1 �����ཬ������
�����ཬ��Ȼ���ɺ�ѷ��ں���Լ35 m�����ʪ��Ϊ50%~80%��ƽ������Ϊ15 ��Ŀ����У�1���º�����γɴ�����ɫ���ɵķ�״�ͼ2��ʾ�Ƿ�״���X��������ķ����������ͼ2���Կ��������ַ�״�����Ҫ�ɷ���CuCl2��2H2O��Cu2Cl(OH)3��Cu2(OH)3Cl��Ȼ������Ȼ��1�У�Ti�����ӽ�7%����X�����������δ�����ѵ����࣬��˵��Ti(OH)2Cl2��TiO(OH)2�������ͽṹ��
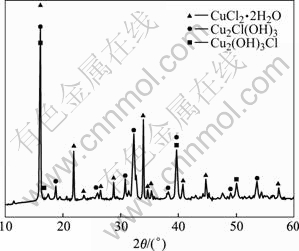
ͼ2 �����ཬ��������XRD��
Fig. 2 XRD pattern of precipitate after self-oxidization
�ɱ�1���Կ����������ཬ�к��д�����Ti(OH)2Cl2����ͭ˿����ij�������ˮ��ϴʱ�����в�����TiCl4ˮ������Ti(OH)2Cl2������[6]��CuCl�绯��Cu��CuCl2��������м�û��Ľ��У���ˮ��pHֵ���ͣ�Ti(OH)2Cl2��һ��ˮ�����ˮ����Ti(OH)3Cl��TiOCl2���ڳ�ʪ�Ŀ����У�����Cl-���ӵIJ��룬�������ཬ��Cu�����������̡�

������CuCl2��2H2O����Cu2Cl(OH)3��Cu2(OH)3- Cl��������Һ�ж��ǿ��ܵģ���ˣ�ͭ�Ľ�����ֱ�ӷ�ӳ�ཬ���������̶ȡ�ͼ3��ʾ�dz����ཬ��ͭ�Ľ���������������ʱ��Ĺ�ϵ����ͼ3���Կ����������ཬ�ӵؿ����ͳ��������ڿ����жѷ�ʱ����ӳ���ͭ�Ľ�����Ѹ�����ߡ����ѷ�ʱ��ﵽ1��������ʱ��ͭ�Ľ����ʴ�90%�������ӳ������ཬ�ڿ����жѷ�ʱ�䣬ͭ�Ľ����ʱ仯��������Ҫ��CuCl2��2H2O��Cu2Cl(OH)3��Cu2(OH)3Cl�Ĵ����γɣ��谭���ཬ��δ�������Ľ���ͭ������е�������ˮ�ֽӴ���ʵ�鷢�֣������ཬ�ڿ����жѷ�1���º���������������������TiCl4ͭ˿��������ˮ�н��ݺ����ɣ����еĽ���ͭ�ڿ������������ٶ�Ҳ����������������в���Ľ���ͭ��TiO(OH)2��Fe2O3�Ȱ�����

ͼ3 �����ཬ������ʱ����ͭ�Ľ����ʵĹ�ϵ
Fig.3 Relationship between self-oxidization time of precipitate and copper leaching rate
2.2 �������ཬ��ϴ����
��1��ʾ�������ཬ�к��д�����Cl��ֱ��������������ͭ��ԭ�ϣ������Բ�Ʒ������Ӱ�죬���һ���������豸���ظ�ʴ����ˣ��ڳ����ཬ��������Ҫ�����ȡ��ѳ�CuCl2��2H2O��Cu2Cl(OH)3��Cu2(OH)3Cl�е��ȵ����㷽���Ǽ�ϴ��

��������ij����ཬ������NaOH��Һ�н��С�ʵ���������������ཬ��ϴ������Ҫ��Һ�̱ȵ�Ӱ�졣��80 �����1 h����ҺpHֵΪ11����ϴ����Һ�̱����������ཬ����Ч���Ĺ�ϵ��ͼ4��ʾ������Һ�̱������ȵ��ѳ���Ѹ�����ߣ���Һ�̱�����4ʱ���ȵ��ѳ����ѽӽ�97%����������Һ�̱ȣ��ȵ��ѳ��ʱ仯������ˣ������ཬ��ϴ���ȵ���ѹ���������ȷ��Ϊ��Һ�̱�Ϊ4?1��pHֵΪ11����80 �����1 h��

ͼ4 Һ�̱�������Ч�ʵĹ�ϵ
Fig.4 Relationship between liquid-to-solid ratio and dechlorination rate
�����ཬ����Һ�����к���м�û���Һ��Ŀ���ǣ������û�����Һ��pHֵ����СV(IV)����Һ�е��ܽ�ȣ�����м۽������Ļ����ʡ�
2.3 ͭ�뷰���ۺϻ���
���������ᷰ������Һ�̱�4?1����ˮ�����ᣬ80 �����1.5 h����ͭ��pHֵ��������ͭ�����ʵ�Ӱ����ͼ5��ʾ��ͼ5��ʾ�������Һ��pHֵ��ͭ�Ľ�����Ӱ��ܴ�������ҺpHֵ�Ľ��ͣ�ͭ�Ľ��������ߡ�����ҺpHֵ����2.5ʱ��ͭ�Ľ�����������88%������������Һ����ȣ�ͭ�Ľ���������������������Ϊ����ҺpHֵΪ2.5ʱ���������д�ͭ����������Ti��Fe�������������У���Щ���ʶ�ͭ�Ľ������谭����[7-8]��Ҫ��һ�����ͭ�Ľ����ʾ͵�������Һ����ȣ��Ӷ����V��Fe���ܽ⣬�ⲻ��Ӱ������ͭ��Ʒ�����������Ҳ����ڷ��Ļ��ա���ˣ�������ͭ����Һ��pHֵ������2.0~2.5��Ϊ���ˡ�����ͭ����Һ�ϸ�pHֵ����һ��ԭ���ǣ�һ��������ᷰ��Ҫ���ж������(��ͼ1)�����������Һ�������������20~40 g/L H2SO4ʱ�������������Cu��V�ĺ����ֱ�ɽ���0.5%��0.3%����[9-12]�����������Һ��������ͭ��һ�����Һ����pHֵ������2.0~2.5ʱ��Cu������Һ�У�V����ͭ�����������ʽ����һ��������С��������չ���ͭ���ܻ����ʴ�98.61%�������ܻ�����Ϊ95.65%��
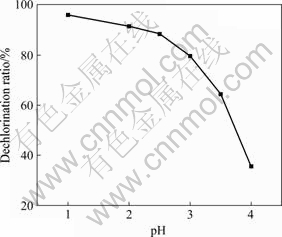
ͼ5 pHֵ��ͭ�����ʵ�Ӱ��
Fig. 5 Effect of pH value on copper leaching rate
������������ͭ��Һ�̱�4?1����ˮ�����ᣬ��80 �������ҺpHֵΪ2.5���������1.5 h������ҺŨ�����ܶ�Ϊ1.38 g/cm3��ȴ�ᾧ�Ʊ�����ͭ��ʵ�������2��ʾ���ӱ�2���Կ����������ཬ���������յõ�������ͭ��Ʒ�����ﵽ���ұ�GB437��93��
��2 ����������ͭ��ʵ����
Table 2 Experimental results of copper recovery
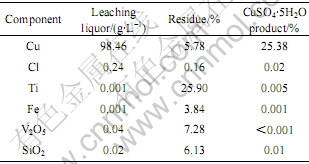
�ɱ�2���Կ����������ཬ������������ϴ���ȡ����������������С���ȡ������еķ��� �ɲ����Ȼ��Ʊ���-ˮ����Ҳ�ɲ���̼���Ʊ���-ˮ��[13-16]�������Ȼ��Ʊ��ղ���HCl���к����壬ʵ��ѡ��̼���Ʊ���-ˮ�����ջ���������еķ�����������а���ѧ������2.5�����մ���700 �決��3 h�������ϰ�Һ�̱�3?1��ˮ��70 �����1 h��ˮ��Һ�ٰ���ѧ������3�����Ȼ�麟���ƫ����泥�ƫ�������550 ���Ƚ�2 h��ʵ�������3��ʾ����3��ʾ��ʵ��õ���V2O5�������ﵽGB3283��87����
��3 ������ᷰʵ����
Table 3 Experimental result of vanadium recovery

3 ����
1) ��TiCl4��������ˮ�����ཬ�ڿ����жѷ�1���£�����Ҫ�������գ����еĽ���ͭ�ӽ�90%ת���CuCl2��2H2O��Cu2Cl(OH)3��Cu2(OH)3Cl�������ཬ�ڿ������������Ƚ��ܸ�Ч��������
2) �����ཬ����������Һ�̱�Ϊ4?1��pH ֵΪ11�ļ�����Һ����80 �����1 h���ɽ����е�����������ת����Cu(OH)2����Cu(OH)2���������� ��Һ�̱�4?1��������Һ�н�����������ƽ����յ�pH ֵΪ2.0~2.5������ҺŨ���ᾧ�ɵõ����Ϲ��� GB437��93����Ҫ�������ͭ��Ʒ��
3) �����ཬ��������մ��պ�ɰˮ��������Һ���Ȼ�麟���ƫ����泥�ƫ������پ��Ƚ��ܵõ�������98.5%���ϵ�V2O5��Ʒ����TiCl4ͭ˿��������ˮ�����ཬ����������������ϴ���ȡ��������ͭ���մ����ᷰ�����е�ͭ�ͷ����õ���Ч���ա�
REFERENCES
[1] ����, �ָ���, �� ��, �� ��, ���Ʒ�. 2006���й��ѹ�ҵ��չ����[J]. �ѹ�ҵ��չ, 2007, 23(2): 1-5.
WANG Xiang-dong, LU Fu-sheng, JIA Hong, HAO Bing, MA Yun-feng. Development report on titanium industry in 2006[J]. Titanium Industry Progress, 2007, 23(2): 1-5.
[2] �� ��, �� ��. �����⺣��������������״[J]. �ѹ�ҵ��չ, 2006(2): 7-14.
ZHANG Jian, WU Xian. Development of process of sponge titanium[J]. Titanium Industry Progress, 2006(2): 7-14.
[3] Ī δ, �˹���, ����. ��ұ��[M]. ��2��. ����: ұ��ҵ������, 1998: 248-266.
MO Wei, DENG Guo-zhu, LUO Fang-cheng. Titanium metallurgy[M]. 2nd ed. Beijing: Metallurgical Industry Press, 1998: 248-266.
[4] ���Ǿ�, �ﻢ��, ��ΰ��. �����Ȼ��ѳ���������״����չ����[J]. �ִ�����, 2007, 27(6): 24-26.
LI Ya-jun, SUN Hu-min, XU Wei-chun. Status of process for removing vanadium from tetrachloride titanium and its development trends[J]. Modern Chemical Industry, 2007, 27(6): 24-26.
[5] XU Cong. Preparation of TiCl4 with the titanium slag containing magnesia and calcia in a combined bed[J]. Chinese J Chem Eng, 2006, 14(3): 281-288.
[6] �Ԫ. �ҹ����Ȼ��ѵ�ͭ˿��������[J]. �ѹ�ҵ��չ, 2000(4): 12-14.
LI Ding-yuan. Process of removal vanadium from raw titanium tetrachloride with copper wire in China[J]. Development for Titanium Industry, 2000(4): 12-14.
[7] �� ͮ, �� ��, �� ��. ����������Ȼ����������������ͭ������[J]. �й���ɫ����ѧ��, 2001, 11(2): 302-306.
DENG Tong, WEN Zhen, LIU Dong. Leaching of copper residue with oxygen in sulfuric acid with participation of chloride[J]. The Chinese Journal of Nonferrous Metals, 2001, 11(2): 302-306.
[8] OWUSU G. Selective extraction of copper from acidic zinc sulfate leach solution using LIX622[J]. Hydrometallurgy, 1999, 51(1): 1-8.
[9] �� ΰ, ������. �ӻ��ͭ��������Һ�г�ȥCa��Fe�ᾧ�Ʊ�CuSO4��5H2O�����о�[J]. ʪ��ұ��, 2000, 29(l): 16-20.
YAN Wei, CAI Wang-ling. Study on removing Fe and Ca and crystallizing CuSO4��5H2O from leaching solution of mixed copper ore with mixed acid[J]. Hydrometallurgy of China, 2000, 29(l): 16-20.
[10] ������. ��ͭ������ͭ�Ļ��ռ�������������[J]. ��������, 2001(6): 248-249.
LIU Cheng-xian. Recovery of copper from copper-containing sludge and innocent treatment of sludge[J]. Liaoning Chemical Industry, 2001(6): 248-249.
[11] ������, �� ��, ����ƽ. �õ�Ʒλͭ��ʯ����Һ�Ʊ�����ͭ��Һ[J]. ʪ��ұ��, 2006, 25(3): 141-144.
ZENG Qing-yun, YANG Dan, LIU Yong-ping. Preparation of copper sulfate solution using leaching solution of low grade copper ore[J]. Hydrometallurgy of China, 2006, 25(3): 141-144.
[12] �� ҫ. ���÷�ͭ����������ͭ�������м۽������о�[J]. ��ɫұ��, 1999, 28(4): 38-39.
HE Yao. Producing copper sulfate and recovering valuable metals from waste copper slag[J]. Non-Ferrous Smelting, 1999, 28(4): 38-39.
[13] ������, ���۾�, ʷ�ĸ�, ������, ������, �� ��. ʪ��ұ���ᷰ�����¹���[J]. �й���ҵ, 2006, 15(7): 64-66.
LIANG Jian-long, LIU Hui-juan, SHI Wen-ge, HU E-ming, LI Xi-qi, PENG Jun. A study of a new technology leaching of vanadium from vanadium ores with hydrometallurgy[J]. China Mining Magazine, 2006, 15(7): 64-66.
[14] �� Ƽ, ��𥻪. ������Ϊ�������Ӽ���ʯú��ȡ����������[J]. ϡ�н���, 2000, 24(2): 115-118.
ZHANG Ping, JIANG Fu-hua. Extraction of vanadium pentoxide from stone coal by using causticizing mud as roasting additive[J]. Chinese Journal of Rare Metals, 2000, 24(2): 115-118.
[15] LOZANO L J, JUAN D. Leaching of vanadium from spent sulphuric acid catalysts[J]. Minerals Engineering, 2001, 14(5): 543-546.
[16] ������, ����ͨ. HDSʧ����������ᷰ�Ķ���ѧ[J]. �й���ɫ����ѧ��, 2002 , 12(5): 1065-1068.
LIU Gong-zhao, SUI Zhi-tong. Kinetics of extracting vanadium from HDS spent catalyst by alkali leaching[J]. The Chinese Journal of Nonferrous Metals, 2002, 12(5): 1065-1068.
ͨѶ���ߣ�����Ƽ��˶ʿ�о������绰��0731-8830143��E-mail: zhangliping0123@126.com
(�༭ �� ��)