���±�ţ�1004-0609(2008)01-0151-08
Mycobacterium Phlei�ڻ�����ͷ�Ǧ������
ѡ�����������û���
�ִ��ƣ�κ���ޣ����Ұأ����ĸգ�����꣬������
(������ѧ ��Դ����ľ����ѧԺ������ 110004)
ժ Ҫ�������������ⶨ����-��λ�о����������X���߹������������̽��Mycobacterium Phlei�ڻ�����ͷ�Ǧ������ѡ�����������û��������������������ʵ�������̶�������£�����Һ�ij�ʼpHֵ����5ʱ��Mycobacterium Phlei�ڻ���������������ԶԶ���ڷ�Ǧ�������ò�����ʹMycobacterium Phlei�ڻ�����ͷ�Ǧ��������ѡ������������Ҫ��������Mycobacterium Phleiϸ�������C��N��OԪ��ͨ����������Fe��Pb��SԪ���������淢���˻�ѧ��������������������Ԫ�ص����ó̶ȴ��ڷ�Ǧ����ı���ṹ�������ʡ�ϸ�����������������������ӵļ������ô�С��������ʹMycobacterium Phlei����ѡ������������Ҫ ԭ��
�ؼ��ʣ�Mycobacterium Phlei��������Ǧ��ѡ�����������û�������-��λ������
��ͼ����ţ�TD 925.5���� ���ױ�ʶ�룺A
Mechanism of selective adsorption of Mycobacterium Phlei on pyrite and galena surface
JIA Chun-yun, WEI De-zhou, SHEN Yan-bai, LIU Wen-gang, DAI Shu-juan, GAO Shu-ling
(School of Resource and Civil Engineering, Northeastern University, Shenyang 110004, China)
Abstract: By means of adsorption rate measurement, zeta-potential, infrared spectroscopy and X-ray photoelectron spectroscopy, the mechanism of selective adsorption of Mycobacterium Phlei on the surfaces of pyrite and galena was studied. The results show that Mycobacterium Phlei adsorbs preferentially on pyrite than on galena when pH is over 5 and other parameters are fixed, which is also observed by scanning electron microscopy. Static force is not the main function to make Mycobacterium Phlei has an obvious selective adsorption on the surfaces of pyrite and galena from the zeta potential. IR and XPS results indicate that chemical adsorption occurred on the surfaces of two minerals by Fe, Pb and S, and the reaction degree of elements C, N and O on the surface of Mycobacterium Phlei to surface elements of pyrite is larger than that of galena. It is concluded that the crystal frame and surface property of two minerals and the linking between groups on the surface of Mycobacterium Phlei and metal ions on the surface of two minerals are main factors that cause the selective adsorption of Mycobacterium Phlei.
Key words: Mycobacterium Phlei; pyrite; galena; selective adsorption mechanism; zeta-potential; spectroscopy
�������������\���븡ѡ������Ч��϶����������︡ѡ������Ϊ�����о���һ���ȵ㡣���︡ѡ���̾��ǽ�������Ϊҩ���������ռ����������ʹ����ѡ���Է�ѡ�Ĺ���[1]������Ҫ��Ϊѡ��ҩ��ʹ�ã����ڿ���������������ﵽһ�����������ܵ����ı����ı������ʣ�����ʵ�����ֻ���ֿ���֮��ķ��롣����������������Ļ���������Ҳ��������������õĵ�һ����������ұ��Ļ����о��У�Ŀǰ��ɹ�ʶ���������ڿ�����������������������������������õ�ǰ��[2?3]��
������������о��У��о��ߴ��ѡ��һЩ���Ա��۵�������ѧ������ΪӰ�������о�����������̵�Ӱ�죬���Ũ�ȡ��������ȡ��¶ȡ�pHֵ���ж�Ԫ�ص�Ũ�ȵȵȣ���Щ���ض�������������Ч��������ͬ��Ӱ��[4?8]���������о��˰���������ϸ�������е�����[9]���ѽ��е�һЩ����ѡ�����������о���������Ҫ��ͨ������������������Ŀ�ĵ�ǿ��ѡ�����������Է���ѡ���������Ļ���ֻ�����˳�������[10]������������������������������ѡ������������ͨ��һЩ����ֶ�����̽���������ڿ�������ѡ�����������û�����Ϊ����ѡ��ҩ���Ŀ����ṩ�������ݡ�
1 ʵ��
1.1 ����
ʵ���þ���ΪMycobacterium Phlei������ΪAS.4.1180�����й���ѧԺ�����о������ֱ��������ṩ��
ʵ���ÿ���Ϊ������ͷ�Ǧ��ȡ������ʡ�˼���Ǧп��ѧ�ɷ�Ϊ����������45.91%������49.42%����Ǧ��Ǧ85.28%������14.19%����������������ֿ����Ĵ��Ⱥܸߡ����ֿ���ֱ����顪ɸ�֡�ҡ����ѡ��ĥ����Ȼ���ɺ�ȡС��0.074 mm�Ŀ�����������ʵ���о���
1.2 Mycobacterium Phlei������
Mycobacterium Phlei���������䷽Ϊ���Ȼ���5 g��������10 g��ţ���3 g������ˮ1 L��pH 7.0~7.2���������������������CBV?1000A����ྻ̨�Ͻ��ֺ���HZQ?C��������������(28 �棬150 r/min)����6 d��
1.3 Mycobacterium Phlei����Һ���Ʊ�
ȡ����6 d��Mycobacterium Phlei����Һ��TGL?16G���ķ��������16 000 r/minת���·���10 min������õ�Mycobacterium Phleiʪ����������ɢ��һ�����������ˮ�У�Ȼ�����85?2�ͺ��´������Ƚ�����ϳ�ֽ��裬ʹϸ�����ȷ�ɢ�����Ա�ʵ���á�
1.4 �����ʵIJⶨ����
ȡŨ��һ����Mycobacterium Phleiϸ������Һ50 mL�����ݻ�Ϊ100 mL���ձ��У�����pHֵ��Ȼ����붨���Ŀ���̶�����ʵ���������ں��´����������Ͻ��н��裬��ʹϸ���Ϳ������Ӵ�������������Ȼ��������ˮ��Ϊ�α���Һ���ⶨ����ǰ��Mycobacterium Phlei����Һ�������ֵ�����ӱ������ϲ�ö�Ӧ��ϸ������ҺŨ�ȣ�ͨ������Ĺ�ʽ���������ʣ�

ϸ������Һ�������ֵ��Ũ�ȹ�ϵ�ı�������ͼ1��ʾ��
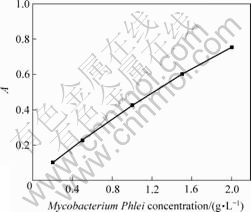
ͼ1 Mycobacterium Phleiϸ������Һ�������ֵ��Ũ�ȵĹ�ϵ
Fig.1 Relationship between absorbency A and concentration of Mycobacterium Phlei
1.5 ������ⷽ��
��-��λ�IJⶨ�������£���ȡ0.5 g����(��0.054 mm)��500 mL����ˮ�з�ɢ��������HCl��NaOH��ϡ��Һ����pHֵ���������pH��Χ(1.6~12)����JS94H����Ӿ�Dzⶨ�����Ħ�-��λ�������ȡ0.1 g����������500 mL����ˮ�У���ͬ���ķ����ⶨϸ���Ħ�-��λ��
��ⷽ���������£�ȡ0.5 g����(��0.054 mm)����50 mL(pH 7.63��Ũ��1.5 g/L)��ϸ������Һ�н���(400 r/min)����10 min����2 000 r/min��ת�������ķ���5 min����ȡ������ϸ���Ŀ�����Ȼ��������ˮ������ϴ3�Σ���ȥ�����������ι̵�ϸ������Mycobacterium Phlei���塢ԭ������������Mycobacterium Phlei�Ŀ�������ո���(?60 �棬12 h)����к�����ס�X���߹��������������ͬ�������£��ñ�����Ŀ�״����(1 cm��1 cm��1 cm)������ʵ�飬Ȼ�������Mycobacterium Phlei��Ŀ�������ɨ��羵�о���
2 ���������
2.1 ѡ�������������о�
2.1.1 ��Һ��ʼpHֵ������Ч����Ӱ��
�ڿ���Ũ��10 g/L��ϸ������ҺŨ��1.553 g/L������ʱ��10 min���¶�15 ���ʵ�������£��ı�������Һ��ϵ�ij�ʼpHֵ������pHֵ������Ч����Ӱ�죬�����ͼ2��ʾ��
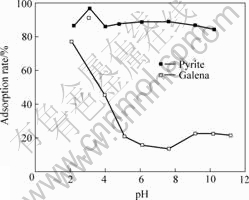
ͼ2 ��Һ��ʼpHֵ�������ʵ�Ӱ��
Fig.2 Effects of initial pH value of solution on adsorption rate
��ͼ2���Կ�������pHС��4ʱ��Mycobacterium Phlei�ڻ�����ͷ�Ǧ������������������������ѡ���ԣ�����pHΪ3.10ʱ��Mycobacterium Phlei�����������������ϵ������ʾ��������Ϊ96.75%��91.09%������ϸ������Һ��ǿ����(pH��4)ʱ��ϸ����������������Mycobacterium Phleiϸ���ۺϳɴ��Ŷ���Ȼ�³�����ʹҺ����������ϸ�������������ͣ���˼�������������ʶ��Ƚ�ƫ�ߡ�����pHֵ�����ߣ�Mycobacterium Phlei�ڻ���������ϵ������ʻ����ϱ��ֲ��䣬90%���ң����ڷ�Ǧ�����������������½�����pH����5.00ʱ��Mycobacterium Phlei�ڷ�Ǧ������������������ƽ�⣬�����ʾ���20%���ҡ��ܵĿ�������pHֵ����5.00ʱ��Mycobacterium Phlei������������������������������Ե�ѡ���ԡ�
2.1.2 ɨ�������������
ͼ3��ʾΪ��Mycobacterium Phlei���ú������ͷ�Ǧ���SEM��

ͼ3 ����Mycobacterium Phlei�Ļ�����ͷ�Ǧ���SEM��
Fig.3 SEM images of pyrite and galena after interaction with Mycobacterium Phlei: (a) Pyrite; (b) Galena
��ͼ3(a)���Կ�����Mycobacterium Phlei �ڻ��������������������Ƚ϶࣬���е���ϸ����������Ҳ����������ϸ��������������Ҫ�Ƕ��ϸ������������ͼ3(b)���Կ�����Mycobacterium Phlei �ڷ�Ǧ�������������������٣����ǵķֲ��ż���ϸ���塣��ͼ3(a)��ͼ3(b)���ԱȽϣ����Ե�֪������������ͬ������£�Mycobacterium Phlei�ڻ�����ͷ�Ǧ����淢�������Ե�ѡ���������������ڻ���������������ԶԶ���ڷ�Ǧ��
2.2 ��-�����
ͼ4��ʾΪMycobacterium Phlei�Ħ�-��λ��pH�Ĺ�ϵ��ͼ5��ʾΪ������ͷ�Ǧ��Ħ�-��λ��pH�Ĺ�ϵ��
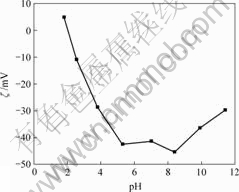
ͼ4 Mycobacterium Phlei�Ħ�-��λ
Fig.4 Zeta-potential of Mycobacterium Phlei
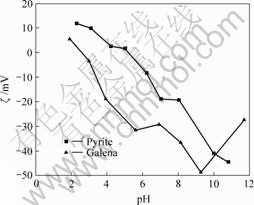
ͼ5 ������ͷ�Ǧ��Ħ�-��λ
Fig.5 Zeta-potential of pyrite and galena
��ͼ4���Կ�����Mycobacterium Phleiϸ������ĵȵ��Ϊ2.0���������ױ��������Mycobacterium Phlei��ϸ���ڴ��ﵽ����4��ṹ���ľ��Dz㡢֬���ײ㡢��Ĥ��֬���Dz�[11]�������߷������ۺϵ���ʣ���Ϊ���Ǵ��д�����ţ����ǻ����Ȼ��������ȡ������Ӻ������ӵĴ���ʹϸ���ھ������ԣ�������pH�IJ�ͬ��ϸ���ڵľ���ɿ�Ϊ����ɡ�����ɻ��㡣��ͼ4��ʾ��Mycobacterium Phleiϸ�������ںܿ���pH��Χ��(2~12)�����硣
��ͼ5���Կ�����������ͷ�Ǧ��ĵȵ������ΪpH 5.2��pH 2.6�����������б�������ֵ������ġ�����Ԥ�����ֿ�����Mycobacterium Phleiϸ��֮�侲�������õ�pH��Χ�����ڻ�������ԣ��õ�λ��Χ��pH��2.0~5.2֮�䣬�����ڷ�Ǧ����ԣ��õ�λ��Χ���խ��ΪpH��2.0~2.6֮�䡣��ˣ�ǿ����(pH��2)�����£�Mycobacterium Phleiϸ����������֮�������Ϊ�����������pH��2.0~2.6ʱ��Mycobacterium Phleiϸ�������ֿ���֮�������Ϊ������������pH��2.6~5.2֮��ʱ��Mycobacterium Phleiϸ���������֮����־������������뷽Ǧ��֮��Ϊ�����������ʱ��Mycobacterium Phlei�ڻ��������������ʴ����ڷ�Ǧ�����Ŀɹ�������һ�㣻��pH��5.2ʱ��Mycobacterium Phleiϸ�������ֿ������֮�������Ϊ�������������Mycobacterium Phlei�ڻ���������������ȴԶԶ�����ڷ�Ǧ�����ģ��ɼ���ʱ�������ò�ռ������λ�������ǻ�ѧ���ϵ��������õĽ����
2.3 ���������
ͼ6��ʾΪMycobacterium Phlei�ĺ�����ס���ͼ6�е��״����й���[12?13]��3 290.78 cm?1������ǿ����Ϊ�ϵ�O��H��N��H�����壻2 958.99 cm?1��2 921.66 cm?1������С˫��Ϊ֬�����������ϡ�CH3�͡�CH2���Գ������壻1 648.39 cm?1Ϊ�ϵ��������C=O�����壻1 544.70 cm?1ΪN��H�ı������C��N������ż����ɵ����������1 457.60 cm?1Ϊ��CH2�����͡�CH3���ԳƱ����壻1 399.54 cm?1Ϊ��C(CH3)3�����ڱ�����1 229.49 cm?1Ϊ����C��O�ı�����֬���尷��C��N�����壻1 063.59 cm?1Ϊ�������崼������C��O��������S=O�����干ͬ���ý����
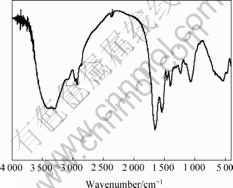
ͼ6 Mycobacterium Phlei�ĺ������
Fig.6 Infrared spectroscopy of Mycobacterium Phlei
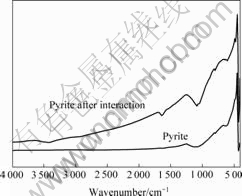
ͼ7 ��Mycobacterium Phlei����ǰ�������ĺ������
Fig.7 Infrared spectroscopy of pyrite before and after interaction with Mycobacterium Phlei
ͼ7��ʾΪ��Mycobacterium Phlei����ǰ��� ����ĺ������ͼ���Աȷ��֣���Mycobacterium Phlei���ú������������ϳ�����3 430.40 cm?1��1 635.94 cm?1�µ����շ塣����3 430.40 cm?1ΪMycobacterium Phleiϸ�������O��H��N��H���������������Ӱ���3 290.78 cm?1��Ư���γɵģ�1 635.94 cm?1ΪMycobacterium Phleiϸ������ϵ��������C=O�����塣�ⲻ��˵����Mycobacterium Phleiϸ�������Ĵ��ڣ����һ���ӳ��ϸ���ڻ����������������˷��Ӽ������⣬����������á����⣬��Mycobacterium Phlei���ú�����������1 084.35 cm?1���� �Ƶ���1 092.63 cm?1�����ҷ�ǿ�����α�ļ��ɼ�����������SԪ��Ҳ������ϸ��������λ�㡣
�Ƶ���1 092.63 cm?1�����ҷ�ǿ�����α�ļ��ɼ�����������SԪ��Ҳ������ϸ��������λ�㡣
ͼ8��ʾΪ��Mycobacterium Phlei����ǰ��Ǧ��ĺ������ͼ����Mycobacterium Phlei���ú�Ǧ��������3 430.20 cm?1ΪO��H��N��H�����������շ壬1 640.09 cm?1������Ϊϸ������ĵϵ�C=O������塣������Ǧ��������Mycobacterium Phleiϸ�������������⣬��Mycobacterium Phlei���ú�Ǧ��������1 063.59 cm?1���� �Ƶ���1 051.15 cm?1���ҷ�ǿ���ɼ���Ǧ������SԪ��Ҳ������ϸ��������λ�㡣
�Ƶ���1 051.15 cm?1���ҷ�ǿ���ɼ���Ǧ������SԪ��Ҳ������ϸ��������λ�㡣
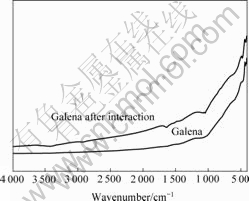
ͼ8 ��Mycobacterium Phlei����ǰ��Ǧ��ĺ������
Fig.8 Infrared spectroscopy of galena before and after interaction with Mycobacterium Phlei
��ͼ7��8��ͼ6���ԱȽϣ����Կ�������Mycobacterium Phleiϸ�����ú��������C=O���ŵIJ�����С��12.45 cm?1������Ǧ������C=O���ŵIJ�����С��8.3 cm?1�����������O��H��N��H���ŵIJ���������139.62 cm?1������Ǧ������C=O���ŵIJ���������139.42 cm?1����Щ��ĸı���˵����Mycobacterium Phleiϸ�������C=O��O��H��N��H�����������������õij̶ȴ����뷽Ǧ��������õģ�ͬʱҲ˵������Щ�����е�O��NԪ�ز�������λ��
2.4 X���߹����������
����Ȼ״̬�µ�Mycobacterium Phlei��2��������P������Mycobacterium Phlei��Ŀ���ȫ��ͼ�г��ֵ�ÿ��Ԫ�ؽ����˾�ϸ����ɨ�衣ͨ������ó��˸��ֿ������Ԫ�صĵ��ӽ���ܡ���̬����ӦŨ�ȵ�[14?15]��������1���С�
�ӱ�1�п��Կ�����Mycobacterium Phlei��X���߹��������ͼ�г�����C��O��N��P��SԪ�ء�����XPS������ͼ������ȷ����C1s����Ӧ�Ĺ�����ΪC=O��C��O����C��N��O1s����Ӧ�Ĺ�����Ҳ֤ʵ��C=O��C��O��O��H �Ĵ��ڣ�N1s����Ӧ�Ĺ�����ΪN��H��C��N��P2p��Ӧ�Ĺ�����P=O��S2p��Ӧ�Ĺ�����ΪS=O��
�ӱ�1�п�֪�������������˱���ɷ�S��Fe�⣬����O��C��δ��������Ԫ�أ�˵����������Ʒ�Ƚϴ������������IJ���Fe2+��������Fe3+(Fe2p3/2=711.87 eV)������[S2]2?Ҳ�������� (S2p3/2=168.85 eV)�������ܿ�����Fe2(SO4)3����Mycobacterium Phlei���ú�����Ĺ��������ͼ�г�����N1s�壬Ũ��Ϊ5.4%�������Mycobacterium Phleiϸ�������NԪ���ڻ�������淢���˻�ѧ���������⣬���������Fe3+��S6+��O�������˽ϴ�Ļ�ѧλ�ƣ�˵����Mycobacterium Phlei���ú���������Fe��S��O�Ļ�ѧ���������˱仯������Ϊϸ����������е����ṩ�¶Ե��ӵ�O��N��ԭ�����������γ��˱��������,�������������S�����˻�ѧ��Ӧ�������������������ʡ�
(S2p3/2=168.85 eV)�������ܿ�����Fe2(SO4)3����Mycobacterium Phlei���ú�����Ĺ��������ͼ�г�����N1s�壬Ũ��Ϊ5.4%�������Mycobacterium Phleiϸ�������NԪ���ڻ�������淢���˻�ѧ���������⣬���������Fe3+��S6+��O�������˽ϴ�Ļ�ѧλ�ƣ�˵����Mycobacterium Phlei���ú���������Fe��S��O�Ļ�ѧ���������˱仯������Ϊϸ����������е����ṩ�¶Ե��ӵ�O��N��ԭ�����������γ��˱��������,�������������S�����˻�ѧ��Ӧ�������������������ʡ�
�ӱ�1��֪����Ǧ����Ʒ�Ĵ���Ҳ�ܸߣ����ұ���Ҳ��������������Mycobacterium Phlei���ú�Ǧ����淢����NԪ�أ���Ժ���Ϊ5.38%�������Mycobacterium Phleiϸ�������NԪ���ڷ�Ǧ����淢���˻�ѧ��������Mycobacterium Phlei���ú�Ǧ�����C��Ժ��������Ӷ�Pb��S��O��Ժ����Ľ��ͱ�����Mycobacterium Phlei�ڿ����������� ������
���ֱ���Mycobacterium Phlei���ú������ͷ�Ǧ���X���߹���������Թ����ܽᣬ���Եó�Mycobacterium Phleiϸ�������C��N��OԪ��ͨ����������Fe��Pb��SԪ���������淢���˻�ѧ��������Mycobacterium Phlei���ú��������Fe��S��O���ӽ���ܵĻ�ѧλ�ƾ��ȷ�Ǧ������Pb��S��O�Ļ�ѧλ�ƴ�˵��Mycobacterium Phleiϸ���������Ի��������ĸ�Ԫ�ػ�ѧ�����ĸı�̶ȴ��ڶԷ�Ǧ�����ģ�Ҳ����˵��Mycobacterium Phleiϸ���ڻ��������������������ڷ�Ǧ�����ģ����ڻ�����ͷ�Ǧ����������ѡ������������
��1 ����Mycobacterium Phleiǰ�������ͷ�Ǧ��ı���Ԫ�ط���
Table 1 Surface elements analysis of pyrite and galena before and after interaction with Mycobacterium Phlei
2.5 ѡ�������������۽���
����Mycobacterium Phlei�ڻ�����ͷ�Ǧ������ѡ��������������������Ϊ���Դ�����������Խ��ͣ�һ�ǻ�����ͷ�Ǧ��ı���ṹ�������ʶ�ϸ������Ч����Ӱ�죻����ϸ�������л����������������Ԫ��֮��������õĴ�С��
�ڻ�����ľ���ṹ�У�Feԭ��λ������������8���Ƕ���6��������ģ�Sԭ���������״�Ķ���[S2]2?���Թ��ۼ����ϣ�[S2]2?λ�ھ������ĺ���������е㡣��������״�������ӵ��쳤�����ڽṹ�н������ã�ʹ�����������������������ȱ����������Ǧ��ľ���ṹ�У������ӳ���������ܶѻ���Ǧ���ӳ��������а������϶�У�����ƽ��{100}���� ȫ[16]�����ԣ������������������IJ�ƽ��������ϸ��������������Ǧ��ȽϹ⻬�Ľ�����������ϸ�������������⣬ˮ��Һ�У�������ͷ�Ǧ����ܽ�ȷֱ�Ϊ48.89��10?6 mol/L��1.21��10?6 mol/L�������������������Σ����ܽ���������ӣ�FeSO4��PbSO4�ܽ������Ϊ1.03(0 ��)��1.3��10?4(18 ��)����˻���������ܽ��������ԶԶ���ڷ�Ǧ������ܽ��Ǧ���ӡ�������ʾ������ȻpHֵ�����£��ӻ��������ܽ��������Ũ��Ϊ1.15 mg/m3���ӷ�Ǧ�����ܽ��Ǧ����Ũ��Ϊ0.1 mg/m3[17]����ˣ������Ի����pH�£�������������ɵ��������������ڷ�Ǧ��������ɵ�������Ǧ����Mycobacterium Phlei�������ͨ������������������õij̶ȴ����뷽Ǧ��������õġ�pH��5ʱ��Mycobacterium Phleiϸ���ڻ�����ͷ�Ǧ�����������Ե�ѡ������������ɹ�������һ�㡣
����������FeԪ����Fe2+��Fe3+����ʽ���ڣ�����Ǧ������Pb��Ҫ��Pb2+����ʽ���ڡ�Fe��Pbԭ�ӵĵ��ӷֲ�ʽ����Ϊ1s22s22p63s23p63d64s2��1s22s22p63s23p63d104s24p64d104f145s25p65d106s26p2�����ǵļ۲���ӹ��ͷֱ�Ϊ(n?1)d6ns2��ns2np2��Fe2+��Fe3+�۲����δ�������ӵĿչ����Pb2+���չ�������пչ���ĵ��ӹ���Ϊ��������ŶԵ����γ���λ��������������ͬʱ�����ڹ��ɽ���Ԫ�ص����Ӱ뾶��С��������нϴ����Ч�˵�ɣ��������н�ǿ���������������к�ǿ���γ���λ�������[18]�����ߣ����ڻ��������ƽ��{100}��{111}������ȫ��������{111}�������ϱ�¶�ļ���ȫ��Feԭ�ӣ�������ϸ��������ŵļ��ϡ���ˣ���Mycobacterium Phleiϸ�������C=O��O��H��N��H�����У�O��N����ԭ������������������λ���������뷽Ǧ�����Ǧ�ġ���Ҳ��ʹMycobacterium Phleiϸ���ڻ���������������ԶԶ�����ڷ�Ǧ�����ġ�
3 ����
1) ������ʵ�������̶�������£�����Һ�ij�ʼpHֵ����5ʱ��Mycobacterium Phlei�ڻ�����ͷ�Ǧ�������������Ե�ѡ������������
2) ����λ�IJ��Խ���������������ò�����ʹMycobacterium Phlei�ڻ�����ͷ�Ǧ��������ѡ������������Ҫ��������
3) �������X���߹�������ķ������������Mycobacterium Phleiϸ�������C��N��OԪ��ͨ����������Fe��Pb��SԪ���������淢���˻�ѧ��������ѧλ�ƵĴ�С˵����ѡ���������̶ȵ�ǿ����
4) ������ͷ�Ǧ��ı���ṹ�������ʡ�ϸ�����������������������ӵ���λ������С����ʹMycobacterium Phlei����ѡ������������Ҫԭ��
REFERENCES
[1] �����, �� ��. ����ѡ���Ӧ���о���״����չ����[J]. �й���ҵ, 2005, 14(9): 76?78.
JIANG Hong-hui, WANG Kun. The present situation of applied research on microbe mineral processing and development direction[J]. China Mining Magazine, 2005, 14(9): 76?78.
[2] CRUNDWELL F K. How do bacteria interact with minerals?[J]. Hydrometallurgy, 2003, 71: 75?81.
[3] CHANDRAPRABHA M N, NATARAJAN K A. Surface chemical and flotation behaviour of chalcopyrite and pyrite in the presence of Acidithiobacillus thiooxidans[J]. Hydrometallurgy, 2006, 83(5): 146?152.
[4] ������, ����, ��÷÷, �����. �������������������������õ��о���չ[J]. ��ұ����, 2006, 26(1): 40?44.
LIU Jian-she, WANG Zhao-hui, GENG Mei-mei, QIU Guan-zhou. Progress in the study of polyphase interfacial interactions between microorganism and mineral in bio-hydrometallurgy[J]. Mining and Metallurgical Engineering, 2006, 26(1): 40?44.
[5] HARNEIT K, GOKSEL A, KOCK D H, GEHRKE T, SAND W. Adhesion to metal sulfide surfaces by cells of Acidithiobacillus ferrooxidans, Acidithiobacillus thiooxidans and Leptospirillum ferrooxidans[J]. Hydrometallurgy, 2006, 83(5): 245?254.
[6] κ����, ���Ұ�, ������, ��һ��, �ִ���, �����, ����. ŵ���Ͼ��ڻ��������п������ѡ��������[J]. �й���ɫ����ѧ��, 2006, 16(6): 1082?1088.
WEI De-zhou, SHEN Yan-bai, LI Xiao-an, ZHU Yi-min, JIA Chun-yun, SU Xiu-juan, QIN Yu-chun. Selective adsorption of Nocardia on surface of pyrite and sphalerite[J]. The Chinese Journal of Nonferrous Metals, 2006, 16(6): 1082?1088.
[7] ���Ұ�, ������, κ����, ��һ��, �ִ���, �� ��. Nocardia�ڻ�����ͷ�Ǧ������ѡ��������[J]. �й���ɫ����ѧ��, 2005, 15(12): 2016?2022.
SHEN Yan-bai, LI Xiao-an, WEI De-zhou, ZHU Yi-min, JIA Chun-yun, HAN Cong. Selective adsorption of Nocardia on surface of pyrite and galena[J]. The Chinese Journal of Nonferrous Metals, 2005, 15(12): 2016?2022.
[8] ZHENG Xia-peng, ARPS PEGGY J, SMITH ROSS W. Adhesion of two bacteria onto dolomite and apatite: their effect on dolomite depression in anionic flotation[J]. International Journal of Mineral Processing, 2001, 62: 159?172.
[9] SANTHIYA D, SUBRAMANIAN S, NATARAJAN K A, ZHENG Xia-peng, ARPS Peggy J, SMITH Ross W. Surface chemical studies on sphalerite and galena using bacillus polymyxa ��.mechanisms of microbe-mineral interactions[J]. Journal of Colloid and Interface Science, 2001, 235(9): 298?309.
[10] NAMITA D, NATARAJAN K A, SOMASUNDARAN P. Mechanisms of adhesion of Paenibacillus polymyxa onto hematite, corundum and quartz[J]. Mineral Processing, 2001, 62(7): 27?39.
[11] ��۷�, �� ǿ. �ݷ�֦�˾��볣�沶�ռ���ϸ���������������ıȽ�[J]. ��ұ����, 2003, 23(4): 32?34.
YANG Hui-fen, ZHANG Qiang. Collecting ability comparison between Mycobacterium Phlei and general collector for fine particle hematite[J]. Mining and Metallurgical Engineering, 2003, 23(4): 32?34.
[12] ������, ������, ������. �л��ṹ������[M]. ���: ����ѧ������, 2002: 48?147.
LI Run-qing, FAN Guo-liang, QU Rong-lin. Spectral analysis of organic structures[M]. Tianjin: Tianjin University Press, 2002: 48?147.
[13] ������, ��粹�. ����ԭ��������[M]. ����: ��ѧ������, 2005: 59?113.
CHANG Jian-hua, DONG Qi-Gong. Specrum principle and analysis[M]. Beijing: Science Press, 2005: 59?113.
[14] ������, ������, �˳��. X���߹����������[M]. ����: ��ѧ������, 1988: 67?112.
LIU Shi-hong, WANG Dang-han, PAN Cheng-huang. X-ray photoelectron spectroscopy analysis[M]. Beijing: Science Press, 1988: 67?112.
[15] �ﴫҢ, ӡ����. �����ο��︡ѡԭ��[M]. ����: ��ѧ������, 2001: 365?392.
SUN Chuan-yao, YIN Wan-zhong. Floatation mechanism of silicate mineral[M]. Beijing: Science Press, 2001: 365?392.
[16] �� ƽ. �ᾧ����ѧ[M]. ����: ��ѧ��ҵ������, 2006: 128?131.
CHEN Ping. Mineral crystal chemistry[M]. Beijing: Chemical Industry Press, 2006: 128?131.
[17] κ����. �������Ϸ�ѡѧ[M]. ����: ұ��ҵ������, 2000: 308?330.
WEI De-zhou. Separation theory of solid material[M]. Beijing: Metallurgy Industry Press, 2000: 308?330.
[18] ����ѧ����ѧ������. ����ѧ[M]. ����: �ߵȽ���������, 1992: 514�C626.
Inorganic chemistry staff room in Tianjing University. Inorganic chemistry[M]. Beijing: Higher Education Press, 1992: 514?626.
������Ŀ��������Ȼ��ѧ����������Ŀ(50174014)������ʡ��Ȼ��ѧ����������Ŀ(20042021)������ʡ���¿Ƽ��ƻ�������Ŀ(2006223002)
�ո����ڣ�2007-05-11�������ڣ�2007-08-01
ͨѶ���ߣ��ִ��ƣ���ʿ�о������绰��13516084868��E-mail: jiachunyun@126.com
(�༭ �°���)