文章编号:1004-0609(2011)04-0796-08
聚苯胺在LiCoO2和LiMn2O4正极中的双重功能
范长岭1,徐仲榆1,苏玉长2
(1. 湖南大学 新型炭材料研究所,长沙 410082;
2. 中南大学 材料科学与工程学院,长沙 410083)
摘 要:用化学聚合法合成聚苯胺(PAn),并考察其在LiCoO2和LiMn2O4正极中的双重功能。结果表明:在优化条件下PAn的产率y=94.06%、导电率σ=18.39 S/cm,大于乙炔黑(AB)的导电率σ=7.77 S/cm;以制备的PAn为锂离子电池正极活性材料,在不添加其他导电剂对其进行恒电流充、放电试验(电流密度J=15 mA/g)时,第三循环的比放电容量D3=60.8 mA?h/g、充、放电效率η3=94.56%;PAn在正极中兼有活性材料的功能;以LiCoO2和尖晶石LiMn2O4为正极活性材料,以PAn替代AB作为导电剂进行恒电流充、放电试验,在电流密度分别为15、30、45和60 mA/g时,比充、放电容量都增大,表明正极的极化程度减小;正极在经过较大电流密度(60 mA/g)充、放电后,再以小电流密度(15 mA/g)进行充、放电时,比充、放电容量几乎没有变化,表明经较大电流密度(60 mA/g)充、放电后,LiCoO2和尖晶石LiMn2O4的贮锂结构没有改变。
关键词:锂离子电池;LiCoO2;LiMn2O4;聚苯胺;化学聚合;双重功能
中图分类号:TM912.9 文献标志码:A
Dual function of polyaniline in positive electrodes of LiCoO2 and LiMn2O4
FAN Chang-ling1, XU Zhong-yu1, SU Yu-chang2
(1. Institute of New Carbon Materials, Hunan University, Changsha 410082, China;
2. School of Materials Science and Engineering, Central South University, Changsha 410083, China)
Abstract: Polyaniline (PAn) was produced by chemical polymerization. The dual function of PAn in positive electrodes of LiCoO2 and LiMn2O4 was investigated. The results show that under the optimized conditions, the yield of PAn is y=94.06% and its electronic conductivity is σ=18.39 S/cm, which is greater than that of acetylene black (AB) (σ=7.77 S/cm). The galvanostatic experiment (current density J=15 mA/g) with the above PAn as the positive electrode active material was carried out, and no other electronic conductive reagent was used. In the third cycle, the specific discharge capacity (D3) is 60.8 mA?h/g, the charge and discharge efficiency η3 is 94.56%. PAn in the positive electrodes has the function of active materials. The galvanostatic experiments were carried out with the LiCoO2 and spinel LiMn2O4 as the positive electrode active materials and the PAn was used as the electronic conductive reagent to take place of AB. When the current densities are 15, 30, 45 and 60 mA/g, all the specific charge and discharge capacities increase. After charging and discharging with large current density (60 mA/g), the positive electrode charged and discharged with the original small current density (15 mA/g). The specific charge and discharge capacities are almost unchanged. It shows that the storing lithium ions structures of LiCoO2 and spinel LiMn2O4 do not change.
Key words: lithium ion batteries; LiCoO2; LiMn2O4; polyaniline; chemical polymerization; dual function
由于锂离子电池(LIB)中的电化学反应是氧化还原反应,因此,当锂离子从电解液嵌入电极中的活性(贮锂)材料或从电极中的活性(贮锂)材料中脱嵌进入电解液时,必须有电子同时从集电极进入电极中的活性材料,或从电极中的活性材料中离开进入集电极[1]。这类电子流动途经活性材料颗粒内部以及在活性材料颗粒外围由导电剂及粘结剂所组成的导电网络。LiCoO2及尖晶石LiMn2O4的电子导电率比较低,一般在10-5 S/cm左右。对生产(装配)LIB的工厂来说,要提高正极活性材料颗粒外围由导电剂和粘结剂所组成的电子网络的导电率,这可通过选用电子导电率高的导电剂来完成。显然,所选导电剂的电子导电率愈高时,正极活性材料颗粒外围导电网络的电阻愈小,LIB充、放电时正极的极化程度就愈小,从而使比充、放电容量增大,充、放电的电流密度(倍率)可以提高。由此可见导电剂的电子导电率在LIB中的重要性。
长期以来,在LIB的正极中一直都采用AB作为导电剂。近年来,一些学者考虑将具有线状的气相沉积炭纤维(VDCFs)和多壁碳纳米管(MWCNTs)来替代具有颗粒状的AB。王国平等[2]根据X射线衍射(XRD)和高分辨透射电镜(HRTEM)分析指出:MWCNTs内外层表现出比较规整的层状石墨结构,结晶度较高;而VDCFs尽管其内层与MWCNTs的结构类似,但其外层则为不完整的乱层结构,结晶度最低;而AB则为无定形结构,结晶度最低。LI X L等[3]对MWCNTs进行了HRTEM和扫描电镜(SEM)分析,指出:MWCNTs具有结晶度完好的有序层状石墨结构。这些学者认为:MWCNTs和VDCFs具有结晶度完好的石墨层状结构,因此,它们的导电率一定远大于AB的。但是,他们没有考虑到石墨晶体的各向异性程度非常高,以鳞片石墨的导电率为例,沿石墨烯平面方向(a方向)的导电率约为104 S/cm,而与石墨烯平面垂直方向(c方向)的导电率仅为1 S/cm左右[4],二者相差104倍。据此可以推理:MWCNTs沿轴向与石墨烯曲面平行方向的导电率σ∥一定远大于MWCNTs径向垂直于石墨烯曲面的导电率σ⊥。使用MWCNTs作为正极中的导电剂时,MWCNTs通过外管壁与集电极和正极活性材料颗粒进行接触而导电,因此,正极的导电率受到σ⊥的制约。此外,线状的VDCFs或MWCNTs的长径比太大与颗粒状的正极活性材料不可能混合得非常均匀,因此,以VDCFs或MWCNTs单独用作正极中的导电剂时其电化学性能并不很理想[2-3]。再者,VDCFs特别是MWCNTs的价格都远比AB的高,因此,作为导电剂前两者在LIB工业中并未得到推广应用。理想的导电剂应该是价廉、导电率高、各向同性、且长径比较小的粉状颗粒。
自从1977年日本筑波大学的SHIRAKAWA、美国宾夕法尼亚大学的MACDIARMID和美国加利福尼亚大学的HEEGER等发现碘掺杂聚乙炔的导电率可提高10亿倍、能与金属铜、银相媲美以来[5],导电活性聚合物(CEP)作为一种新型的有机导电材料已成为各国研究的热点。CEP通过掺杂和脱杂能使其电导率覆盖范围在10-9~103 S/cm之间变动,如此宽的范围是目前任何其他种类的材料都无法与其相比的。在众多的CEP中,PAn以其单体价格低廉,合成工艺简单,导电性能优良,在空气中和受热情况下稳定性高而受到人们的关注。本文作者以化学聚合法合成了长径比较小的粉状PAn,考察了用其来取代AB作为LiCoO2和LiMn2O4正极中的导电剂时所起的作用。
应当指出的是,在电池的发展过程中,CEP常用作正极与锂(负极)组成电压为3 V的锂电池[6],如果PAn在LIB的正极中也应有一定的比充、放电容 量,则说明其在正极中具有导电剂和活性材料的双重功能。
1 实验
1.1 PAn的化学聚合
PAn已被确认具有如图1(a)所示的结构,在其结构中存在着3种状态[6-7]:充分还原态(y=1)的隐翠绿亚胺式(Leuco emeraldine);半氧化态(y=0.5)的翠绿亚胺式(Emeraldine)和完全氧化态(y=0)的过苯胺黑式(Pernigraniline)。与翠绿亚胺式对应的翠绿亚胺盐(见图1(b))是导电率最高的状态。
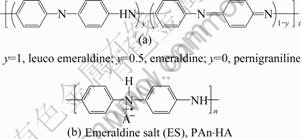
图1 PAn的3种氧化态及翠绿亚胺盐
Fig.1 Three oxidation states of Pan(a) and emeraldine salt(b)
PAn最常见的合成方法是在酸性溶液中对苯胺(An)单体进行化学聚合或电化学聚合,由于化学聚合过程简单,并可进行批量生产,因此,本文作者采用化学聚合法,以PAn的导电率和产率为考核指标,对其聚合条件进行了优化。
能用于An单体聚合反应的氧化剂有很多种,包括(NH4)4Ce(SO4)4[8]、K2Cr2O7[8-9]、KIO3[9]以及H2O2[9-10],然而,以(NH4)2S2O8[11]为氧化剂的产物具有最佳的导电性能,溶剂一般都采用水。通常情况下由于S2O82-阴离子是两电子的氧化剂(电子受体),而在聚合时从每个An单体所移出的电子数应稍大于2,因此,所用的(NH4)2S2O8与An的摩尔比应在1.2左右[6]。据文献[12]报道,An聚合中所用质子酸的种类以盐酸最好,其导电率高,产率也高,所要求的酸性条件是pH≤3,可以帮助An在水中的溶剂化,同时避免过量的、不希望产生的支化物的生成。
结构规整性最好的PAn产物是在低温下得到 的[13],应用最广泛的反应温度为1~5 ℃[14-15]。
除了上述因素外,还对反应时间tp和反应后停放的时间ts进行了优化,具体步骤如下。
取250 mL的三口烧瓶,在其中加入60 mL给定浓度的盐酸(分析纯),将烧瓶置于给定温度的冰浴或水浴中,在不断搅拌的情况下通入纯净Ar气30 min,然后加入一定量的An(分析纯),继续通入纯净Ar气并搅拌;称取一定量的(NH4)2S2O8(分析纯),将其溶解于40 mL给定浓度的盐酸中,然后向烧瓶中缓慢滴加(NH4)2S2O8溶液,滴加完毕后,在冰浴(或水浴)中反应一定时间;接着,将烧瓶从冰浴(或水浴)中取出、在室温下放置一定时间,然后,将产物用布氏漏斗过滤,同时用去离子水清洗沉淀,直至滤液的pH=7;最后,将合成的PAn在60 ℃的真空干燥箱中干燥24 h。
1.2 正极材料的结构和性能分析
实验中采用2种正极活性材料:LiCoO2(湖南长远锂科有限公司生产)和尖晶石LiMn2O4(德国Merck公司生产);两种导电剂:AB(电池级)和PAn(本实验用化学聚合法合成)以及一种黏结剂:60%聚四氟乙烯(PTFE)水乳浊液。
1.2.1 正极活性材料和导电剂粉末的XRD分析
所选用的正极活性材料(LiCoO2和尖晶石LiMn2O4试样)必须具有良好的结晶度和完整的贮锂结构,而所采用的导电剂(AB和PAn)应具有无定形结构,以保证其导电率的各向同性,因此,使用德国Siemens公司生产的D5000型XRD衍射仪对上述粉样进行微观结构的测定,辐射源为Cu Ka。
1.2.2 正极活性材料和导电剂粉末的颗粒分布特性
所选用的正极活性材料(LiCoO2和尖晶石LiMn2O4)试样粉末颗粒不应太大,以免Li+在其中扩散时因路径过长、电阻过大而引起充、放电时的极化。导电剂粉末的粒径必须小于正极活性材料粉末的粒径,这样导电剂的颗粒才能充填于活性材料颗粒之间的空隙中,形成良好的导电网络。为此使用成都树立新粉体仪器有限公司的JL-1177型激光粒度测试仪对其进行了颗粒分布特性的测定,测定前使用单宁酸(分析纯)作为分散剂,同时添加氨水(25%~28%)作为pH调整剂[16]。
1.2.3 正极活性材料和导电剂粉末导电率(电阻率)的测定
将中国科学院山西煤炭化学研究所制造的GM-II型多功能电阻率自动测定仪进行了改造,将其与Agilent公司的34401A型6 1/2 Digit 繁用表(Multimeter)结合起来,从而扩大了粉末导电率的测量范围。具体测定的方法如下:取一定量的粉末试样加入模筒内(截面积A=200 mm2),将内、外导向筒组装好后置于加压装置上,逐渐加压并在不同压强下稳定片刻。然后,根据不同压强下试样的高度h(mm)以及电阻值R(Ω),用电阻率ρ的定义式即可计算出一定压强下的粉末导电率σ:σ =1/ρ=h/(20R)。
1.2.4 正极的制备与恒电流充、放电实验
为了验证PAn是否兼有正极活性材料的功能,制备了1#正电极,其组分质量比为m(PAn):m(PTFE)= 95:5。将此组分进行充分混合后再用辊压法制成0.1 mm厚的薄膜,然后将其碾压在集电极上即成正电极(工作电极),辅助电极和参比电极均为锂片,电解液采用LiPF6/EC+DMC+EMC(1:1:1) (广州天赐高新材料股份有限公司生产,EC为碳酸乙烯酯,DMC为碳酸二甲酯,EMC为碳酸甲乙酯),电解池的槽体材料为PTFE,隔膜采用聚丙烯微孔膜(Celgard 2400),在充满高纯氩气的手套箱内装配成模拟电池。采用美国Arbin公司生产的BT2000型电池测试系统进行实验。充、放电的电位范围为2.500~4.300 V(vs Li+/Li),电流密度为15 mA/g,在此条件下进行了3个充、放电循环。
为了对比AB和PAn在用作正极中的导电剂时对LiCoO2和尖晶石LiMn2O4活性材料电化学性能的影响,一共制备了4种正电极,其组分质量比分别如下:
2#正电极: m(LiCoO2):m(AB):m(PTFE)=85:10:5;
3#正电极: m(LiCoO2):m(PAn):m(PTFE)=85:10:5;
4#正电极: m(LiMn2O4):m(AB):m(PTFE)= 85:10:5;
5#正电极: m(LiMn2O4):m(PAn):m(PTFE)=85:10:5。
上述2#~5#正电极极片的制备、电解液的种类以及模拟电池的组装均与前相同,电流密度依次为15、30、45和60 mA/g,充、放电的电位范围为3.300~4.300 V(vs Li+/Li),在上述各种电流密度下都进行了3个充、放电循环。为了考察在经过大电流密度60 mA/g充、放电后正极中活性材料的结构是否已经破坏,在此之后每种电极又进行了3个电流密度为15 mA/g的充、放电循环试验。
2 结果与讨论
2.1 PAn化学聚合条件的优化
表1所列为采用单因素法优化PAn化学聚合条件的实验结果,考核指标为PAn的产率y和导电率σ。从表1可知,PAn化学聚合的最佳条件如下:n((NH4)2S2O8):n(PAn)=1.2:1,An的浓度为0.4 mol/L,HCl的浓度为1.5 mol/L,反应温度t为1 ℃,反应时间tp为2 h,反应后停放的时间ts为24 h。在此条件 下,聚合所得的PAn产率为94.06%,导电率为 18.39 S/cm。
表1 PAn化学聚合条件的优化结果
Table 1 Optimization results of chemical polymerization conditions of PAn
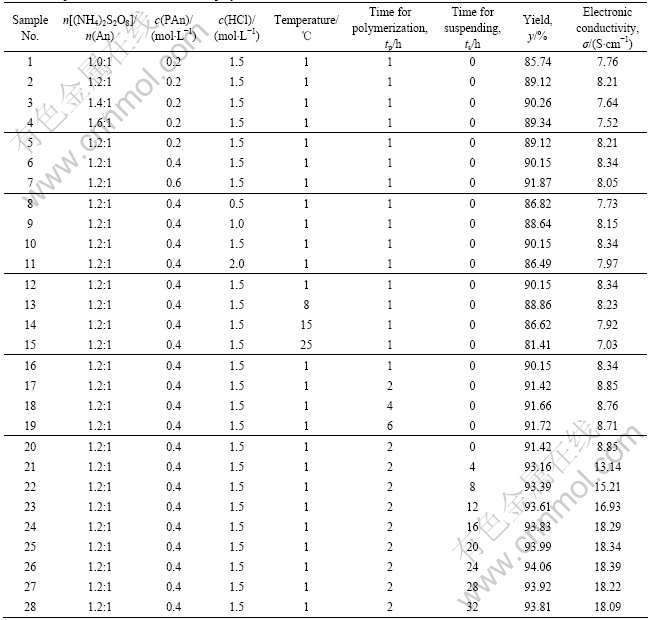
从表1可以看出,由于停放时间ts的延长,所得PAn的导电率增幅较大,这是因为在静止溶液中PAn链的生长和排列比较规整,支化程度较小,因此导电率较高。
2.2 正极活性材料和导电剂粉末的XRD分析
图2所示为LiCoO2和尖晶石LiMn2O4粉样的XRD谱。从图2 (a)和图2 (b)可知,所采用的LiCoO2与尖晶石LiMn2O4粉样的XRD谱,其中特征峰的峰位和对应的强度与LiCoO2和尖晶石LiMn2O4 PDF卡片(LiCoO2的号码为50―0653,LiMn2O4的号码为35―0782)中的完全一致,可见它们都具有完善的结晶度。从表2可知,LiCoO2与尖晶石LiMn2O4试样中的晶粒都较大,从而可以保证Li+的贮存。
从表3可知:L002和L100都很小,即AB中的石墨微晶尺寸很小;d002=0.356 1 nm,远大于石墨单晶中石墨烯平面的间距d002= 0.335 4 nm,说明石墨微晶内的石墨烯平面取向极不一致,因此AB为各向同性。由图3 (b) PAn的XRD谱可知,聚合所得的PAn为无定形态。综上所述可知所采用的导电剂AB和PAn在导电率方面都具有各向同性。
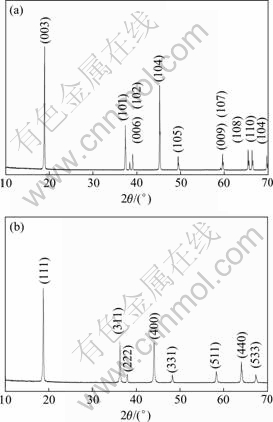
图2 LiCoO2和尖晶石LiMn2O4粉样的XRD谱
Fig.2 XRD patterns of powder samples LiCoO2 (a) and spinel LiMn2O4 (b)
表2 LiCoO2和尖晶石LiMn2O4粉样的XRD结构参数
Table 2 XRD structural parameters of powder samples LiCoO2 and spinel LiMn2O4

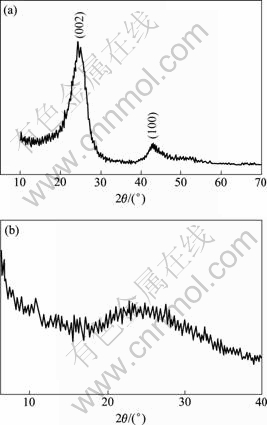
图3 AB和PAn粉样的XRD谱
Fig.3 XRD patterns of powder samples AB (a) and PAn (b)
表3 AB粉样的XRD结构参数
Table 3 XRD structural parameters of powder sample AB
2.3 正极活性材料和导电剂粉末的粒度分布
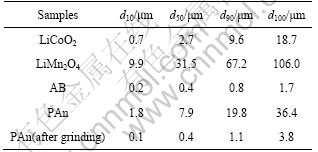
为了保证导电剂的颗粒能充填于正极活性材料颗粒间的空隙中形成良好的导电网络,导电剂粉末的粒径必须小于正极活性材料粉末的粒径。但从表4可以看出,化学聚合后所得PAn粉末的粒度太大,因此,必须再用武汉探矿机械厂生产的XZM100型振动磨样机进行细磨。
表4 LiCoO2、尖晶石LiMn2O4、AB、PAn和PAn(细磨)试样的粒度分布特性
Table 4 Granularity distribution of samples LiCoO2, spinel LiMn2O4, AB, PAn and PAn after grinding

2.4 正极活性材料和导电剂粉末的导电率
表5所列为几种正极活性材料和导电剂粉粉末的导电率。从表5可以看出:正极活性材料LiCoO2和尖晶石LiMn2O4的导电率的数量级均为10-5 S・cm-1,尖晶石LiMn2O4的导电率略高于LiCoO2的;导电剂PAn与AB的导电率均远大于正极活性材料的。经过细磨后的PAn由于链的共轭长度变短,其导电率从18.39 S/cm降为15.29 S/cm,降幅不大。
2.5 恒电流充、放电实验结果
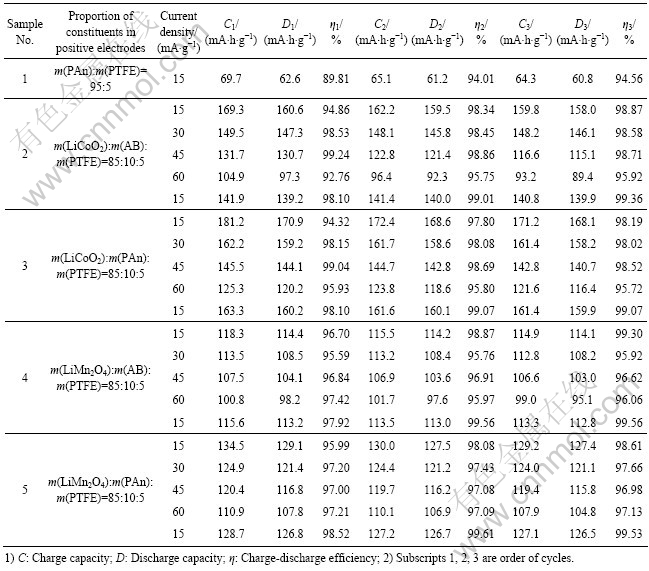
表6所列为正极活性材料的恒电流比充、放电容量及充、放电效率。从表6可以看出,当恒电流 充、放电电流密度为15 mA/g、不添加其他导电剂时,PAn本身的比充、放电容量为60 mA?h/g左右。文献[12]指出,当PAn充电(氧化)和放电(还原)时,阴离子(PF6-)在PAn聚合物链上进行掺杂和去掺杂。当PAn的电位达到3.779~3.861 V(vs Li+/Li)时,PF6-从电解液中掺入聚合物链上的阳离子空位处,当其电位在3.132~3.195 V(vs Li+/Li)时,PF6-将从聚合物链上返回电解液中。由此可见,PAn在LiCoO2和LiMn2O4正极中除用作导电剂外,还应有增加比容量的作用,即具有双重功能,但进出PAn的载流子是PF6-而非Li+。
从表6还可以看出:在正极中以PAn代替AB作为导电剂后,无论是LiCoO2还是尖晶石LiMn2O4在各种电流密度下各个循环中的比充、放电容量均增加。其原因是PAn的导电率(σ=15.29 S/cm)差不多是AB导电率(σ=7.77 S/cm)的两倍,由PAn组成的导电网络运输电子的能力大于AB组成的导电网络的,因此,充、放电时正极的极化程度减弱,比充、放电的容量增加。此外,由于PAn兼有正极活性材料的功能,组成正极时有一定的比充、放电容量,对提高正极的总充、放电容量也有一定的贡献,而AB则无此功能。
以PAn替代AB作为导电剂,在经过较大电流密度(60 mA/g)充、放电后再以最初的小电流密度(15 mA/g)进行充、放电时,尖晶石LiMn2O4的比放电容量从127.4 mA?h/g变为126.5 mA?h/g,几乎没有改变;LiCoO2的比放电容量从168.1 mA?h/g变为159.9 mA?h/g,变化也不大,这说明以在较大的电流密度下进行充、放电后正极活性材料的贮锂结构并未破坏,具有耐“过充”的能力。
表5 LiCoO2、尖晶石LiMn2O4、AB、PAn和PAn(细磨)粉样的导电率
Table 5 Electronic conductivities of samples LiCoO2, spinel LiMn2O4, AB, PAn and PAn (after grinding)
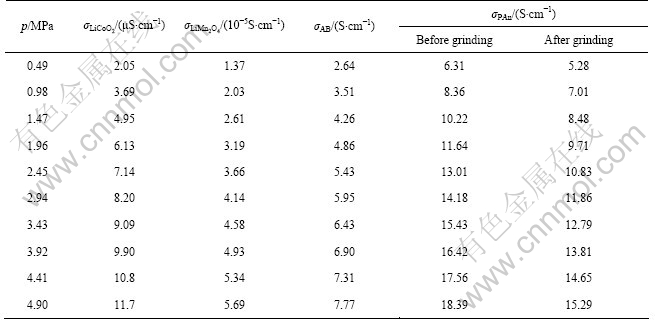
表6 不同正极活性材料的恒电流比充、放电容量及充、放电效率
Table 6 Galvanostatic specific charge and discharge capacities and efficiencies of different positive electrodes
3 结论
1) 聚合PAn经细磨后,其导电率(σ=15.29 S/cm)几乎为LIB常用正极导电剂AB(σ=7.77 S/cm)的两倍。以PAn替代AB时,正极的极化程度大幅降低,LiCoO2和LiMn2O4的比充、放电容量增加。
2) 由于PAn兼有导电功能和正极活性材料的功能,作为正极的组分时,PAn有一定的比充、放电容量(约60 mA?h/g),正极的总比充、放电容量增加;而AB则无此功能。
3) 由于正极的极化程度降低后,所允许的最大电流密度增大,LiCoO2和LiMn2O4的耐“过充”能力增强。
REFERENCES
[1] 尹笃林. 石墨化软炭材料用作锂离子电池负极活性材料时的共性[D]. 长沙: 湖南大学新型炭材料研究所, 2006: 79.
YIN Du-lin. Common characteristics of graphitized soft carbon materials using as the negative electrode active materials for lithium ion batteries[D]. Changsha: Institute of New Carbon Materials, Hunan University, 2006: 79.
[2] 王国平, 张庆堂, 瞿美臻, 于作龙. 纳米级碳导电剂的种类对LiCoO2电化学性能的影响[J]. 应用化学, 2006, 23(12): 1385-1390.
WANG Guo-ping, ZHANG Qing-tang, QU Mei-zhen, YU Zuo-long. Effects of different kinds of nano carbon conductive additives on the electro-chemical character of LiCoO2[J]. Chinese Journal of Applied Chemistry, 2006, 23(12): 1385-1390.
[3] LI X L, KANG F Y, BAI X D, SHEN W C. A novel network composite cathode of LiFePO4/multiwalled carbon nanotubes with high rate capability for lithium ion batteries[J]. Electrochem Commun, 2007, 9: 663-666.
[4] 《炭素材料》编委会. 中国冶金百科全书―炭素材料[M]. 北京: 冶金工业出版社, 2004: 472.
Editorial Committee of Carbon Materials. Metallurgical encyclopedia of China―Carbon materials[M]. Beijing: Metallurgical Industry Press, 2004: 472.
[5] NIGREY P J, MACDIARMID A G, HEEGER A J. Electrochemistry of polyacetylene, (CH)x: Electrochemical doping of (CH)x film to the metallic state[J]. J Chem Soc Chem Commun, 1979, 14: 594-595.
[6] WALLACE G G, SPINKS G M, KANE-MAGUIRE L A P, TEASDALE P R. 导电活性聚合物: 智能材料体系[M]. 吴世康, 译. 北京: 科学出版社, 2007: 11, 109, 115.
WALLACE G G, SPINKS G M, KANE-MAGUIRE L A P, TEASDALE P R. Conductive electroactive polymers: Intelligent materials systems[M]. WU Shi-kang, transl. Beijing: Science Press, 2007: 11, 109, 115.
[7] 陈振兴. 高分子电池材料[M]. 北京: 化学工业出版社, 2006: 108.
CHEN Zhen-xing. Polymer battery material[M]. Beijing: Chemical Industry Press, 2006: 108.
[8] SYED A A, DINESAN M K. Review: Polyaniline: A novel polymeric material[J]. Talanta, 1991, 38(8): 815-837.
[9] PRON A, GENOUD F MENARDO C, NECHSTEIN M. The effect of the oxidation conditions on the chemical polymerization of polyaniline[J]. Synth Met, 1988, 24(3): 193-201.
[10] SUN Z C, GENG Y H, LI J, JING X B, WANG F S. Chemical polymerization of aniline with hydrogen peroxide as oxidant[J]. Synth Met, 1997, 84(1/3): 99-100.
[11] CAO Y, ANDREATTA A, HEEGER A J, SMITH P. Influence of chemical polymerization conditions on the properties of polyaniline[J]. Polymer, 1989, 30(12): 2305-2311.
[12] 邓凌峰. 锂二次电池聚合物正极材料的合成与性能研究[D]. 长沙: 中南大学冶金科学与工程学院, 2004: 100, 107-108.
DENG Ling-feng. Studies on synthesis and properties of polymer positive electrode materials for lithium second batteries[D]. Changsha: School of Metallurgical Science and Engineering, Central South University, 2004: 100, 107-108.
[13] LEE C W, CHI K W, HWANG H Y, JEONG H M. Synthesis and properties of high performance nanostructured polyaniline: Effect of initiator dosage and molecular oxygen[J]. Synth Met, 2009, 159: 1757-1760.
[14] ZHANG L, WAN M. Chiral polyaniline nanotubes synthesized via a self-assembly process[J]. Thin Solid Films, 2005, 477: 24-31.
[15] XU H L, CAO Q, WANG X Y, LI W J, LI X Y, DENG H Y. Properties and chemical oxidation polymerization of polyaniline/neutral red/TiO2 composite electrodes[J]. Materials Science and Engineering B, 2010, 171: 104-108.
[16] 徐仲榆, 范长岭. 用激光法测定石墨微粉粒度分布特性时单宁酸所起的分散作用[J]. 炭素技术, 2009, 28(6): 1-5.
XU Zhong-yu, FAN Chang-ling. The dispersing action of tannic acid for determination the granularity distribution characteristic of graphite powder with laser method[J]. Carbon Techniques, 2009, 28(6): 1-5.
(编辑 龙怀中)
基金项目:教育部博士点基金资助项目(20060532018);湖南省科技厅重点资助项目(00GK1006)
收稿日期:2010-02-22;修订日期:2010-06-01
通信作者:徐仲榆,教授;电话:0731-88822967;E-mail: zyxincmhnu@yahoo.com.cn