文章编号:1004-0609(2008)10-1937-08
西门子体系中SiHCl3和SiCl4的热力学行为
苗军舰1,丘克强1,顾 珩2,陈少纯2
(1. 中南大学 化学化工学院,长沙 410083;
2. 广州有色金属研究院,广州 510651)
摘 要:在选取与实际生产相近的温度、氢气配比(H2与SiHCl3的初始比例)和压力的基础上,计算西门子体系中硅源气体SiHCl3的剩余量与副产物SiCl4的生成量,分别绘制二者随所选条件的变化图,并利用这些热力学图,分析温度、氢气配比及压力对西门子法生产多晶硅反应体系中SiHCl3和SiCl4热力学行为影响的规律。结果表明:当压力、氢气配比一定时,SiHCl3的剩余量与温度呈反比,SiCl4的生成量则是先随温度的升高而增加,后又变小;当温度和压力一定时,增大氢气配比SiCl4生成量减少,只有在氢气配比大于5以后SiHCl3的剩余量才与它呈反比关系;当温度和氢气配比一定时,随着压力的降低,SiHCl3的剩余量减少,SiCl4则呈先增加再减少的变化趋势。
关键词:SiHCl3;SiCl4;西门子体系;热力学行为
中图分类号:O 642.4; O 613.72 文献标识码: A
Thermodynamic behavior of SiHCl3and SiCl4in Siemens system
MIAO Jun-jian1, QIU Ke-qiang1, GU Heng2, CHEN Shao-chun2
(1. School of Chemistry and Chemical Engineering, Central South University, Changsha 410083, China;
2. Guangzhou Nonferrous Research Institute, Guangzhou 510651, China)
Abstract: On the basis of selecting the temperature, initial molar ratio of H2 to SiHCl3 and total pressure close to the practical production conditions, the residual amount of SiHCl3 and the yield of byproduct SiCl4 in the Siemens system for the production of semiconductor grade Si were calculated. The diagrams of the residual amount of SiHCl3 and the yield of byproduct SiCl4 versus the selected conditions were plotted respectively. With the help of these thermodynamic diagrams, the influence of the temperature, initial molar ratio of H2 to SiHCl3 and total pressure on the thermodynamic behaviors of SiHCl3 and SiCl4 were discussed. The results show that when the total pressure and initial molar ratio of H2 to SiHCl3 are kept constant, the residual amount of SiHCl3 is inversely proportional to the temperature, and the yield of SiCl4 increases firstly, then decreases with increasing temperature. When the temperature and total pressure are kept constant, the yield of SiCl4 decreases with increase in initial molar ratio of H2 to SiHCl3, but in regard to SiHCl3, its residual amount is in inverse proportion to the initial molar ratio of H2 to SiHCl3. When the temperature and initial molar ratio of H2 to SiHCl3 were held constant, the residual amount of SiHCl3 decreases with decreasing total pressure, and for SiCl4, its yield first increases, and then decreases.
Key words: SiHCl3; SiCl4; Siemens system; thermodynamic behavior
近几年,随着太阳能光伏发电技术的飞速发展和半导体产业的复苏,多晶硅的需求量急剧增加,价格暴涨,严重地制约了光伏发电产业的发展。因此,大力发展太阳能高纯多晶硅的大规模生产技术,成为新的竞争趋势。从20世纪五六十年代至今,高纯多晶硅的生产广泛采用西门子法[1-2],硅源气体为电子级SiHCl3还原气体采用高纯H2。一直以来在文献中未见关于西门子反应体系中SiHCl3热力学行为的研究报道。为此,对SiHCl3随温度、氢气配比以及体系压力的变化状况进行了研究。作为副产物,SiCl4不但很大程度上降低了SiHCl3的利用率,而且增加了尾气回收的难度,因此很有必要揭示SiCl4的生成规律,以便更好地控制反应过程。基于此,本文作者详述了SiCl4在西门子法生产多晶硅反应体系中的热力学行为。
1 体系特点及计算过程
在用H2还原SiHCl3进行多晶硅生产时,体系内发生了众多的反应[3-8],西门子体系在一定温度、压力和初始成分条件下的平衡状态,可以看作体系内所有反应相互作用同时平衡的结果。在不同条件下,通过实验测定平衡成分是很困难的,但是通过热力学计算可以获得有关的平衡信息。据热力学和实际化学分析的结果[7, 9-14],该体系存在的物质达十几种,如Si(s)、H2(g)、HCl(g)、SiCl4(g)、SiHCl3(g)、SiH2Cl2(g)、SiH3Cl(g)、SiCl2(g)、SiCl(g)、Si2Cl4(g)等,其中前8种物质为该体系的主要物种,其余物种含量非常少,可不加考虑。
从体系中存在的独立反应出发,根据它们在一定条件下的平衡常数可列出5个方程,再利用SiHCl3初始物质的量和H2/SiHCl3初始比例一定以及气体总量等于气相中各组分物质的量之和,可得出另外3个方程,体系在不同氢气配比、温度和压力下,解此方程组即可计算气相中各组分物质的量。计算所选条件为氢气配比(SV)SV=2~50、温度T=1 023~1 498 K、p= 0.01~10.00 Pa,取点较为稠密,较准确地反映了体系的变化状况。有关详细分析参见文献[15]。
该体系中的一组独立反应如下[16]:

该组反应的反应物均为初始原料气成分,可便于分析问题。按体积是否变化可将其分为两类,第一类为体积增大的反应,包括反应(1)、(2)和(5),第二类为体积不变的反应,包含反应(3)和(4)。单独来看,当压力变化时,第二类反应的平衡不发生移动。而第一类反应则有所变化,具体来说,增大压力,反应左移,反之,反应右移。
2 计算结果及讨论
2.1 SiHCl3的热力学行为
2.1.1 SiHCl3的剩余量随温度的变化
图1所示为不同压力时SiHCl3的剩余量随温度的变化。从图1可以看出,当压力和氢气配比一定时,随着温度的升高,SiHCl3的剩余量(nres)不断减少。由于反应(1)~(5)的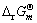 均随温度的增高而减小[15],因此,高温下SiHCl3的消耗量就相应增加,使得体系中SiHCl3的含量减小。比如,在体系压力p=0.1 MPa、氢气配比SV=10时,当温度由1 373 K升高为1 398和1 423 K时,由图1(b)可知,SiHCl3的剩余量依次减小,分别为0.531 2、0.495 0、0.451 1 mol。由此可见,实际生产时升高反应温度除了能加快反应速率外,还可以提高SiHCl3的一次利用率,从而增加产量。
均随温度的增高而减小[15],因此,高温下SiHCl3的消耗量就相应增加,使得体系中SiHCl3的含量减小。比如,在体系压力p=0.1 MPa、氢气配比SV=10时,当温度由1 373 K升高为1 398和1 423 K时,由图1(b)可知,SiHCl3的剩余量依次减小,分别为0.531 2、0.495 0、0.451 1 mol。由此可见,实际生产时升高反应温度除了能加快反应速率外,还可以提高SiHCl3的一次利用率,从而增加产量。

图1 不同压力时SiHCl3剩余量随温度的变化
Fig.1 Changes of residual SiHCl3 in Siemens system with equilibrium temperature at different pressures: (a) p = 0.2 MPa; (b) p = 0.1 MPa; (c) p = 0.05 MPa; (d) p = 0.02 MPa
从图1还可知,在同一压力下,温度较低时氢气配比SV对nres的影响很小。例如p=0.1 MPa,T=1 048 K时,对应于SV=50、30、25、20、15、10、5、2的nres分别为0.828 6、0.847 6、0.851 9、0.855 5、0.857 9、0.857 0、0.845 6、0.812 2 mol,相邻数值之差很小,这表明:反应温度低于一定值以后,增大氢气配比没有意义。但是,当温度较高时,SV对nres的影响就变得较为显著,例如,在p=0.1 MPa时,当温度升高到1 373 K,nres分别为0.289 9、0.386 0、0.416 9、0.451 2、0.489 5、0.531 2、0.570 7、0.571 0 mol,由此可以明显看出:相邻值差别比温度为1 048 K时的要大。通过计算发现,造成该现象的原因是:低温时SV对反应(1)~(5)的平衡反应进度影响很小,而高温时SV对反应(1)的平衡反应进度影响甚为显著。
另外,图中曲线出现相交的现象,最为明显的是SV=2的曲线,它同其他曲线都有交点。譬如,p=0.1 MPa时,SV=2的体系与SV=10的体系在1 232 K的nres相同,为0.693 8 mol。这种现象的原因有待进一步的研究。
2.1.2 氢气配比SV对SiHCl3剩余量的影响
图2所示为不同压力时氢气配比对SiHCl3剩余量的影响。由图2可知,在SV>5时,SiHCl3的剩余量随SV的增大而减小,即氢气含量越高对SiHCl3的还原越有利。当SV<5时,并且在体系压力较低时,如图2(d)所示,SiHCl3的剩余量也是随着氢气配比SV的增大而减小。但是体系压力较大时,如图2(a)和(b)所示,当温度不高时,如T=1 348 K时,SiHCl3的剩余量在SV<50时随SV的增大不是减小而是增大,并且体系压力越大,这种“反常现象”越明显。原因分析如下:在T=1 348 K,p=0.2 MPa,SV=2.5时,由于SV很小且体系压力较大,主反应为反应(2),而且SV越小反应(2)进行的趋势就越大。结合计算给出的数据可以更加明确地对此给予说明:在SV=2时,反应(1)~(5)的平衡反应进度顺次为0.052 3、0.058 3、0.009 8、 0.000 3和0.050 1 mol,SiHCl3的剩余量nres(SV=2)=1- (0.052 3+4×0.058 3+0.009 8+0.000 3+0.050 1)=0.654 3 mol;而在SV=5时,反应(1)~(5)的平衡反应进度顺序为0.097 5、0.041 3、0.014 3、0.000 5和0.059 0 mol,SiHCl3的剩余量nres(SV=5)=0.663 6 mol,显然nres(SV=5)>nres(SV=2),于是曲线在SV=2~5之间呈现上升趋势。
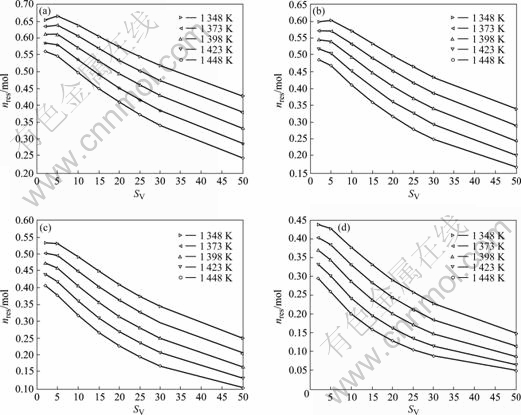
图2 不同压力时氢气配比对SiHCl3剩余量的影响
Fig.2 Effects of initial molar ratio of H2 to SiHCl3 on amount of residual SiHCl3 at different pressures: (a) p=0.2 MPa; (b) p=0.1 MPa; (c) p=0.05 MPa; (d) p=0.02 MPa
对比同一幅图中的曲线可以发现:其他条件均相同时,温度越高,SiHCl3剩余量越少。这与2.1.1节中所得结论一致。比较图2中4个分图中同一温度时的曲线可知,随着压力的减小,SiHCl3的剩余量在减少。根据以上论述,实践中应使氢气配比在5以上,以提高SiHCl3的一次利用率并抑制副产物的生成。
2.1.3 压力对SiHCl3的作用
图3所示为不同压力时SiHCl3剩余量随压力的变化。图4(a)~(d)曲线的变化趋势完全相同,即随着体系压力的减小,SiHCl3的剩余量也减少,并且在p=0.01~0.1 MPa之间,nres变化非常大。由于在反应(1)~(5)中,只有两类反应―体积增大的反应和体积不变的反应,因此,降低体系压力使SiHCl3的消耗增加,nres减小。在p=0.01~0.1 MPa之间,虽然压力的绝对数值变化小,但相对数值变化很大,于是曲线一次变化率较高压时的为大,曲线十分陡峭。

图3 不同温度时SiHCl3剩余量与压力的关系
Fig.3 Relationships between amount of residual SiHCl3 and system total pressure at different temperatures
在图3(a)~(d)中,同一压力下,除SV=2和5外,SV越大SiHCl3剩余量越少。此结论和2.1.2节所得结论相同。在实际中,是升高还是降低压力应根据反应体系而定,比如,以SiHCl3为原料气进行硅外延生长时,降低体系压力是有利的[5]。
2.2 SiCl4的热力学行为
2.2.1 SiCl4生成量随温度的变化
图4所示为SiCl4的生成量n随体系温度的变化规律:升高温度,SiCl4生成量先增加,达到最大值后又减小。在图4(b)中,分析SV=10的曲线发现:温度低于1 273 K时,升温使得SiCl4的生成量增加;在1 273 K时,SiCl4的生成量达到最大,此后温度的升高反而造成SiCl4生成量的减少。其余曲线也有类似的变化规律,差别仅在于SiCl4生成量达到最大值对应的温度不同。根据以上分析,在一定条件下为了减少排出尾气中SiCl4的量,反应温度要么选择低温,要么选择SiCl4达到峰值后尽可能高的温度。在生产中,为了确保较高的反应速率,则应选择后者。
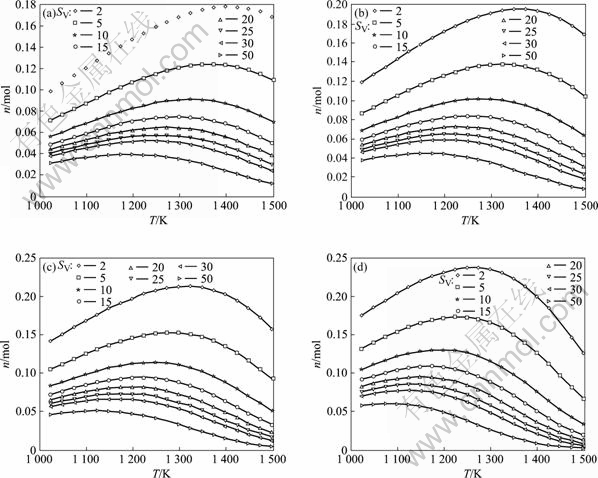
图4 不同压力时SiCl4生成量对温度的变化
Fig.4 Yield of SiCl4 as function of equilibrium temperature at different pressures: (a) p=0.2 MPa; (b) p=0.1 MPa; (c) p=0.05 MPa; (d) p=0.02 MPa
观察同一图中所有曲线可以发现,一定温度下,SV越大生成的SiCl4越少。图中另一个值得注意的特点是SV增大后,SiCl4最大生成量对应的温度降低,这表明:如果增大氢气配比,那么相同的SiCl4生成量所需控制的反应温度可以降低。比较不同的曲线图可知,同一SV的曲线其最大值及形状均有所变化。产生这些结果的原因将在下文给出。
2.2.2 氢气配比对SiCl4生成量的影响
图5表明,增大SV,SiCl4的生成量减少,也即是说H2有抑制SiCl4生成的作用。考虑反应(2),其产物之一为H2,因此增加初始混合气体中H2的含量必然导致反应(2)反应进度的减小,生成的SiCl4变少。生产实践已经证明,通过适当提高H2含量来减少SiCl4的生成是一个十分方便而且有效的方法。从图5(b)中1 373 K对应的曲线可知,在SV=5时,SiCl4的生成量为0.135 3 mol;而当SV=10时,SiCl4的生成量则降为0.094 8 mol,二者相差0.040 5 mol,减少30%。

图5 不同压力时SiCl4生成量随氢气配比的变化
Fig.5 Variations of yield SiCl4 with initial molar ratio of H2 to SiHCl3 at different pressures: (a) p=0.2 MPa; (b) p=0.1 MPa; (c) p=0.05 MPa; (d) p=0.02 MPa
图5中曲线还有另一变化规律:SV<15时,曲线变化较快;SV大于15后,曲线变化缓慢。据此可以推测,如采用提高氢气含量的方案来减少SiCl4的生成量,可将SV的值在2~15之间选择,效益较好。否则虽能较大程度地抑制SiCl4的生成,却不经济。
在图5(a)~(d)中,固定SV,对比不同温度时SiCl4的生成量可得到在2.2.1节中已得到的结论。比较图5(a)~(d)中各曲线发现,压力越高,相邻曲线靠越近,表明温度对SiCl4的生成量影响越小,该特点在SV较小时表现尤其突出。
2.2.3 压力对SiCl4生成量的作用
图6所示为SiCl4生成量随体系压力的变化。图中曲线在所给压力范围内可以分为两类:一类是随着压力的升高,曲线先呈上升趋势,达到最大值后转变为下降态势的曲线;另一类是与压力为正比关系曲线,即压力增大,曲线上升,SiCl4生产量增加。前者包括图6中除(d)中SV=50之外的所有曲线,后者仅有图6(d)中的SV=50的曲线。实际上,对于后一类曲线,当将其放在更大的压力范围内(pmax>1 MPa)考察时,它与第一类曲线有相同的变化规律呈先上升,再下降的趋势。根据化学平衡原理很容易得到该结论。

图6 不同温度时SiCl4生成量随压力的变化
Fig.6 Variations of yield SiCl4 with total pressure at different initial molar ratios of H2 to SiHCl3 and different temperatures: (a) 1 348 K; (b) 1 373 K; (c) 1 398 K; (d) 1 423 K
以下结合具体条件分析两类曲线出现的原因。在T=1 373 K,SV=10时,SiCl4的生成量在0.05 MPa达到最大值,即曲线在0.01~0.05 MPa之间上升而以后下降。之所以上升是因为压力对反应(5)和(1)的影响很大,对反应(2)影响小,因受压力上升影响未能进行反应(5)和(1)反应的部分SiHCl3进行了反应(2)反应,使得反应(2)的反应进度在0.01~0.05 MPa之间与压力呈正比,相应地,SiCl4生成量随压力的增大而增多。比如在压力为0.01、0.02和0.05 MPa时,反应(1)的平衡反应进度分别为0.294 9、0.271 0和0.232 9 mol;反应(2)的平衡反应进度为别为0.024 5、0.029 1和0.031 9 mol;反应(5)的平衡反应进度依次为0.359 4、0.275 6和0.181 5 mol。从这些数据可以看出,压力对反应(5)和(1)的抑制远大于对反应(2)的抑制。曲线在压力较大时出现下降的原因是:反应(2)的平衡位置受SiHCl3浓度和体系压力等因素的影响,增大压力后,反应(5)、(2)和(1)均左移,SiHCl3浓度增加,它反作用于反应(2),使其右移,不过此反作用不及压力对反应(2)的直接作用,以致SiCl4生成量减少。其他条件下的讨论与此相似。
图6(d)中SV=50的曲线与压力呈正比关系。这是由体系温度较高(1 423 K),压力对反应(2)的直接左移作用不及因压力变化导致的SiHCl3浓度增加对反应(2)的右移反作用所致。由于该曲线和第一类曲线本质上相同,参照上面分析同样能得出该结论。
比较图6的任一分图中同一压力下不同SV时的SiCl4生成量可知,SV越大,体系中SiCl4越少。这与从图5得到的结论一致。
3 结论
1) 在压力、氢气配比一定时,温度越高,参加反应的SiHCl3越多,其一次利用率也越大;在压力、温度恒定时,当氢气配比大于5时,SiHCl3剩余量随氢气配比的增大而减小,但在氢气配比小于5且压力与温度均较高时,出现相反的变化;在氢气配比和温度保持不变时,随着压力的降低,SiHCl3的剩余量在减少,并且低压时减少更快。
2) 在压力、氢气配比恒定时,SiCl4的生成量先随温度的升高而增加,达到最大值后又随温度的升高而减小;相同压力不同氢气配比时,SiCl4生成量达到最大值的温度不同,它随氢气配比的增大而减小;氢气配比的增加有助于抑制SiCl4的生成;在温度和氢气配比一定时,SiCl4的生成量先与压力呈正比关系,当压力增大到某一值后呈反比。
3) 温度选1 350~1 450 K,氢气配比为5~15,体系压力0.1 MPa左右时为较合适的条件。这同现行工艺参数吻合相当好。计算结果还可以为现行工艺优化和今后新工艺的开发提供理论指导。
REFERENCES
[1] 梁骏吾. 电子级多晶硅的生产工艺[J]. 中国工程科学, 2000, 2(12): 34-39.
LIANG Jun-wu. The production technology of electronic grade polycrystalline silicon[J]. Engineering Science, 2000, 2(12): 34-39.
[2] 沈 辉, 曾祖勤. 太阳能光伏发电技术[M]. 北京: 化工工业出版社, 2005: 1-15.
SHEN Hui, ZENG Zu-qin. Solar energy photovoltaic power technology[M]. Beijing: Chemical Industry Press, 2005: 1-15.
[3] 徐宝琨, 赵慕愚. 低压硅外延生长的热力学研究[J]. 半导体学报, 1982, 3(5): 343-350.
XU Bao-kun, ZHAO Mu-yu. Thermodynamic study of low-pressure epitaxy of silicon[J]. Chinese Journal of Semiconductors, 1982, 3(5): 343-350.
[4] 徐宝琨, 赵慕愚. SiCl4外延生长硅晶体中碳玷污的热力学分析[J]. 半导体学报, 1984, 5(3): 247-256.
XU Bao-kun, ZHAO Mu-yu. A thermodynamical analysis of carbon contamination in silicon epitaxyal growth from SiCl4[J]. Chinese Journal of Semiconductors, 1984, 5(3): 247-256.
[5] CHARIG J M, JOYCE B A. Epitaxial growth of silicon by hydrogen reduction of SiHCl3 onto silicon substrates[J]. Journal of the Electrochemical Society, 1962, 109(10): 957-962.
[6] HUNT L P, SIRTL E. A thorough thermodynamic evaluation of the silicon-hydrogen-chlorine system[J]. Journal of the Electrochemical Society, 1972, 119(12): 1741-1745.
[7] SIRTL E, HUNT L P, SAWYER D H. High temperature reactions in the silicon-hydrogen-chlorine system[J]. Journal of the Electrochemical Socoety, 1974, 121(7): 919-925.
[8] VLADIMIR S B, STEPHEN L G. Chemical processes in vapor deposition of silicon[J]. Journal of the Electrochemical Socoety, 1975, 122(10): 1382-1391.
[9] DIANA M, MARINO L D, MASTRANT L, ROSSI R. Thermodynamic analysis of the reduction of silicon chlorides with hydrogen in the 300-4 500 K temperature range[J]. Rev Int Hautes Tempér Refact, 1981, 18(3): 203-213.
[10] LI C H. Epitaxial growth of silicon[J]. Journal of the Electrochemical Society, 1962, 109(10): 952-956.
[11] ANDREW M S. The kinetics of epitaxial growth of silicon from the trichlorosilane-hydrogen reaction[J]. Journal of the Electrochemical Society, 1964, 111(4): 483-484.
[12] BRADSHAW S E. The effects of gas pressure and velocity on epitaxial silicon deposition by the hydrogen reduction of chlorosilanes[J]. INT J Electronics, 1967, 23(4): 381-391.
[13] ASHEN D J, BROMBERGER G C, LEWIS T J. Kinetics of the reduction of silicon tetrachloride and trichlorosilane by hydrogen[J]. J Appl Chem, 1968, 18: 348-352.
[14] ANDERS L. Epitaxial growth of silicon from dichlorosilane[J]. Journal of the Electrochemical Society, 1972, 119(8): 1122-1123.
[15] 苗军舰, 陈少纯, 丘克强. 西门子法生产多晶硅的热力学[J]. 无机化学学报, 2007, 23(5): 795-801.
MIAO Jun-jian, CHEN Shao-chun, QIU Ke-qiang. Thermodynamic study on production of the multicrystalline silicon by Siemens process[J]. Chin J Inorg Chem, 2007, 23(5): 795-801.
[16] 苗军舰. 西门子法生产多晶硅的热力学[D]. 长沙: 中南大学, 2007.
MIAO Jun-jian. Thermodynamic study on production of the multicrystalline silicon by Siemens process[D]. Changsha: Central South University, 2007.
基金项目:广东省教育部产学研结合专项基金资助项目(2006D90404001)
收稿日期:2008-01-21;修订日期:2008-06-06
通讯作者:丘克强,教授;电话:0731-8877364;E-mail: qiuwhs@sina.com
(编辑 陈爱华)