�����γ�������SO2��AZ91Dþ�Ͻ������ʴ��Эͬ����
�� ��1, 2, �ϴ�ΰ1
(1. �й���ѧԺ�����о��� ������ʴ����������ص�ʵ����, ���� 110016;
2. ����������ѧ ���Ͽ�ѧ�빤��ѧԺ, ���� 110168)
ժ Ҫ: ��ʵ����ģ��������(25��, 85%��5% RH), ͨ��ʧ�ط��� ɨ��羵�� ����Ҷ�������X���������о��˿����κ�SO2��AZ91Dþ�Ͻ������ʴ��Ϊ��Ӱ�졣 �������: �����κ�SO2����������Եؼ���AZ91Dþ�Ͻ�ĸ�ʴ, ��������֮����丯ʴ����Эͬ���á� ���丯ʴ������Эͬ���ý��������ۡ�
�ؼ���: ������ʴ; þ�Ͻ�; ������; SO2 ��ͼ�����: TG172.3
���ױ�ʶ��: A
Synergetic effect of soluble salts and SO2 on atmospheric corrosion of diecast AZ91D magnesium alloy
WAN Ye1, 2, YAN Chuan-wei1
(1. State Key Laboratory for Corrosion and Protection, Institute of Metal Research,Chinese Academy of Sciences, Shenyang 110016, China;
2. School of Materials Science and Engineering, Shenyang Jianzhu University,Shenyang 110168, China)
Abstract: The atmospheric corrosion behavior of diecast AZ91D magnesium alloy deposited with different salts and in the presence of SO2 (25�� and 85%��5% RH) was studied by gravimetry, Fourier transform infrared spectroscope, scanning electron microscopy and X-ray diffraction. The result shows that there is synergetic effect of the soluble salts and SO2. Both the soluble salts and SO2 can accelerate the atmospheric corrosion of AZ91D magnesium alloy. The synergetic effect of the soluble salts and SO2 may enable the atmospheric corrosion of metallic materials greater than that caused by single component of the two respectively.
Key words: atmospheric corrosion; magnesium alloy; soluble salts; SO2
þ������Ľṹ����֮һ, ����������������, ��߱�ǿ�ȡ� ɢ���Լѡ� �����Ժá� ��������Ժ�, ���Ծ��丯ʴ��Ӧ����ʴ����(SCC)�����жȵ�, �Լ��Ի�������ȾС���ص�[1-4], ��˳�Ϊ�������ϡ� ���Ͻ�ֲĸ����������ľ��������Ʒ[5, 6], �������� ͨѶ�豸�� ������ҵ�� ���պ��졢 �����Լ����ܵȹ�ҵ���������õ�����㷺��Ӧ��[7-11], ������Ϊ21��������ǰ;����ɫ�ṹ����[12, 13]�� ����, AZ91Dþ�Ͻ���������ܡ� ��ѧ���ܽϺ�, ��þ�Ͻ�������Ӧ����Ϊ�㷺��
Ȼ��, ����þ�ڳ�ʪ�����е�����ѧ���ȶ���, ��ѧ���Ը�, �ڿ����к����������� ��Ⱦ�����ر��ǹ�ҵ��Ⱦ�����ܴ�����þ�Ͻ�ĸ�ʴ�ƻ�, ͬʱҲ��������Ϊ�ṹ���ϵ�ʹ�ÿɿ��ԡ� SO2�ǹ�ҵ���������е���Ҫ������Ⱦ��֮һ, ���Խ����Ĵ�����ʴ���Ų��ɺ��ӵ�Ӱ�졣 ��1935��Vernon[14]����֤��������һЩ�����Ĵ�����ʴ���м�����������, ����ѧ�߾ͶԴ˽����˹㷺���о�, ̽�������Ը��ֽ���������ʴ�ľ���Ӱ�졣 Haynie��Upham[15]�Լ�����ѧ����ΪZn�ڲ�ͬ���������и�ʴ�����Բ����Ҫ����Ϊ������SO2�ĺ�����ͬ��
һЩ�о���[16]�Ѿ������˶�����̼���Ȼ��Ƶij����Լ���þ�Ͻ�Ĵ�����ʴ��Ӱ��, ������Ϊ��NaCl����������, CO2�Ĵ��ڽ����м���þ�Ͻ������ʴ�����ơ� ����û�м������ֿ����κͶ��������þ�Ͻ�ĸ�ʴ�����о��ı�����
��������ͨ��ģ���������, �о���ͬ�����κ�SO2��AZ91Dþ�Ͻ���ڴ�����ʴ��Ӱ�졣 ͬʱ������Fourier�任�������(FTIR)�� ɨ��羵/X����������(SEM/EDAX)��X�����������(XRD)���ֶζԸ�ʴ���漰��ʴ������з���, �о��丯ʴ����, ̽�ֲ�ͬ�����κ�SO2֮���ЭͬЧӦ��AZ91Dþ�Ͻ�ʴ��Ӱ�졣
1 ʵ��
ʵ���ò�Ϊѹ��AZ91Dþ�Ͻ�, �仯ѧ�ɷ����1��ʾ�� �����ߴ�Ϊ10mm��10mm��1.5mm, һ�����й����ס� ��800#~1000#ɰֽ��ĥ, ��������Ϊ1.5��m�Ľ��ʯ��ĥ����, ����������ˮ��ֳ�ϴ, Ȼ�����Ҵ��ͱ�ͪ������������ϴ�ɾ�, ������ȡ������ ��������Ϊ��ʿMettler-Toledo��ƽ(����Ϊ10-7g)��
��1 AZ91Dþ�Ͻ�Ļ�ѧ�ɷ�(��������, %)
Table 1 Chemical composition of AZ91D magnesium alloy (mass fraction, %)
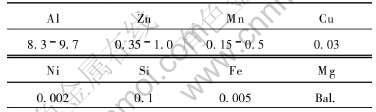
��ʵ�����õ�(NH4)2SO4�� Na2SO4�� NaCl��NH4Cl��Һ�ǰ�һ�����������������ˮ����ˮ�Ҵ����ƶ��ɵ�, ���������ε�Ũ�Ⱦ�Ϊ3.03��10-2mol/L, �������ε�Ũ�Ⱦ�Ϊ6.06��10-2mol/L�� ��������������������ֱ���Ϳ(NH4)2SO4�� Na2SO4�� NaCl��NH4Cl��15��L, ��ʹ�������չ���������档 �հ�����Ϊ����δ�����γ������ڸ�ʴ���н��в�ͬ��¶ʱ��������� ��ͬ����Һ�ľ������ƺͳ�������������[20]��
��ʴ�������Ի����, ��������ʴ���巢����, ����SO2��ʴ���塣 �����Ϳ�ѹ��������ѹ����������ʪ�� ����������, �ֳ�����֧·, һ·Ϊ�ɿ�����SO2������������, ��һ·Ϊ��60����������ˮ���͵�ʪ����, ��ʪ��·�����ڻ�����ϡ� ����������������, ���ƻ��������������ʪ��(RH)��85%��5%֮��, ʹ��ʴ������SO2����ԼΪ10-6, ͨ�븯ʴ�䡣 �ú���ˮԡ�Ϳյ�����ϵͳ���¶���(25��1)�淶Χ�ڡ� ����ϵͳ��Ҫװ�ü��������þ��ķ���ϩ���������Ƴɡ� ������ʴģ��ϵͳװ�òμ�����[18]�� ��ϸ�����������������ڸ�ʴ����, ��ʵ�����ʱ��Ϊ28d, ������ÿ��7dȡ��1��, ����ÿ�������µ������������������� ���Ƚ���Ʒ������������ˮ��ȥ�������Ե���, ���Ų��û�ѧ���������ʴ����, �������½������������Һ(200g CrO3+10g AgNO3+20g Ba(NO3)2+ ����ˮ���1000mL��Һ)��ȥ����ʴ����, Ȼ������������ˮ��ϴ�ɾ�, ����, ���������� ÿ��7d��3����ȫû�и�ʴ�Ŀհ���������������ʧУ����
�Ը�ʴ����ķ�����Ҫ����: ��������Nicolet��˾��Magna-IR560���������(VeeMax���丽��)���к�����ײ���, ɨ�����Ϊ64, �ֱ���Ϊ8cm-1�� ������ò���ú���Philips��˾������XL-30 FEG��(��¶��SO2�������е�����)������ɨ�������������ɨ��羵����; �����ձ���ѧ(Rigaku) D/max-2500pc ��X���������ǽ���XRD���ԡ�
2 ���������
ͼ1��ʾΪ�������γ����������ھ��������б�¶��ͬʱ���λ����ĸ�ʴ������ʧ��m/A(mg��cm-2), (���µ�λ����ĸ�ʴ������ʧ�����Ϊ��ʴ������ʧ)�� ͨ���Ƚ�ͼ1�и��������µĸ�ʴ������ʧ��֪, ��ʵ�����, �������γ�����������ʴ������ʧԶԶ���ڿհ������ĸ�ʴ������ʧ, �����γ������������ڸ�ʴ������ʧ��Ӱ��˳��ΪNH4Cl>NaCl>(NH4)2SO4>Na2SO4�� ��˵�����ֿ����ζ���AZ91Dþ�Ͻ�ij��ڴ�����ʴ�������Ե��շ����á� ���ε��շ����ø�������, �������������Ӱ뾶�����������С, �Ƚ����������������档 ���Ҿ�NH4Cl������������ʴ��չ���ƽϴ�
ͼ2��ʾΪ��4�ֿ����γ�����������SO2�����и�ʴ��ͬʱ���ĸ�ʴ������ʧ��m/A(mg��cm-2), ���Կ����������γ�����������ʴ������ʧԶԶ���ڿհ������ĸ�ʴ������ʧ, ��ͬ�����γ������������ڸ�ʴ������ʧ��Ӱ��˳��ΪNaCl>NH4Cl>(NH4)2SO4>Na2SO4>blank�� �Ƚ�ͼ1��ͼ2��֪, ��SO2�����е�������ʴ������ʧ�����ھ��������еĸ�ʴ������ʧ, ���SO2�Ϳ����γ������߿��ܶ�AZ91Dþ�Ͻ�Ĵ�����ʴ����Эͬ����, ������SO2�����еĸ�ʴ������ʧ�����ھ��������еĸ�ʴ������ʧ��
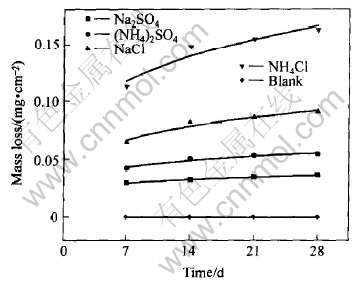
ͼ1 ����ͬ�γ����������ھ��������еĸ�ʴ������ʧ
Fig.1 Mass loss of AZ91D magnesium alloy deposited with salts vs exposure time in clean atmosphere
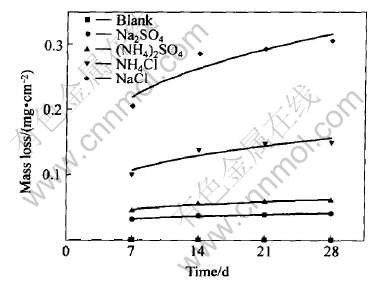
ͼ2 ����ͬ�γ����������ں�SO2�����еĸ�ʴ������ʧ
Fig.2 Mass loss of AZ91D deposited with salts vs exposure time in SO2-containing atmosphere
ͼ3��ʾΪ����4�ֿ����ε������ں�SO2�����и�ʴ28d���SEM��ò�� ��ɨ��羵ͼƬ���Կ���, 4�ֿ����γ�����ĸ�ʴ�����ı�����ò�нϴ�ͬ, ��ʴ����ֲ��������ȡ� ���Ȼ��Ƴ��������ĸ�ʴ��Ϊ����, ������ֽϴ��Ƭ״��ʴ�������Ƥ, �����нϴ�����ơ� ���ִ����ƶԸ�ʴ����(ˮ�ݡ� ������)�Ĵ���������С, ����ڸ������µĸ�ʴ������ʧ�ϴ� ����������ֱȽϾ��ȵĸ�ʴ��ò, ���º��ڵĸ�ʴ��չ���ƽϾ��Ȼ�炙����� �����γ������������港ʴ�������γ��������ĸ�ʴ�̶�����, �������������Ӱ뾶��С, ���Խ�ǿ, ��þ�Ͻ�ĸ�ʴ��ʴ�Խϴ��Ե�ʡ�
����ͬ�����γ����������ں�SO2�����б�¶28d����港ʴ����ṹ������ͬ�� ������к����������֪, ���ܳ����Ŀ����β�����ͬ, ��4�ֿ����γ��������ĸ�ʴ�����о��������ǻ�����������ӵ��������շ塣 ��NH4Cl�����;�NaCl�����������ں�SO2�����и�ʴ28d��ĺ��������ͼ4(a)��ͼ5(a)��ʾ�� ����λ��1640cm-1��1790cm-1���������շ�ΪOH-�������շ�[19, 20], ����λ��1106cm-1, 1023cm-1��691cm-1���������շ�ΪSO2-4�������շ�[19, 21]�� �Ը���������ĸ�ʴ���������X�����������, �õ���ͼ4(b)��5(b)��ʾ�Ľ���� ��NH4Cl���������ĸ�ʴ������Ҫ��MgCl2��H2O��MgSO4��H2O���, ��NaCl������������ʴ������Ҫ����MgCl2��H2O�� MgSO4��H2O��Na21Mg(SO4)10Cl3��ɡ� ˵��SO2��������˸�ʴ�Ĺ��̡�
þ��һ�ַdz����õĽ���, ����缫����Ϊ-2.37V, �����нṹ��������͵ġ� ��ͼ6��ʾ, þ����������ѧ�ȶ�����������ˮ���ȶ����� ����¶�ڿ�����ʱ, ����þ�������������γ�һ����Mg(OH)2�� MgO����μ�����(�����ˮ��MgCO3�� MgSO3��)Ϊ���Ļ�ɫ��Ĥ[7, 22-25]�� ��������������ѧ�ȶ��Բ���, ���������Ĥֻ�ܶԻ�������ṩ������ʱ�Ա����� ����þ��һ��ǿ��ԭ��, ������pHֵ��, ����������ˮ��Ӧ, ʹˮ��ԭ����H2, �������γ�Mg+��Mg2+�����ܽ⡣ ��pHΪ8.5��11.5ʱ, þ�����ɻ����ٵر����������������������������, ���ܽⷴӦ���谭����, ��ǿ���Խ�����(pHֵ11~12����), ���������ȶ���Mg(OH)2Ĥ���ۻ�[26]�� �����ԡ� ���Ժ���������Һ��, þһ��ᷢ����ʴ, �丯ʴ������pH�Ľ��Ͷ�����, þ�Ͻ�ĸ�ʴ���Ե绯ѧ���ƽ��е�[27]��
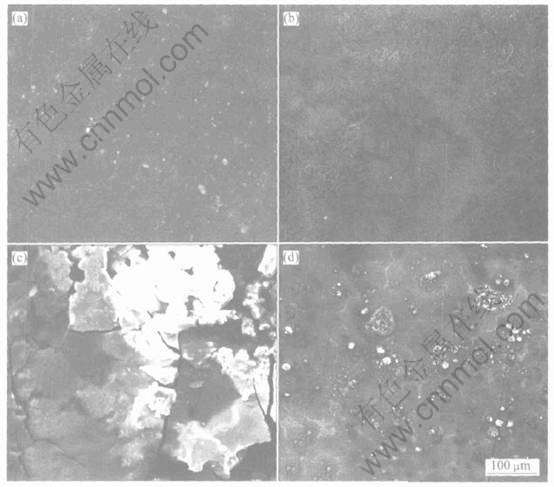
ͼ3 ���������ε������ں�SO2�����и�ʴ28d������SEM��ò
Fig.3 SEM micrographs of AZ91D deposited with Na2SO4(a), (NH4)2SO4(b), NaCl(c) and NH4Cl(d) after exposed for 28d in SO2-containing atmosphere
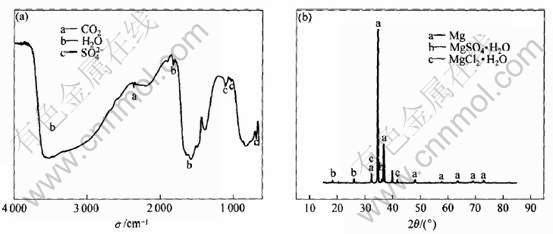
ͼ4 ��NH4Cl�����������ں�SO2�����и�ʴ28d��ĺ������(a)��X����������(b)
Fig.4 FTIR spectrum(a) and XRD pattern(b)of samples deposited with NH4Cl after exposed for 28d in SO2-containing atmosphere
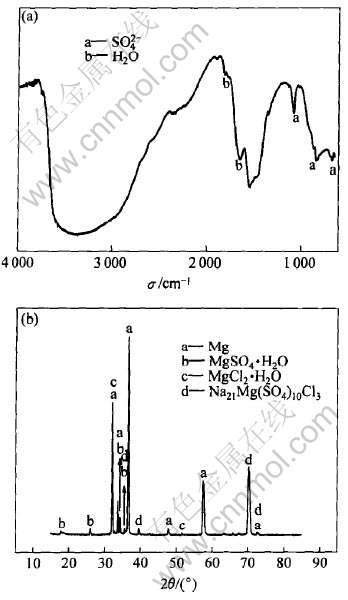
ͼ5 ��NaCl�����������ں�SO2�����и�ʴ28d��ĺ������(a)��X����������(b)
Fig.5 FTIR spectrum(a) and XRD pattern(b) of samples with NaCl after exposed for 28d in SO2-containing atmosphere
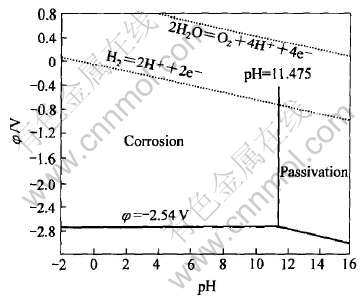
ͼ6 Mg-H2Oϵ��λ��pHƽ��ͼ
Fig.6 Potential��pH diagram of Mg-H2O at 25��
����NaCl��Na2SO4���к�ǿ��������, һ������������������ܴ���Χ����������ˮ��, �γ�NaCl(ads)��Na2SO4(ads)��ˮ��ҺҺĤ�� �ں�SO2��������, SO2������������Ʒ��������ˮĤ��, �Ӷ�����ˮ��͵���, ʹ��Ʒ�����������, �����丯ʴ����, ��ͼ1��ͼ2��ʾ�� �������ֵ������ԭ��, ������Cl-(ads)��SO2-4(ads)ͨ��Ǩ�ƾۼ���������, �γ�MgCl2(ads)��MgSO4(ads), ������������pHֵ����, ��������������������þ���ܽ�; ���������ڴ�����OH-, �Ӷ�����Na+�������Ǩ�ƶ��ۼ��� �ɺ������X������������֪, ��NaCl������������ʴ����ΪMgSO4��H2O�� MgCl2��H2O���Լ�����ӵ�Na21Mg(SO4)10Cl3, ��Ϊ����ĸ�ʴ�����, ��ͼ3�еĸ�ʴ��ò�� ��ʴ����������ʾ:
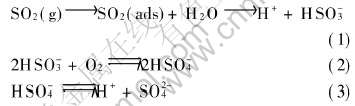
ͬʱ, ��AZ91Dþ�Ͻ���Ʒ����ľֲ�����þ�������ܽ�, �缫��ӦΪ
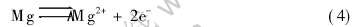
һ����Ϊ����Ϊ��Ļ�ԭ:
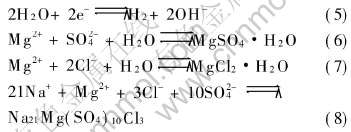
��Na2SO4���������������ƵĽ���� ������SO2-4(ads)ͨ��Ǩ�ƾۼ���������, �Ӷ����������γ�MgSO4(ads)��Һ, ������������pHֵ����, ������������þ���ܽ�; ���������ڴ�����OH-, �Ӷ�����Na+�������Ǩ�ƶ��ۼ���
��NH4Cl��(NH4)2SO4��������������笠����ӷ���ˮ��, ����H+, ����AZ91Dþ�Ͻ�Ĵ�����ʴ�� ͬ���������ֵ������ԭ��, ������Cl-(ads)��SO2-4(ads)ͨ��Ǩ�ƾۼ���������, �Ӷ����������γ�MgCl2(ads)��MgSO4(ads)�� �ɺ���������֪, ��ʴ����Ϊ���ᾧˮ��MgCl2��MgSO4, ��Щ��ʴ�����Թ�����ʽ�ۼ���������, ��ͼ3�еĸ�ʴ��ò��ʾ�� ��ʴ������ʽ(1)~(5)�Լ����µķ���ʽ��ʾ:
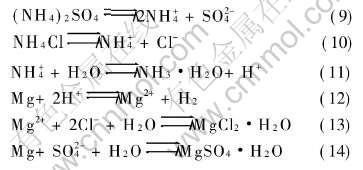
���������ε�AZ91Dþ�Ͻ���SO2�����еĸ�ʴ��Ϊ����SO2��������ˮ����, �������SO2-4��ѭ�����Ʋ��ϵ�������[28-30], ���¸�ʴ���̵IJ��Ͻ��С�
3 ����
AZ91Dþ�Ͻ������ھ���������SO2�����еĸ�ʴ������ʧ�����������졣 ������ʴ������ʧ�ķ�չ����ʱ����ӳ��нϴ�ı仯: �����7d�︯ʴ������ʧ�ϴ�, ��14d��ʴ������ʧ��Ϊ������ ��������ʴ������нṹ����, ��֪��SO2�����еĸ�ʴ�����о��к��ᾧˮ����, ����������SO2�����еĸ�ʴ������ʧ�����ھ��������еĸ�ʴ������ʧ, ֤ʵ��SO2�����˸�ʴ�Ľ���, ���ҺͿ�����֮���AZ91Dþ�Ͻ�Ĵ�����ʴ����Эͬ���á�
���������Ӷ�AZ91Dþ�Ͻ����ʴ��Ϊ����, ��˾�NaCl��NH4Cl�����������ĸ�ʴ�Ͼ�Na2SO4��(NH4)2SO4����������; ����SO2��NaCl��Эͬ���������ɵ�������ʴ����Ƚϴִ� ����, ���ڽϴ������, �丯ʴ����Ͼ����������γ����������ء�
REFERENCES
[1]Froes F H, Eliezer D, Aghion E. The science, technology and application of magnesium[J]. J Mine Metals and Material Society, 1998, 5(9): 30-34.
[2]Decker R F. The Renaissance in magnesium[J]. Advanced Material Process, 1998, 154(3): 31-33.
[3]Nakatsugawa I, Martin R, Knystautas E J. Improving corrosion resistance of AZ91D magnesium alloy by nitrogen ion implantation[J]. Corrosion, 1996, 52(12): 921-926.
[4]Froats A, Aune T K, Hawke D, et al. Corrosion of magnesium and magnesium alloys[A]. ASTM International. Metal Handbook. 9th Edition[C]. USA: ASM International, 1987. 740-754.
[5]Zozulin A J, Bartak D E. Anodized coatings for magnesium alloys[J]. Metal Finishing, 1994, 92(3): 39-44.
[6]Makar G L, Kruger J. Corrosion of magnesium[J]. International Materials Reviews, 1993, 38(3): 138-153.
[7]Mordike B L, Ebert T. Magnesium: properties-applications-potential[J]. Mater Sci Eng A, 2001, A302: 37-45.
[8]American Society for Metals on Cleaning and Finishing of Magnesium Alloys. Cleaning and finishing of magnesium alloys[A]. ASM. Metal Handbook, 9th Edition Vol.5 Surface Cleaning, Finishing and Coating[M]. USA: ASM International, 1982. 628-649.
[9]Polmear I J. Recent developments in light alloy[J]. Trans JIM, 1996, 37(1): 12-15.
[10]Idris M H. Precision casting of a magnesium-base alloy[J]. Br Foundryman, 1997, 90(4): 140.
[11]Idris M H. Processing and evaluation of investment cast magnesium-base alloy[J]. AFS Trans, l996, 104: 237.
[12]Groshart E. Preparation of nonferrous metals for plating[J]. Metal Finishing, 2002,98(A): 82-86.
[13]Voytko J E. Organic finishing & plating & surface finishing[J]. Plating & Surface Finishing, 2000(8): 54-56.
[14]Vernon W H J. Effects of SO2 on corrosion of zinc[J]. Trans Faraday Soc, 1935(31): 1668-1670.
[15]Haynie F H, Upham J B. Effects of atmospheric sulfur dioxide on the corrosion of zinc[J]. Material Performance, 1970, 9(8): 35-40.
[16]Lindstr��m R, Svensson J E, Johansson L G. The influence of carbon dioxide on the atmospheric corrosion of some magnesium alloys in the presence of NaCl[J]. Journal of the Electrochemical Society, 2002, 149(4): B103-B107.
[17]����, �ϴ�ΰ, �ܳ���. �����γ�����̼�ִ�����ʴ��Ӱ��[J]. ������ѧѧ��, 2004, 2(6): 659-663.
WAN Ye, YAN Chuan-wei, CAO Chu-nan. Atmospheric corrosion of A3 steel deposited with different salts[J]. Acta Physchim Sin, 2004, 2(6): 659-663.
[18]WAN Ye, YAN Chuan-wei, CAO Chu-nan. Atmospheric corrosion of steel A3 deposited with ammonium sulfate and in the present of sulfur dioxide[J]. J Mater Sci Technol, 2003, 19(5): 453-455.
[19]��誹�. ��������Ҷ�任�����������Ӧ��(�¾�)[M]. ����: ��ѧ�������׳�����, 1994. 269-271.
WU Jin-guang. Technique and Application of Infrared Fourier Transform Spectroscopy (Vol.2)[M]. Beijing: Science and Technology Information Press, 1994. 269-271.
[20]Yamashita M, Miyuki H, Matsuda Y, et al. The long term growth of the protective rust layer formed on weathering steel by atmospheric corrosion during a quarter of a century[J]. Corrosion Science, 1994, 36(2): 291.
[21]Nyquist R A, Kagel R O. Infrared Spectra of Inorganic Compounds[M]. New York and London: Academic Press, 1971. 12.
[22]Mcintyre N S, Chen C. Role of impurities on Mg surfaces under ambient exposure conditions[J]. Corrosion Science, 1998, 40(10): 1697-1709.
[23]Nordlien J H, Ono S, et al. A TEM investigation of naturally formed oxide films on pure magnesium[J]. Corrosion Science, 1997, 39(8): 1397-1414.
[24]Nordlien J H, Nisancioglu K, et al. Morphology and structure of water-formed oxides on ternary MgAl alloys[J]. Journal of Electrochemical Society, 1997, 144(2): 461-466.
[25]Pebere N, Riera C, et al. Investigation of magnesium corrosion in aerated sodium sulfate solution by electrochemical impedance spectroscopy[J]. Electrochimica Acta, 1990, 35(2): 555-561.
[26]Reichek K N, CLak K J, Hillis J E. Sea Technical Paper series[M]. 1985. 1.
[27]Godard H P, Jepson W B, Bothwell M R, et al. The Corrosion of Light Metals[M]. New York: John Wiley & Sons, 1967. 81.
[28]Skerry B S, Johnsson J B, Wood G C. Corrosion in smoke, hydrocarbon and SO2 polluted atmospheres����. General behaviour of iron[J]. Corrosion Science, 1988, 28(7): 657-667.
[29]Skerry B S, Johnsson J B, Wood G C. Corrosion in smoke, hydrocarbon and SO2 polluted atmospheres����. Mechanistic implications for iron from surface analytical and allied techniques[J]. Corrosion Science, 1988, 28(7): 697-719.
[30]Skerry B S, Johnsson J B, Wood G C. Corrosion in smoke, hydrocarbon and SO2 polluted atmospheres����. The general behaviour of zinc[J]. Corrosion Science, 1988, 28(7): 721-727.
(�༭��ѧ��)
������Ŀ: ������Ȼ��ѧ����������Ŀ(50499336)
�ո�����: 2005-04-08; ������: 2005-11-16
�����: �� ��(1972-), ������, ��ʿ
ͨѶ����: �� ��, ������; �绰: 024-23921875; E-mail: ywan@imr.ac.cn